对羟基苯甲醛的合成研究现状及新进展
王思宇 王相承
(中国人民解放军陆军防化学院,北京 102205)
对羟基苯甲醛(p-Hydroxybenzaldehyde,简记为PHB),广泛用于医药、农药、香料、化工、电镀、液晶材料等领域。随着市场需求量的不断增加,高纯度的对羟基苯甲醛产品更为市场青睐,但是国内对羟基苯甲醛的生产厂家较为零散,规模较小,低水平重复建设严重。科研工作者也在持续关注对羟基苯甲醛的合成改进研究[1],但近几十年来一直没有突破性进展。
现有对羟基苯甲醛的合成方法有很多种。依据起始原料的不同,主要以对硝基甲苯[2,3]、对氯苯酚[4]、对甲酚[5-7]、苯酚[6,8-11]为原料合成对羟基苯甲醛。这4种起始化合物,经过不同的途径转化为对羟基苯甲醛,常常因催化剂的选用而表现出动力学效果的差异,但没有解决副产物多或“三废”严重的关键难题。此外,还有以对羟基苯甲醇、对羟基苯甲醛苯腙、对羟基苯甲醛肟以及缩醛类衍生物、苯甲醛衍生物为原料合成对羟基苯甲醛的方法,这些方法仅有一定的理论价值,实际应用意义不大[12]。
以苯酚为原料合成对羟基苯甲醛具有原子经济性,在苯酚的对位引入醛基的技术方案具有竞争优势。日本的对羟基苯甲醛生产技术有垄断全球的趋势,但具体的技术动态鲜见报道。
本文对比分析对羟基苯甲醛的几种合成方法,重点讨论改进酚羟基对位引入醛基的可行性及可采取的技术措施。
1 现有对羟基苯甲醛的合成方法及存在的问题分析
1.1 以对硝基甲苯为原料[2,3]
以对硝基甲苯为原料,在Na2Sx的碱性水-乙醇环境中,经氧化-还原生成对氨基苯甲醛,而后通过硫酸酸化形成硫酸盐,加入NaNO2溶液,经过重氮化、水解得到对羟基苯甲醛(PHB)。如图1所示。
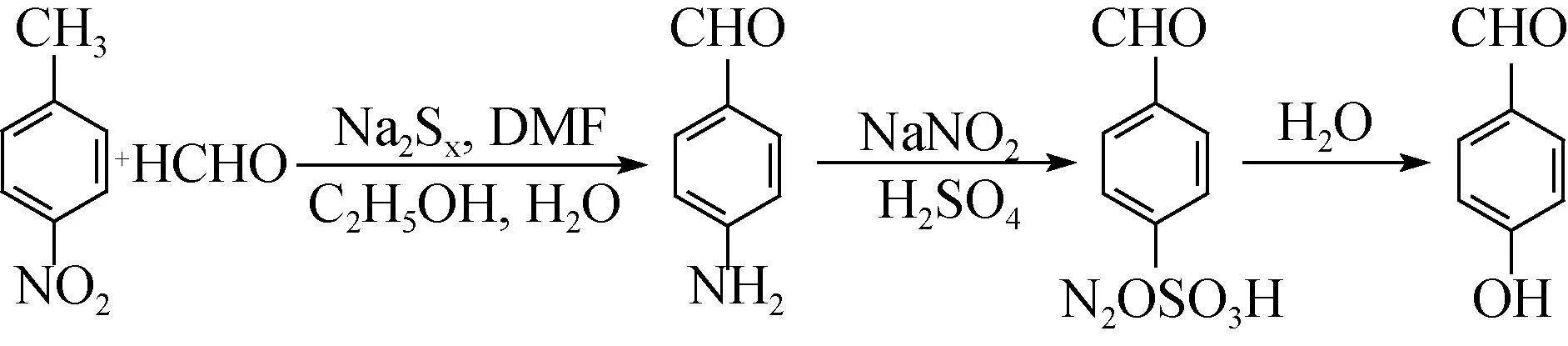
图1 对硝基甲苯合成对羟基苯甲醛Fig.1 Synthesis of p-hydroxybenzaldehyde from p-nitrotoluene
反应先生成的对氨基苯甲醛,可分子间缩合成席夫碱,易发生自缩聚,影响产率。如图2所示。
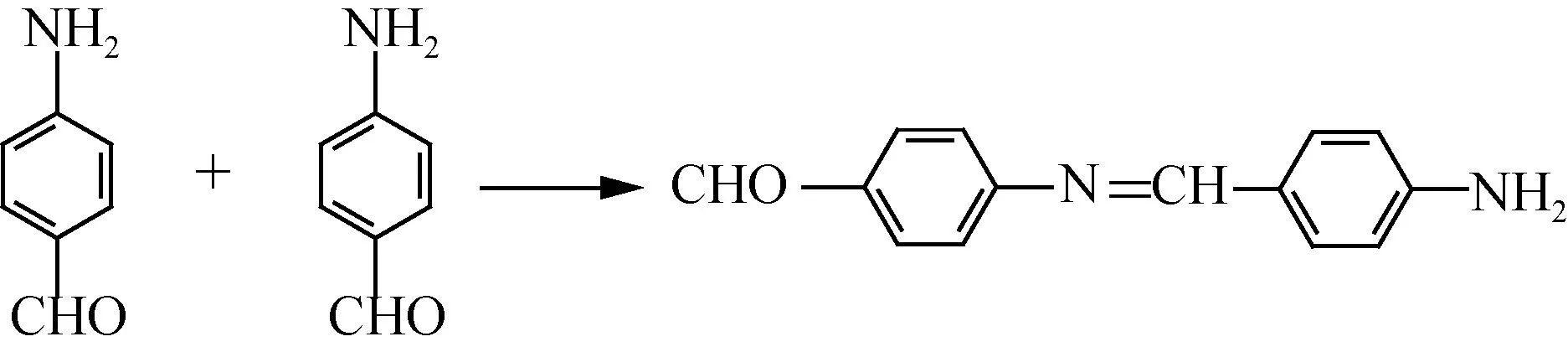
图2 中间体对氨基苯甲醛的自聚Fig.2 Self polymerization of intermediate p-aminobenzaldehyde
除此,它还能与反应生成的副产物对氨基苯甲醛缩合,缩合产物的分子中也有氨基,可与对羟基苯甲醛进一步缩合,如图3所示。
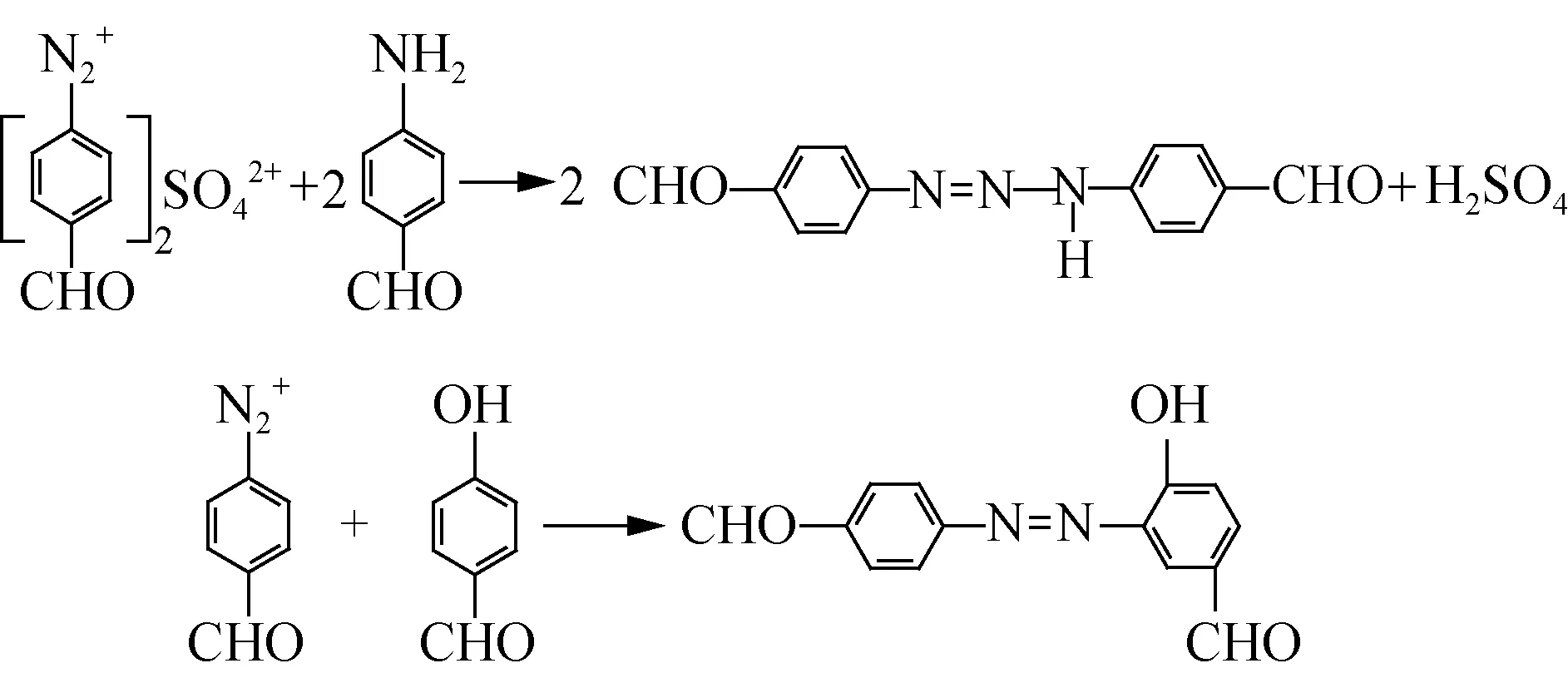
图3 对氨基苯甲醛与对羟基苯甲醛的自聚与偶联反应Fig.3 Self polymerization and coupling reaction of p-aminobenzaldehyde and p-hydroxybenzaldehyde
该反应对pH要求较高,对氨基苯甲醛在碱性环境中会发生聚合反应,生成深红色不溶性固体。重氮化反应过程中,pH值对生成重氮盐的稳定性有较大影响,生成的不稳定重氮盐容易与未反应的对氨基苯甲醛形成不溶解的重氮氨基苯甲醛化合物;重氮盐水解生成对羟基苯甲醛时,产物有可能和重氮盐发生偶联副反应。
1.2 以对氯苯酚为原料[4]
对氯苯酚在复合催化剂醋酸钯、三环己基膦和4-(二甲氨基)吡啶等催化剂作用下,可在较低温度和压力下顺利进行反应。如图4所示。
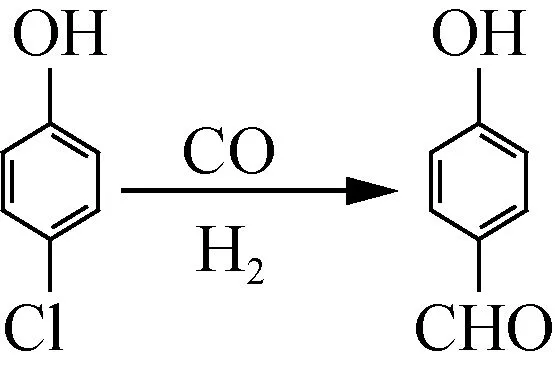
图4 对氯苯酚复合催化制备对羟基苯甲醛Fig.4 preparation of p-hydroxybenzaldehyde from p-chlorophenol by composite catalysis
但该法工业化过程中遇到的难题是设备要求高、危险性大,催化剂成本高,再生效果差,产率不稳定。
1.3 以对甲苯酚为原料
以对甲苯酚为原料合成对羟基苯甲醛的研究报道较多,典型的有对甲苯酚酯化法、Mn2O3氧化法、过渡金属盐催化氧化法、Etard氧化法和电化学氧化法,其中电化学氧化法工业化前景较好,但氧化电极的寿命和氧化的工艺安全问题需要进一步深入研究。如表1所示。
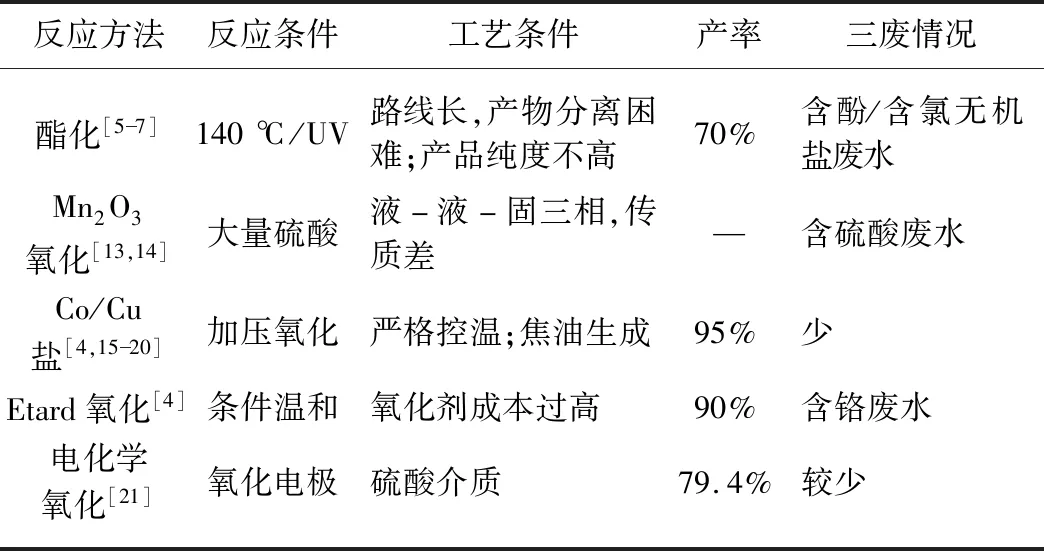
表1 以对甲苯酚为原料合成PHB比较表Tab.1 Comparison of synthesis of PHB from p-cresol
以对甲苯酚为原料合成对羟基苯甲醛的现有方法中,要么催化剂的寿命及活性受限,要么工艺条件较为苛刻,离规模化应用还有较远的距离。
1.4 以苯酚为原料
以苯酚为原料合成对羟基苯甲醛的研究报道也较多。苯酚为原料,在碱金属氢氧化物作用下,苯酚与氯仿发生Reimer-Tiemann反应;碳酸钾的催化下,苯酚与三氯乙醛缩合;苯酚与甲醛在稀碱或弱酸作用下在邻位和对位上发生缩合;苯酚和N,N-二甲基甲酰胺在POCl3作用下进行Vilsmierm反应;苯酚和液体氢氰酸在三氯化铝催化下进行Gattermann反应。这几种反应都可以制备对羟基苯甲醛,如表2所示。
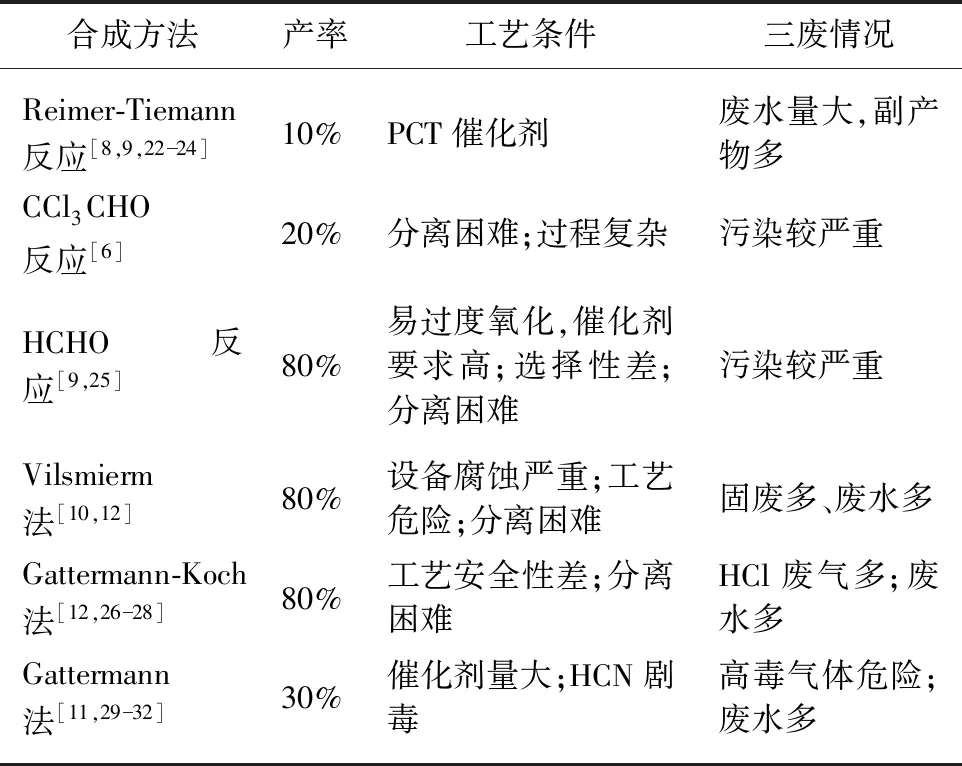
表2 以苯酚为原料合成PHB比较表Tab.2 Comparison of synthesis of PHB from phenol
目前国内外化工企业大多采用Reimer-Tiemann反应制备水杨醛,同时副产对羟基苯甲醛。如图5所示。
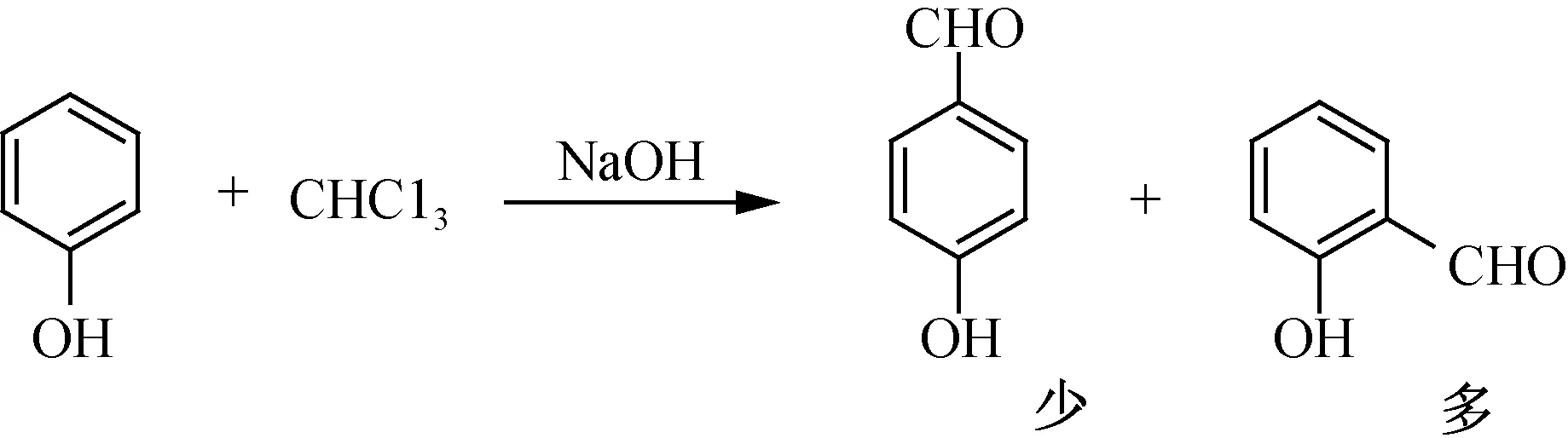
图5 苯酚与氯仿Reimer-Tiemann反应制备水杨醛Fig.5 preparation of salicylaldehyde by Reimer-Tiemann reaction of phenol and chloroform
该法原料价廉易得,但是该反应以邻位产物(水杨醛)为主,对羟基苯甲醛的收率较低。
2 Gattermann反应合成对羟基苯甲醛的方法改进
苯酚和液体氢氰酸在三氯化铝催化下制备对羟基苯甲醛是经典的Gattermann反应,如图6所示。
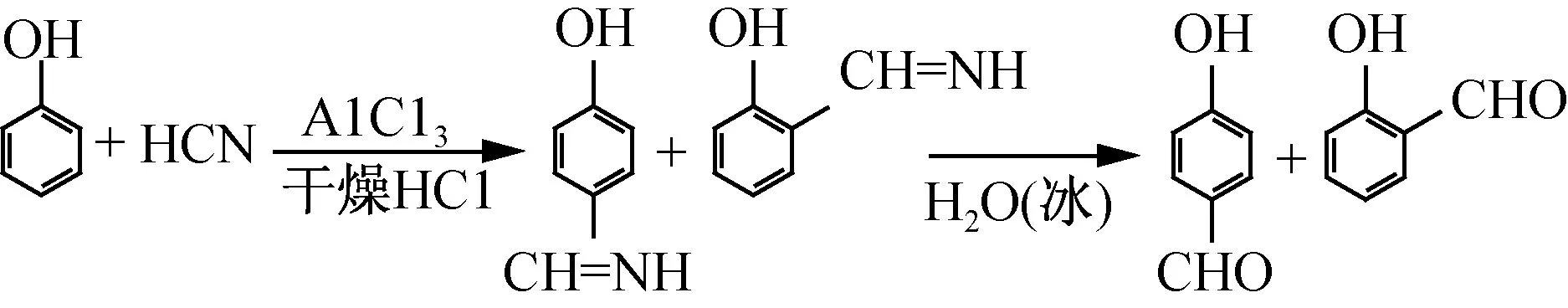
图6 苯酚与氢氰酸合成对羟基苯甲醛Fig.6 synthesis of p-hydroxybenzaldehyde from phenol and hydrocyanic acid
国内研究工作者在关注改进对羟基苯甲醛合成方法的同时,对Gattermann反应制备对羟基苯甲醛给予了充分肯定[4,33,34]。尤其是改进后的Gattermann反应[29,31,32],通过氰盐直接制备对羟基苯甲醛,如图7所示,更显示了其合成对羟基苯甲醛的巨大优势。
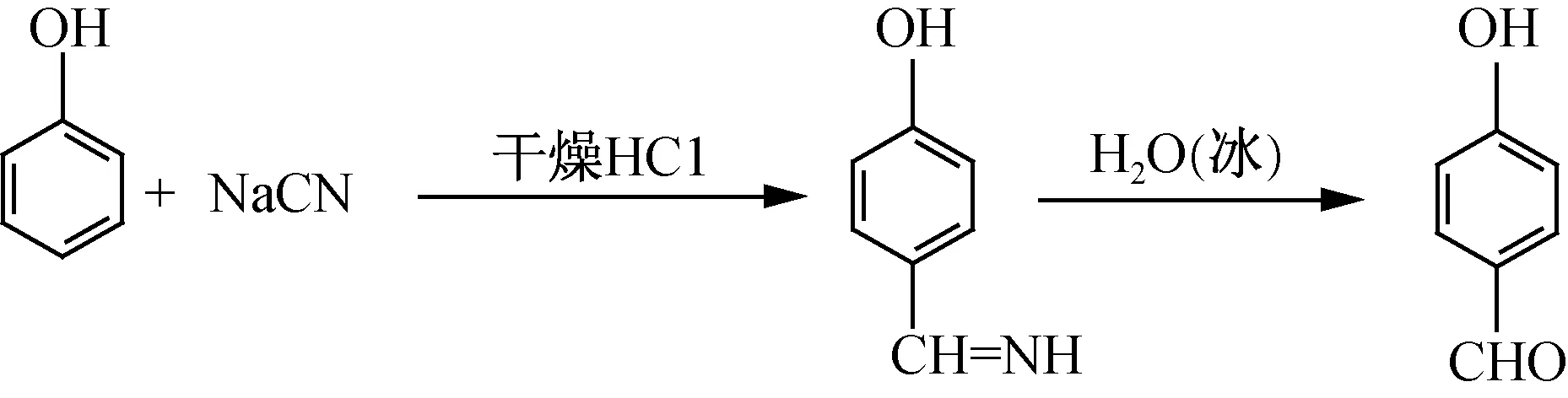
图7 苯酚与氰盐合成对羟基苯甲醛Fig.7 synthesis of p-hydroxybenzaldehyde from phenol and cyanate
2.1 原子经济性高
改进后的Gattermann反应,通过苯酚亚胺化制备对羟基苯甲醛,在酚羟基对位通过氰盐(NaCN)的氰根质子化引入亚甲胺基,质子源来自氯化氢,理论上的副产物仅为氯化钠,因此该反应的原子利用率高。
2.2 工艺安全性好
以氰盐作为反应原料,固体投料,比传统的氢氰酸法改进了安全性。通入无水氯化氢的过程可以采用微正压,在密封的反应器内完成,一是体系密封更有利于保持通气过程的干燥;二是反应过程消耗气体氯化氢,从动力学角度,微正压更有利于反应的进行;三是无尾气外排,消除了因尾气携带HCN可能产生的危险。
2.3 有绿色化工前景
国内的相关学者几乎都给出了该反应能定量反应的结论,以引用的二次文献居多,但都没有数据支持,其中重要的原因是限于氰化钠(氰化钾)的高毒剧毒不便于展开相关研究。其实随着国内菊酯类(尤其甲氰菊酯)农药的大量生产,氰化物的生产安全已经积累了成熟的经验,形成了完善的处置方案。通常采取双氧水氧化技术,产生的工艺废水含氯化钠,可封闭运行,三废压力小。
3 改进Gattermann反应合成对羟基苯甲醛的发展建议
以改进后的Gattermann反应制备对羟基苯甲醛,不再局限于无水三氯化铝路易斯酸催化剂,这种研制工作无论在理论上,还是实际应用上都有重要意义。改进过程有几个方面的问题需要解决。(1)催化剂体系的改进:固体超强酸技术,尤其树脂负载的固体超强酸技术的引入有可能突破现有路易斯酸催化方法;(2)溶剂回收过程的安全措施是工程化过程务必解决的难题,因为反应体系分相完成后的溶剂中会残留一定的HCN,需要进行必要的消除处理。
从节约资源和减少污染源的观点来重新审视设计改造传统化学,期望实现化学工业的环境、经济和社会的和谐发展,符合绿色化学研究的理念。

