舒芬太尼联合普瑞巴林和羟考酮治疗晚期胰腺癌的临床效果
赵新华 夏 晶
胰腺癌约有90%起源于腺管上皮的导管腺癌,是恶性程度极高、预后极差的消化道恶性肿瘤之一,患病后5 年内生存率不足1%,临床诊断和治疗难度较大[1]。由于早期确诊率不高,患者接受正规治疗时往往已进入中晚期阶段,手术死亡率较高而治愈率很低[2]。据统计,胰腺癌男性患者与女性比例为(1.5 ~2):1,而绝经后女性发病率与男性较为相近[3]。胰腺癌变灶解剖学位置隐匿特殊,尤其容易侵害周围组织和神经,故患者常伴发神经病理性疼痛和感受性疼痛,病程进入晚期时疼痛加剧,患者生存质量急剧下降[4]。阿片类药物是临床常用止痛药,成分主要为从阿片中提取的生物碱及体内外衍生物,可与中枢特异性受体相互作用,从而有效缓解疼痛[5]。在癌痛治疗中,患者往往会对一种阿片类药物产生耐受性,导致药物效果欠佳。研究发现,联合抗惊厥或抗抑郁药物有助于提高癌痛控制效果,本研究选取102 例晚期胰腺癌患者,旨在探讨舒芬太尼联合普瑞巴林和羟考酮的应用效果和价值,报告如下。
1.资料与方法
1.1 一般资料 研究对象为2015 年5 月至2019 年10 月于本院住院治疗的晚期胰腺癌患者,共计102 例。纳入标准:年龄≥60岁;临床经病理组织学检验确诊胰腺癌;符合TNM 分期Ⅲ~Ⅳ期[6];预计生存时间≥6 个月;疼痛VAS 评分≥6分;精神意识正常,可正确表述主观感受;签署研究知情同意书。排除标准:对研究药物不适用者;合并其他原因引起的疼痛。根据止痛方法对患者进行分组对照研究,A 组32 例,给予单纯羟考酮止痛;B 组34 例,给予普瑞巴林联合羟考酮止痛;C组36例,给予舒芬太尼联合普瑞巴林和羟考酮止痛。A组中男性17例、女性15例,平均年龄(67.8 ±4.3)岁,Ⅲ期18例、Ⅳ期14 例;B 组中男性19 例、女性15 例,平均年龄(68.1 ±4.5)岁,Ⅲ期19例、Ⅳ期15 例;C组中男性21 例、女性15 例,平均年龄(68.3 ±4.2)岁,Ⅲ期22 例、Ⅳ期14 例。上述资料差异无统计学意义,具有可比性(P >0.05)。研究获伦理委员会审批。
1.2 研究方法
1.2.1 A组给予单纯羟考酮止痛:口服盐酸羟考酮缓释片[奥施康定,萌蒂(中国)制药有限公司,批准文号J20140125,规格10mg],初始剂量10mg,每隔12小时服用1次;根据患者实际病情严格控制后续滴定剂量,以达到理想止痛效果。
1.2.2 B组给予普瑞巴林联合羟考酮止痛:在A组基础上加用普瑞巴林胶囊(乐瑞卡,美国辉瑞制药公司,批准文号J20160021,规格75mg),初始剂量75mg,第1 ~3天每隔12 小时服用1次;第4 ~7 天剂量调整为150mg;患者不可耐受时酌情减量。
1.2.3 C组给予舒芬太尼联合普瑞巴林和羟考酮止痛:普瑞巴林和羟考酮用药同B组,并行持续泵注枸橼酸舒芬太尼注射液(宜昌人福药业有限责任公司,批准文号H20054171,规格1ml:50μg),电子泵注入2.5μg 为负荷剂量,泵中浓度1.0μg/ml,采用滴定法逐步调整单位时间内给药量,出现不耐受不良反应或止痛效果理想时保持维持剂量。
1.2.4 三组患者住院期间发生爆发痛可根据具体情况即时皮下注射吗啡注射液。
1.3 评价指标 ①采用EORTC QLQ-C30量表分别评估三组患者治疗前后生活质量[7],包括角色功能、躯体功能、社会功能、疲乏、整体生活质量5 个方面,评分越高说明生活质量越好。②采用疼痛视觉模拟评分法(VAS 评分)评估患者治疗前、治疗7天、14天、30天全天最剧烈癌痛程度[8],0 ~10 分,分值越高说明疼痛程度越严重。③比较治疗前后各组患者每日吗啡使用量。④记录治疗期间药物不良反应情况,包括头晕、口干、便秘、恶心、嗜睡,统计总发生率。
1.4 统计学方法 研究所得数据均由SPSS 20.0 软件处理,计 量资料用(±s)表示,计数资料用百分率表示,分别采用t、χ2检验,三组间比较用F 检验。P <0.05 时差异有统计学意义。
2.结果
2.1 三组患者治疗前后VAS评分变化 见表1。治疗前,三组VAS评分差异不大(P >0.05);治疗后7 天、14 天、30 天,各组评分逐渐降低,C 组优于B 组、A 组,组间差异有明显统计学意义(P <0.05)。

表1 治疗前后三组患者VAS评分变化单位:分
2.2 三组患者治疗前后生活质量变化 见表2。治疗前,三组生活质量各项评分差异无统计学意义(P >0.05);治疗后,三组间比较有显著差异(P <0.05)。
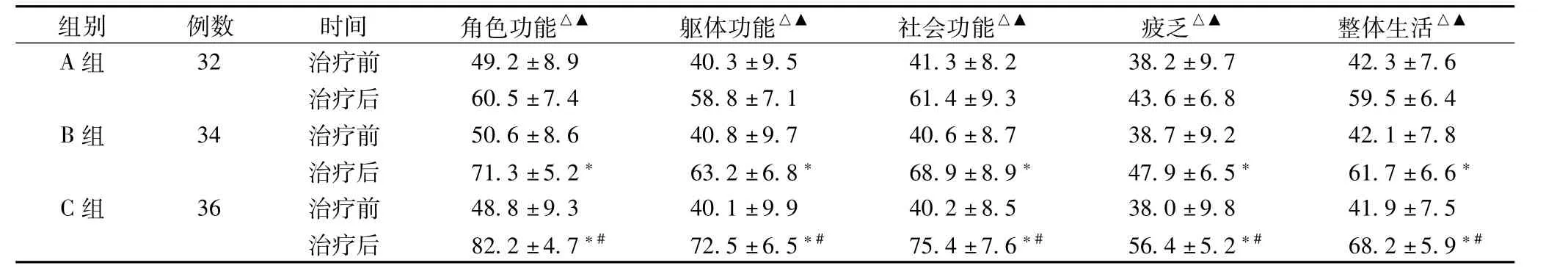
表2 治疗前后三组患者生活质量变化 单位:分
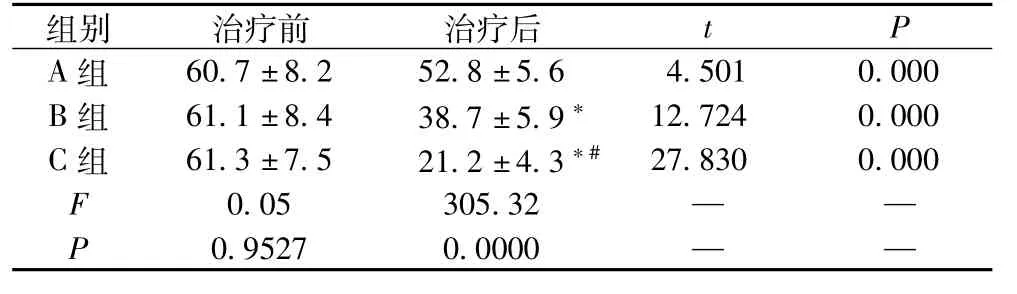
表3 治疗前后三组患者吗啡使用情况 单位:mg/d
2.3 三组患者治疗前后吗啡使用情况 见表3。相较于治疗前,C组患者每日吗啡使用量显著降低,且低于B 组和A组,差异有统计学意义(P <0.05)。
2.4 三组治疗期间不良反应发生率比较 见表4。C组各种不良反应总发生率低于其他两组,组间差异存在统计学意义(P <0.05)。
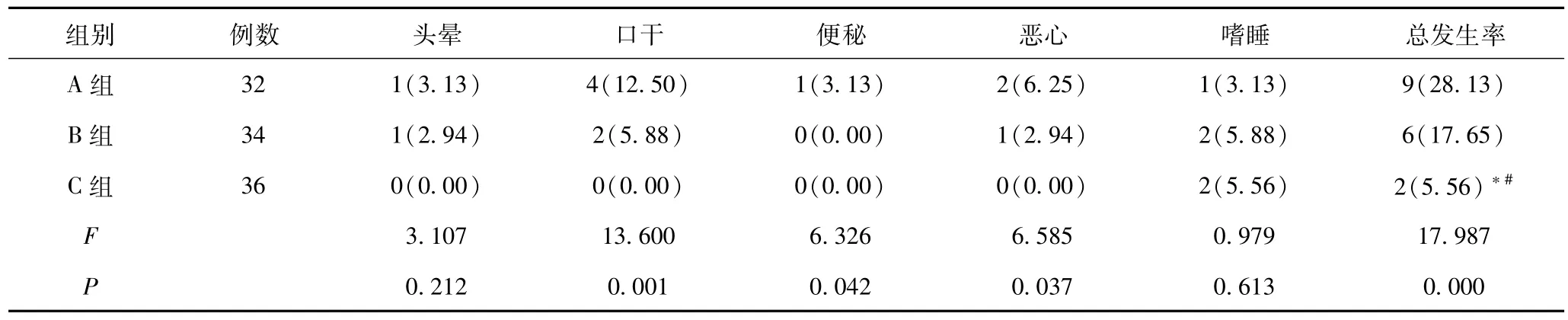
表4 治疗期间三组不良反应发生率比较 单位:例(%)
3.讨论
胰腺癌是高度恶性肿瘤之一,具体病因尚不完全明确,一般认为吸烟、饮酒、过量饮用咖啡、环境污染、遗传基因、高脂肪和高蛋白饮食等因素均与之有一定关联[9]。既往研究中表明,糖尿病患者发生胰腺癌概率明显高于普通人群,而慢性胰腺炎患者也有较高风险发展成为胰腺癌[10]。胰腺癌的病灶位置、病情进展以及邻近器官受损程度在一定程度上决定了患者临床表现,常见的症状有上腹部饱胀不适和疼痛,部分早期患者存在自觉痛但无压痛感[11]。癌灶入侵内脏包膜、腹膜或腹膜后组织时,可产生明显压痛。晚期胰腺癌患者癌痛剧烈且难以控制,对于机体功能减退、痛阈下降、疼痛敏化人群,尤其是老年患者来说,常因顾虑药物副作用和疼痛控制效果不佳而畏惧治疗,甚至产生自杀念头[12]。根据病理解剖位置,胰腺癌灶极易累及周围组织和神经,从而形成感受与神经病理混合性疼痛,也是造成癌痛的主要原因,积极控制癌痛是临床改善胰腺癌住院患者病情的首要任务。
羟考酮是一种具有强效镇痛效果的半合成阿片类药物,生物利用度高,给药途径多,在临床中应用广泛[13]。其药理机制与吗啡相似,主要是通过激动中枢神经系统内的阿片受体作用起到镇痛效果,但实践表明连续使用高剂量羟考酮后中断药物或减量可导致戒断综合征,提示本品与其他阿片类药物一样存在常见不良反应[14]。晚期胰腺癌神经病理性疼痛机制复杂,止痛仍以口服药物为主。成人癌痛指南提出联合抗惊厥或抗抑郁药物可作为神经病理性疼痛一线治疗方式。普瑞巴林是抗惊厥药物,是一种新型的神经递质γ-氨基丁酸类似物,在外周神经系统发生作用,可阻断钙通道,减少兴奋性神经递质释放,从而对神经元兴奋性产生抑制,起到控制疼痛和疼痛敏化效果。普瑞巴林联合羟考酮使用药物副作用有所叠加,因此患者对用药多持犹豫态度,临床推广存在一定难度。
舒芬太尼临床用作镇痛药,亲脂性是芬太尼的2 倍左右,作用于μ阿片受体,更容易通过血脑屏障与血浆蛋白结合。本品通过静脉泵注快速吸收后,在蛛网膜间隙与脊髓背角阿片μ1受体高选择性结合,同时干预中枢神经系统及外周神经系统的痛觉敏化,减少爆发痛次数和强度,经过肝内生物转化,舒芬太尼能够形成N-去烃基、O-去甲基代谢物,由肾脏代谢排出。学者杨影[15]等人研究普瑞巴林联合羟考酮与单纯羟考酮在老年晚期胰腺癌治疗中的止痛效果,发现联合用药优于单纯羟考酮组,普瑞巴林的应用对疼痛控制迅速有效,还有利于减少阿片类药物剂量。本研究在此基础上比较单纯羟考酮、普瑞巴林联合羟考酮以及舒芬太尼联合普瑞巴林和羟考酮3种用药方式对晚期胰腺癌的止痛效果,结果发现C 组患者VAS评分显著降低,且低于B组、A组,患者生活质量明显提高,提示舒芬太尼联合普瑞巴林和羟考酮效果更为理想;与治疗前比较,C组每日吗啡使用量降低,不良反应发生率也远远低于其他两组,表明本组治疗方式临床具有良好的安全性。
综上所述,舒芬太尼联合普瑞巴林和羟考酮对改善晚期胰腺癌患者疼痛、提高生活质量效果显著,有助于减少吗啡使用量,降低不良反应发生率,值得推广应用。

