CT模拟机及模拟定位机在颅内肿瘤调强放射治疗靶区勾画与计划制定中的应用*
1.湖北省恩施土家族苗族自治州中心医院肿瘤放疗中心(湖北 恩施 445000)
2.湖北民族学院附属民大医院放射科 (湖北 恩施 445000)
刘红艳1 鲁启洪1 陈佳权1廖明全2
近年来,随着医学影像技术和计算机技术的飞速发展,调强放射治疗(intensity modulated radiotherapy,IMRT)、三维适形放疗已成为当下肿瘤放射治疗的主流[1]。IMRT计划靶区内高剂量分布均匀,靶区边缘的剂量梯度差衰减更快,为更准确地勾画肿瘤靶区形状和周围正常组织、器官的轮廓,这就对精确的模拟定位方法有更高的要求[2]。与传统X线模拟定位相比,CT模拟定位能更精确划分肿瘤边界和周围相关组织、器官的图像,可在不增加正常组织照射量的同时,提高肿瘤靶区的有效放射剂量,提高放疗增益比,凭借这些优势CT模拟定位成为肿瘤精确放疗的首选[3-4]。选择2018年1月至2018年12月110例颅内肿瘤患者应用CT模拟机及X线模拟定位机进行IMRT模拟定位,现报告如下。
1 资料与方法
1.1 一般资料 选择2018年1月至2018年12月行IMRT的110例颅内肿瘤患者为研究对象,采用随机数字表法,将110例患者分为CT组和X线组,各55例,观察组行CT模拟机IMRT,对照组行模拟定位机IMRT。CT组男性32例,女性23例;年龄19~75岁,中位年龄56岁;颅脑内原发肿瘤21例,肺癌脑转移20例,其部位转移性脑瘤14例;有明显临床症状36例,主要表现为恶心、呕吐、头晕、头痛、肢体障碍、记忆力下降等。X线组男性31例,女性24例;年龄20~75岁,中位年龄55岁;颅脑内原发肿瘤23例,肺癌脑转移21例,其部位转移性脑瘤11例;有明显临床症状35例,临床表现与观察组一致。两组性别、年龄、肿瘤类型、临床症状比较,差异无统计学意义(P>0.05),所有患者均签署知情同意书。
1.2 方法
1.2.1 设备:BrightSpeed Elite Select 16排多功能CT(美国GE公司),UNIQE型6M直线加速器(美国瓦里安公司),山东新华SL-ID模拟定位机(山东新华医疗器械股份有限公司),WDM放射治疗模拟机(广东威达集团股份有限公司),Eclipse三维治疗计划系统。
1.2.2 影像定位:①CT定位:采用16排多功能CT,患者仰卧在定位床上,选择合适的头模、面模,达到固定患者头面部和器官的目的,采用三维可移动激光灯系统和定位刻度板确定摆位点,并告知患者操作流程,扫面期间禁动,扫描前在肿瘤部位中心体表用铅粒标记“+”的体表参考标记,采用高压注射器经肘静脉注射碘海醇(100mL/30g,国药准字H10970358,扬子江药业集团有限公司)进行增强扫描。
②模拟定位机定位:采用山东新华SL-ID模拟定位机,患者平卧于定位床,头模、面模的选择及体表参考标记同CT定位,采用三维固定激光灯,通过移动定位床和调整患者头部位置让三维“+”标记对准激光灯的十字中心。
1.2.3 靶区勾画:所有患者均行横断面、冠状面、矢状面扫描,将CT扫描图像和X线扫描图像传输至工作站,进行CT三维图像重建,由2名经验丰富的医师共同阅片,记录肿瘤病变部位和数目,勾画病灶感兴趣区(ROI),逐层勾画靶区及周围脏器的轮廓,靶区包括大体肿瘤体积(GTV)和临床靶区体积(CTV)。
1.2.4 计划制定:将勾画好的靶区轮廓、定位影像资料传输至Eclipse三维治疗计划系统,选择头部为治疗部位,显示CT三维图像,选择合适的CT中心和治疗时的摆位点,生成45°数字化重建X射线摄影图像(DRR),制定治疗计划,选择大小合适的准直器优化计算,DRR图像经网络传输至位置验证系统,测量X、Y、Z轴三个方向上的偏差,进行修正,以±1mm为位置验证合格的标准,重新标记治疗点,选择90%以上包围靶区的剂量作为治疗总剂量,采用3~5次的分割方式,行4~21次分次治疗,单次剂量为2.5~8Gy,兼顾射束数量和总跳数,经主管医师确认后方可进行治疗。
1.3 统计学分析 所有数据输入SPSS20.0软件进行统计学分析,连续型资料以()表示,组间比较行独立样本t检验;分类资料以[n(%)]表示,组间比较行χ2检验,等级资料采用非参数Mann-Whitney U检验,P<0.05表示差异有统计学意义。
2 结 果
2.1 两组GTV、CTV比较 通过CT模拟机、X线模拟定位机定位扫描,CT组GTV、CTV均高于X线组(P<0.05)。见表1。
2.2 两组三维方向上复位误差比较 两组三维方向上的复位误差分为Ea(≤±1mm)、Eb(在±1mm和±2mm之间)、Ec(>±2mm)三个等级,两组Y轴方向上的等级误差有显著差异(P<0.05),X轴和Z轴方向上的等级误差无显著差异(P>0.05)。见表2。
2.3 两组三维方向上平均误差比较 X线组Y轴方向上平均误差大于CT组,(P<0.05),两组X轴和Z轴方向上平均误差无显著差异(P>0.05)。见表3。
2.4 两组治疗计划制定比较在制定治疗计划中,由于X线组GTV、CTV低于CT组,选择靶区制定IMRT计划,会导致肿瘤边缘低剂量,X线组Y轴方向上平均误差大于CT组,但两组复位平均误差都小于2mm,GTV一般会外放2mm,以减少靶区边界的不确定性。
3 讨 论
颅内肿瘤部分为多发,且因病灶部位的特殊性致使手术难以彻底切除,甚至无法手术,放射治疗常作为颅内恶性肿瘤的首选治疗方法,但颅内肿瘤大多对放射治疗的敏感性较差,又受肿瘤形状、周围脑组织等的影响,因而常规放射治疗的疗效较差[5]。目前,肿瘤放射治疗已进入“三精”时代,如何充分应用现有的计算机技术和医疗设备来提高放疗的精确度是当下的研究热点之一[6-7]。IMRT开创了精准放疗的新纪元,它可根据肿瘤的三维形状调节辐射强度,使靶区内和靶表面的剂量分布均匀,从而实现对肿瘤组织的高剂量放疗,并良好地保护了周围正常组织和器官,降低局部复发率,延长患者生存期[8]。对肿瘤靶区的准确勾画是IMRT计划的重要前提,因而准确定位显得尤为重要[9]。
表1 两组GTV、CTV比较

表1 两组GTV、CTV比较
组别 n GTV CTV CT组 55 29.66±2.83 200.36±7.95 X线组 55 28.19±2.41 190.11±6.34 t值 2.933 7.476 P值 0.004 0.000
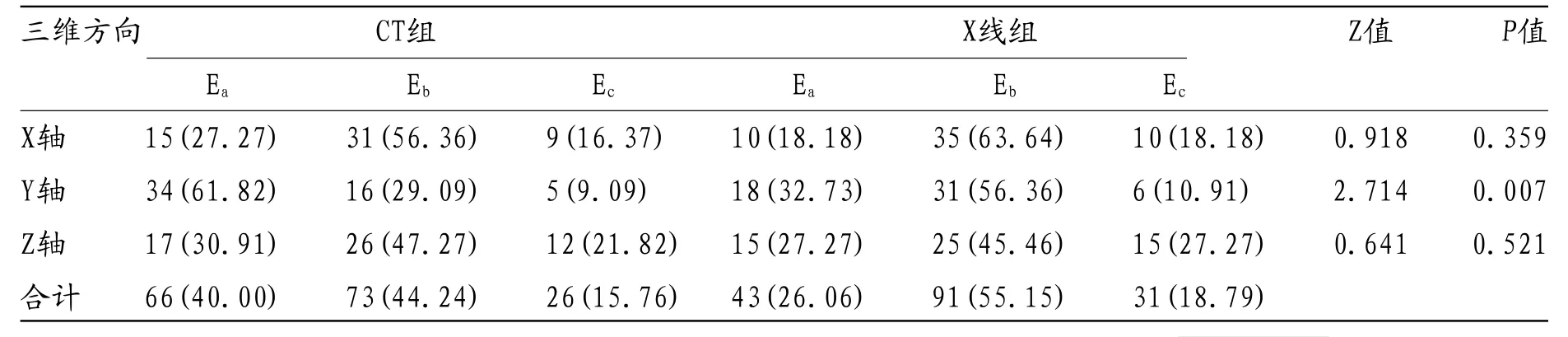
表2 两组三维方向上复位误差比较[n(%)]
表3 两组三维方向上平均误差比较

表3 两组三维方向上平均误差比较
组别 n X轴 Y轴 Z轴CT组 55 1.42±0.44 0.76±0.23 1.53±0.47 X线组 55 1.49±0.46 1.28±0.37 1.61±0.49 t值 0.816 8.852 0.874 P值 0.417 0.000 0.384
相对于传统X线定位而言,CT模拟定位技术具有以下优势:①具有较高的组织对比度、优质的软组织分辨率、极高的空间准确性,能非常客观地反映人体各个部分组织器官相对应的电子密度,在相同辐射剂量下得到的图像更优质,其定位精度大大优于传统X线模拟定位机[10-11]。②CT模拟定位机的显示野更大,对颅内组织的显示优于传统X线模拟定位机,对IMRT计划制定也更有利[12]。③CT模拟定位机扫描速度快,增加扫描范围,使照射范围显示更直观、可靠,肿瘤靶区定位更准确,靶区勾画更精确,不均匀组织校正更为合理,剂量优化更精确,更有利于保护周围正常组织和器官,从而进一步提高肿瘤治疗增益比,有效控制患者的放疗不良反应[13]。靶区中心位置验证是IMRT计划实施前必不可少的环节,需将定位误差控制在容许范围内(±1mm),本研究结果显示,X线组Y轴方向上平均误差大于CT组,X先祖Y轴方向上误差大于±1mm的例数也明显多于CT组;证实CT模拟定位机定位更准确,靶区勾画精确度更高,与肖友立等[14]研究结果一致。
放疗的质量保证和质量控制是实现精确放疗的重要基础,在IMRT中,检查CT图像、X线图像的完整性,仪器的稳定性和精确性是非常有必要的。由于X线图像显示的肿瘤体积偏小,病灶周围组织区分不明显,医师怕遗漏瘤体,勾画的GTV偏大,会把一部分水肿区囊括进去,容易造成靶区勾画的不确定性,影响IMRT疗效。为保证颅内肿瘤的IMRT疗效,需进行位置验证、修正、重新标记治疗点,在IMRT靶区勾画与计划制定中,CT模拟定位机和X线模拟定位机各具优势,X线模拟定位机的低千伏透视图像具有较高空间分辨率,能清晰分辨各种重要骨性标志,有助于位置验证时匹配率的提高;CT模拟定位机能更直观对显示中心层面的高密度分辨率图像;两种定位方法都有助于提高IMRT设备的使用率和工作效率。
综上所述,CT模拟机及X线模拟定位机都适用于颅内肿瘤IMRT靶区勾画与计划制定,CT模拟机更有助于提高靶区勾画准确性,为IMRT计划制定提供可靠依据。

