不同碱性材料对酸性重金属污染土壤的钝化效果及其作用机理简析
周志威
(福建龙净环保股份有限公司,福建 龙岩 361000)
近年来,随着我国经济社会各项事业的持续快速发展,随之而产生的环境污染问题也日益凸显。
工业经济的快速发展,导致大量的工业废气如硫氧化物(SO2、SO3)、氮氧化物(NXOY)等的大量排放,导致我国酸雨及土壤酸化问题日益突出。我国南方地区土壤酸化问题尤其突出,据全国农用技术推广服务中心2015年公布的2015~2014全国测土配方施肥土壤基础养分数据显示,湖南(120县市区)、广西(104县市区)、浙江(74县市区)、广东(94县市区)、江西(91县市区)、福建(41县市区)六省农田土壤平均pH值低于5.5的县市区分别占29.2%、28.8%、41.9%、54.3%、92.3%和85.4%[1]。严重的土壤酸化作用,不仅会导致土壤肥力流失,作物减产,同时也会活化土壤重金属,间接的对人体产生危害。
电镀、矿冶、化工等行业废水中,含有大量的危害性重金属,代表性重金属品种包括铅(Pb)、镉(Cd)、汞(Hg)、砷(As)、铬(Cr)等,重金属不仅会影响到土壤植被、土壤动物、土壤养分等,还会伴随着粉尘、食物链等进入人体,对人体健康产生巨大危害。
在土壤重金属治理领域,碱性材料具有效果明显、价格低廉、施用方便等优势,在该领域应用非常广泛。从广义上来看,碱性材料品种繁多,除常见的氧化钙、氢氧化钙等材料外,还包括部分硫化物、碳酸盐、碳酸氢盐等,不同碱性材料化学结构、成分各异,对各种重金属的作用效果也存在较大差异。
按Tessier法进行分类,重金属污染土壤中的重金属的赋存形态包括可交换态、碳酸盐结合态、铁锰氧化态、有机结合态和残渣态5中,其中尤以可交换态最容易为植物所吸收,危害最大;其次为碳酸盐结合态和铁锰氧化态。污染土壤中重金属的赋存形态不是一成不变的,他们会随着土壤性质(氧化还原条件、pH值等)的变化而发生转换,在pH值较低的酸性环境下,碳酸盐结合态、铁锰氧化态重金属可转化为易为植物吸收的可交换态[2]。碱性材料的使用,不仅可调节土壤pH值,抑制土壤中可交换态重金属的形成,还可与土壤中的重金属形成残渣态化合物,达到稳定化土壤重金属、安全利用土壤的目的。
本文将具有一定代表性的碱性材料分别应用于重金属铅(Pb)、镉(Cd)污染的土壤中,研究了其对土壤中重金属铅、镉的钝化效果,并分析了它们的作用机理。
1 材料与方法
1.1 实验土壤
本研究所采用的实验土壤取自福建西部某由于铅锌矿采矿导致的污染耕地土壤。该土壤中的主要重金属污染物为铅(Pb)和镉(Cd)污染物。经分析检测,该土壤pH值为5.7(NY/T 1377-2007),铅镉有效态含量分别为220 mg/kg和3.42 mg/kg(检测方法:HJ 8014-2016),铅镉总量分别为1158 mg/kg和7.2 mg/kg(检测方法:CJ/T 221-2016)。
1.2 主要材料及规格
氢氧化钙(Ca(OH)2):分析纯,西陇科学股份有限公司;氧化钙(CaO):分析纯,西陇科学有限公司;碳酸钙(CaCO3):分析纯,西陇科学股份有限公司;方解石砂:碳酸钙含量≥95.0%,粒径100~120目;九水硫化钠(Na2S·9H2O):分析纯,西陇科学股份有限公司;硫化铁(硫化亚铁,FeS):化学纯,西陇科学股份有限公司;改性粉煤灰:自制,原料来源于某电厂粉煤灰,自改性。
1.3 实验方法
1.3.1 钝化材料应用实验方法
1.3.1.1 土壤处理
取土壤样品,置于阴凉通风处,摊开形成约1 mm厚度的薄层,定期翻动自然风干,采用四分法将风干后的土壤样品混合均匀。将混匀后的土壤样品过2 mm尼龙筛,取筛下物,而后手工细致的去除土壤中的草根、杂草、砂石、叶类等杂物。按要求做好标记,储藏于自封袋中备用。
1.3.1.2 应用实验
①应用实验样品制备:取250 mL玻璃烧杯若干,称取一定量的土壤样品(精确至0.1 g),置于玻璃烧杯中。按设计比例,向烧杯中加入一定比例的钝化实验材料。使用非金属材质的药勺将钝化实验材料与受试土壤混合均匀。向烧杯中加入一定质量的水,使土壤含水量达到田间饱和持水量的40%,将土壤、钝化材料、水混合均匀,以具孔塑料薄膜封口,放置于阴凉、通风、干燥处。
②应用实验样品维护:需每日对样品进行称重,以评估其水分流失状况。当土壤样品中水分流失率≥5%时,需对样品进行补水操作,即加入与损失量同等质量的水分以保持土壤水分,并按要求将样品/水分再次混匀,完成后继续进行保养维护。
样品维护保养时间到达预定的实验周期后,需从烧杯中取出一定质量土样,置于阴凉干燥处进行自然风干,取样送检,通过考察土壤中对应重金属的有效态含量值变化趋势及土壤状态等其它指标,对钝化材料的钝化性能进行综合评估。
③为保证数据的准确可靠性,同期进行空白实验和平行对照实验。
1.3.2 粉煤灰改性方法
粉煤灰是燃煤后所残留下来的工业废弃物,的主要成分包括二氧化硅(SiO2)、氧化铝(Al2O3)、氧化钙(CaO)等,在水存在的情况下呈现碱性。同时,粉煤灰也是一种多孔性物质,比表面积大,对土壤重金属具有一定的吸附性能[4-5]。
本研究采用碱(30%的NaOH溶液)改性法对粉煤灰进行改性,改性完成后,在150℃的条件下进行干燥。采用改性粉煤灰作为碱性化学材料的对照,以明确(碱性)工业固废多孔材料对比传统化学类碱性钝化材料的优势和不足。
1.3.3 土壤pH测定方法
土壤pH变化趋势是考察碱性钝化材料使用性能的重要指标之一,pH值太高(≥8.5),会导致土壤盐碱化,不适于作物生长[3]。
土壤pH测定参考中国农业行业标准标准,标准号NY/T 1377-2007 《土壤pH的测定》。
称取(10±0.1) g处理后的风干土壤,置于50 mL的高脚烧杯中,向烧杯中加入25 mL的水,密封烧杯,剧烈搅拌5 min,而后静置2 h,测定上层清液pH值,即为土壤pH值。
2 结果与分析
2.1 不同碱性材料对酸性重金属铅、镉污染土壤的钝化效果
2.1.1 材料与用量
为考察不同碱性材料对重金属铅、镉的钝化性能,选取氧化钙、氢氧化钙、碳酸钙、方解石粉、九水硫化钠、粉煤灰、改性粉煤灰7种碱性材料,按上文所述方法,考察其对土壤中有效态重金属铅、镉的钝化效果。
考察周期:3、7、15、30 d。
材料用量(相对土壤干重的质量百分比):九水硫化钠3.0%(纯硫化钠0.98%),氧化钙(3.80%),其它材料5.0%。
2.1.2 对土壤pH值的影响
土壤养护30天,考察土壤pH值,其结果如图1所示。
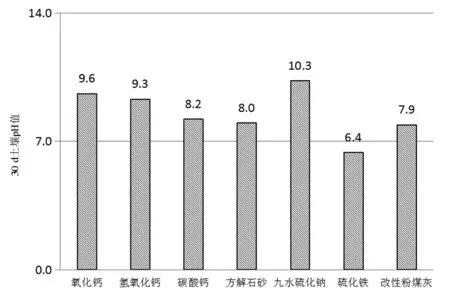
图1 碱性材料对土壤pH值的影响
由图1可知,各种碱性材料均会一定程度上提高土壤的pH值。其中以硫化钠对土壤pH值影响最大,在3.0%(九水硫化钠用量)的情况下,土壤pH值就已提高至10.3,同时导致土壤出现较为严重的板结,并持续释放出臭鸡蛋味的有毒硫化氢气体,对土壤副作用影响最为明显。
Na2S+H2O→Na++OH-+S2-+H2S↑
在前述用量下,氧化钙、氢氧化钙、硫化钠材料对应的土壤pH值都高于8.5,会导致土壤出现一定程度的盐碱化。氧化钙、氢氧化钙在实际应用中需减少用量,硫化钠材料由于副作用太大,实际应用过程中不推荐直接使用;碳酸钙类材料(包括方解石砂)、硫化铁、改性粉煤灰作用温和,对土壤pH值提升有一定作用,副作用较小。
2.1.3 碱性材料对土壤中重金属铅(Pb)、镉(Cd)的钝化效果
以上文1.3.1中应用实验方法,考察碱性材料对重金属铅、镉污染土壤的钝化效果。不同验证周期下,各材料(使用量5.0%)对重金属镉(Cd)的钝化效果如图2所示。
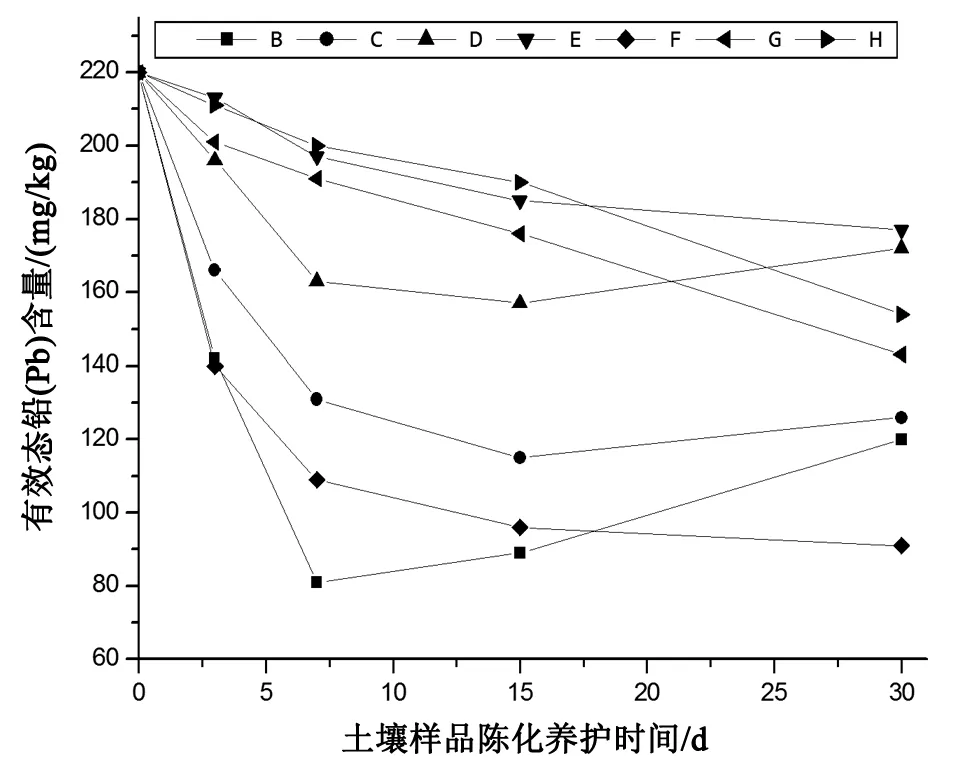
B 氧化钙;C 氢氧化钙;D 碳酸钙;E 方解石砂;F 九水硫化钠;G 硫化铁;H 改性粉煤灰图2 各碱性材料对土壤重金属铅(Pb)的钝化作用
钝化效果以不同考察周期下土壤中重金属有效态的降低率为衡量依据,如下式所示:
R=[(ω1-ω2)/ω1]×100%
其中 R:降低率,%;
ω1:钝化处理前土壤重金属有效态含量,mg/kg;
ω2:钝化处理后土壤重金属有效态含量,mg/kg。
2.1.3.1 碱性材料对土壤中铅的钝化效果
不同验证周期下,重金属污染土壤中重金属铅、镉有效态含量的变化趋势如图2所示。
由图2可知,碱性材料的应用,使得污染土壤中重金属铅(Pb)的有效态含量发生了较为明显的降低。
①九水硫化钠对土壤中重金属铅(Pb)的钝化效果最为明显,用量仅为3%的九水硫化钠(硫化钠含量约为0.975%)30 d使污染土壤中的重金属铅有效态含量由220 mg/kg降至91 mg/kg,降低率R达58.6%。
②5%的氧化钙对土壤重金属铅(Pb)的钝化效果最为明显,第7天,土壤中重金属铅(Pb)的有效态含量降低率由220 mg/kg降至81 mg/kg,降低率R达63.2%,但随着陈化时间的延长,有效态含量有所提高,30 d时升至120 mg/kg;氢氧化钙也存在同样的问题。
③硫化钠对土壤重金属铅(Pb)的钝化时效性明显强于氧化钙、氢氧化钙。
④改性粉煤灰材料对土壤重金属铅(Pb)的钝化速度较慢,需要较长的养护时间。
2.1.3.2 碱性材料对土壤中重金属镉(Cd)的钝化效果
由图3可知,碱性材料对污染土壤中重金属镉(Cd)也具有明显的钝化作用:
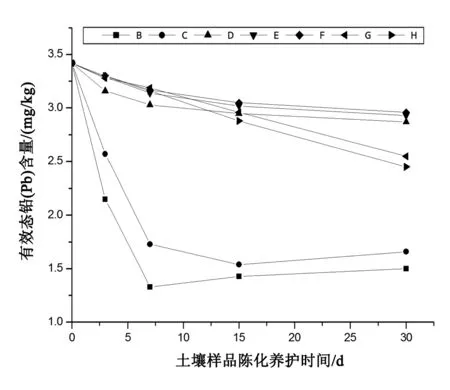
B 氧化钙;C 氢氧化钙;D 碳酸钙;E 方解石砂;F 九水硫化钠;G 硫化铁;H 改性粉煤灰图3 各碱性材料对土壤重金属镉(Cd)的钝化作用
① 5%的氧化钙对土壤重金属镉(Cd)的钝化效果最为明显,第7天,土壤中重金属镉(Cd)的有效态含量由3.42 mg/kg降至1.33 mg/kg,降低率R达61.1%,但随着陈化时间的延长,有效态含量有所提高,30 d时升至1.5 mg/kg,降低率累计升高达5%;氢氧化钙也存在这同样的问题。
②改性粉煤灰材料对土壤重金属镉(Cd)的钝化速度较慢,在30 d内能稳定的降低污染土壤中有效态重金属镉(Cd)的含量。
2.2 小结
由以上实验结果可知,不同类型的碱性材料均能在一定程度上降低酸性土壤中重金属铅(Pb)和镉(Cd)的有效态含量,但不同材料的性能特点也各不相同。
(1)氧化钙(CaO)和氢氧化钙(Ca(OH)2)。传统碱性材料氧化钙、氢氧化钙均能较为高效的调节酸性土壤的pH值,同时也能有效降低土壤中重金属铅(Pb)、镉(Cd)有效态含量,但其同时也具有作用周期较短的缺点,7 d后土壤中重金属铅(Pb)、镉(Cd)有效态含量均出现了反弹,主要机理可能在于:这两种材料均可通过提高土壤pH值的方法使土壤中的大部分游离态重金属铅(Pb)、镉(Cd)生成了碱式沉淀而发生一定程度上的稳定化,但这种物质极易受到环境变化因素的影响(降水、酸性物质等),而发生再次溶出。
氧化钙在土壤中发生如下反应:
CaO+H2O→Ca(OH)2
导致二者在应用性能上存在一定差异,氧化钙吸收土壤中已有水分(包括其中所含有的游离态重金属),短期效果更好,长期来看,二者效果趋向一致。同时,也需考虑由于氧化钙溶解放热而导致的对土壤环境的负面影响。
(2)硫化钠。硫化钠材料在短期内就能较快的降低土壤中重金属铅(Pb)的有效态含量,30d内并未出现反弹的趋势,在于其能与土壤中的重金属铅(Pb)形成较为稳定的硫化物等重金属残渣态物质[6]。但其对重金属镉(Cd)钝化效果一般。
硫化钠材料在使用过程中会释放出有害物质硫化氢,同时会造成土壤较为严重的板结,副作用明显,在土壤领域的使用需要慎重。
(3)难溶性弱碱性材料。本研究所使用的难溶性碱性材料包括碳酸钙、方解石砂、硫化铁。方解石砂的主要成分也是碳酸钙,应用结果表明,随着粒径的增加,碳酸钙类难溶性碱性材料的缓释时间有所延长。从碳酸钙的使用效果来看,7 d时,碳酸钙对有效态铅(Pb)的降低率达25.9%,30 d则该值则降低至21.8%。由此可见,30 d中,碳酸钙活化的土壤有效态铅发生了再溶出现象。对镉则没有出现这种现象。
(4)改性后的粉煤灰也具有明显的重金属钝化效果。其重金属钝化效果由于碳酸钙、方解石砂和硫化铁。粉煤灰对土壤重金属钝化的机理不仅在于其对土壤pH值得提高,同时也在于其内在的多孔结构及表面丰富的基团,对土壤重金属存在吸附作用。
(5)对土壤pH值及土壤环境的影响:各种碱性材料对土壤pH影响的大小依次为:硫化钠、氧化钙、氢氧化钙、碳酸钙、方解石砂、改性粉煤灰和硫化铁。硫化钠对土壤pH影响很大,同时会导致土壤板结等问题;氧化钙、氢氧化钙类材料对土壤环境有一定影响;其它材料则对酸化土壤的pH存在着较为温和的提升,粉煤灰对土壤板结的影响程度明显小于其它化学材料。
3 结论
由以上研究可以得出以下结论:
(1)碱性材料均可以在一定程度上改善酸性土壤pH值,降低土壤中有效态重金属铅(Pb)、镉(Cd)的有效态含量,传统的碱性材料氧化钙、氢氧化钙效果明显,但存在着明显的钝化重金属再次溶出问题;
(2)易溶性硫化物类碱性材料,如硫化钠对部分土壤重金属的稳定持久性明显优于氧化钙类材料,但由于其较为活跃的化学反应性,在使用中仍存在明显短板。
(3)缓溶性碱性材料,如本研究中使用的碳酸钙类、硫化铁材料,对土壤pH值等影响平缓,但钝化效果不如氧化钙材料,可用于污染程度较轻的土壤钝化改良。
(4)粉煤灰类多孔工业固废材料,价格低廉,在提高酸性土壤pH值的同时,其具备的多孔结构还能在一定程度上对重金属产生吸附作用,同时对土壤产生的负面影响远低于化学类材料,具有较为广泛的应用前景。但需要注意其自身所含有的有害物质,避免二次污染。

