微创Ivor-Lewis食管切除术与Sweet手术治疗Siewert Ⅱ型食管胃结合部腺癌的前瞻性对比研究*
李国雷 王保华 李 忠 王占文 闫红江 马晓钰 张占学
(河北医科大学第二医院胸外科,石家庄 050000)
Siewert等[1]将食管胃结合部腺癌(adenocarcinoma of esophagogastric junction,AEG)按肿瘤中心的解剖位置分为3型:肿瘤中心位于齿状线上方1~5 cm为Ⅰ型;位于齿状线以上1 cm和齿状线以下2 cm之间为Ⅱ型;位于齿状线下方2~5 cm为Ⅲ型。Siewert Ⅱ型是实际意义上的贲门癌,近年来发病率呈明显上升趋势[2,3]。2019年美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)食管癌与食管胃结合部癌临床实践指南指出SiewertⅠ型、Ⅱ型肿瘤的分期及治疗按照食管癌指南执行,Ⅲ型归入胃癌指南[4]。这为选择合适的手术入路提供了参考,但即便如此,对于Siewert Ⅱ型AEG的手术争议仍然较多。胸外科学者对于Siewert Ⅱ型AEG多采用经左胸手术(Sweet手术)[5,6]。Ivor-Lewis手术是经右胸入路治疗胸下段食管癌的常用方式,可获得更广泛的胸腹淋巴结清扫,但由于其需要胸腹两切口,创伤相对较大[7]。微创Ivor-Lewis手术(minimally invasive Ivor-Lewis esophagectomy,MI-ILE)采用腹腔镜与胸腔镜联合手术。我们设计前瞻性研究,比较MI-ILE与传统Sweet术式治疗Siewert Ⅱ型AEG的效果,以期为临床提供更多参考。
1 对象与方法
1.1 研究对象
本研究经河北医科大学第二医院科研伦理委员会审批(2017-R195)。选择2017年12月~2019年3月Siewert Ⅱ型AEG 82例,详细解释两种手术方式利弊后按照患者意愿行MI-ILE手术或Sweet手术各41例。
入组标准:①术前经胃镜及活检病理、上消化道造影、胸及上腹增强CT确诊为Siewert Ⅱ型AEG;②无手术禁忌证;③术前临床分期≤Ⅲ期[8]且拒绝术前新辅助治疗。
排除标准:有手术禁忌或只能行姑息手术(如存在其他脏器转移预期寿命较短);合并其他脏器肿瘤。
2组术前一般资料差异无显著性(P>0.05),具有可比性,见表1。

表1 2组一般资料比较(n=41)
1.2 手术方法
1.2.1 MI-ILE ①平卧位行腹腔镜操作:五孔法(呈V字形),游离胃及清扫腹腔淋巴结均按照《腹腔镜胃癌手术操作指南(2016版)》进行[9],小弯侧保证4 cm下切缘基础上,以直线切割闭合器制作管状胃,管状胃的宽度为3~5 cm,接近贲门时保留3 cm宽度不再继续切割,保持食管与管状胃的连接,保留部分为胃小囊,以利于胸部吻合时圆形吻合器体部置入。适当打开食管裂孔,清扫腹段食管及食管裂孔周围脂肪淋巴组织。②改左侧卧位行胸腔镜操作:主操作孔位于腋后线第6肋间(5~6 cm,采用切口保护套外套手套形式防止漏气),辅助操作孔分别为腋前线第4肋间和肩胛前缘第5肋间(均为1 cm),左肺通气,制造人工气胸(6~8 mm Hg)。常规游离食管至安全距离,根据实际情况清扫105、106tbL、106recL和106recR淋巴结,并清扫食管周围、支气管和隆突下淋巴结(107~111站)。在胸腔内保证上切缘足够安全后离断食管,置入钉砧,利用保留的胃小囊置入吻合器体部,完成胸内食管和胃的端侧吻合。具体方法见我们先前的报道[10]。
1.2.2 左开胸Sweet手术 右侧卧位,经左胸第7肋间18~20 cm切口进胸,常规游离食管,清扫胸腔淋巴结。打开膈肌,游离胃,并清扫腹腔各站淋巴结。制作管胃,宽度与MI-ILE一致,使用圆型吻合器完成食管胃主动脉弓下吻合[11]。
为了使吻合更加确切,2种术式均用3-0可吸收缝线全层加固残胃闭合口及吻合口各6针,并行食管胃套叠减少术后反酸症状。
1.3 观察指标
比较2组手术时间、术中出血量(吸引器血量及纱布血量)、术后第1天胸腔引流量、胸腔引流时间(引流液清亮且<100 ml/d后拔除引流管)、术后排气时间、术后住院时间(进半流食后无不适即可出院),以及术后并发症(吻合口漏、切口感染、肺部感染、胃排空障碍、心律失常等)。比较2组淋巴结清扫数目、切除正常食管长度。术后随访1年,比较2组生存率和复发率(胃镜、胸腹增强CT诊断)。
所有原始数据均由双人盲态录入,定期核查,统计学分析均由非手术医生外的两人盲态下进行处理。
1.4 统计学方法
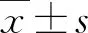
2 结果
2组82例均顺利完成手术,无围术期死亡,MI-ILE组无中转开放手术。2组观察指标比较见表2。与Sweet组相比,MI-ILE组手术时间长,但术中出血量、术后第1天胸腔引流量、胸腔引流时间、术后排气时间、术后住院时间均优于Sweet组。术后病理,MI-ILE组清扫淋巴结总数及胸腔、腹腔清扫淋巴结数均多于Sweet组,虽然2组胸、腹腔淋巴结转移数目差异无显著性,但MI-ILE组4例存在右上纵隔淋巴结转移(1例上纵隔淋巴转移,2例隆突下淋巴转移,1例右主支气管旁淋巴转移);切除正常食管长度MI-ILE组显著长于Sweet组。2组术后并发症发生率差异无显著性,2组并发症包括4例吻合口漏均保守治疗痊愈。术后随访1年,无失访,无死亡,2组复发率差异无显著性,MI-ILE组1例术后第8个月复发,Sweet组3例分别在术后第6、11、11个月复发。

表2 2组观察指标比较(n=41)
3 讨论
治疗Siewert Ⅱ型AEG的手术入路包括经左胸、经腹、经右胸及颈胸腹三切口手术[12]。研究表明经胸入路可以清扫更多的纵隔淋巴结,获得更安全的手术上切缘;经腹入路可以降低肺部并发症和术后持续胸痛的风险。随着手术技术的提高,经胸与经腹食管胃切除术在术后肺部并发症的发生率上已经无明显差异[13]。因此,对于大多数Siewert Ⅱ型AEG,胸外科医生将经胸食管胃切除术作为首选。经胸入路包括经左胸和右胸入路,主要根据肿瘤位置、大小、分期、淋巴结转移、术者经验决定。经左胸入路(Sweet术)是我国胸外科医生治疗Siewert Ⅱ型AEG的常用方法[14],但是对于右侧纵隔淋巴结以及腹腔淋巴结的清扫,该术式存在明显不足,而Ivor-Lewis手术能够弥补这些不足,也是实现胸腹淋巴结彻底清扫最有效的方法,但考虑到该术式需要胸腹两切口,相对经左胸一切口创伤较大,国内学者在治疗AEG时很少选择。随着微创技术的发展,MI-ILE手术已经是治疗食管下段癌的主流术式,创伤小,恢复快,效果好[15]。MI-ILE手术用于Siewert Ⅱ型AEG的效果如何,本研究进行了前瞻性非随机对照研究。
本研究结果显示,MI-ILE组手术时间虽然长于Sweet组,但术中出血量、术后排气时间、术后胸腔引流时间、术后住院时间均优于Sweet组,这也体现了微创手术的优势。而其手术时间延长的主要原因是微创操作相对繁琐,且需要术中翻身,也会耽误一定时间,但随着操作的不断熟练和流程的进一步优化,相信这种时间差距会不断缩短。在术后并发症方面,肺部并发症发生率为8.5%(7/82),其中MI-ILE组为4.9%(2/41),低于Sweet组的12.2%(5/41),但差异无显著性,可能是因为样本量较少。Zheng等[16]报道经胸手术肺部并发症的发生率为6%(17/286)。本研究2组吻合口漏均为2例,这与Blank等[17]报道的Ivor-Lewis手术与左开胸治疗AEG吻合口漏发生率相近。2组在术后心律失常、切口感染等方面差异均无显著性,提示MI-ILE较左开胸手术不会增加术后并发症,安全性较好。
临床上AEG发现时多为中晚期,淋巴结转移率高,本研究纳入的Siewert Ⅱ型AEG 82例中,术后病理分期Ⅱ期28例,Ⅲ期42例,其中腹腔淋巴结转移63例,胸部淋巴结转移34例。术中完整切除可疑转移淋巴结对术后准确分期和改善预后具有重要临床意义[18]。淋巴结转移和淋巴结清扫数目是影响Siewert Ⅱ型AEG长期生存的独立危险因素[19,20]。本研究中MI-ILE组总淋巴结清扫数目以及胸、腹腔淋巴结清扫数目均显著多于Sweet组,这也提示MI-ILE组淋巴结清扫更为彻底。我们体会AEG的贲门、胃小弯、胃左动脉淋巴结转移率较高,2种手术入路均能较好地清除这些区域的淋巴结,但MI-ILE对胃大弯、肝动脉、脾动脉、腹腔干淋巴结的清扫效果更好。许多文献[21~24]表明,对Siewert Ⅱ型AEG,清扫胃周各组淋巴结对于预后有积极意义,但是切除远端胃和清扫脾门淋巴结在预后上并没有很大价值,因此,对于Siewert Ⅱ型AEG,采取近端胃大部切除较全胃切除和进行扩大的淋巴结清扫已经能够很好地达到根治效果。
多项研究[21,25,26]表明Siewert Ⅱ型AEG的中下纵隔淋巴结转移较为常见,所以中下纵隔即食管中下段旁淋巴结的清扫对生存有显著益处。手术中我们体会MI-ILE和Sweet入路均可以很好地完成食管中下段旁淋巴结清扫。但在本研究中MI-ILE组1例上纵隔淋巴转移,2例隆突下淋巴转移,1例右主支气管旁淋巴转移。Okholm等[26]报道Siewert Ⅱ型AEG的上纵隔淋巴结转移率为4%,Parry等[27]报道为11%。因此,在Siewert Ⅱ型AEG的手术中,除对常见的淋巴转移部位进行清扫外,还需要对上述区域淋巴结进行评估和清扫,以保证根治性切除,而MI-ILE在这些区域的淋巴结清扫中具有显著优势。
此外,不能保证足够的上切缘食管切除长度是AEG复发的危险因素,但对于此类患者的手术上切缘安全距离仍存在争议[28]。Mine等[29]认为近端2 cm的手术切缘是安全的。Barbour等[30]报道T2期及以上AEG根治性切除应至少在病灶上5 cm离断食管和保证3.8 cm离体近端切缘才是安全的。在本研究中,MI-ILE组切除的近端食管长度平均5.1 cm,而Sweet组为4.0 cm。因此,MI-ILE可获得更满意的手术上切缘,对预防亚临床转移及改善预后有一定的临床价值。
综上,MI-ILE与传统的左胸入路Sweet手术相比,手术时间虽然延长,但减少术中失血,缩短术后胸腔引流时间及术后住院时间,不增加术后并发症发生率,可获得更为满意长度的近端切缘,在胸腹淋巴结清扫中优势明显,说明MI-ILE手术治疗Siewert Ⅱ型AEG是安全有效的。虽然1年生存率和复发率2组差异无显著性,可能限于样本量较少及术后随访时间较短,需待进一步验证。

