“双轮驱动”的创新型医疗器械产业服务新模式
——以中关村发展集团成员企业中关村水木医疗科技有限公司为例
蔡良圆,庄海,张金辉,王艳,刘贞,孙京昇(通信作者),贾一伟(通信作者)
中关村发展集团股份有限公司博士后科研工作站 (北京 100000)
医疗器械行业属于我国重点支持的战略新兴产业,涉及临床、机械、电子、电气、光学、核技术、材料等多学科,对人才知识的复合度要求较高,且发展前景广阔。2018年,我国医疗器械市场规模为5 304亿元,年增速超过20%,预计2019年医疗器械市场规模超过6 000亿[1]。与国际市场比较,我国医疗器械市场仍有极大的成长空间[2]。
为保证医疗器械使用的安全性和有效性,产品上市、生产销售等全过程均需由政府严格监管[3-4]。但是,我国的高端医疗器械市场存在被发达国家垄断的问题[5-6],在此背景下,深入挖掘医疗器械企业痛点、整合资源、建立全流程系统性的医疗器械服务平台就变得非常必要[7]。医疗器械服务平台不仅可为企业提供系统、便捷的整体服务,还可以通过资源协同降低服务公司的成本,提高运营效率和质量;此外,政府应充分利用自身的资源禀赋和公信力,在平台的搭建中发挥产业组织和引导的作用。本研究拟在医疗器械行业分析、痛点剖析的基础上,以中关村水木医疗科技有限公司为例,深入探讨构建医疗器械服务平台的新模式。
1 医疗器械商业化的“自行车理论”
医疗器械产品商业化的完整链条包括产品化和商品化(图1)两个阶段,所需经历的环节似自行车的“两个轮子”。企业的创始人为自行车的掌舵人,使用资金、人才和场地形成的“铁三角”,支撑上述产品化和商品化环节;但是,初创公司不可避免地面临资金、人才和场地匮乏的问题,导致对产品和商品化环节的把控能力较弱,极大地阻碍了创新型医疗器械产品的商业化进程。为了搭建全链条、系统性的产业服务平台,需要帮助企业打通“两个轮子”的各个环节,并帮助企业度过产品化和商品化的两个关键期。
在产品化阶段,企业通过功能性研发、工程化研发、动物实验、型式检验、临床试验、注册等环节,获得医疗器械注册证。功能性研发通常由企业研发部完成,得到概念样机;在产品功能研发已经完成的基础上,产品还需要经历合规性、可靠性、易用性、批量性4个维度的研发环节(合规性研发指使产品符合相关法律法规[8-9]及行业标准的技术研发;可靠性研发指关乎产品使用的稳定性、生命周期的相关技术研发;易用性研发指从产品使用者的角度帮助产品真正能够得到市场认可的相关技术研发;批量性研发指关于产品真正实现批量性生产的相关技术研发),才能称为真正意义上的研发完成。我国医疗器械企业受规模小、起点低、资金少和经营观念的限制,只能将更多资源投入功能研发阶段,而忽视合规性、可靠性、易用性等方面的研发投入,许多项目因此夭折于注册过程中,据统计,2017年,有源类医疗器械送检产品约15 860个,注册检测不通过率高达80%。此外,工程化研发的缺乏也严重影响了后续的动物实验、临床试验等注册进程,而国家无此类机构及专业技术团队帮助医疗器械企业进行工程化设计服务,已成为整个行业发展的最主要瓶颈。
商品化阶段主要包括品牌宣传,物价、医保申报,市场推广、销售、售后服务等体系建设环节[10]。对于创新型医疗器械初创企业,商品化较产品化难度更大,据统计,截至2019年第一季度,我国已有225个产品进入创新型医疗器械特别审查通道,其中57个创新型医疗器械通过特别审查程序上市,但真正有商业价值的产品不足5%。结合国内外数据分析,销售导向已经成为医疗器械行业发展的主要特点,被欧美垄断的国际高端医疗器械企业均以销售通道为支撑,再通过并购来完成产品的开发和迭代。而目前,我国创新型医疗器械初创企业的核心领导人多是研发或生产领域的专家,欠缺对商业化运作体系的认知,尤其是市场能力。
初创企业为了顺利实现创新型医疗器械产品的上市,需要使产品化和商品化“两个轮子”共同转动;但是,初创企业受资金、资源的限制,在产品化和商品化环节均存在不足,间接导致初创医疗器械企业融资难、发展难,资金的缺乏又进一步制约产品化、商品化能力的提升,因此,搭建产品化、商品化“双轮驱动”的医疗器械产业服务平台非常必要,但由于限制因素较多,需要政府、园区、基金、专业技术团队和相关资源方的协同努力。
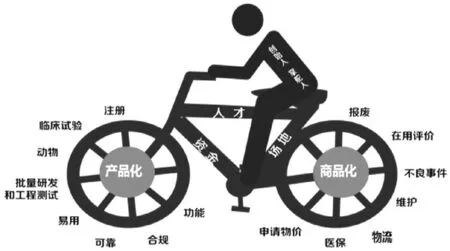
图1 医疗器械商业化的“自行车理论”
2 “双轮驱动”的医疗器械产业服务新模式
针对创新型医疗器械产品化和商品化两个关键环节,中关村发展集团和专业市场化团队以“团队主导+政府引导+园区参与+基金支持”的形式,引入多方资源共建“工程化+检测认证+合同研究组织(contract research organization,CRO)+合同研发生产组织(contract development manufacture organization,CDMO)+合同销售组织(contract sales organization,CSO)”的全产业链医疗器械产业服务生态。
医疗器械服务平台主体为中关村水木医疗科技有限公司,主要从事医疗器械工程化研发和检测业务,并通过控股和参股相关下游公司,打通医疗器械产业服务的各个环节(图2)。
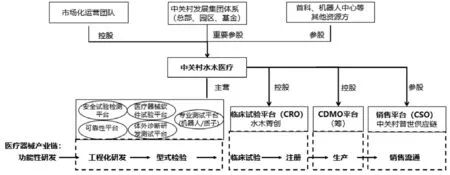
图2 医疗器械产业服务平台的搭建
2.1 打造医疗器械工程化和检测认证平台
该平台为国内外医疗器械公司提供一系列全方位的功能性研发、合规性研发、易用性研发、可靠性研发、批量性研发的工程化设计服务,帮助企业缩短产品研发周期,弥补研发缺陷,为医疗器械的工程化、产业化提供了有效的支撑。实验室场地面积3 415 m2,目前主要服务于有源类医疗器械,具有国内稀缺、技术领先的医疗器械专业电磁兼容实验室,包括3 m 法和10 m 法半电波暗室、屏蔽室和性能监测设备,下设5个子平台,包括安全试验检测平台、医疗器械软件试验平台、专业医疗器械研发测试平台、医疗器械可靠性试验平台、体外诊断(in vitro diagnosis,IVD)研发及检测试验平台。
2.2 打造临床注册CRO 平台
临床注册CRO平台与前一平台的“研、医、检、产”紧密结合,搭建有效的公共研发支撑平台和战略研究平台,为企业提供了医疗器械临床研究、数据管理与统计分析、第三方核查、临床质量管理体系建设、注册、医学写作等专业化技术服务与解决方案,在心脑血管、骨科、眼科、植入、医学影像、手术导航、口腔等领域具备丰富的项目经验。
2.3 打造销售流通CSO 平台
该平台主要包括针对较成熟产品的销售流通平台和针对早期创新产品品牌建立、学术推广的垂直流通平台的服务。其核心成员均来自著名医疗器械流通公司和医疗器械厂家,具有丰富的专业渠道资源,将与其他平台提供企业导流、技术支持等协同服务。
2.4 CDMO 平台(筹建)
随着我国医疗器械上市许可持有人制度的推行,医疗器械研发机构(持证人)可以委托CDMO 进行医疗器械产品的小批量生产,从而降低创新型医疗器械企业在资金、场地等方面的高额投入。目前,市场化的医疗器械CDMO平台主要提供场地和设备,缺乏工程技术支持。中关村发展集团和中关村水木医疗科技有限公司拟依托现有的工程化平台,筹建创新型医疗器械的CDMO 平台,充分保证创新产品的可靠性和批次稳定性,缩短产品化周期。
3 总结与展望
医疗器械行业是一个多学科交叉、知识及资金密集的高技术产业,产品化和商品化壁垒都非常高。《中国制造2025》将生物医药和高性能医疗器械列为重点发展领域,需要从国家战略层面,扶持民族企业向高端发展。中关村发展集团和成员单位中关村水木医疗科技有限公司深挖医疗器械上市前和上市后的产品化、商品化两大痛点,汇聚顶级专业团队、政府、园区、基金、产业等多方面资源,以人才队伍为核心,硬件实力和全方位实力做支撑,共同搭建科技创新型医疗器械专业服务平台,帮助企业打通从技术到产品和商品的“最后一公里”,带动我国创新型医疗器械的高质量发展。