温度对乙醇电催化氧化的影响
涂昆芳,李广,姜艳霞
厦门大学化学化工学院化学系,固体表面物理化学国家重点实验室,福建 厦门 361005
1 引言
目前人类面临的化石能源枯竭和严重的环境污染问题,使得高效、无污染的绿色新能源成为国际研究热点之一1,在可替代的环境友好能源中,燃料电池是一种可直接且连续地把化学能转化为电能的装置2。乙醇是最简单的链醇分子,不仅来源丰富可以由生物质通过发酵制得、易储存和运输,且乙醇理论能量密度比甲醇高(8.1 kW·h·kg-1),产物无毒。但是直接乙醇燃料电池还没有在工业上得到广泛的运用,主要是目前的催化剂对乙醇电催化氧化的活性比较低,并且C-C键难断裂,-CH3容易被还原成甲烷和乙烷,使得乙醇经过12e-转移实现完全氧化生成CO2的过程不易进行,主要还是经过2e-和4e-不完全氧化形成的副产物CH3CHO和CH3COOH,导致燃料利用效率大大降低3。除此之外,铂等贵金属对乙醇氧化的催化反应,其中某些吸附态的中间产物在低电位下很难被继续氧化,吸附在催化剂的表面使得催化剂发生中毒而失去催化活性4,5。
到目前为止,大多数关于乙醇氧化的研究都是在室温下进行的,有关高温下反应行为的信息很少,是因为设计高温原位红外光谱的电化学池较困难6。而燃料电池的工作温度主要在60-80 °C,且化学反应的热活化是化学中的基本问题中最常见之一,控制着反应速率以及复杂的反应过程中不同反应产物的量和分布,所以深入理解温度对乙醇氧化机理和动力学的影响非常重要。因此本工作发展了不同温度下电化学原位红外光谱的研究方法,并用于研究乙醇电催化反应机理。
2 实验部分
2.1 实验试剂和仪器
乙醇(99.7%),高氯酸(99.999%),氯化钾(98%),铁氰化钾(98%)、亚铁氰化钾(98%)。

图1 温控加热电极的结构图 Fig. 1 Structure diagram of the temperature controlled heating electrode.
温控电极由南京金慧策仪器科技有限公司制作,其结构如图1所示,PT100是铂热敏电阻,它的阻值会跟随温度上升而成匀速增长,通过此线性关系由5,6,7连接反馈温度到温控仪器,再通过8,9,10改变加热功率进而控制温度。
2.2 电化学实验测试
循环伏安测试在典型的三电极电解池中进行,饱和甘汞电极为参比电极。
电化学原位红外反射光谱实验采用的是课题组制作的特殊玻璃电解池。该电解池的设计构造与普通电解池类似,不同之处在于底端为开口,检测时氟化钙窗片对底端封口。结果光谱为电位差谱,即分别在研究电位ES和参考电位ER下采集单光束光谱(分别记录为R(ES)、R(ER)),结果光谱根据公式ΔR/R = (R(ES)- R(ER))/R(ER)得到7。
3 结果与讨论
3.1 温控电极的温度校准
3.1.1 理论推导
电化学测温方法用到的是电势测温法,其原理是:在一定条件下氧化还原电对的电势-温度系数是常数8。通过实验得出不同温度下的电势并通过换算得到电极表面温度,设计用于检测铁氰化物和亚铁氰化物离子在高温下扩散系数的温度依赖性的各种系统已在文献中描述9,10。
其由Nernst方程进行推导:

(1)式中,EӨ为标准电极电势,T为温度,R为气体常数,n为反应中电子转移数,F为法拉第常数,aO和aR分别为氧化物质与还原物质的活度。
由公式(1)对T求导得:
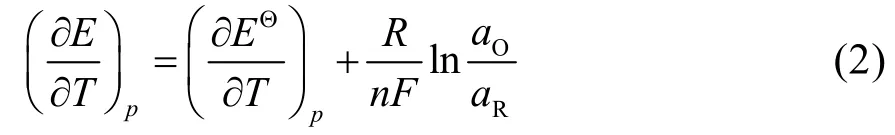
由热力学第一定律推导公式:

等压下等式(3)对T求导得:

由热力学和动力学联合公式ΔG = -nFEӨ得:

最后(2)式可换算为:

所以其温度系数可以由开路电位-温度图的斜率求得,系数理论上为常数。测试中,用5 mmol·L-1K3[Fe(CN)6] + 5 mmol·L-1K4[Fe(CN)6] +0.5 mol·L-1KCl溶液来求电极电势温度系数。
3.1.2 电极温度系数及温控电极表面薄层溶液温度的测量
实验装置如图2所示,将温控电极放入到电解池中,将整个装置置于恒温水浴槽中进行加热。T1测量水浴锅的温度,为保证电解液温度的准确测量,这里用T2来测量电解液的温度。通过盐桥连接参比电极溶液,并放置于室温中。温控电极开路电位通过电化学工作站测得。此步骤中,不需要用温控器对可控温热电极加热,所以温控器可以关闭。设置不同的恒温水浴槽温度,测得不同水浴温度下对应的稳定开路电位E。

图2 电极电势温度系数测量装置示意图Fig. 2 Schematic diagram of the electrode potential temperature coefficient measuring device.
如图3a所示,测得T2分别为27.3 °C、35.0 °C、42.0 °C、49.0 °C、55.0 °C时的稳定开路电位E,用开路电位-温度做图(插图),斜率即为电极电势温度系数。由于温度和开路电位的测量存在误差,四次实验得到斜率分别为-1.56 mV·°C-1、-1.65 mV·°C-1、-1.62 mV·°C-1、-1.57 mV·°C-1,相差不大。选择最小-1.56 mV·°C-1(图3a)、中间的-1.62 mV·°C-1(图3b)、最大的-1.65 mV·°C-1(图3c)做一个误差棒来分析误差温度。如图d所示。将温控电极放入原位红外电解池进行加热后,测得不同的加热温度30-80 °C下对应的开路电位,由不同的电势温度系数换算即可得到控温电极的表面溶液温度TS。本工作中的温控仪器采用人工智能的PID温控仪对体系溶液进行直接加热,存在温度的小幅波动。在对电极表面电势温度的拟合中根据拟合情况分为两部份:低温(30-50 °C)和高温(50-80 °C)两个区间。电极表面电势与温度关系式为TS=0.57Th+ 7.71 (30 °C < Th≤ 50 °C);TS= 0.62Th+5.12 (50 °C < Th≤ 80 °C)。在加热温度为80 °C时,温差计算误差±1.0 °C,误差最大为±1.25%。在40.5 °C,63.0 °C,72.0 °C的加热温度设定下的电极开路电位-时间曲线如图4所示,通过图4可以发现,在较高的温度下温控电极的温度误差也可以较好地控制在1 °C以内。

图3 (a-c)在 5 mmol·L-1 K3 [Fe(CN)6] + 5 mmol·L-1 K4 [Fe(CN)6] + 0.5 mol·L-1 KCl溶液中不同温度下测量的开路电位;(d)加热温度(Th)与电极表面温度(TS)关系Fig. 3 (a-c)Open circuit electrode potentials (OCP)measured at different temperatures in 5 mmol·L-1 K3[Fe(CN)6] + 5 mmol·L-1 K4[Fe(CN)6] + 0.5 mol·L-1 KCl solution; (d)relationship between heating temperature (Th)and electrode surface temperature (TS).

图4 不同加热温度Th下的开路电位图Fig. 4 Open circuit potential diagram at different heating temperatures Th.

图5 不同温度下商业Pt/C催化剂在0.1 mol·L-1 CH3CH2OH + 0.1 mol·L-1 HClO4溶液中的循环伏安曲线图Fig. 5 Cyclic voltammogram of commercial Pt/C catalyst at different temperatures in 0.1 mol·L-1 CH3CH2OH + 0.1 mol·L-1 HClO4 solution
3.2 不同温度下乙醇电催化氧化的循环伏安研究
循环伏安曲线上可以给出电化学反应的宏观信息,图5为酸性条件下商业Pt/C催化剂在25-65 °C时乙醇的电催化氧化循环伏安图。在得到的循环伏安曲线中,商业Pt/C催化剂在不同温度下,曲线形状非常相似,只是随着温度的升高,氧化电流明显增大,说明反应速率变快。正向扫描时明显看到两个氧化峰,在0.53-0.60 V区间时,出现第一个氧化峰(Peak 1),在0.91-0.96 V区间时,又出现第二个氧化峰(Peak 2)。Peak 1归于乙醇不完全氧化生成的CH3CHO和CH3COOH,以及完全氧化生成CO2的叠加电流,而Peak 2归于乙醇不完全氧化生成的CH3CHO和CH3COOH11,12,Peak 1/Peak 2的电流比值可用于定性表征乙醇C-C键断裂的程度13,其比值在商业Pt/C催化剂上由25 °C的0.838到65 °C变为1.295,增大了30% (见表1),说明高温有利于CO2的形成。

表1 不同温度下商业Pt/C催化剂上第一个峰电流与第二个峰电流的比值Table 1 Ratio of the first peak current to the second peak current on a commercial Pt/C catalyst at different temperatures.

表2 红外光谱中乙醇氧化的各个振动频率Table 2 The various vibration frequencies of ethanol oxidation in the infrared spectrum.

图6 (a-c)不同温度下商业Pt/C催化剂在0.1 mol·L-1 CH3CH2OH + 0.1 mol·L-1 HClO4溶液中的原位红外光谱图,参考电位为-0.25 V,间隔0.05 V;(d)各个产物的起始电位Fig. 6 (a-c)In situ FTIRS of ethanol electrooxidation on commercial Pt/C catalyst at different temperatures and various potentials in 0.1 mol·L-1 CH3CH2OH + 0.1 mol·L-1 HClO4 solution. ER = -0.25 V, EStep = 0.05 V;(d)onset potential of each product.
3.3 不同温度下乙醇电催化氧化的原位红外光谱研究
图6是按照多步电位阶跃方法进行采集的25 °C、35 °C、50 °C时乙醇电氧化的原位红外光谱图。表2是乙醇氧化反应各个物质的振动频率,1713-1723 cm-1左右的峰,归属于乙醛或者乙酸的羰基C=O振动14,1640 cm-1处归属于水的弯曲模式振动15,1274-1284 cm-1处的峰归属于乙酸的C-O伸缩振动和O-H变形振动的耦合16,2040-2060 cm-1处的峰归属于线性吸附COL,2341-2345 cm-1的峰归属于O-C-O的不对称振动17。
从图6原位红外光谱图中可以看到,随着温度变化,峰的强度和起始电位有较大差异。除在高温下受1650 cm-1水峰影响,1714 cm-1左右的羰基振动峰被覆盖而难以观察,其他谱峰均明显观察到。同时在较高的温度下没有观察到新的振动峰,说明没有产生新的物质。根据差谱公式,向下的峰代表着物种的生成,向上的峰代表着物种的消耗。由于CO吸附在纳米材料上会表现出异常红外效应18,使得CO谱峰方向倒反,出现在2050 cm-1左右向上的线性吸附CO属于研究电位下的生成,从图a到c这三个图上都可以看到在-100 mV时就有向上的CO峰,说明在低电位下已经开始C-C键断裂,还可以观察到,室温与50 °C下CO谱峰的峰型的差别,说明高温使得CO快速被氧化脱离催化剂表面。对比图6a和图6b,c,商业Pt/C催化剂上CO2起始电位在25 °C为100 mV,35 °C和50 °C为-100 mV,且CO2的峰强度明显增大,说明温度升高使得Pt/C能在更低电位下解离水产生OH-等含氧物种,加速CO的氧化;在25 °C、35 °C,50 °C时表示CH3CHO或者CH3COOH的羰基C=O振动的1714 cm-1左右的峰在200 mV出现,而只代表CH3COOH的C-O伸缩振动和OH变形振动的耦合在1280 cm-1左右的峰在350 mV出现,说明CH3COOH的起始电位是350 mV,CH3CHO的起始电位是200 mV,温度的升高没有改变其起始电位,说明在此温度范围内脱氢生成乙醛并进一步氧化生成乙酸的过程不受温度影响。
二氧化碳和乙酸的积分面积比率[A(CO2)/A(CH3COOH)]经常用于评估乙醇电氧化过程中CO2选择性(SCO2)19。商业Pt/C催化剂在25 °C、35 °C、50 °C时0.35-0.6 V的CO2选择性如图7所示,在0.35 V,商业Pt/C 50 °C时CO2选择性是25 °C时的1.4倍,从图7可以看到CO2选择性随着电位的升高逐渐降低,是因为电位越高,更多含氧物种吸附表面占据活性位,使得C-C键断裂受到阻碍,且含氧物种提供氧原子促进了乙醇氧化成乙酸20。结果半定量地证实,当前的CO2形成效率很大程度上取决于电极电位,这与文献中DEMS21和FTIR22光谱测量乙醇氧化的结果一致。CO2选择性随着温度的升高也增大,说明热效应有利于完全氧化过程的进行,可能是因为温度升高,一方面,使乙醇以桥式吸附到催化剂表面的数量增加,有利于C-C键断裂;另一方面,氧化反应速率随温度的固有增加,并且加速了OHad的形成和随后的COad与OHad氧化反应,或者由于热解吸增加,稳态COad覆盖率降低。

图7 商业Pt/C催化剂中二氧化碳和乙酸积分强度比例与电位的关系 Fig. 7 The relationship between CO2 and CH3COOH integrated intensities ratio and potential on commercial Pt/C catalyst.
图8的采谱条件与图6中几乎一致,只是研究电位变成ES= -0.10 V-1.0 V,电位间隔0.1 V,从图8c,d看到,电位高于800 mV时CO2面积不再增大,而CH3COOH随着电位的增加一直在增大,是因为高电位惰性Pt-O物种的出现占据了活性位,减少了乙醇以桥式吸附到催化剂表面的数量,阻碍了C-C键的断裂,且此含氧物种有利于CH3COOH的形成。
3.4 同位素示踪电化学原位红外光谱表征
一个乙醇分子含有一个α-C和一个β-C,乙醇C-C键断裂后,这两种C1物种CO和CHX氧化成CO2的能力如何,我们使用C源标记的同位素示踪电化学原位红外光谱表征方法进行研究,以13CH312CH2OH作为探针分子,从图9可以看出,改变温度,β-C完全氧化的最终产物13CO2的起始电位在0.25 V不变化,结合图6可知,α-C在-100 mV就已经氧化了。这表明,-13CH2完全氧化需要更高的能量。从图9乙醇电氧化原位红外光谱中只看到2050 cm-1左右的属于12CO的峰,而没有看到1980 cm-1左右的属于13CO的峰,一是因为13CO含量及其少,二是因为低波数的峰会向高波数转换23。为了更进一步区分其中分别来自α-C和β-C完全氧化为12CO2和13CO2的占比,分别对25 °C和50 °C反应条件下的13CO2和12CO2积分面积比值[A(13CO2)/A(12CO2)]进行定量分析,结果如图9b所示。从图中可以看到,随着电位的增加,13CO2/12CO2比值均逐渐增大,25 °C时0.6 V的比值是0.25 V时的3.5倍。另一方面,相同电位不同温度下的13CO2/12CO2比值均随温度增加而增大,其中0.45 V时50 °C是25 °C的1.32倍。这表明随着电位的增加或温度的升高,有利于β-C完全氧化为CO2。

图8 (a,b)不同温度下商业Pt/C催化剂在0.1 mol·L-1 CH3CH2OH + 0.1 mol·L-1 HClO4溶液中的原位红外光谱图,参考电位为-0.25 V,间隔0.1 V;(c,d)不同电位下CO2和CH3COOH的积分面积Fig. 8 In situ FTIRS on commercial Pt/C catalyst at different temperatures in 0.1 mol·L-1 CH3CH2OH + 0.1 mol·L-1 HClO4 solution. ER = -0.25 V, EStep = 0.1 V; (c, d)integral area of CO2 and CH3COOH at different potentials.

图9 商业Pt/C催化剂分别在25 °C和50 °C条件下(a)电位区间0.05 V至0.6 V范围内的同位素示踪(13CH312CH2OH)原位多步阶跃红外光谱图,参考电位为-0.25 V;(b)不同研究电位下的13CO2/12CO2比值Fig. 9 (a)Isotopic tracer method (13CH312CH2OH)in situ MS-FTIRS on commercial Pt/C at 25 °C and 50 °C under different potentials from 0.05 V to 0.6 V, ER = -0.25 V. (b)The ratio of 13CO2/12CO2 under different potentials.

图10 不同温度中乙醇在商业Pt/C催化剂上的氧化机理Fig. 10 Oxidation mechanism of ethanol at different temperatures under acidic conditions on commercial Pt/C catalyst.
结合我们之前的工作和文献24,25,以及前述结果,我们推测乙醇在25 °C、35 °C、50 °C下的氧化机理,如图10所示。在商业Pt/C催化剂上CO2的起始电位分别为100 mV、-100 mV、-100 mV,因为β-C完全氧化为CO2的起始电位均为250 mV且与温度无关,所以起始的CO2来自于α-C的氧化。商业Pt/C催化剂上乙醇通过断α-H和O-H生成乙醛的起始电位都为200 mV,乙醛进一步与-OH发生氧化反应生成乙酸电位都是350 mV,表明在研究的温度范围内,升高温度不足以使CH3CHOH*脱OH中的H形成乙醛。
4 结论
用电势测温法校准温控电极,在较低的加热温度下,温度最大误差为1 °C。温控仪器设置温度Th与电极表面温度TS之间的关系式为TS= 0.57Th+7.71 (30 °C < Th≤ 50 °C);TS= 0.62Th+ 5.12 (50 °C< Th≤ 80 °C)。此升温电极具有加热快、局部加热不影响整体溶液等优点,初步建立了变温原位红外测定方法,可以运用到其他体系中。在乙醇电催化氧化循环伏安图和原位红外光谱中,可以得到随着温度的升高,氧化反应速率更快,反应更容易进行,并且CO2的选择性也增大。在25-50 °C 时CH3CHO,CH3COOH的起始电位与温高温低电位有利于CO2的选择性。同位素标记的实验表明早期氧化的CO2主要来源于乙醇的α-C的氧化,β-C的氧化则是在0.25 V以后,且随温度的升高β-C氧化的速度更快。这对于设计和改进催化剂有着重要的参考价值,并且有利于燃料电池的应用,但温度过高产生气泡会对薄层溶液有扰动,影响数据的采集,因而需要对变温原位红外光谱方法不断改进和完善。

