莪术醇长循环脂质体的制备及体外抗乳腺癌作用研究
,*
(1.桂林医学院药学院,广西桂林 541004;2.井冈山大学附属医院,江西吉安 343000)
莪术醇(curcumol,Cur)又名姜黄醇,属于倍半萜类化合物,存在于姜科植物蓬莪术、广西莪术或温郁金的干燥根茎中,是莪术挥发油的主要抗肿瘤成分[1-2];分子式为C15H24O2,分子量为236.35;在有机溶剂中溶解度较大,易溶于乙醚、氯仿,溶于乙醇,几乎不溶于水,在水中的溶解度仅为0.3%。莪术醇被证明在肝癌、宫颈癌、卵巢癌、乳腺癌、前列腺癌等多种人类癌症中具有体内和体外抑制增殖及诱导凋亡效应[3-4]。
脂质体(Liposome,Lp)具有良好的生物相容性和肿瘤靶向性,是近年来研究较多的一种药物载体,可以作为各类化疗药物的传递载体[5-6]。利用脂质体包裹莪术醇可提高其溶解度,增强其稳定性。但是,普通脂质体易从体内清除,聚乙二醇[Poly(ethylene glycol),PEG]修饰普通脂质体制备而得的长循环脂质体可躲避巨噬细胞对脂质体的识别和吞噬,延长脂质体在体内的循环时间,从而提高制剂在肿瘤部位的蓄积,达到更好的抗肿瘤效果[6-7]。Walkey等[8]报道称随着PEG修饰密度的升高,血清蛋白吸附量和巨噬细胞对制剂的摄取能力均显著下降,证明两者显著相关。
本研究采用薄膜分散法制备莪术醇长循环脂质体,测定了其形态、粒径、电位、包封率;考察其体外释放和初步稳定性;并进一步考察了莪术醇长循环脂质体的细胞摄取及细胞毒性作用。
1 材料与方法
1.1 材料与仪器
莪术醇(98%,批号:CC070518) 上海沪云医药开发有限公司;二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000,批号:B03011) 上海芃硕生物有限公司;噻唑蓝 MTT,美国Sigma公司;香豆素-6 批号:MKBV4602V,美国Alorich公司;DMEM培养基、胎牛血清、0.25%胰酶、青霉素-链霉素溶液 美国Gibco公司;胆固醇 上海行知化工厂;卵磷脂 德国Lipoid公司;透析袋,截留相对分子量8000-14000 上海生工生物工程技术服务公司;微孔滤膜(0.22 μm) 天津市津腾实验设备有限公司,人三阴性乳腺癌细胞MDA-MB231 桂林医学院实验中心赠予。
LC-20A高效液相色谱仪 日本Shimadzu公司;EYEL4旋转蒸发仪 上海爱朗仪器有限公司;JY88-Ⅱ超声波细胞粉碎机 宁波新芝生物科技股份有限公司;透射电子显微镜 日本Hitachi公司;SHA-B恒温震荡器 常州国华电器有限公司;CP225D型电子天平 德国Sartorius公司;DF-101集热式恒温磁力搅拌器 巩义市英峪予华仪器厂;Nano ZS90激光散射粒度分析仪 英国Malvern公司;SynergyHTX多功能酶标仪 美国Bio Tek公司。
1.2 实验方法
1.2.1 莪术醇含量测定方法的建立
1.2.1.1 色谱条件 色谱柱:Hypersil BDS C18反相柱(4.6 mm×250 mm,5 μm);流速1.0 mL·min-1,检测波长203 nm;柱温:30 ℃;流动相:乙腈:0.2%醋酸水溶液(体积55∶45);进样量:20 μL[9]。
1.2.1.2 标准曲线的绘制 精密称定莪术醇对照品于容量瓶中,用甲醇溶解并定容至10 mL容量瓶,摇匀,得对照品储备液。浓度分别为10、20、40、80、160 μg·mL-1,精密吸取20 μL进样,以峰面积对质量浓度进行线性回归[10]。
1.2.1.3 精密度试验 精密称取莪术醇对照品于容量瓶中,用甲醇溶解稀释并定容至10 mL,浓度为40 μg·mL-1,摇匀,按“1.2.1.1”项下色谱条件,连续进样测定5次,记录莪术醇峰面积,计算日内精密度[10]。
1.2.1.4 稳定性考察 精密称取莪术醇对照品于容量瓶中,适量甲醇溶解后,用甲醇稀释并定容至10 mL,浓度为40 μg·mL-1,摇匀,于0、1、2、4、6、8 h,按“1.2.1.1”项下色谱条件,进样分析,测定记录莪术醇峰面积。
1.2.1.5 加样回收率试验 精密量取已知质量浓度的莪术醇脂质体样品溶液9份,各0.5 mL,分别加入80%、100%、120%的莪术醇对照品,加甲醇溶解超声10 min(200 W,30 ℃),0.22 μm微孔滤膜滤过,精密吸取20 μL,HPLC测定。将结果代入标准曲线计算质量浓度,与实际质量浓度相比,得到样品回收率[9]。
1.2.2 莪术醇长循环脂质体的制备 采用薄膜分散法制备长循环脂质体[11-13],精确称取处方量的莪术醇0.018 g,卵磷脂0.09 g,胆固醇0.009 g和DSPE-PEG2000 0.0018 g,加入三氯甲烷溶解,置于圆底烧瓶中,旋转蒸发成膜(45 ℃,转速为80 r/min),真空干燥2 h,加0.05 mol·L-1,pH6.5的磷酸盐缓冲液,于恒温水浴里水化30 min,超声波细胞粉碎机探头超声6 min(150 W),过0.22 μm滤膜,即得莪术醇长循环脂质体。载荧光探针香豆素-6(Coumarin-6,C6)长循环脂质体制备:只需把莪术醇换成香豆素-6即可,其他步骤同莪术醇长循环脂质体。
1.2.3 莪术醇长循环脂质体的表征
1.2.3.1 粒径和电位测定 取一定量脂质体,稀释后,置于比色皿中,于激光粒度分析仪中测定,观察其粒径和电位及其分布[14-15]。
1.2.3.2 透射电镜下形态观察 取脂质体少量,滴加到电镜专用铜网,放置3 min,吸取过多的样品,1% 磷钨酸溶液负染,将铜网自然晾干,在透射电镜下观察其形态[16]。
1.2.3.3 包封率的测定 按“1.2.2项”下工艺及处方制备3批莪术醇长循环脂质体。精密量取莪术醇长循环脂质体2 mL,加入透析袋(截留相对分子量8000~14000)中,置于磷酸盐缓冲液(pH6.5,90 mL)中,每个样品平行3份,避光,30 ℃恒温振荡8 h后,收集透析袋中的液体1 mL,转移至10 mL容量瓶中,加入适量甲醇超声破乳,待脂质体结构被充分破坏后,加入甲醇定容。另精密量取1 mL未透析莪术醇长循环脂质体置10 mL容量瓶中,甲醇定容。所得溶液分别过0.22 μm滤孔滤膜,进HPLC检测莪术醇的含量。计算包封率(EE)[17-18]。
EE(%):为包封率,W1和W2分别表示包封于长循环脂质体中莪术醇的质量和莪术醇的总质量。
1.2.3.4 体外释放的测定 精密量取莪术醇长循环脂质体,莪术醇脂质体以及莪术醇溶液2 mL,加入透析袋(截留相对分子量8000~14000)中,两端加紧后置于磷酸盐缓冲液(pH6.5,30 mL)中,每个样品平行3份,避光,37 ℃恒温振荡。分别于1、2、4、6、8、10、12、24、48、72 h吸取2 mL透析液,并补加等体积磷酸盐缓冲液[19-20]。按“1.2.1.1”项下色谱条件测定其含量,并计算药物的累积释放百分率。
1.2.3.5 放置稳定性 取莪术醇长循环脂质体3批,分别在4 ℃和常温条件下放置保存,分别于第0、1、2个月取样,观察是否有分层、沉淀现象,考察粒径及药物含量变化情况[21-22]。
1.2.4 细胞实验
1.2.4.1 体外细胞摄取实验 采用荧光强度值定量测定细胞的摄取情况。取对数生长期MDA-MB231细胞加至96孔板,细胞密度为1×105个·mL-1,0.1 mL/孔,培养24 h。用含6.25、12.50、25 μg·mL-1载香豆素6的长循环脂质体和普通脂质体(PEG-Lp-C6,Lp-C6)的完全培养基,空白对照组为完全培养基,在37 ℃下孵育4 h,观察细胞状态正常,符合实验要求,冷PBS洗3次,每次5 min。1% TritonX-100处理细胞45 min,荧光酶标仪测定OD值(激发和发射波长分别为466 nm,505 nm)[23-24]。
1.2.4.2 MDA-MB231细胞毒性实验 采用MTT法考察脂质体对细胞的毒性[25-26]。取对数生长期MDA-MB231细胞,以1×105个·mL-1的密度接种于96孔板,0.1 mL/孔,37 ℃培养24 h后,按6.25、12.5、25、50、100 μg·mL-1的浓度分组加入载莪术醇的长循环脂质体(PEG-Lp-Cur,Lp-Cur)和莪术醇溶液(Cur)的完全培养基,空白对照组为完全培养基,作用24 h后,每孔加入MTT溶液200 μL,孵育4 h后,每孔加DMSO 150 μL,振荡10 min。采用酶标仪570 nm波长处测定各孔的OD值,计算细胞存活率(Cell Viability,CV)及IC50。
1.3 数据处理
采用SPSS 22.0软件进行显著性分析,独立样本T检验法(T-test)考察组间差异。计量数据用Mean±SD表示(n=3)。两组数据间显著性差异表示为P<0.05,采用GraphPad-Prism5进行绘图。
2 结果与分析
2.1 含量测定方法学考察结果
方法学考察结果显示,HPLC测定系列浓度的莪术醇对照品溶液,以峰面积(A)对浓度(C)进行线性回归分析,得莪术醇标准曲线:A=35.574C+128.17(r=0.9993),表明莪术醇在10~160 μg·mL-1内峰面积与浓度线性关系良好。方法的日内、日间精密度分别为1.56%、1.87%,均小于2.0%;莪术醇在8 h内的稳定性良好,RSD小于2.0%;高中低三个浓度莪术醇的平均方法回收率为96.8%,RSD小于2.0%;符合HPLC样品测定的方法学要求。可进行莪术醇含量测定。
2.2 莪术醇长循环脂质体的表征
2.2.1 粒径和zeta电位测定 脂质体的粒径和电位如表1和图1所示。莪术醇长循环脂质体的粒径(150.3±4.0) nm,PDI为0.197±0.009,粒径分布较窄,zeta电位(-24.5±0.7) mV,莪术醇长循环脂质体粒径较莪术醇脂质体稍大,可能是PEG长链在脂质体表面形成了一层水化膜的缘故,其表面负电性强于莪术醇脂质体,粒子间的静电排斥可提高脂质体的分散性,有利于其稳定性。
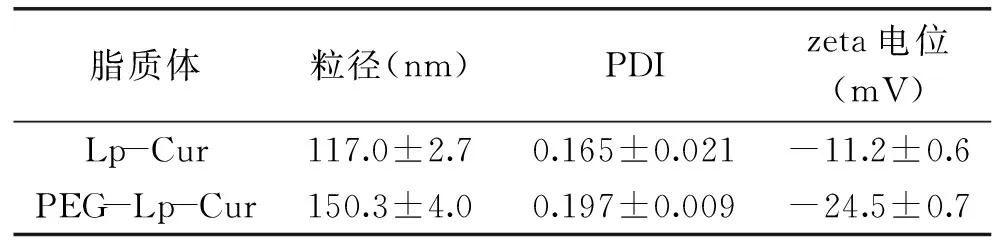
表1 莪术醇脂质体的粒径和zeta电位Table 1 The particle size and zeta potential ofLp-Cur and PEG-Lp-Cur
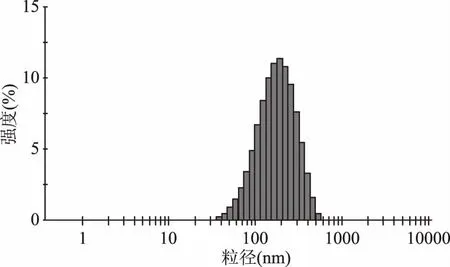
图1 莪术醇长循环脂质体粒径分布Fig.1 The particle size distribution of PEG-Lp-Cur
2.2.2 透射电镜下形态观察 透射电镜结果见图2,莪术醇长循环脂质体外观形态均为类球形小囊泡,偶见空心囊泡结构,粒子间无聚集现象,分布较均匀。

图2 莪术醇长循环脂质体透射电镜形态Fig.2 Morphology of PEG-Lp-Curby transmission electron microscope
2.2.3 包封率测定 制备3批莪术醇长循环脂质体,包封率测定结果见表2。莪术醇长循环脂质体的平均包封率为80.24%,表明制备工艺稳定可行。
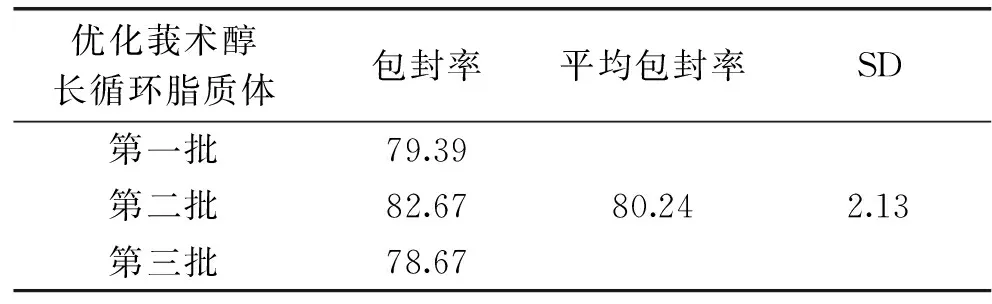
表2 包封率测定结果(%)Table 2 Results of determination of entrapment efficiency(%)

表3 莪术醇长循环脂质体在常温条件下的稳定性(n=3)Table 3 Stability of PEG-Lp-Cur at room temperature(n=3)

表4 莪术醇长循环脂质体在4 ℃条件下的稳定性(n=3)Table 4 Stability of PEG-Lp-Cur at 4 ℃(n=3)
2.2.4 体外释放的测定 莪术醇体外释放结果见图3。在1 h时,游离莪术醇溶液、莪术醇脂质体及莪术醇长循环脂质体的累积释放率分别为96.40%、19.96%和13.70%,HPLC法测定莪术醇长循环脂质体在初期释放较慢,可能是PEG在脂质体外形成的水化膜而减慢药物的释放,72 h累积体外释放百分率为52.6%,与脂质体释放基本一致。原因可能是脂质体本身可使药物具有一定的缓释作用,加之莪术醇为脂溶性药物和释放介质的影响,使得药物释放缓慢[27]。
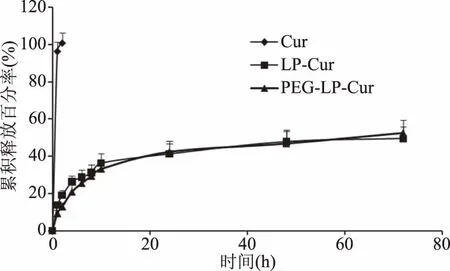
图3 莪术醇长循环脂质体的体外释放曲线Fig.3 The curve of release of PEG-Lp-Cur in vitro
2.2.5 放置稳定性 结果见表3和表4,莪术醇长循环脂质体在常温条件下存放2个月,有较多沉淀产生,振摇亦不可完全复原,粒径有较大幅度增大,药物含量下降明显。在4 ℃条件下存放2个月,有少量沉淀和絮凝产生,经振摇可复原,均匀性良好,含药量为79.76%,粒径变化不大。结果表明,莪术醇长循环脂质体在4 ℃条件下稳定性较好。
2.3 体外细胞摄取实验
为了考察长循环脂质体的体外靶向性,以普通脂质体作为对照,定量观察MDA-MB231细胞对包载香豆素-6的长循环脂质体摄取情况。在37 ℃条件下,结果如图4所示,随着香豆素-6浓度的增加,MDA-MB231细胞对载有香豆素-6的长循环和普通脂质体的摄取量逐渐增大,提示MDA-MB231细胞对长循环和普通脂质体的摄取呈浓度依赖性,并且在香豆素-6相同浓度下MDA-MB231细胞对长循环脂质体摄取明显高于普通脂质体。提示DSPE-PEG2000可能增加了MDA-MB231细胞对脂质体的摄取[28]。

图4 MDA-MB231细胞对脂质体的细胞摄取效率(n=3)Fig.4 Cellular uptake efficiency of the liposomeson MDA-MB231 cells(n=3)注:组间比较,*表示具有显著差异,P<0.05。
2.4 细胞毒性实验

图5 莪术醇对MDA-MB231细胞的细胞毒性评价Fig.5 Cytotoxicity of curcumolon MDA-MB231 cells in vitro
莪术醇各种制剂的细胞毒性如图5所示。与空白对照组对比,莪术醇各制剂组随药物浓度的增加细胞毒性均明显增强,莪术醇长循环脂质体的体外抗肿瘤活性强于同浓度的莪术醇普通脂质体和游离莪术醇,经计算Cur、Lp-Cur和PEG-Lp-Cur的半数抑制浓度(IC50)分别为45.14、23.50、10.22 μg·mL-1。表明莪术醇包载于脂质体后可以提高其体外抗肿瘤活性,尤其是经DSPE-PEG2000修饰后的长循环脂质体,体外抗肿瘤活性更强。机制可能与长循环脂质体能够显著提高乳腺癌细胞对莪术醇的摄取和延长莪术醇在乳腺癌细胞中的滞留时间有关。在机体中聚乙二醇(PEG)修饰的脂质体可以减少网状内皮系统(RES)吞噬细胞的摄取,经实体肿瘤新生血管的渗透滞留增强作用(EPR)实现肿瘤靶向[29]。
3 讨论
本研究采用薄膜分散法制备了莪术醇长循环脂质体,粒径分布较集中,分散较为均匀,制备3批脂质体,平均包封率为80.24%,体外释放缓慢具有明显的缓释效应,可能由于DSPE-PEG2000的加入脂质体中,伸展的PEG长链在脂质体表面形成了一层水化膜,导致药物释放减慢[21]。在4 ℃条件下存放2个月粒径和含药量无明显变化,稳定性较好,符合制备工艺要求。
细胞摄取实验中,由于莪术醇无荧光,无法观察肿瘤细胞对莪术醇长循环脂质体的摄取情况,故采用载香豆素-6的长循环脂质体考察MDA-MB231细胞对长循环脂质体的摄取情况。人三阴性乳腺癌MDA-MB231细胞对长循环脂质体的体外摄取作用优于普通脂质体,这可能与长循环脂质体表面的PEG链的水化作用和细胞有更好的亲和力有关,增加了细胞对长循环脂质体的摄取[29]。
细胞毒性实验中,莪术醇长循环脂质体的体外抗肿瘤活性强于同浓度的莪术醇普通脂质体和游离莪术醇,推测可能与脂质体能改善莪术醇在水中的溶解度和延长莪术醇在胞内的滞留时间有关,从而发挥更强的抑制肿瘤细胞作用,另外长循环脂质体可通过增加细胞摄取,进而发挥莪术醇对MDA-MB231细胞的毒性作用[30],故表现出较强的肿瘤细胞毒性作用。
4 结论
本研究通过薄膜分散法制备莪术醇长循环脂质体,外观形状规整均一,理化性质稳定,包封率较高;体外释放具有缓释效果,稳定性较好;长循环脂质体具有比普通脂质体更高的摄取效率;体外细胞毒性实验证明了载药脂质体制剂对MDA-MB231细胞的毒性具有浓度依赖性,在相同浓度下,莪术醇长循环脂质体IC50值明显低于莪术醇普通脂质体和游离莪术醇,说明莪术醇长循环脂质体具有较强的MDA-MB231细胞的毒性,证明了莪术醇长循环脂质体的抗人三阴性乳腺癌细胞作用。
以上研究结果表明,长循环脂质体能高效包载莪术醇,改善其在水中的溶解度,增加其稳定性,提高肿瘤细胞对莪术醇的摄取,体外抗肿瘤作用较强,为后续进行药物代谢动力学研究和荷瘤鼠体内药效学的研究打下基础。

