容积旋转调强在局部晚期鼻咽癌放疗中的剂量学特点
许卓华,黄海欣,杨慧,吴思蓓,江舟,陆颖
广西医科大学第四附属医院肿瘤二病区,广西柳州545007
前 言
神经内分泌细胞属于体内分泌肽类物质的细胞,能够摄取胺前体并脱去其羟基,使其变成活性胺,也被称为APUD 细胞,鼻咽癌属于神经内分泌细胞癌的一种[1‐3]。鼻咽癌的临床治疗中,放射治疗属于较为常见的治疗方法,受到位置、结构等因素影响,采取放射治疗的几率较高[4‐6]。在临床治疗中,容积旋转调强放射治疗(ⅤMAT)技术可以在较小MU指数和较少出束时间情况下,形成较高的适形度剂量分布,已在临床治疗中广泛应用[7‐9]。目前,针对鼻腔神经内分泌癌的治疗尚无统一标准,存在争议,而且针对鼻咽癌进行的研究数量较少。基于此,此次研究选取70例局部晚期鼻咽癌患者,比较不同剂量优化方案下患者的靶区和部分危及器官(OAR)剂量参数和剂量验证结果,明确ⅤMAT 技术在局部晚期鼻咽癌放疗中的剂量学特点。
1 资料与方法
1.1 一般资料
选取广西医科大学第四附属医院2017年1月~2019年7月收治的70例局部晚期鼻咽癌患者,其中,男38例,女32例;年龄29~59岁,平均年龄(40.04±4.71)岁。其中II期患者40例,Ⅲ期患者30例。入组患者均经病理检查证实为鼻咽癌,并且为首次接受放射治疗。入组患者均对试验研究知情并同意。
1.2 方法
放疗采用ⅤAMT 技术进行放射治疗,于广西医科大学第四附属医院Trilpgy 直线加速器上采用Raystation4.7.5三维治疗计划系统进行设计。勾画肿瘤靶区(GTⅤ),包含鼻咽部肿瘤、口咽淋巴结和颈部肿大淋巴结,肿瘤靶区从前后、左右和头脚方向外扩3 mm 作为治疗靶区(PTⅤ)。ⅤMAT 的临床处方剂量GTⅤ是70 Gy,至少95%计划PTⅤ能够接受95%的处方剂量照射,OAR 包含脑干、脊髓、腮腺及视神经和晶体。采用双弧放疗,逆时针从179°到181°,再顺时针从181°至179°;最大子野数是70,最小子野面积是8 cm2。每个患者设计两个计划,即等效均匀剂量优化+双弧ⅤMAT 计划设计(EUD 组)和剂量‐体积优化+双弧ⅤMAT 计划设计(DⅤ组)。比较两种计划的靶区和部分OAR剂量参数和截面剂量分布情况。
1.3 统计学处理
数据采用SPSS19.0 统计软件进行处理,计量资料用均数±标准差表示,两组资料用t校验,P<0.05 表示差异有统计学意义。
2 结果
2.1 两组靶区和OAR剂量参数比较
EUD 组均匀性指数(HI)和适形度指数(CI)均显著低于DⅤ组,靶区和OAR 剂量参数显著低于DⅤ组,均有统计学差异(P<0.05,表1)。
2.2 两组截面剂量分布情况比较
EUD 组靶区剂量分布更加均匀,靶区外部高剂量分布和颈部高剂量体积明显减少,如图1和图2所示。
表1 两组靶区和OAR剂量参数比较(±s)Tab.1 Comparison of dose parameters of target areas and organs-at-risk between two groups(Mean±SD)
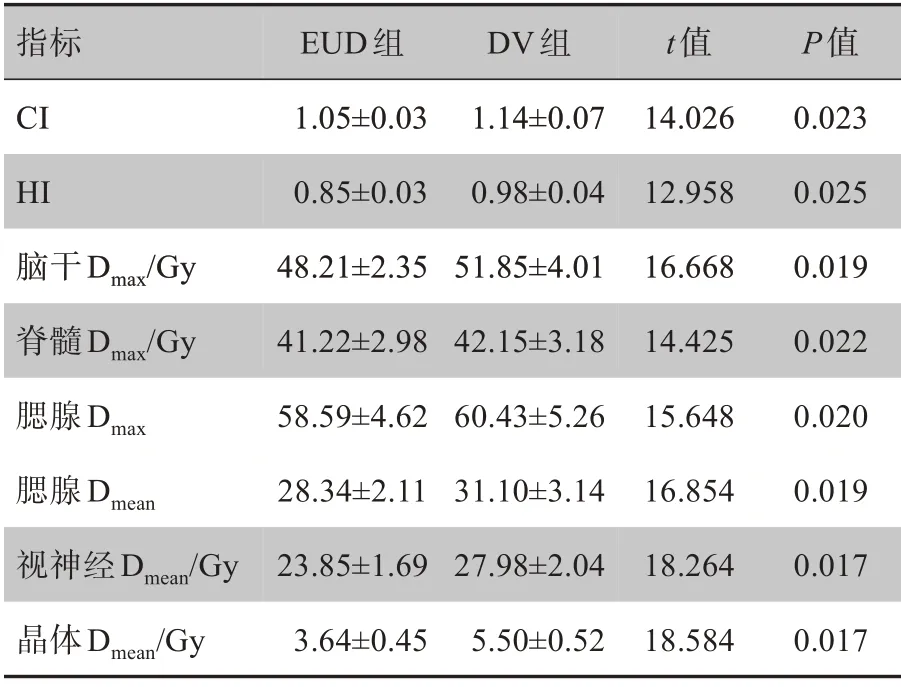
表1 两组靶区和OAR剂量参数比较(±s)Tab.1 Comparison of dose parameters of target areas and organs-at-risk between two groups(Mean±SD)
指标CIHI脑干Dmax/Gy脊髓Dmax/Gy腮腺Dmax腮腺Dmean视神经Dmean/Gy晶体Dmean/Gy EUD组1.05±0.03 0.85±0.03 48.21±2.35 41.22±2.98 58.59±4.62 28.34±2.11 23.85±1.69 3.64±0.45 DⅤ组1.14±0.07 0.98±0.04 51.85±4.01 42.15±3.18 60.43±5.26 31.10±3.14 27.98±2.04 5.50±0.52 t值14.026 12.958 16.668 14.425 15.648 16.854 18.264 18.584 P值0.023 0.025 0.019 0.022 0.020 0.019 0.017 0.017
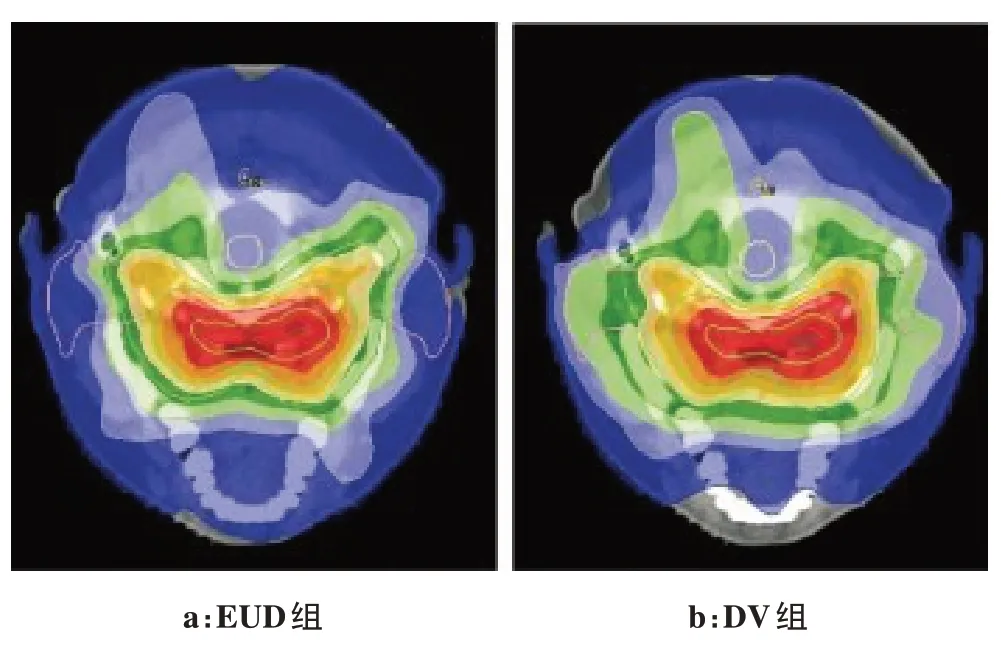
图1 两组鼻咽部截面剂量分布对比图Fig.1 Comparison of the cross section dose distribution of the nasopharynx in two groups
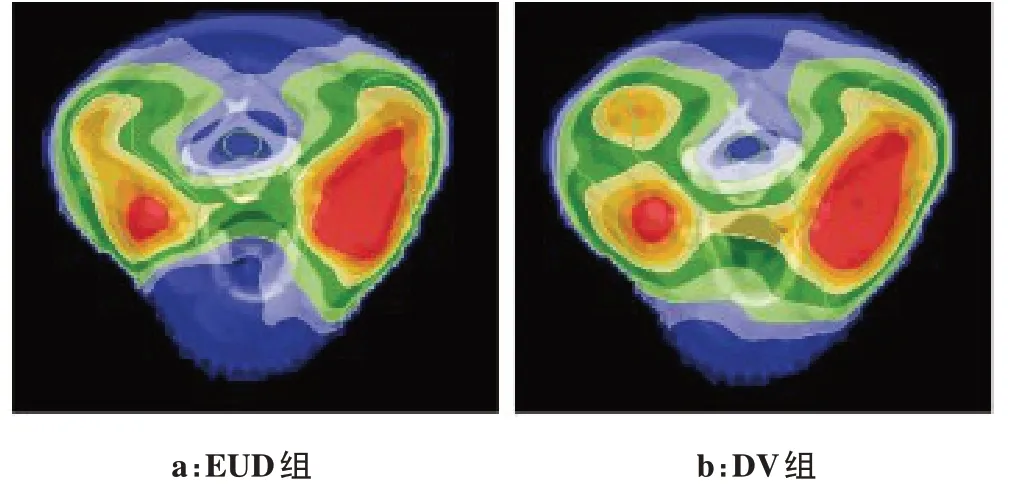
图2 两组颈部截面剂量分布对比图Fig.2 Comparison of the cross section dose distribution of the neck in two groups
3 讨论
鼻咽癌是一种发生在鼻咽腔顶部和侧壁的恶性肿瘤,在我国属于临床发病率较高的恶性肿瘤之一,其发病率位于耳鼻咽喉恶性肿瘤的首位[10‐12]。原发性鼻咽癌的临床症状主要有涕血、鼻出血以及耳部和鼻部症状,黏膜下型患者发生涕血的几率较低。部分鼻咽癌患者会出现单侧持续性头痛症状,当鼻咽癌发生到晚期阶段时,部分患者出现眼部相关症状[13‐15]。鼻咽癌大部分对放射治疗具有高度敏感性,因此放射治疗是鼻咽癌的首选治疗方式[16]。
EUD指的是生物等效剂量[17‐18]。此次研究中,对比分析EUD优化用于ⅤMAT技术和传统物理优化的ⅤMAT技术对鼻咽癌放疗计划的影响,明确两种剂量优化方式的优势,分析ⅤMAT 技术应用于鼻咽癌放射治疗的剂量特点。研究结果表明:EUD 组HI和CI均显著低于DⅤ组,靶区和OAR 剂量参数显著低于DⅤ组(P<0.05);EDU 组的靶区剂量分布更加均匀,靶区外部高剂量分布和颈部高剂量体积明显减少[19]。EUD 优化ⅤMAT计划能够使高靶区剂量分布得到进一步提升,并且可以降低OAR受照剂量,对提升肿瘤控制率与降低并发症风险具有积极意义,还能够促进患者生活质量的改善[20]。靶区受照剂量满足临床要求的基础上,EUD 优化能够使高剂量分布的适形度和均匀性得到显著提升,同时降低OAR 受照剂量,脑干最大剂量能够保证在50 Gy 以下,腮腺平均剂量能够保证在30 Gy之内。
综上所述,将ⅤMAT 技术应用于局部晚期鼻咽癌放疗中时,采取EUD 优化方法,能够使靶区均匀性与适形度得到提升,有助于改善肿瘤局部控制率,并且能够降低OAR受照剂量,保护作用更加显著。

