白内障超声乳化术对已行小梁切除术患者滤过泡和眼压的影响
石小佳 黄婧 赵婧 张文松
白内障是小梁切除术后的常见并发症[1-4]。白内障发展到一定程度,既影响患者的生活质量,也影响青光眼医生对视神经的判断,因此必须行手术治疗。然而以往的研究大多认为小梁切除术后行白内障超声乳化吸除手术会增加眼压控制不良的风险,这一结论主要是以原发性开角型青光眼(primary open-angle glaucoma,POAG)为研究对象。由于青光眼患者需要终身管理眼压,对有功能性滤过泡的眼睛行白内障手术是一项棘手的任务。近些年以原发性闭角型青光眼(primary angle-closure glaucomy,PACG)为研究对象的相关研究逐渐增多,并且得出了相反的结论。本综述就白内障超声乳化手术对功能性滤过泡是否有影响这一问题进行讨论,并评述影响滤过泡失败的因素。
一、研究设置的不同
1.青光眼的类型 小梁切除术后的PACG患者,超声乳化术后眼压以下降为主[5-7]。Sasan等(2013)研究了37例已行小梁切除术的PACG患者,发现白内障超声乳化术后2年平均眼压下降2.79 mmHg(1 mmHg=0.133 kPa),且使用降眼压药物的数量减少[6]。杨文慧等(2016)研究了47例PACG患者,得出了与Sasan相似的结论[7]。Wang X等(2009)的研究结果与以上不同。他们分析了24例有功能性滤过泡的青光眼患者(27只眼,其中19只眼为PACG,8只眼为POAG),发现行白内障超声乳化术后眼压较术前明显升高[8]。有分析认为Wang X的研究纳入的患者,在白内障术前存在低眼压(4~19.7 mmHg),而超声乳化手术可以用来治疗过度滤过和慢性低眼压,所以不难理解白内障术后眼压升高[9]。Wang X和洪颖等的研究均既纳入了PACG患者,也纳入了POAG患者,但PACG所占比例更大(表1)。
小梁切除术后的POAG的患者,白内障超声乳化术后眼压以升高为主,眼压升高可达3.1 mmHg[10-15]。相关的研究很多,部分研究设置了单纯的小梁切除术组作为对照,发现在超声乳化术后相同随访时间内,研究组的眼压明显高于对照组,而眼压控制成功率低于对照组。不同研究的纳入标准、眼压控制成功的标准不尽相同,但结论相似(表2)。但也部分研究认为,小梁切除术后伴有滤过泡的POAG患者,白内障手术对其长期的眼压控制无不良影响[16,17]。
Almobarak等(2017)发现,行白内障超声乳化术的葡萄膜炎并发青光眼的患者与未行超声乳化术的患者在小梁切除术生存率上没有差异。但接受白内障超声乳化术的眼睛比对照组需要更多的药物来控制眼压[18]。
2.随访时间 在Nguyen等(2014)的一项回顾性研究中,发现小梁切除术后行超声乳化术组和单纯小梁切除术组相比,在随访12个月时滤过泡失败率显著增加,但在24个月时两组的滤过泡失败率没有明显差异[19]。
二、超声乳化手术对滤过术后眼压产生影响的原因
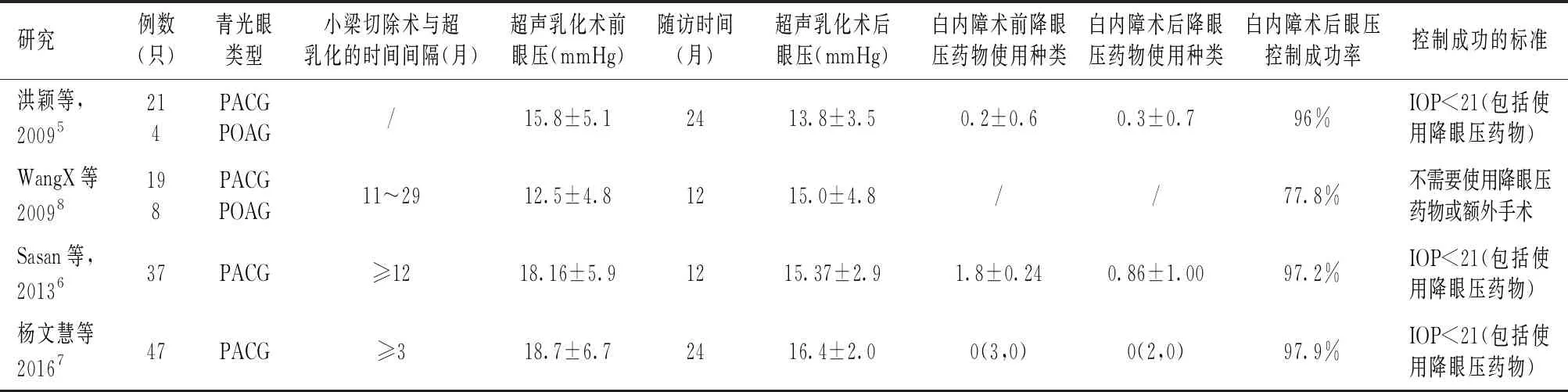
表1 以PACG为主的研究
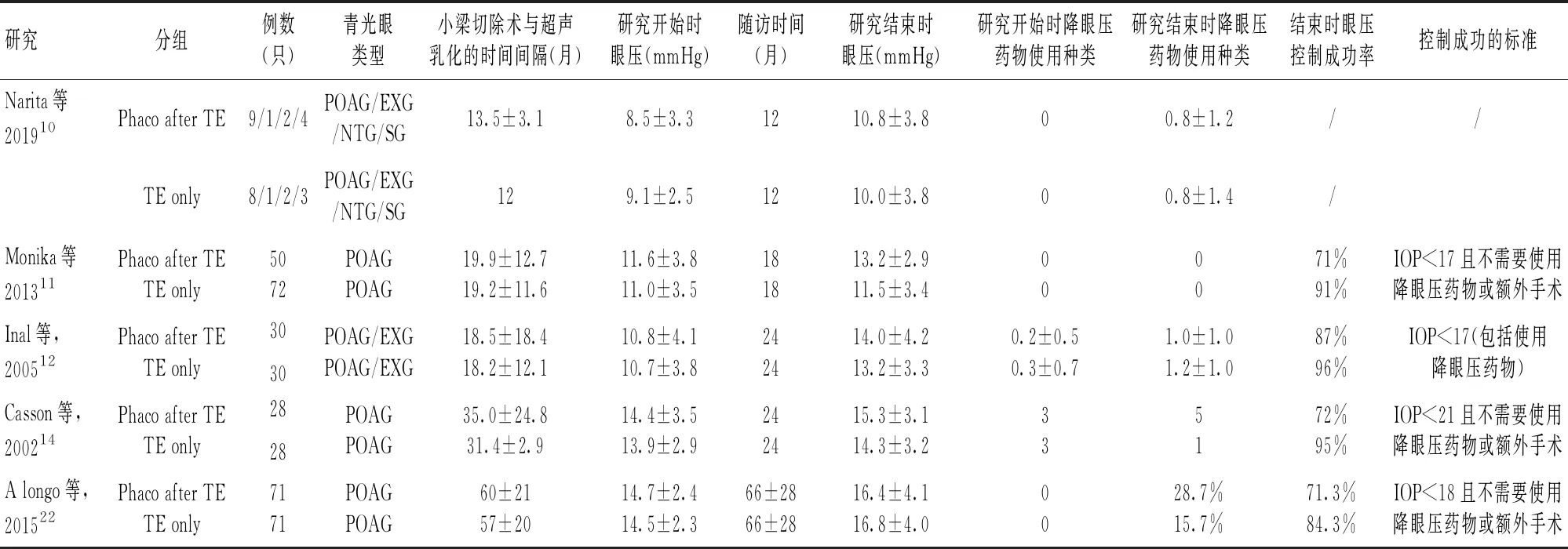
表2 以POAG为主的研究
1.炎症反应产生负面影响 白内障超声乳化手术所产生的炎症反应是对滤过泡及眼压产生负面影响的主要原因。在白内障超声乳化手术过程中,大量的液体和黏弹剂物质进入滤过泡,导致了滤过通道和滤过泡的损伤。晶状体蛋白和晶状体上皮细胞释放进入房水、超声能量的损伤,导致了房水中的炎症介质如纤维细胞因子等上调[10]。房水中的炎症介质通过巩膜瓣下的滤过通道进入结膜下,导致巨噬细胞和成纤维细胞的活化、聚集、胶原合成和沉积,最终瘢痕化,进而滤过泡失败的风险增加[18]。Siriwardena等观察到白内障超声乳化术后相较于小梁切除术后有更长时间的房水闪辉,白内障术后6个月房水闪辉情况恢复到术前基线水平,而小梁切除术只需要4周。超声乳化术后这种长期的低水平的炎症反应是滤过泡失败的危险因素[20]。
2.PACG的解剖因素带来的正面影响 对于PACG患者,一般认为白内障术后瞳孔阻滞的解除、房角开放、虹膜粘连的范围减少是这些患者眼压下降的主要原因,特别是减少了房角接触性关闭的范围[21]。这些优点抵消了白内障术后炎症反应对滤过泡的负面影响。Sasan等用房角镜观察到平均房角宽度从术前(0.31±0.51)级增加到术后1年(2.01±0.73)级(P<0.001)。作者还发现,白内障术前眼压越高、前房越浅的患者,白内障术后眼压下降幅度越大[6]。这与POAG患者的研究中,认为白内障术前眼压越高,术后滤过泡失败的风险越大这一观点恰恰相反[11,13,22]。除了与房角加宽的因素有关以外,在术前更浅的前房中,超声乳化术后囊袋皱缩对睫状体作用力的变化导致房水产生的减少[23]。
3.白内障超声乳化术对POAG的小幅度降眼压作用 白内障超声乳化手术对PACG的降眼压作用已经得到公认[24-26],有研究证明其对POAG、正常眼也有降眼压作用[26-28]。Bradford等研究了48例(55只眼)POAG、41例(44只眼)疑似青光眼及59例(59只眼)正常眼,持续随访3~5年,发现3组在白内障超声乳化手术后均有小幅度的、明确的眼压降低,其中POAG组在白内障术后3年眼压下降(1.4±4.2)mmHg (P=0.004)[27]。
4.小梁切除术的自然发展过程 有学者认为,白内障超声乳化手术对功能性滤过泡没有明显的影响,眼压控制成功率的改变与小梁切除术自身的发展过程有关,即小梁切除术本身存在一定的远期手术成功率[5,29]。结膜-巩膜或巩膜瓣交界面瘢痕过多是小梁切除术失败的主要原因[30]。同时随访时间越长的研究,更容易受小梁切除术自身发展的影响[18]。但是也有研究认为,小梁切除术后行白内障超声乳化手术,滤过泡的形态变化与单纯小梁切除术的自然发展轨迹并不相同。单纯小梁切除组在随访期间内,滤过泡随着时间的变化缓慢变平,而行白内障手术组在术后滤过泡高度陡然降低。推测与超声乳化术后的炎症反应引起睫状体产生房水减少、葡萄膜巩膜外流途径增加有关[12]。
因此,白内障超声乳化手术对于既往行小梁切除术的患者眼压产生的影响,并不是单一的因素,而是多种过程同时发生的结果[11]。
三、白内障超声乳化术后滤过泡形态的改变
Narita等(2017)使用3D AS-OCT证明小梁切除术后1年滤过泡的高度、滤过泡壁的厚度、滤过泡壁的低反射空间比例与眼压控制密切相关。较高的滤过泡、较厚的滤过泡壁和低反射空间比例大的滤过泡壁可能是功能良好的滤过泡的特征[31]。
1.滤过泡高度降低 Negrete等用裂隙灯观察了滤过泡隆起≥90°的患者,发现在超声乳化术后滤过泡高度明显降低[13]。洪颖等通过超声生物显微镜(ultrasound biomicroscopy,UBM)观察滤过泡的形态,发现滤过泡高度较超声乳化术前低,而滤过泡内反射率没有变化[5]。
2.滤过泡内高反射信号 洪颖等发现术后短期出现滤过泡的明显变小和内反射增强是眼压升高的危险因素[5]。Wang X等用UBM观察到超声乳化术后滤过泡的失败与巩膜瓣下的滤过通道不可见和滤过泡内的高反射信号明显相关[8]。
3.滤过泡形态改变的定量 Narita等(2019)通过眼前节相干光层析成像术(anterior segment optical coherence tomography,AS-OCT)检查,第一次量化了滤过泡的改变。他们发现白内障术后1年,滤过泡的最大高度下降(11.9%±17.2)%、最大壁厚下降(14.2%±21.0)%,滤过泡壁低反射空间的比例降低(27.0%±36.1)%。这反映了滤过泡功能的下降。而对照组单纯小梁切除术的患者在同样的随访时间内,OCT没有发现滤过泡在最大高度、最大壁厚及低反射空间比率的明显变化[10]。
以上的研究既有以PACG为研究对象,也有以POAG为研究对象,均发现超声乳化术后滤过泡的高度降低。超声乳化术后滤过泡形态的改变反映其功能的下降,这可能与眼压控制不良有关。
四、影响超声乳化术后滤过泡存活率的因素
不论是从手术操作的难度,还是从术前、术后对滤过泡的评估来讲,对有功能性滤过泡的眼睛行白内障手术是一种挑战。
1.术前滤过泡评分和眼压基线 超声乳化术前需要严格评估滤过泡的功能、测量术前眼压基线。白内障术前滤过泡评分与术后滤过泡存活率相关[22]。可以通过裂隙灯检查评估滤过泡级别,UBM或眼前节OCT检查判断滤过通道是否全程可见,甚至前房角镜检查判断小梁切除部位是否通畅。白内障术前眼压越高,则术后滤过泡失败的可能性越大,因为较高的眼压也反映了较差的滤过功能[12,13,22]。
2.时间间隔 滤过泡的降眼压效果随着时间推移逐渐减弱,而在这个自然过程中,行超声乳化术的时间节点将进一步改变这种影响。小梁切除术与超声乳化术之间的时间间隔越短,滤过泡失败的风险越大[30]。小梁切除术后必须至少间隔6个月再行白内障手术,因为小梁切除术后前6个月,滤过泡对炎症反应比较敏感[15]。Awai-Kasaoka等认为小梁切除术后1年内行白内障手术,滤过泡失败的风险会增加[32]。
3.术中评估和操作 超声乳化术中可以通过撕囊时染色剂/粘弹剂通过小梁切口进入结膜下的量、滤过泡高度的改变来评估滤过泡的功能[15]。同时术中要选择远离滤过泡的透明角膜切口,彻底吸出皮质和黏弹剂,尽量避免虹膜操作,因为虹膜操作破坏血-房水屏障,导致严重的炎症反应,威胁滤过泡的存活[12]。此外,手术时间、超声乳化使用的功率、白内障的分级也影响术后的炎症反应程度[30]。
4.术后注意事项 超声乳化术后需使用激素性眼药水对抗炎症反应,严密监测眼压改变和滤过泡的早期不良征兆。如果出现螺旋形血管或滤过泡包裹,可给予结膜下注射5-FU[15]。术后早期眼压峰值高于25 mmHg,也需要格外注意,眼压控制失败风险较大[33]。
五、总结
白内障超声乳化术对滤过术后POAG、PACG患者的眼压影响可能不同,对于有滤过的POAG患者,白内障超声乳化术后眼压升高,眼压控制成功率降低。而对于PACG患者,大部分研究认为超声乳化术后眼压降低。造成这样不同的结果,是由PACG的解剖结构、超声乳化术后的炎症反应、小梁切除术的自然发展过程等多种因素所致。
影响白内障超声乳化术后滤过泡的存活率的因素有很多,如超声乳化术前眼压基线、滤过泡评分,小梁切除术与白内障超声乳化术的时间间隔等。超声乳化术后早期一些不良征兆可能预示着滤过泡的失败,如眼压峰值高于25 mmHg,螺旋形血管或滤过泡包裹等。白内障超声乳化术前对滤过泡的严格评估、术中谨慎操作防止并发症、对术后早期征兆的及时干预可以提高滤过泡的存活率。

