腹腔镜与开腹胰十二指肠切除术临床疗效比较
黎官印,彭勇,何振兴,马海
(南充市中心医院 肝胆外科,四川 南充 637000)
胰腺是腹膜后器官,解剖位置深在,而且紧邻门静脉、肠系膜上动静脉等大血管,因而胰腺手术技术要求高,手术风险较大,传统成熟的开腹胰腺手术已然成为既往数十年的经典术式,但其腹部切口巨大,术后疼痛感明显,严重影响患者的康复。自从1992年国外学者Gagner首次报道了腹腔镜胰十二指肠切除术以来,胰腺疾病的微创治疗已经成为国内外专家学者的研究热点,但在随后的二十年来发展缓慢,全世界范围内报道腹腔镜胰腺手术的病例较少[1-2]。随着腹腔镜器械的不断改进,腹腔镜操作技术的不断进步,近8年来腹腔镜胰腺手术在全国乃至全世界已经经历了二次发展,目前在国内已经由大的胰腺中心或附属医院逐渐开始推广至全国各大医院。南充市中心医院肝胆外科也经历了这一阶段,从2017年开始尝试腹腔镜胰腺手术,前期经历过中转开腹,最后过渡到常规开展全腹腔镜胰腺手术。笔者整理并分析了2014年6月至2019年8月在我科开展的开腹及全腹腔镜胰十二指肠切除术共104例,比较两种术式的相关指标,现报道如下。
1 资料和方法
1.1 研究对象
回顾性收集2014年6月2019年8月在南充市中心医院肝胆外科接受胰十二指肠切除术患者的资料。纳入标准:(1)患者一般状况可,无心、肺、肾功能严重障碍,能够耐受手术;(2)肿瘤无远处转移,无血管侵犯。排除标准:(1)不能耐受手术者;(2)晚期肿瘤或恶病质者;(3)腹腔镜中转开腹。经医院伦理委员会批准,所有患者均签署知情同意书。
1.2 研究分组
根据上述纳入和排除标准,本研究最终纳入104例患者资料,根据已行的手术方式分为腹腔镜胰十二指肠切除术组(A组,n=40)和开腹胰十二指肠切除术组(B组,n=64)。入院时均行腹部增强CT或MRI评估病灶位置、大小及与周围血管脏器毗邻关系。
1.3 手术方法
1.3.1 腹腔镜十二指肠切除术组:参照彭兵《腹腔镜胰腺外科手术学》[3]手术流程,对胰头癌、十二指肠乳头癌和胆管下段癌共40例患者行腹腔镜胰十二指肠切除术,见图1。
所有患者均行气管插管全身麻醉,采取头高脚低“大”字形体位,分别于脐部做切口置入戳卡和腹腔镜镜头,两个12 mm戳卡位于左右锁骨中线,两个5 mm位于左右腋前线。行胰十二指肠切除范围包括胃的1/2左右、胆总管、胆囊、胰头、胰腺钩突、十二指肠以及周围淋巴结。所有患者手术切缘术中冰冻结果示肿瘤阴性。
重建方式:胆管和空肠行端侧胆肠吻合(肝胆管直径较细者可放入支撑管);胃与空肠行胃空肠端侧吻合;胰腺断端与空肠行胰腺空肠导管对黏膜端侧吻合。分别于肝后、胆肠吻合口处、胰肠吻合口上方、胰肠吻合口下方各放置骨科引流管一根。
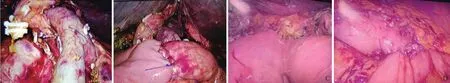
图1 术中操作图
1.3.2 开腹胰十二指肠切除术组:对胰头癌、十二指肠乳头癌和胆管下段癌共64例患者行开腹胰十二指肠切除术,所有患者同样行气管插管全身麻醉,采取平卧体位,均采用腹部正中绕脐切口,切除范围及吻合方式同腹腔镜组。
1.4 围手术期处理
术前患者常规胃肠减压和清洁肠道准备。术中常规放置经鼻空肠喂养管。术后患者常规给予奥曲肽抑制胰液分泌、质子泵抑制剂保护胃黏膜、保肝、抗感染及营养支持治疗,术后第3、7天常规复查腹腔引流液淀粉酶。
1.5 指标记录
记录患者的手术时间、术中出血量、平均排气时间、术后下床活动时间、住院时间及术后并发症发生情况。
1.6 统计学分析
采用SPSS 19.0软件进行统计学分析,符合正态分布计数资料采用(±s)表示,组间比较采用独立样本t检验;计数资料采用例数和百分率(%)表示,组间比较比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组一般情况
纳入的104例患者中,男59例,女45例;年龄40~75岁。原发疾病为胰头癌47例,十二指肠乳头癌31例,胆管下段癌26例。两组术前一般资料比较差异无统计学意义(P>0.05)。见表1。
2.2 两组临床手术疗效
两组手术时间和术中出血量无统计学差异(P>0.05),平均排气时间、术后下床活动时间及住院时间A组小于B组,差异有统计学意义(P<0.05)。见表2。
2.3 两组术后并发症情况
参照中华医学会胰腺术后外科常见并发症诊治及预防的专家共识(2017)[4],胰瘘分为生化漏、B级和C级。其中A组术后发生胰瘘5例(其中生化漏4例,B级胰瘘1例),胆漏4例,均经保守治疗后痊愈,发生腹腔内出血1例,经开腹手术止血痊愈,发生胃瘫综合征3例,经保守治疗后痊愈。B组术后发生胰瘘9例(其中生化漏7例,B级胰瘘2例),胆漏5例,均经保守治疗后痊愈,发生腹腔内出血1例,经介入栓塞止血痊愈,发生胃瘫综合征4例,经保守治疗后痊愈,余无明显严重并发症发生(P>0.05)。见表3。
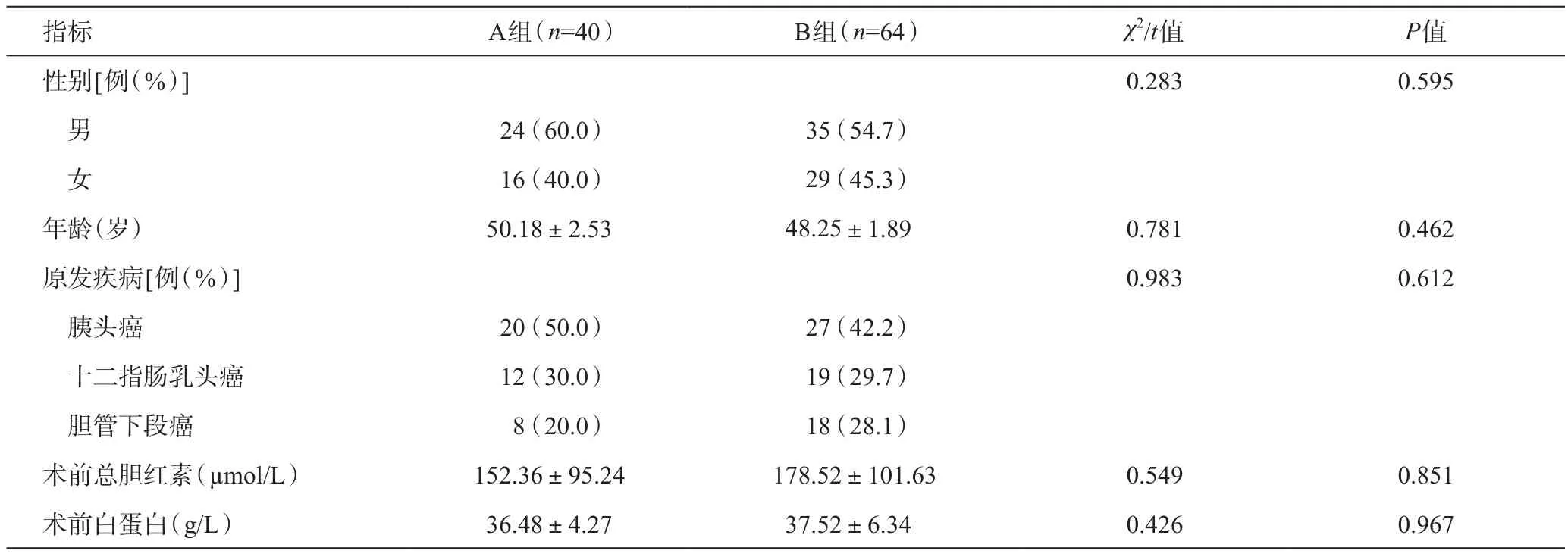
表1 两组术前一般资料比较
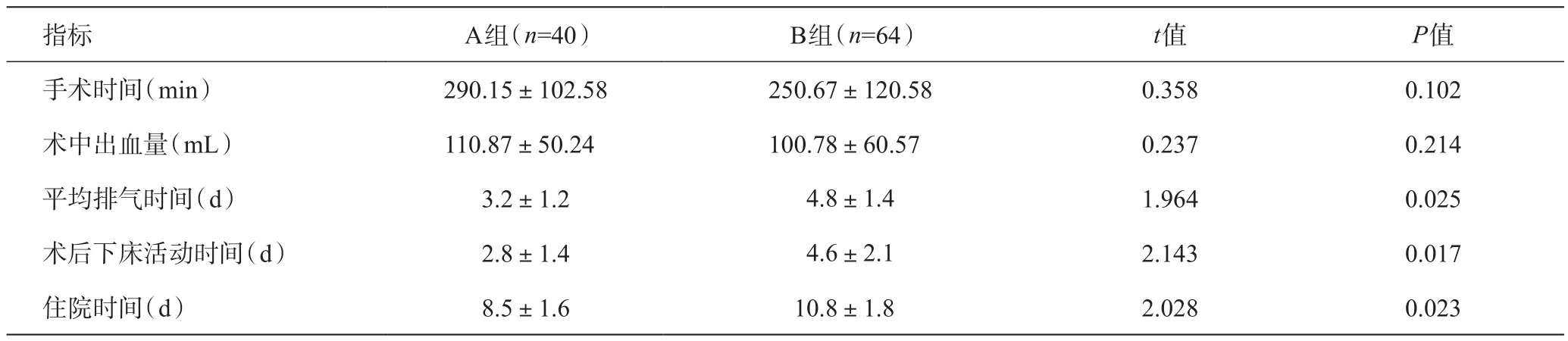
表2 两组临床手术疗效比较

表3 两组术后并发症比较[例(%)]
3 讨论
微创外科是当今时代的主题,特别是腹腔镜技术已经广泛应用于胆道外科、肝脏外科、胃肠外科、妇科、泌尿外科、心胸外科等领域[5-7],而在胰腺外科的发展显得较为缓慢。因为胰腺位于腹膜后,血运丰富,周边毗邻众多大血管及脏器,手术暴露差,难度大,风险高,因此胰腺手术历来都被认为是肝胆外科高难度、高风险的大手术之一。特别是胰十二指肠切除术,因其不仅要切除胰头、十二指肠、部分胃、部分空肠、胆总管,更需要进行三个吻合(胰肠、胆肠、胃肠),其手术时间长、手术创伤大、术后并发症发生率高。传统的胰腺开腹手术切口巨大,患者术后的疼痛感明显,带来的后果就是患者无法早期下床活动,难以达到快速康复的目的,且术后切口并发症(感染、愈合不良、切口疝等)的发生也屡见不鲜,因此胰腺微创外科已经成为当前国内外专家学者的研究热点[8-10]。追溯历史,腹腔镜用于胰腺外科最早是腹腔镜探查用于获取胰腺病理标本和评价肿瘤的可切除性,随着技术的发展,逐渐有学者报道腹腔镜用于胰腺假性囊肿内引流、重症胰腺炎坏死胰腺组织清除、胰腺内分泌肿瘤剜除、胰体尾部切除(保留或不保留脾脏)等术式[11-13]。但难度最大和最具有挑战性的还是全腹腔镜下胰十二指肠切除术。因为胰十二指肠切除术不仅包括复杂的多器官切除,还要进行三个部位吻合,因此要求的腹腔镜器械设备多、腹腔镜操作技术高,同时学习曲线时间长。但随着腹腔镜器械的不断改进和腹腔镜操作技术的进步,国内外腹腔镜胰腺外科已经从手辅助过渡到全腹腔镜下完成的阶段,特别是近8年来胰腺微创外科的第二次发展浪潮推动下不断有医院报道逐步施行甚至大量开展腹腔镜胰十二指肠切除术。目前在我国许多三甲医院已经能够常规开展胰腺外科的所有手术并且在全国范围内已经处于全面推广阶段[14-17]。
我们医院胰腺微创外科的发展也是顺应时代的发展趋势,我们从2017年开始尝试开展腹腔镜胰十二指肠切除术,经历了中转开腹到完全腹腔镜切除吻合阶段,期间也多次请专家来院指导手术,同时安排人员到上级医院学习腹腔镜胰腺手术,目前我们单位已经能够独立常规开展全腹腔镜胰十二指肠术、全腹腔镜胰体尾切除及胰腺假性囊肿空肠吻合术。我们的体会是:(1)学习并应用大中心的成熟手术流程模块:我们单位专门派人去上级医院系统性的学习了腹腔镜胰十二指肠切除术等各种胰腺手术流程,从而借鉴并运用他人的成熟手术模块,同时吸取他人的经验教训,便于自己独立开展手术时少走弯路。(2)固定的团队配合:我们最开始行腹腔镜胰十二指肠切除时将手术人员固定的分成切除组和吻合组,切除组只负责切除,吻合组专职吻合,分工明确,各司其职,便于尽快缩短学习曲线,待两组技术成熟和团队磨合熟练后再互换角色最后达到两团队均能独立完成整台手术。(3)强化基本功的训练:每位手术人员上台前均在腹腔镜模拟器上熟练掌握调针、缝合、打结等基本技能,每台手术均录像,术后反复观看手术录像,总结自己的不足并不断改进。本研究中腹腔镜胰十二指肠切除术组手术时间和术中出血量稍大于开腹组,但平均排气时间、术后下床活动时间及住院时间均小于开腹组,且差异有统计学意义。我们的腹腔镜组手术时间稍长于开腹组,分析原因为目前我院腹腔镜胰十二指肠切除术刚渡过学习曲线,积累的例数量不够,因此需要积累更多的病例以及团队配合的不断改进后才能缩短手术时间。但腹腔镜组的平均排气时间、术后下床活动时间和住院时间均较开腹组明显缩短,这正体现出腹腔镜微创外科患者能获得快速康复的优势。本组有1例腹腔镜胰十二指肠切除术后出现腹腔内出血,开腹手术探查发现是胰十二指肠下动脉出血,分析原因为术中处理胰头钩突时只是使用了Ligasure凝闭切断了胰十二指肠下动脉导致术后胰十二指肠下动脉再出血,在后来的腹腔镜胰十二指肠切除术中我们均解剖清楚血管后使用Hem-o-lock夹闭胰十二指肠下动脉后就未再出现术后出血等并发症。
综上所述,腹腔镜和开腹胰十二指肠切除术均安全有效,但腹腔镜胰十二指肠切除术后患者的恢复情况明显优于开腹手术,更能达到快速康复的目的。