伴皮质下梗死和白质脑病的常染色体显性遗传性脑动脉病1例
赵倩倩,王雅珺,孙家栋,陈娇,李雪梅
作者单位
1261000 潍坊潍坊医学院神经病学教研室
2潍坊医学院附属医院神经内科
1 病例介绍
患者女性,57岁。主因“突发右侧肢体活动不灵、言语不利13 h”于2019年1月21日至潍坊医学院附属医院门诊就诊。患者于13 h前无明显诱因出现右侧肢体活动不灵、言语不利,右上肢抬举费力、持物欠稳,不能自行站立行走,言语含糊不清,可理解他人语言,表达尚可,症状持续不缓解。急诊行头颅CT检查示:右侧基底节区、脑桥腔隙性脑梗死,脑白质疏松改变。为进一步诊治收入神经内科。
既往史:否认高血压、糖尿病、冠心病史;否认吸烟、饮酒史;否认近亲结婚史;患者父亲57岁时因“脑梗死”去世,三弟53岁患“脑梗死”,目前生活不能自理。
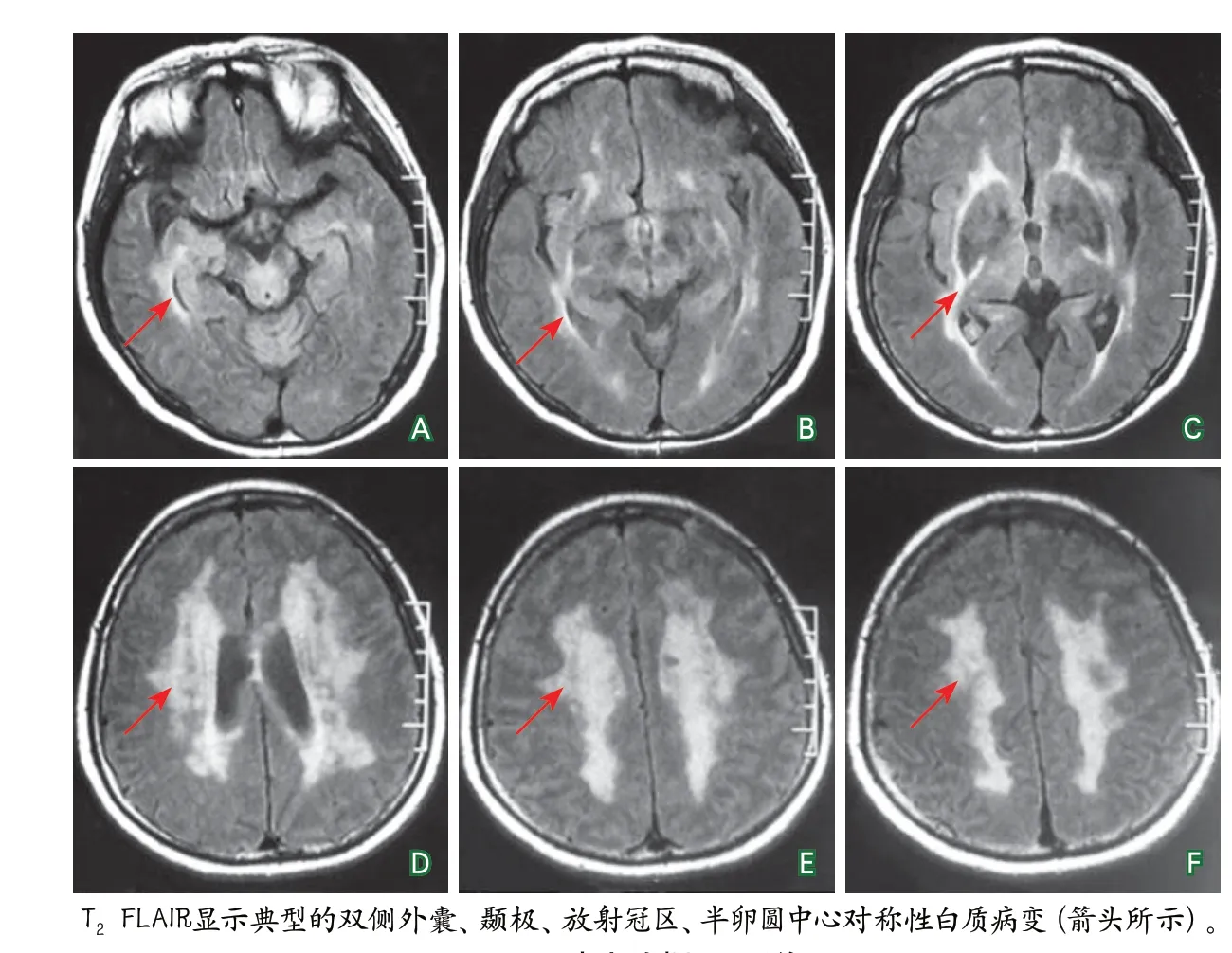
图1 患者头颅MRI影像
入院查体:血压130/80 mm Hg,双肺呼吸音清,未闻及干、湿性啰音,心率82次/分,律齐,各瓣膜区未闻及病理性杂音,腹软,无压痛及反跳痛,肝、脾肋下未触及肿大。神经系统查体:神志清楚,精神可,言语清晰度、流利度下降,无感觉性失语、运动性失语和命名障碍,咽反射正常,右侧鼻唇沟浅,伸舌偏右,右上肢肌力4级、右下肢肌力3级,四肢肌张力增高,双侧腱反射(+++),双侧Babinski征阳性,双足内翻,右侧面部及上下肢痛温觉减退。NIHSS评分6分。洼田饮水试验1级。
实验室检查:血清同型半胱氨酸22.75 μmol/L;LDL-C 3.12 mmol/L;血常规、血沉、肝功、肾功、血糖、电解质、凝血常规、甲功三项、心肌酶谱、免疫功能检测、风湿三项、抗核抗体谱、脂抗体三项、血管炎三项均未见异常。
头颅MRI(2019-01-21):双侧外囊及胼胝体、前颞极、双侧放射冠、双侧半卵圆中心高信号;脑桥、双侧额顶枕叶、基底节区、放射冠区多发腔隙性脑梗死并部分软化;双侧脑室周围脑白质脱髓鞘改变(图1)。
头颅MRA(2019-01-21):左侧大脑后动脉多发狭窄;左侧胚胎型大脑后动脉;左侧大脑前动脉A1段狭窄;脑血管动脉硬化改变。
心电图、心脏血管超声、颈部血管超声及TCD等检查(2019-01-22)均正常。
入院诊断:
多发腔隙性脑梗死
广泛脑白质病变
诊疗经过:入院后予阿司匹林100 mg/d抗血小板聚集,阿托伐他汀钙片20 mg/d稳定斑块及改善侧支循环等治疗。该患者表现为卒中样发作,影像学检查发现腔隙和白质高信号等脑小血管病的影像学标志,考虑缺血性卒中。本例患者双侧大脑半球多发脑梗死,颅脑MRA仅提示左侧血管多发狭窄,右侧大动脉未见异常,结合病灶大小、临床表现及影像检查,根据TOAST分型,考虑为小动脉闭塞导致的脑小血管病。脑小血管病种类较多,包括动脉硬化性脑小血管病、脑淀粉样血管病、伴皮质下梗死和白质脑病的常染色体显性遗传性脑动脉病(cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy,CADASIL)、伴皮质下梗死和白质脑病的常染色体隐性遗传性脑动脉病(cerebral autosomal recessive arteriopathy with subcortical infarcts and leukoencephalopathy,CARASIL)、遗传性视网膜血管病伴脑白质营养不良、Fabry病、炎性或免疫因素介导的脑小血管病等。该患者父亲和弟弟均有脑梗死病史,颅脑MRI表现为广泛脑白质病变及多发基底节区腔隙性脑梗死,无高血压、吸烟史等卒中危险因素,无反复脑叶出血、皮质微出血等其他病因证据,考虑遗传性脑小血管病可能性大。为明确诊断,入院3 d后行基因检测,结果显示NOTCH3基因外显因子EXON4,c.544C>T(p.Arg182Cys)(杂合)位点发生错义突变,该突变被HGMD收录为病理性变异位点(PMID:8878478);HTRA1基因外显子未见病理性突变。患者诊断为CADASIL。
治疗12 d后症状明显改善,可自行站立行走,步态拖曳,遂办理出院。出院查体:言语稍欠清晰、流利,右侧鼻唇沟稍浅,伸舌稍偏右,右上肢肌力5-级、右下肢肌力4+级,右侧面部及上下肢痛温觉稍减退。NIHSS评分4分。
出院诊断:
多发腔隙性脑梗死
CADASIL
2 讨论
本例患者为首次卒中发作,临床表现为失语和右侧偏瘫,极易误诊为左侧大动脉狭窄导致的大动脉粥样硬化性病变。仔细追问病史后得知其有脑梗死家族史,无导致心脑血管疾病的相关基础疾病,结合影像学检查怀疑为脑小血管病变,进一步行基因检测后确诊为CADASIL。通过本病例的逐层分析,提示对于初次发生卒中的患者,如果是非老年患者且无相关的血管危险因素,除及时行影像学检查外,还应考虑到遗传性脑血管病的可能性。
CADASIL于1977年由Sourander等[1]首先报道,临床少见,发病率为2/10万~5/10万[2],多中年起病,有明显的家族遗传倾向,多无高血压、糖尿病、高胆固醇等血管危险因素,本例患者与既往报道相符合。CADASAL的典型进程分为三个阶段,20~40岁:频发先兆性偏头痛,影像学有明确的脑白质病灶;40~60岁:缺血性小卒中反复发作、多发腔隙性脑梗死、脑白质融合灶;60岁以后:多伴有皮质下痴呆与假性延髓性麻痹。本例患者仅表现为第二进程的脑梗死症状,且为初发,临床上较易误诊。
CADASIL的初步诊断目前主要依靠影像学检查,常见的影像学表现包括:病灶多在侧脑室周围、半卵圆中心的皮质下白质病变(前颞极、胼胝体和外囊好发)对称分布,范围与疾病严重程度呈正相关,也可以出现在脑桥、中脑、胼胝体,但皮质通常不受累[3]。Wang[4]认为双侧颞叶前部高信号诊断CADASIL的敏感性和特异性均较高,分别为90%和100%。Stojanov等[3]也认为前颞叶受累较外囊受累更具特征性,可作为与其他脑小动脉病鉴别的重要指标。CADASIL患者多伴颞、顶叶和额叶白质、内囊、外囊、基底节、丘脑和脑干(脑桥为多)等部位的脑白质高信号,是该病较独特的影像学表现,本例患者的颅脑MRI的病变特点完全符合此征象。结合影像学诊断CADASIL时,需注意其与CARASIL和1型强直性肌营养不良(myotonic dystrophy type 1,DM1)鉴别。三者MRI神经影像学比较相似,但CARASIL为隐性遗传性突变,以20~30岁近亲结婚者多见,多有秃发、腰痛病史,无偏头痛和嗜锇颗粒沉积,基因检测可见10号染色体的HTRA1基因突变。CADASIL的颞叶、外囊、基底节区微出血发生率高于DM1[5]。
本例患者基因检测显示NOTCH3基因外显因子EXON4,c.544C>T(p.Arg182Cys)(杂合)位点发生错义突变,HTRA1基因外显子未见病理性突变,从而确诊。皮肤、肌肉活检发现血管平滑肌细胞表面嗜锇颗粒沉积及基因检测有NOTCH3基因突变是诊断CADASIL的金标准。Wang等[6]报道我国大陆CADASIL家系基因突变约85%发生在第4和第3外显子上,其次为第11外显子。研究表明,携带不同外显子突变的CADASIL患者其首发临床症状可能存在差异,例如第4外显子突变的患者以运动和语言障碍起病多见,本病例以右侧肢体活动不灵和言语不利起病,是典型的第4外显子突变的患者;第11外显子突变的患者以头痛起病多见,而非突变热点(第19、20外显子)突变的患者以认知障碍起病多见[7]。
CADASIL患者颅脑MRI上有特征性的脑白质病变,但其临床症状不够典型,容易与脑梗死、脑出血等相混淆,本病例以肢体活动不灵和言语不利为始发症状,因此CADSIL病例经常被忽略或误诊。本例提示对于不明原因的脑梗死、偏头痛、认知障碍等,若无常见脑血管病危险因素,颅脑MRI可见双侧对称性脑白质病变,要考虑到CADASIL的可能性,进一步行基因检测或皮肤、肌肉活检有助于明确诊断。目前尚未完善该家系其他成员的基因筛查,未来将进一步追踪随访以期建立完善的家系图谱。

