微米α-Fe2O3非均相电Fenton降解罗丹明B*
罗泽伟,潘俊洪,顾亚辉,单灼文,黎翠凤,殷旭东,王儒珍
(广东石油化工学院 环境科学与工程学院,广东 茂名 525000)
工业染料废水因具有排放量大、成分复杂、色度高、毒性强及难生化降解的特点,在治理中颇为棘手,而传统的水处理技术在处理染料废水中难以取得令人满意的结果[1,2]。电Fenton法是目前最受欢迎的高级氧化技术(AOPs)之一,该方法阴极利用溶液中的氧气进行还原反应生成过氧化氢(H2O2),与体系中的Fe2+结合发生Fenton反应,生成强氧化剂羟基自由基(·OH),对废水中多种难降解有机物进行降解处理,氧化为小分子中间体,或者完全氧化生成CO2和H2O,是一种环境友好型的处理方法[3-5]。与传统的Fenton法相比,电Fenton法可以利用电极自行产生过氧化氢,无需额外加入,避免药剂(过氧化氢)在运输和储存方面可能产生的危险,也降低废水的处理成本。然而电Fenton技术在处理废水时,反应条件苛刻,需要在较小的pH范围(pH=2~4)内进行, Fe2+在接近中性条件下极易发生水解形成沉淀,破坏反应环境,失去对H2O2的催化作用,去除效果不理想;而且,加入溶液中的Fe2+需要在降解结束后进行去除,既产生了铁泥,也增加了成本[6,7]。因此,克服pH适应范围窄、减少甚至杜绝铁泥的产生,对电Fenton体系的改进具有重要意义。
氧化铁(Fe2O3)在自然界中广泛存在,有无污染、催化性好等特性,能通过催化溶液中存在的H2O2产生大量羟基自由基(·OH)对污染物进行降解[8]。其中,微米α-Fe2O3能带间隙窄,是一种典型的n型半导体,具有较高的氧化还原电势(为2.0~2.2 eV),能通过异相电Fenton反应催化H2O2产生羟基自由基(·OH)去除有机污染物。金属氧化物作为催化剂在溶液中往往不存在离子水解的问题,因此,以固态金属氧化物作为催化剂的异相电Fenton体系不仅可能克服均相电Fenton法对pH的依赖,且对催化剂的分离回收也较易,可用来替代传统的Fe2+作为催化剂,具有良好的发展前景[9,10]。目前,α-Fe2O3催化剂与电Fenton构成的非均相电Fenton体系研究较少,为此,以自制α-Fe2O3作为催化剂,采用Ti/RuO2-IrO2电极作为阳极和阴极,对模拟废水RhB进行降解,并研究微米α-Fe2O3投加量、pH和电流密度对RhB去除效果的影响。
1 材料与方法
1.1 实验材料与仪器
材料:钛涂钌铱(Ti/RuO2-IrO2)电极;RhB(C28H31ClN2O3)、氯化铁(FeCl3·6H2O)、硫酸(98%H2SO4)、无水乙醇(C2H6O)、无水硫酸钠(Na2SO4)、氢氧化钠(NaOH),所有药品均为分析纯。
仪器:电化学工作站(DH1718E-5,北京大华无线电仪器厂);数显pH计 (PHS-25型,上海仪电科学仪器股份有限公司);紫外-可见分光光度计(UV-2500,岛津分析仪器有限公司);恒温磁力搅拌器(CJJ79-1,金坛市白塔新宝仪器厂);X射线衍射仪(UItima IV,日立理学公司);扫描电子显微镜(TM3030,日本日立公司)。
1.2 α-Fe2O3微米材料的制备
将2.7029 g FeCl3·6H2O固体溶于30 mL蒸馏水中,再加2 mol/L NaOH溶液15 mL,沉淀蒸馏水清洗8次,于50 mL NaOH(2 mol/L)溶液中分散,在磁力搅拌器下搅拌1 h。将悬浮液转入100 mL的反应釜中,置于160 ℃环境中持续反应20 h。反应结束后,用蒸馏水和乙醇对样品各洗涤3次,离心,将黄棕色固体在60 ℃条件下于烘箱中干燥,得到前驱体FeOOH。最后将FeOOH放进马弗炉中400 ℃烘焙3 h[11]。
1.3 降解实验
非均相电Fenton降解RhB的降解装置为500 mL的敞口玻璃烧杯,阳、阴极均采用50 mm×50 mm×0.1 mm Ti/RuO2-IrO2电极,极板间距为3 cm,取350 mL RhB溶液置于反应器中,为提高体系的导电能力,加2.4861 g电解质Na2SO4。反应电流为直流电源,空气流量为1.8 L/min,磁力搅拌器转速为200 r/min。
1.4 分析方法
pH采用PHS-25型数显pH计直接测定;RhB浓度采用紫外-可见分光光度法在波长554 nm处测定吸光度,根据标准曲线计算RhB的浓度[12,13];X射线衍射图谱由UItima IV衍射仪测定;外观形貌由扫描电子显微镜(TM3030)观察。
2 结果与分析
2.1 α-Fe2O3的结构标准
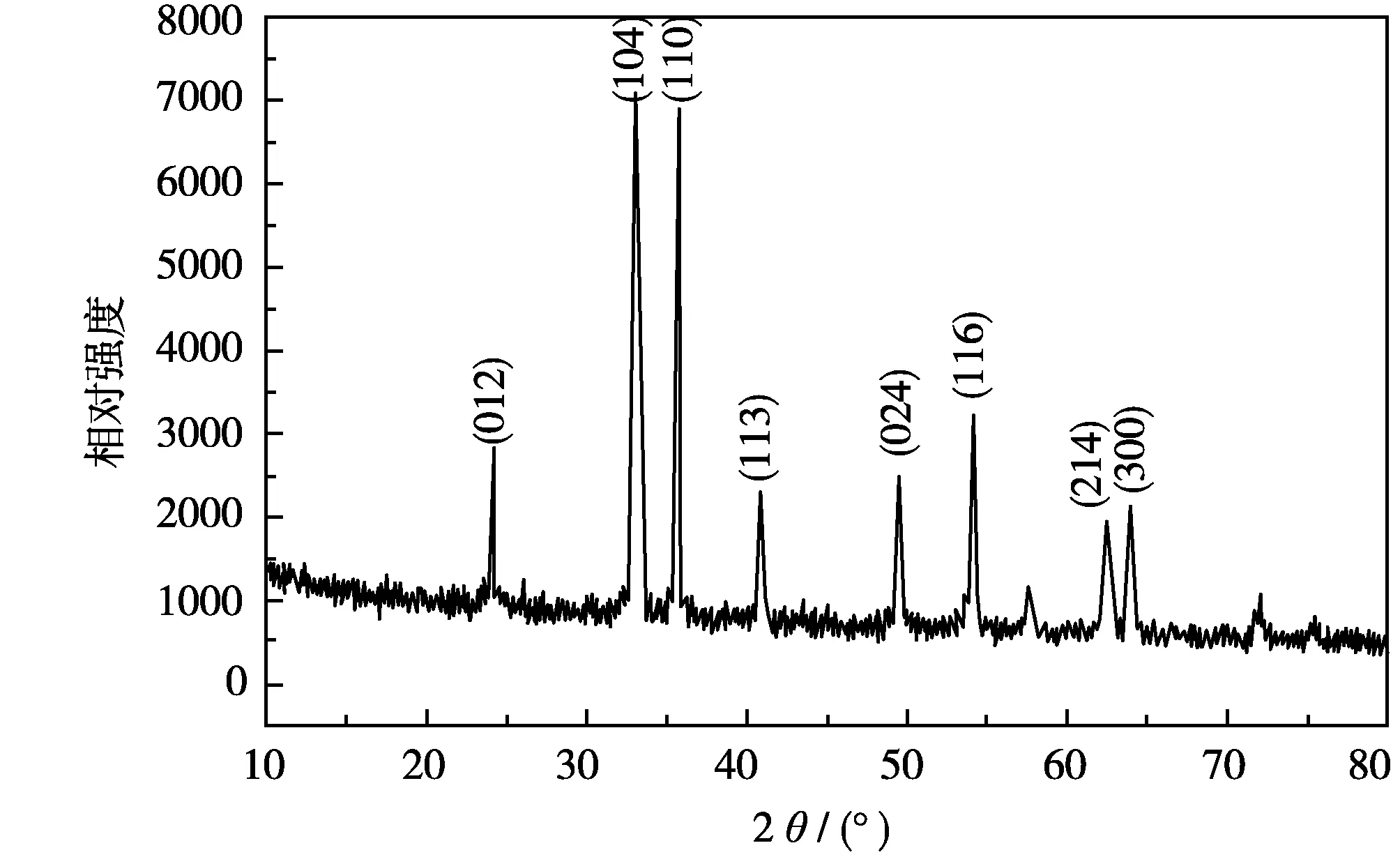
图1 α-Fe2O3的XRD分析
1)晶体结构分析。图1为160 ℃水热法合成产物的X-射线衍射(XRD)图谱(2θ为衍射角)。由图1可知,该条件下合成的产物各衍射峰位置均与标准卡片JSPDS No.33-0664的数据相符合,没有检测到其他杂质峰,表明在160 ℃条件下反应生成的产物是α-Fe2O3晶体。同时,样品的衍射峰清晰明锐,表明该条件下水热法制备的α-Fe2O3其结晶度和纯度较高。其中,在24.12°,33.16°,35.64°,40.94°,49.54°,54.20°,62.54°和63.98°分别对应(012)、(104)、(110)、(113)、(024)、(116)、(214)和(300)晶面,催化剂呈菱形晶体结构,空间结构群为R-3c(167)。
2)形貌结构分析。图2为样品的SEM图。从图中可看出:晶体大小均匀,呈棒状;样品的大致平均晶粒尺寸,长约5 μm,宽约1 μm,处于微米级别;出现α-Fe2O3晶体团聚的现象。
2.2 α-Fe2O3质量浓度对RhB去除率的影响
在RhB初始质量浓度为10 mg/L、电流密度为12 mA/cm2、pH为3.0、降解时间为60 min的条件下,考察α-Fe2O3投加质量浓度对RhB降解率的影响,结果如图3所示。
由图3可知,当α-Fe2O3投加质量浓度为0.5 g/L时,RhB去除率最高。这是因为当催化剂质量浓度过低时,其表面反应界面上的Fe(Ⅲ)不足以与过氧化氢反应转化为Fe(Ⅱ),进而无法生成足量的羟基自由基(见反应式(1)、(2)、(3))去除反应物;而当催化剂的质量浓度过高时,虽可为H2O2提供足够的活性位,产生大量的羟基自由基,但同时过量的催化剂也会对生成的部分羟基自由基产生淬灭作用,使之来不及与RhB反应[14],导致去除效果下降。只有投加适量质量浓度的催化剂α-Fe2O3,RhB去除率才能达到最高,本实验催化剂投加的最佳质量浓度为0.5 g/L。
≡Fe(Ⅲ)+H2O2→≡Fe(HO2)2++H+
(1)
≡Fe(HO2)2+→≡Fe(Ⅱ)+·HO2
(2)
≡Fe(Ⅱ)+H2O2→≡Fe(Ⅲ)+·OH+OH-
(3)
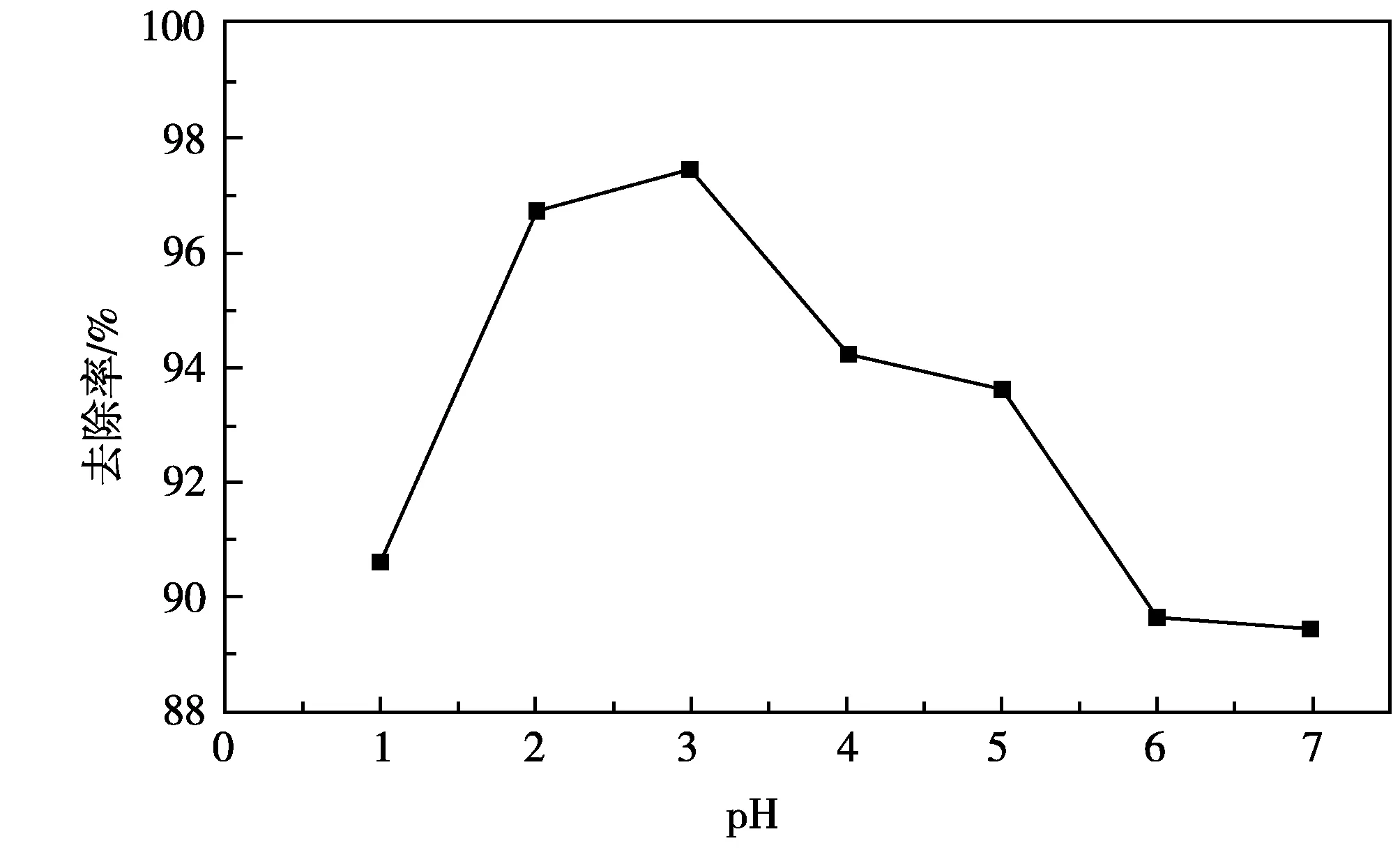
图4 pH对RhB去除率的影响
2.3 pH对RhB去除率的影响
在RhB初始质量浓度为10 mg/L、α-Fe2O3的投加质量浓度为0.5 g/L电流密度为12 mA/cm2、降解时间为60 min的条件下,考察pH对RhB降解率的影响,结果如图4所示。
由图4可知,α-Fe2O3在pH介于1~7,非均相电Fenton体系降解60 min后,RhB的去除率均达89%以上,其中pH为3.0时,降解效果最好,可以达到97.42%,说明微米α-Fe2O3的催化性能良好。当溶液中H+浓度过高时,体系对RhB的降解效果有所下降。这是因为溶液中大量的H+与H2O2结合或发生副反应(见反应式(4)、(5)),从而抑制反应(3),不利于羟基自由基(·OH)产生,阻碍污染物的降解[15]。当pH增大至中性时,RhB的降解率虽大幅下降,但仍达89%以上,远超均相电Fenton体系。这是因为催化剂α-Fe2O3基本不存在Fe(Ⅱ)水解问题,不受pH限制[16],能不断与电极产生的H2O2反应,催化形成·OH去除污染物。
2H++H2O2+2e-→2H2O
(4)
2H++2e-→H2
(5)
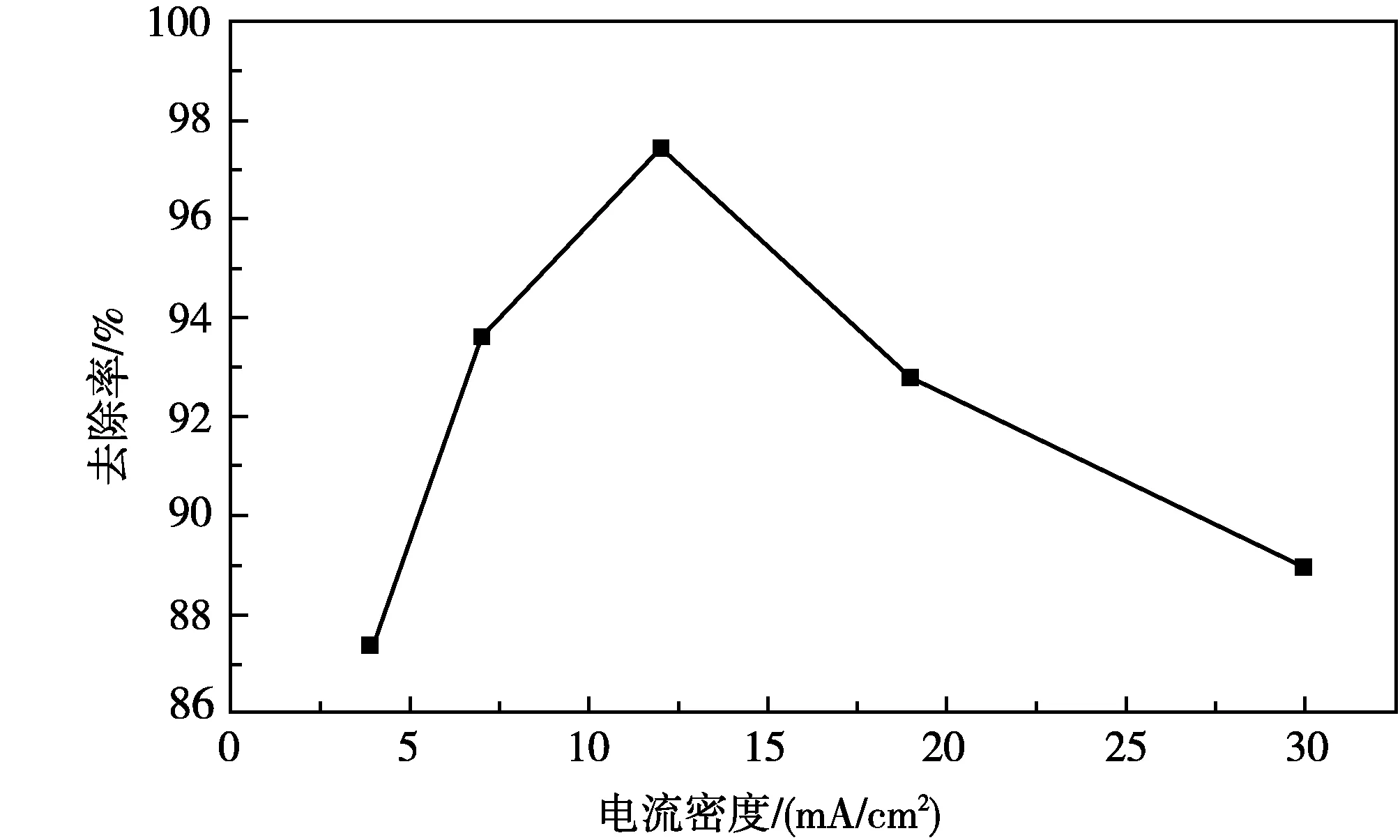
图5 电流密度对RhB去除率的影响
2.4 电流密度对RhB去除率的影响
在RhB初始质量浓度为10 mg/L、α-Fe2O3催化剂的投加质量浓度为0.5 g/L、pH为3.0、降解时间为60 min的条件下,考察电流密度对RhB降解率的影响,结果如图5所示。
由图5可知,当电流密度较小时,随着电流密度的增大,RhB的降解效果不断提高。当电流密度为12 mA/cm2时,RhB去除率为97.42%,效果最好;继续增大电流密度至30 mA/cm2时,RhB去除率反而逐渐降低。这是因为反应开始时,阴极产生的H2O2随电流密度的增大而增多,因此α-Fe2O3催化产生的·OH增多,溶液中的RhB分子被充分降解。但电流密度由12 mA/cm2增大到30 mA/cm2时,两电极间的槽电压逐渐增高,造成系统中电极的析氢、析氧副反应增加(见反应式(5)、(6)),不利于RhB的降解[17]。
2H2O2→2H2O+O2
(6)
2.5 α-Fe2O3循环使用次数对RhB去除率的影响
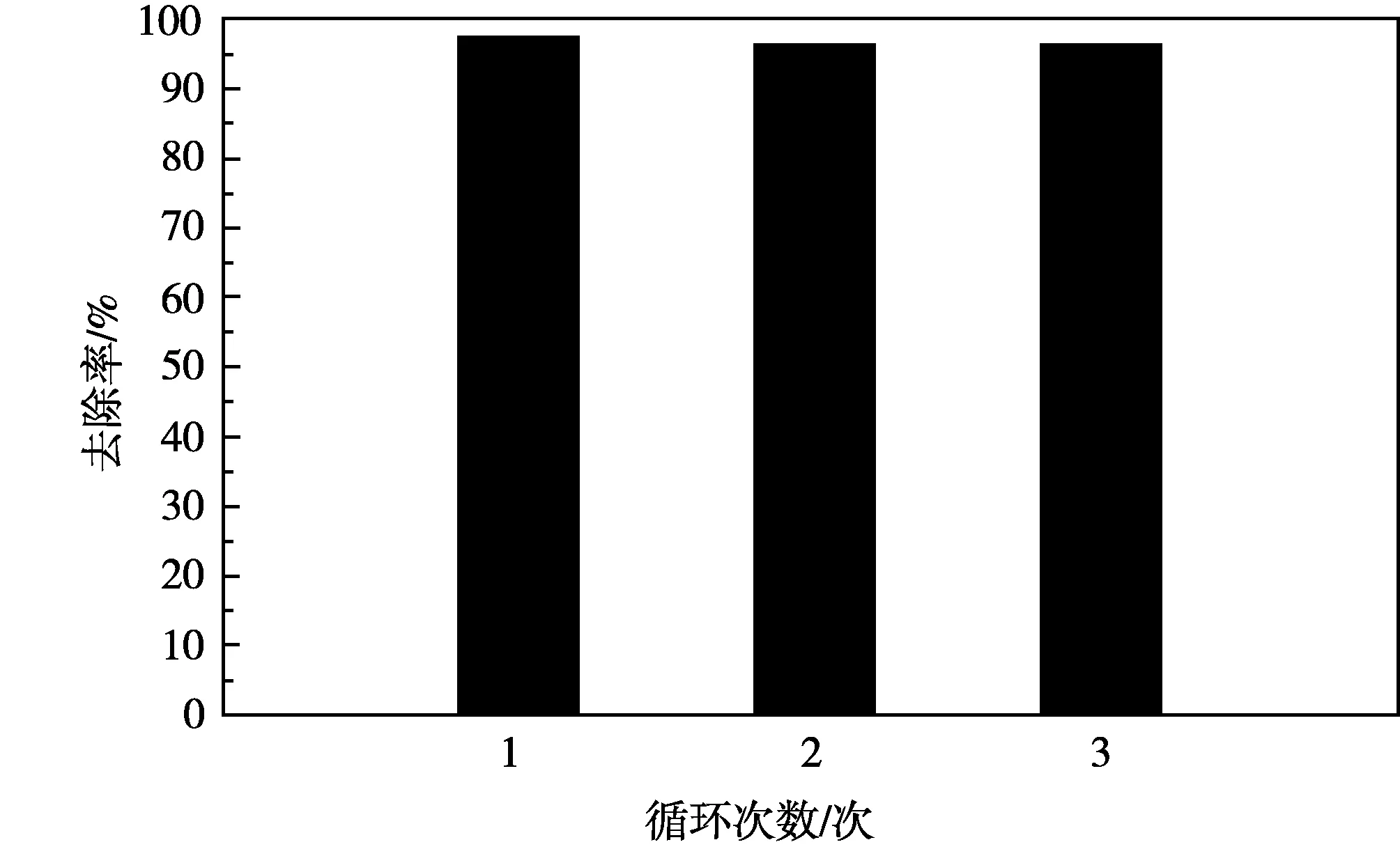
图6 α-Fe2O3循环使用次数对RhB去除率的影响
综上,实验最佳反应条件为:pH为3.0,α-Fe2O3催化剂的投加质量浓度为0.5 g/L,电流密度12 mA/cm2,对初始质量浓度为10 mg/L的RhB溶液进行降解,反应时间为60 min。在此条件下,研究α-Fe2O3循环使用次数对RhB去除率的影响,结果见图6。
由图6可知,α-Fe2O3催化剂在降解RhB循环使用的过程中表现出良好的去除效果,循环使用3次后,其催化效果与原来相比仅有微弱降低。这可能与催化剂表面吸附有机分子导致表面活性位点减少有关,但仍可以保持95%以上的去除率,表明α-Fe2O3具有较好的稳定性。
3 结论
(1)采用非均相电Fenton法(α-Fe2O3)处理RhB废水,研究了α-Fe2O3投加质量浓度、pH和电流密度对RhB降解效果的影响。实验结果表明,经优化后得到最佳反应条件为:微米α-Fe2O3投加质量浓度为0.5 g/L,pH为3.0,电流密度为12 mA/cm2。在此条件下反应60 min,微米α-Fe2O3非均相电Fenton体系对RhB的去除率可达97.42%。而循环使用实验表明,α-Fe2O3微米颗粒具有较好的催化稳定性,循环使用3次后,仍可以保持95%以上的去除率。
(2)当pH为1.0,5.0和7.0时,微米α-Fe2O3非均相电Fenton体系对RhB降解率分别为90.59%、93.62%和89.42%。表明该体系对RhB在较宽的pH范围内均具有高的降解效率,是较为理想的非均相电Fenton处理体系。

