具有抗蛋白附着和再矿化功能的复合树脂的初步研究
梅 美,杨 巍,马永刚,张 宁
由于复合树脂材料美学和力学性能的改进,近年来广泛应用于修复牙体缺损。填料成分和树脂基质的进步改善了复合树脂的性能[1]。研究表明,复合树脂材料表面较其他修复材料更容易堆积菌斑[2]。菌斑产酸引起继发龋,是充填材料脱落的主要原因[3]。唾液蛋白吸附于复合树脂表面形成获得性膜,是形成菌斑的先决条件[4]。如果复合树脂具有抗蛋白附着功能,则可以有效地限制菌斑的形成和继发龋的发生。甲基丙烯酰氧乙基磷酸胆碱(2-methacryloyloxyethyl phosphorylcholine,MPC)是一类常见的具有抗蛋白附着和细菌粘附功能的生物复合物,已经被广泛应用于临床[5-6]。磷酸钙复合树脂是另一类改性复合树脂材料的代表,其可以释放超饱和态的钙、磷离子使牙体硬组织的病损区域发生再矿化。通过雾化干燥技术合成的无定形磷酸钙纳米颗粒(nanoparticles of amorphous calcium phosphate,NACP)的粒径大小仅有100 nm左右。NACP释放的钙、磷离子与传统的磷酸钙复合体相似,但是具有更优的机械强度及性能[7]。本研究将MPC和NACP添加到复合树脂中,从而研发出一种具有抗蛋白和再矿化功能的复合树脂,并研究其对力学性能和菌斑生物膜的影响。
1 材料和方法
1.1 含有MPC和NACP的复合树脂的制备 使用雾化干燥技术合成NACP。将碳酸钙(美国Fisher公司)和无水磷酸氢钙(美国Baker Chemical公司)溶解到乙酸中,以获得终浓度分别为8 mmol/L和5.333 mmol/L的钙离子和磷离子。Ca/P摩尔比为1.5,与无定型磷酸钙(amorphous calcium phosphate,ACP)中一样。将此溶液喷入到加热的喷雾干燥装置中,通过静电沉淀器收集干燥的ACP纳米颗粒(美国Air Quality公司),获得平均粒径为116 nm的粉末状NACP。双酚A-甲基丙烯酸缩水甘油酯和双甲基丙烯酸二缩三乙二醇酯(美国Esstech公司)按照质量分数比为1∶1混合,并混入0.5%的光引发剂樟脑醌(camphorquinone,CQ),从而构成树脂基质[8]。根据以往研究,MPC(美国Sigma-Aldrich公司)粉末以质量分数为10%的比例混入树脂基质中[9]。树脂基质与NACP,以及经过硅烷化处理的无机填料(美国Caulk/Dentsply公司)按照质量分数比为3∶2∶5混合[7-8]。添加MPC和NACP的复合树脂作为实验组,商品化的复合树脂Heliomolar(加拿大Ivoclar公司)作为对照组,根据商品说明,其树脂基质成分与实验组相同。
1.2 力学性能的测试 应用模具将复合树脂制成尺寸为2 mm×2 mm×25 mm的长方形试件。每个试件每个表面光固化1 min。试件在37 ℃蒸馏水中浸泡1 d后,使用万能材料测试机(美国MTS公司)进行三点弯曲试验[9-10]。跨度为10 mm,以1 mm/min的速度加力直到试件断裂。弯曲强度按照公式3PmaxL/(2bh2)计算,其中P为断裂时的载荷,L为跨距,b为试件的宽度,h为试件的厚度。弹性模量按照公式(P/d)[L3/(4bh3)]计算,其中d为线性弹性区域的斜率。每组6个试件。
1.3 抗蛋白附着性能的测试 对于抗蛋白和抗菌性能的测试,每个试件制成直径10 mm、厚2 mm的圆柱型试件,制作时两面用赛璐珞条形成光滑表面。每个试件每个表面光固化1 min,然后将试件浸入蒸馏水,搅拌1 h,以除去任何未固化的单体[9]。所有试件干燥并用环氧乙烷消毒(型号Anprolene AN 74i,美国Andersen Products公司)。
双辛丁酸法测试试件表面蛋白的附着量[5-6,9]。每个试件在磷酸盐缓冲液(phosphate buffered saline,PBS)中浸泡2 h,然后再将试件浸泡在浓度为4.5 g/L的牛血清蛋白溶液中(美国Sigma-Aldrich公司),在37 ℃条件下浸泡2 h。将试件在PBS中漂洗5 min,然后将试件放入含有1%十二烷基硫酸钠的PBS溶液中,超声振荡20 min[5-6,9]。应用蛋白质分析试剂盒(美国Fisher Scientific公司)测试PBS溶液中的蛋白质浓度,从而计算附着在试件表面的蛋白质的量。每组6个试件。
1.4 人唾液的收集和菌斑生物膜的形成 经患者知情同意,签署知情同意书。选择10名拥有天然牙列,无活动性龋病或牙周病的健康成年人作为唾液的捐赠者。捐赠人在过去的3个月内没有使用过抗生素,捐赠唾液前24 h不刷牙,并在捐赠唾液前至少2 h禁饮食。捐赠者在咀嚼封口膜的过程中收集分泌的刺激性唾液,并置于冰上。从每位捐赠者的唾液样本中取出等量的唾液混合,混合的唾液在无菌甘油中稀释至终浓度为70%,储存于-80 ℃[11],用于体外培养人全菌菌斑生物膜。
混合唾液以1∶50的比例稀释于McBain培养基中作为人全菌生物膜的接种液。McBain培养基中含有粘蛋白,2.5 g/L;细菌蛋白胨,2.0 g/L;胰蛋白胨,2.0 g/L;酵母提取物,1.0 g/L;氯化钠,0.35 g/L;氯化钾,0.2 g/L;氯化钙,0.2 g/L;盐酸半胱氨酸,0.1 g/L;血红素,0.001 g/L;维生素K1,0.000 2 g/L,材料均购自美国Sigma-Aldrich公司,pH值调整为7[12]。24孔培养板每个孔放入1个试件,各孔中加入1.5 mL接种液,在37 ℃含5%CO2的培养箱中培养8 h。然后将试件转移至新的24孔板中,用新鲜McBain培养基继续培养16 h。将试件转移至新的24孔板中用新鲜McBain培养基继续培养24 h,最终得到培养2 d的生物膜[9]。
1.5 生物膜活/死细菌染色 将培养2 d的试件在PBS中轻柔漂洗3次,用活/死细菌生存力试剂盒(美国Molecular Probes公司)进行染色[8-9]。Syto 9将活细菌染色,产生绿色荧光;细胞膜受损的细菌会被碘化丙啶染色,产生红色荧光;接近或重叠的死/活细菌会显示出橙黄色。使用荧光显微镜(型号TE2000-S,日本Nikon公司)观察染色的生物膜。每组6个试件,每个试件随机选取3副图,每组试件一共18副图。
1.6 菌落形成单位(colony forming unit,CFU)计数 将培养2 d的菌斑生物膜圆形试件转移到2 mL试管中,通过超声震动收获生物膜,再用涡旋混合震荡仪(美国Fisher公司)混匀。使用3种琼脂平板培养测定CFU:①用胰蛋白大豆血琼脂培养板进行全菌测定[12];②用含有15%的蔗糖的轻型唾液链球菌琼脂(mitis salivarius agar,MSA)培养板来进行总链球菌测定[13];③致龋性的变形链球菌对杆菌肽有抗药性,杆菌肽常被用来从口腔菌群中分离变形链球菌[12],用加0.2 U/mL的杆菌肽的MSA琼脂培养板中来测定变形链球菌。

2 结果
2.1 力学性能和蛋白附着量比较 实验组和对照组间的力学性能比较差异无统计学意义(P>0.05);实验组的蛋白附着量显著低于对照组(P=0.000),大约是对照组的10%。表1。
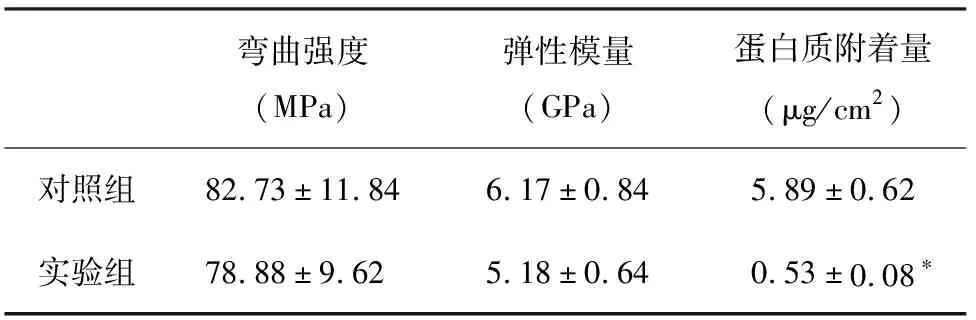
表1 2组试件力学性能和蛋白附着量比较(n=6)
注:与对照组比较,*P<0.05
2.2 CFU计数比较 与对照组比较,实验组的全菌、总链球菌和变形链球菌的CFU计数均降低了约7倍,差异比较具有统计学意义(P<0.05),表2。
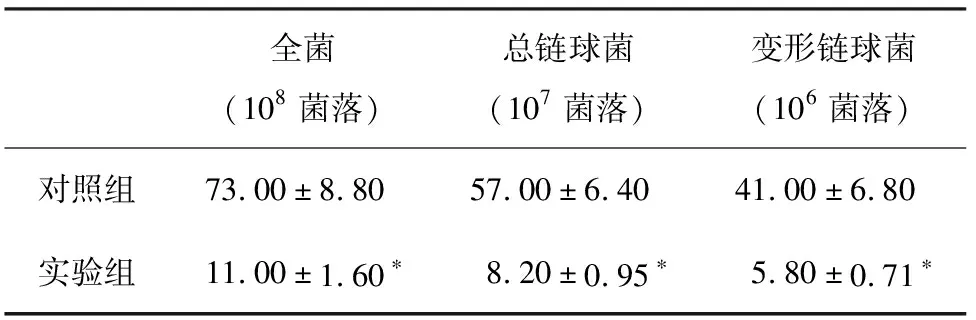
表2 2组试件CFU计数比较(n=6)
注:与对照组比较,*P<0.05
2.3 表面细菌粘附的定性比较 对照组表面覆盖大量活细菌,呈绿色荧光,实验组虽然表面也呈绿色荧光,但是含量明显低于对照组,图1。

图1 菌斑生物膜活/死细菌染色图(n=6)
3 讨论
口腔生物膜模型可以分为单一菌种、特定的混合菌和全菌模型3组[11]。从口腔环境中复制出来的全菌生物膜基本保持了口腔内菌斑生物膜的复杂性和异质性[12]。人唾液微生物中,链球菌在龋病发生发展过程中起了重要的作用。口腔链球菌包含多种菌群,如变形链球菌群、唾液链球菌群等。许多研究已经表明,变形链球菌是龋齿的主要致病菌[12]。变形链球菌组包含变形链球菌和远缘链球菌等,都是重要的致龋菌。因此,体外培养口腔全菌生物膜,研究抗菌材料对菌斑生物膜的影响,对评价材料的性能及其临床应用前景非常重要。
本研究将MPC和NACP添加到复合树脂中,对其力学性能、抗蛋白附着和抗细菌粘附效果进行了评价。结果表明,与对照组比较,实验组在不影响复合树脂力学性能的前提下,显著降低了蛋白附着量和细菌粘附量,因此添加了MPC-NACP的复合树脂能够有效减少蛋白质的附着和细菌的粘附,从而抑制菌斑形成,能够有效的对抗继发龋。
菌斑是引起继发龋的主要原因[3],而蛋白质的附着是细菌粘附和菌斑形成的先决条件[4]。因此,赋予复合树脂抗蛋白附着功能可以有效地减少菌斑的形成。MPC具有较强的抗蛋白附着和抗细菌粘附的功能,其原因是由于MPC具有很强的亲水性,在含水的MPC聚合物中有大量的游离水,而没有结合水。结合水会导致蛋白质的附着,而游离水可以有效地抵抗蛋白质的附着[5-6]。本研究结果显示,含有MPC的复合树脂具有较强的抗蛋白附着功能,其蛋白质附着量约为对照组的10%。蛋白质是细菌粘附的媒介[4],由于实验组显著降低了蛋白质附着量,因此也明显减少了细菌的附着。本研究结果显示,与对照组相比,实验组的全菌、总链球菌和变形链球菌的3个CFU计数均降低了约7倍。生物膜活/死细菌染色显示,实验组表面粘附的细菌量明显低于对照组。
研发具有再矿化功能的磷酸钙复合树脂是对抗继发龋的另一个有效途径。传统的磷酸钙填料粒径在1~55μm。这类复合树脂能够释放钙、磷离子,
使病损牙体组织再矿化。雾化干燥技术合成的NACP具有高的比表面积,粒径约为100 nm。由此产生的纳米复合树脂能释放大量的钙、磷离子,同时机械强度是传统磷酸钙复合树脂的近2倍。NACP复合树脂有一定的“智能性”,它在酸性环境里会大量释放出钙、磷离子,也就是在牙最需要钙、磷离子以对抗细菌产酸和防止龋坏发展的钙、磷离子最佳释放时机。将NACP复合树脂浸泡在pH值为4的酸性溶液里,它将会迅速中和酸,将pH值升高到6左右的安全范围内,而成品的复合树脂修复材料不会对pH值为4的酸性环境发生任何影响[7-8]。本研究同时添加MPC和NACP到复合树脂中,能够起到抗蛋白附着,抗细菌粘附,中和酸和促进再矿化的作用。这种添加双重有效成分(MPC是抗蛋白附着成分,NACP是再矿化成分)的方法具有广泛的应用前景。

