R-FPD方案治疗初治原发中枢神经系统淋巴瘤的前瞻性研究*
高凤华 张旭东 张明智 吴晶晶
原发性中枢神经系统淋巴瘤(primary central ner⁃vous system lymphoma,PCNSL)主要发生于大脑、小脑、脑干、软脑(脊)膜、脊髓和眼,而无全身其他淋巴结和淋巴组织浸润的非霍奇金淋巴瘤(non-Hodg⁃kin's lymphoma,NHL),为一种罕见的浸润性、多源性恶性肿瘤,约占原发中枢神经系统恶性肿瘤的2%~3%,在所有NHL中不足1%[1]。由于其独特的发生部位和侵略性生物学行为,临床表现较为复杂,诊断和治疗比较困难。恶性淋巴瘤在中国常见恶性肿瘤中位居第8 位,发病率的逐年攀升已引起广泛关注[2]。新诊断的PCNSL 患者如未经治疗,中位总生存期(median overall survial,mOS)仅1.5~3.3 个 月[3]。PCNSL 的高死亡率为当前临床治疗的难点。探寻安全且有效的治疗方式来延长PCNSL患者的生存时间并改善其生存质量为研究热点。
1 材料与方法
1.1 病例资料
分析2018 年7 月至2019 年7 月郑州大学第一附属医院确诊的初治PCNSL患者。前瞻性研究入组初治PCNSL 患者:年龄为14~75 岁;KPS 评分≥40 分或ECOG 评分≤2 分;预计生存期≥3 个月;CD20 阳性;经组织活检病理学确诊的PCNSL(局限于脑、脊髓、脑脊膜和眼部,不伴有全身其他部位受累的淋巴瘤);无化疗禁忌证(血象及生理检查结果时间<7天);根据RECIST 1.1标准至少有1个可测量病灶;无与本方案相冲突的其他严重疾病;有随访可能;接受此治疗期间不同时使用其他抗肿瘤药物,可以应用双磷酸盐抗骨转移治疗及其他对症治疗;能理解本研究的情况并签署知情同意书。病理组织学须经省级医院以上病理专家会诊。该研究在郑州大学第一附属医院科研和临床试验伦理委员会注册(编号:SS-2019-035)。在Clinical Trials.gov 网站临床试验注册处注册(编号:NCT04083066)。所有患者或监护人在参与该研究之前均签署知情同意书。
1.2 方法
1.2.1 研究设计 采用前瞻性、开放性、单臂、单中心临床研究设计,所有患者均接受利妥昔单抗联合福莫司汀、培美曲塞、地塞米松方案(R-FPD)治疗:利妥昔单抗375 mg/m2,d0,溶于0.9%NS浓度1 mg/mL微量泵泵入4 h;福莫司汀100 mg/m2,d1,溶于250 mL 5%GS静脉滴注,避光;培美曲塞600 mg/m2,d1,溶于100 mL 0.9%NS静脉注射;地塞米松40 mg d1~5,溶于100 mL 5%GS静脉滴注。利妥昔单抗前应用甘露醇(125 mL,25 mg)。化疗期间鞘内注射化疗药物,细胞学阴性鞘注MTX 12 mg+Ara-C 50 mg+Dex 5 mg,第2天1次,共4次。细胞学阳性鞘注MTX 12 mg+Ara-C 50 mg+Dex 5 mg,d2和d7各1次,共8次。21 d为1个化疗周期,第2、4个周期结束后进行评价疗效,并记录不良反应。化疗4个周期后完全缓解(complete response,CR)者若年龄<60岁,在化疗结束后给予巩固性全脑放疗(whole-brain radio⁃therapy,WBRT)30 Gy或自体造血干细胞移植(autologous stem-cell transplantation,ASCT),若年龄≥60岁采取观察等待;化疗4个周期结束后未达CR的患者无论年龄均给予挽救性WBRT 30 Gy+肿瘤局部索野照射达45 Gy。
1.2.2 疗效评价 采用2005年国际淋巴瘤协作组制订的“PCNSL治疗评价标准”,分为CR、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),计算客观缓解率(objective response rate,ORR),ORR=CR%+PR%和疾病控制率(disease control rate,DCR),DCR=CR%+PR%+SD%。
1.2.3 随访 通过电话进行定期随访,并记录随访结果,以死亡或者失访为终点事件,随访截至2019年9月15日。总生存期(overall survival,OS)为记录患者从确诊至因任何原因引起死亡的时间或末次随访时间,无进展生存期(pression free survival,PFS)为记录患者从确诊到疾病进展、死亡或新治疗开始的时间。
1.3 统计学分析
采用SPSS 22.0 软件进行统计学分析。应用Ka⁃plan-Meier 法计算生存曲线。以P<0.05 为差异具有统计学意义。
2 结果
2.1 临床特点
本研究共纳入12 例患者,其中男性5 例,女性7例,中位年龄为57(46~71)岁。病理类型均为CD20阳性的弥漫性大B 细胞淋巴瘤(diffuse large b cell lymphoma,DLBCL);12 例PCNSL 患者中,5 例首发症状表现为颅内压增高(头痛、恶心和呕吐),神经精神症状如记忆力下降、行为异常3 例,局灶性神经系统损害体征包括语言表达障碍、肢体无力3 例,大小便失禁1 例。头颅MRI 或PET-CT 示单一病灶患者3例,多累及额叶、顶叶,另外9 例累及脑深部结构、胼胝体和小脑。全部患者接受腰椎穿刺,8例行脑脊液细胞学检查发现阳性。免疫组织化学:Bcl-2、Bcl-6、MUM-1和CD20均全部阳性(表1,2)。
2.2 疗效评价
治疗2个周期后评价ORR为91.7%(11/12),10例PR,1例CR,1例PD,无SD,DCR为91.7%(11/12);4个周期评价ORR为66.7%(8/12),6例CR(图1,2),2例PR,3例PD,1例SD,DCR为75%(9/12)(表3)。12例患者随访半年,5例CR,2例PR,1例SD,4例PD。中位无进展生存期(median PFS,mPFS)为7个月(95%CI:4.4~9.6个月),mOS为10.5月(95%CI:6.1~14.9个月)(图3,4)。c-myc≤40%和c-myc>40%患者的mPFS分别为6.0个月和8.7个月,差异无统计学意义(P=0.759)。
2.3 R-FPD方案不良反应
12例患者经R-FPD方案化疗后的不良反应主要包括骨髓抑制、胃肠道反应和感染。长期化疗后,患者出现不同程度的骨髓抑制症状,其中Ⅲ~Ⅳ级白细胞减少2例,中度血红蛋白减少1例,血小板减少3例,可通过停药或对症治疗来消除或缓解骨髓抑制。因粒细胞缺乏合并重症肺部感染1 例。胃肠道反应主要表现为恶心、呕吐,Ⅱ级症状2例,通过接受护胃和止吐药物可缓解症状。Ⅲ~Ⅳ级级肝功能损伤1例,其他反应包括头痛5例、便秘2例、乏力3例、周围神经系统症状5例,无明显肾毒性。特定不良反应见表4。
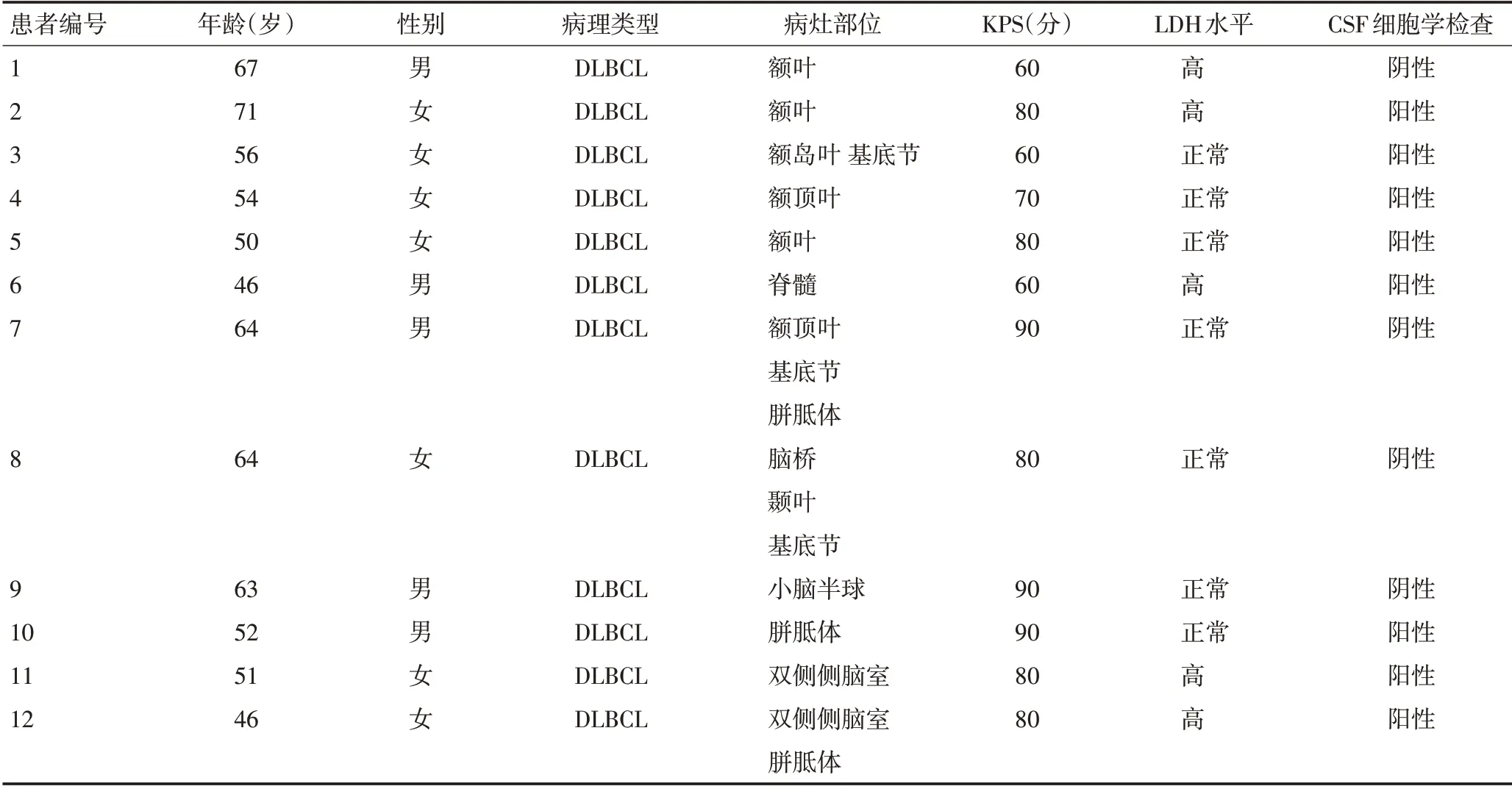
表1 12例患者的临床及疾病特征
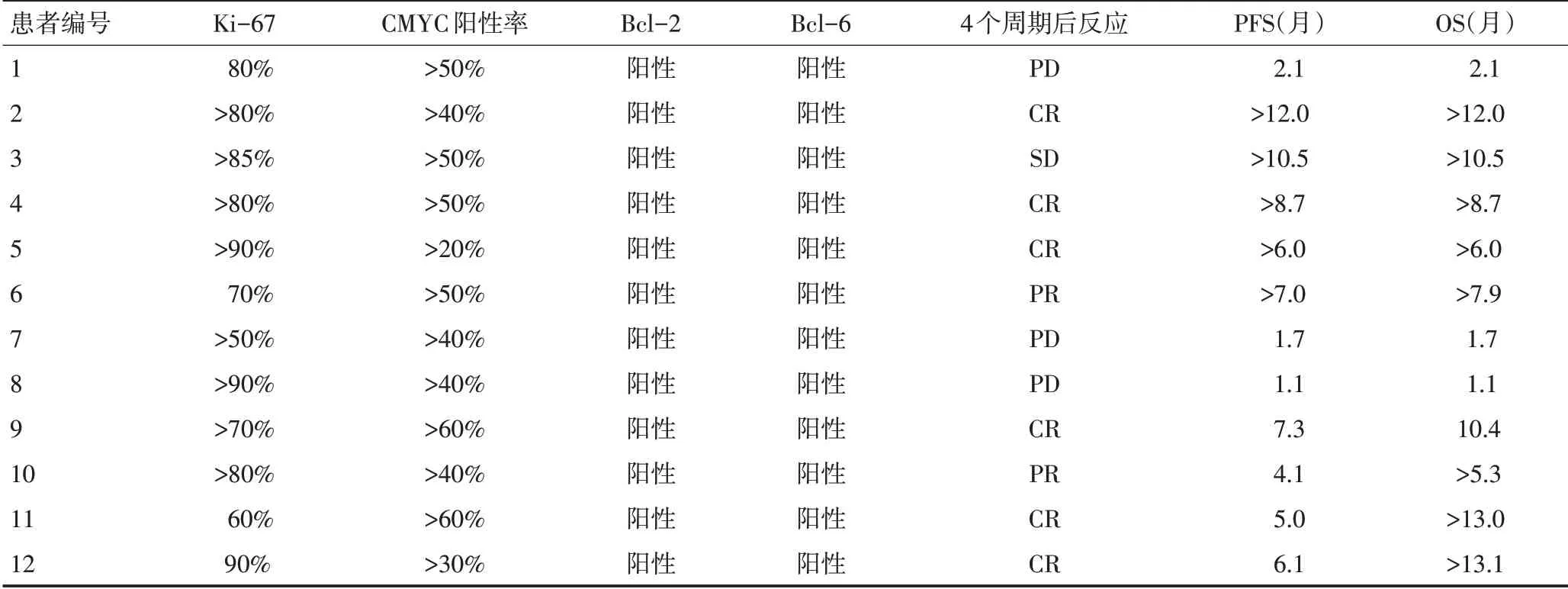
表2 12例患者的治疗反应
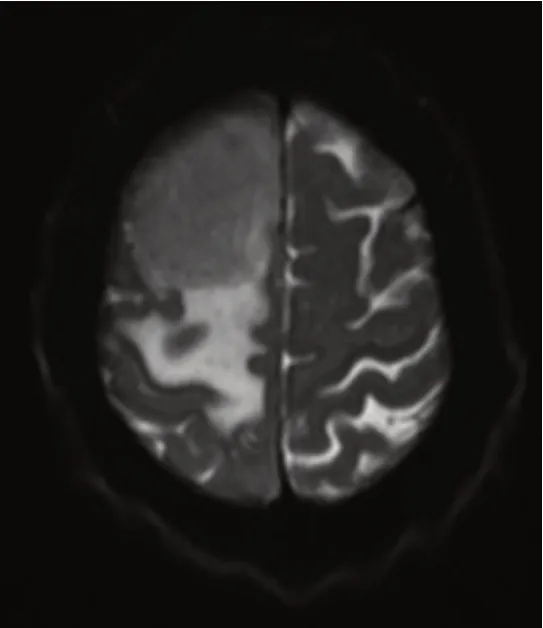
▶图1 右侧额顶叶区淋巴瘤患者治疗前MRI图像

▶图2 治疗后4 个周期后患者MRI示肿瘤消失

表3 12例患者接受2、4个周期治疗后的疗效评价
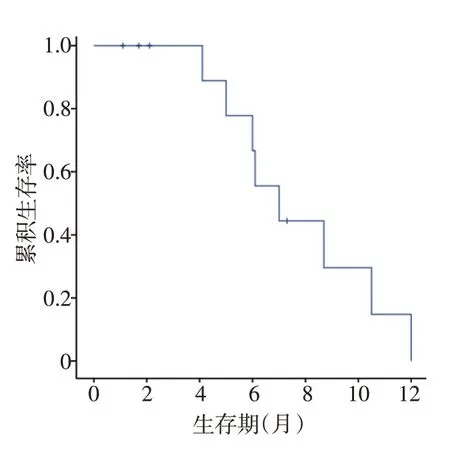
图3 R-FPD方案治疗PCNSL患者的PFS

图4 R-FPD方案治疗PCNSL患者的OS
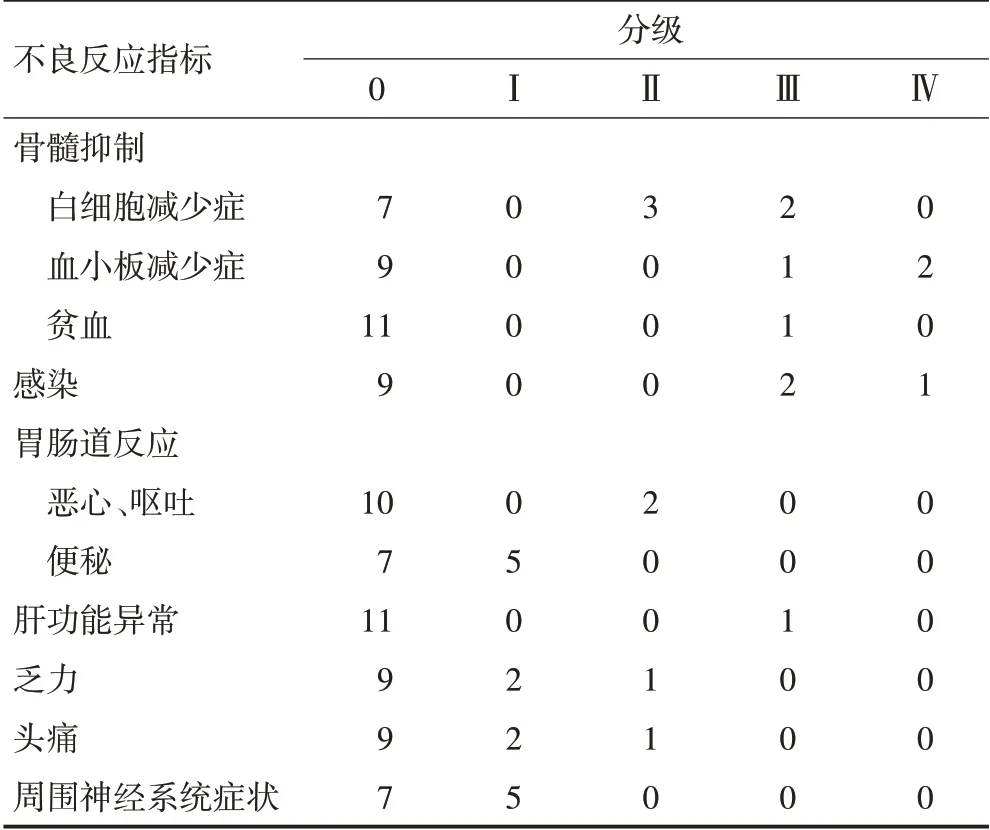
表4 12例患者R-FPD化疗后的不良反应发生情况 例
3 讨论
PCNSL 的诊治较为困难,且预后较差,近几年来发病率呈明显上升趋势,面临着较大的挑战。免疫缺陷为PCNSL发病的高危因素之一,约2%~6%艾滋病病毒感染者发生PCNSL,发病率远高于正常人群[4]。老年患者中PCNSL的发病率持续上升,提示目前大部分患者来自免疫正常的人群。Shiels等[5]分析4 158例PSNCL患者,中位年龄67岁。本研究患者中位年龄57 岁,差异可能与入组患者例数较少有关。病理类型与发生部位与国内研究类似[6]。
目前,PCNSL 尚无标准一线治疗方案,常规化疗选择能够透过血脑屏障(blood brain barrier,BBB)以HD-MTX为基础的联合化疗[7-8]。大宗病例回顾性分析表明[9],PCNSL 未治疗者中位生存时间仅1.5~3.3个月,接受综合治疗者5 年OS 为25%~42%。提示PCNSL 的预后差,生存期短。Roth 等[10]报告基于HD-MTX 的化疗,ORR 为44%,PFS 为4 个月,OS 为12.5个月。不良反应明显,Ⅲ~Ⅳ级粒细胞减少症达34%,治疗相关死亡率达18%,该研究提示,在老年患者中,以HD-MTX为基础的方案疾病控制率低,治疗相关死亡率高。Ferreri 等[11]的IELSG32 试验共纳入227 例患者,其中R-MA 组69 例患者,CR 达30%,ORR 为74%;但是Ⅲ~Ⅳ级粒细胞减少和血小板减少分别为56%和74%,3例患者死于治疗相关不良反应。本研究前瞻性纳入12 例PCNSL 患者,经过RFPD 方案化疗后,CR 达50%,ORR 为66.7%,DCR 为75%,mPFS 为7个月。不良反应方面,Ⅲ~Ⅳ级粒细胞减少和血小板减少分别为16.7%和25.0%,1 例患者死于治疗相关不良反应。与既往研究相比,本研究方案获得了较好的CR,血液学毒性的发生率少,但ORR 和mPFS 仍不理想,这可能与入组患者尚少,随访时间较短有关,因此需纳入更多的患者深入研究。
利妥昔单抗在化疗中的应用显著改善了系统性DLBCL 的预后[12-14],但其对PCNSL 的影响尚未明确。由于利妥昔单抗的中枢神经系统渗透率极低,通过静脉给药其在脑脊液中的血药浓度仅为血清水平的0.1%~4.4%[15]。有研究认为使用部分能够诱导可逆性BBB透化并增强抗癌药物肿瘤渗透的静脉注射剂可提高药物在中枢神经系统的浓度[16],但尚未应用于临床研究。临床前数据表明其可能在中枢神经系统恶性肿瘤中被破坏,允许部分大分子如利妥昔单抗渗透到中枢神经系统[17]。Birnbaum 等[18]回顾性分析利妥昔单抗对PCNSL 患者接受甲氨蝶呤(MTX)和异环磷酰胺(IFO)化疗后的CR的影响。RMI 组的CR 为100%,而MI 组的CR 为68.4%。此外,R-MI 组3 个月的PFS 显著延长(94.1%vs.63.2%,P=0.04),两组之间的不良反应无显著性差异。Madle等[19]认为加用利妥昔单抗未显著延长PCNSL患者的PFS,但是可以延长OS。Kansara 等[20]对86 例PCNSL患者进行回顾性研究发现,大剂量甲氨蝶呤组(highdose methotrexate,HD-MTX)和大剂量甲氨蝶呤+利妥昔单抗组(HD-MTX+rituximab,HD-MTX+R)相比CR、mOS 和mPFS 均无显著差异。目前,利妥昔单抗已经作为临床PCNSL 诱导治疗的一线用药,基于大量的临床试验数据,本研究将利妥昔单抗纳入此方案。既往研究发现利妥昔单抗可能引起的不良反应,如红斑、中性粒细胞减少、乏力和感染等[21]。本研究中PCNSL患者使用利妥昔单抗后主要的不良反应为感染(25%),其中1 例患者死于重症肺炎,其余不良反应的发生率在可控范围内。
相比常用的R-MA(利妥昔单抗+甲氨蝶呤+阿糖胞苷)方案,本研究在选用培美曲塞替代MTX的基础上加用了福莫司汀。研究表明,相对于MTX,培美曲塞作用靶点更多,应用更加简单,且无需水化、尿液碱化和解毒,这些特点使培美曲塞成为MTX 的理想替代药物。Zhao等[22]对27例复发难治性PCNSL患者给予RP(利妥昔单抗+培美曲塞)治疗,ORR 达到62.9%,DCR 达92.5%,mPFS 为6.9 月,mOS 为11.2 个月。Wu等[23]首次进行一项随机Ⅱ期临床试验,对比含福莫司汀的方案与HD-MA 方案在新诊断PCNSL中的疗效,结果显示在含福莫司汀组和HD-MA组之间的ORR未观察到显著性差异,2年PFS和3年OS均无显著性差异。在不良反应方面,HD-MA 组显示出比FTD(福莫司汀+替尼泊苷+地塞米松)组更为严重的中性粒细胞减少症。
本研究中的主要不良反应为血液学毒性,Ⅲ~Ⅳ级粒细胞减少和血小板减少分别为16.7%和25.0%,与既往文献报道的56%和74%明显降低[9]。非血液学毒性均较轻,发生率较低。
国际结外淋巴瘤研究组认为存在5 项因素影响PCNSL 患者预后[24],包括:年龄≥60 岁;ECOG 评分≥2分;脑脊液蛋白含量增高;血清乳酸脱氢酶(lactate dehydrogenase,LDH)水平升高;脑实质深部受累。随着生物分子技术的发展,越来越多学者开始探索PCNSL 患者生物分子预后标志。诸多研究认为在非特殊型DLBCL中c-myc、Bcl-2基因双打击及c-myc、Bcl-2蛋白双表达均与不良预后相关[25-26],而c-myc、Bcl-2 蛋白表达在PCNSL 患者中的意义却尚未完全明确。国内一项回顾性研究发现,c-myc蛋白阳性(>40%)、Bcl-2 蛋白高表达(≥70%)、Bcl-2 基因异常是PCNSL 的不良预后指标[27]。国外开展的一项研究纳入59例PCNSL患者,结果显示,包含c-myc重排或拷贝数增加的组与阴性组无显著性差异(P>0.1),即cmyc蛋白高表达(>40%)与预后无相关性[28]。本研究中高c-myc表达组与低c-myc表达组的mPFS的差异无统计学意义(6.0个月vs.8.7个月,P=0.759)。考虑到本研究入组患者病例数尚少,随访时间短等因素,为进一步、更为准确的探索c-myc蛋白表达在PCNSL中的临床意义,亟需扩大研究病例数和延长随访时间。
对于巩固治疗,包括WBRT和大剂量化学疗法加自体干细胞移植。Houillier 等[29]前瞻性Ⅱ期研究评估WBRT 和自体干细胞移植作为一线巩固治疗的疗效和不良反应,共纳入140例患者,WBRT和ASCT组的2 年PFS 分别为63%(95%CI:49%~81%)和87%(95%CI:77%~98%)。WBRT 组有增加神经毒性的趋势,包括精神运动减慢、神经认知障碍、记忆功能障碍、步态共济失调和行为改变等,且复发率高。而ASCT 后认知功能得以保留或改善。Ferreri 等[30]的IELSG32 试验提出对于年轻PCNSL 患者,首选AS⁃CT。本研究后续将会探讨WBRT或自体干细胞移植作为PCNSL的一线巩固治疗的疗效和不良反应。
综上所述,PCNSL 为一种侵袭性高、预后差的原发结外非NHL亚型。本研究初步确定R-FPD方案对初治的PCNSL 患者为有效且安全的。但是,本研究病例数较少,亟需扩大样本量、延长随访时间,进一步研究来证实本研究的观察结果。

