玉叶金花质量控制研究*
秦兰,刘亭,孙佳,陆苑,潘洁,王永林,李勇军,林昌虎***,刘春花***
(1.贵州医科大学 民族药与中药开发应用教育部工程研究中心 & 省部共建药用植物功效与利用国家重点实验室,贵州 贵阳 550004; 2.贵州医科大学 药学院,贵州 贵阳 550025; 3.贵州医科大学 贵州省药物制剂重点实验室,贵州 贵阳 550004)
玉叶金花为茜草科玉叶金花属植物玉叶金花(MussaendapubescensAit.f.)的干燥地上部分,既是我省常用民间药物,也是苗族常用药物,苗药名为“阿岗奴”[1]。玉叶金花具有清热解毒,祛风利湿的功效,可用于感冒、中暑、肠炎、肾炎水肿、咽喉肿痛及支气管炎等[1-3]。据《湖南省中药材标准》(2009年版)和《广西省中药材标准》(1990年版)记载,玉叶金花的入药部位为根和茎,两“标准”仅对其形状进行描述、质量控制体系较为简单仅包含理化鉴别方法,尚不完善[4-5]。民间常用玉叶金花根研粉拌粥服治疗小儿疳积,或全株水煎当茶饮治疗精神分裂症,也有用鲜叶捣烂调鸡蛋清服用治疗断肠草或野菌中毒[6-8]。有研究发现,玉叶金花含有皂苷类、环烯醚萜类及萜类等成分,具有抗炎、抗菌及抗病毒等生物活性及良好的药用价值[9-12]。玉叶金花的根、枝、叶或全株均可入药[1,6],但至今尚无质量标准,限制了应用和开发,本研究参照《中国药典》2015年版相关规定通过对玉叶金花的性状、显微鉴别、薄层鉴别、检查及浸出物等项目进行系统的研究,为建立玉叶金花的质量标准提供参考依据。
1 材料与方法
1.1 材料
1.1.1药材与主要试剂 玉叶金花药材来自贵州和广东(表1),原植物及样品均由贵州医科大学药学院药用植物与生药学教研室张旭副教授鉴定为MussaendapubescensAit.f.的地上部分,凭证标本存放于贵州医科大学贵州省药物制剂重点实验室;玉叶金花对照药材(批号121404-201502)购自中国食品药品检定研究院;硫酸、甲醇、乙醇、三氯甲烷及甲酸购自国药集团化学试剂有限公司(均为分析纯),青岛海洋硅胶G板购自青岛海洋化工厂分厂,烟台黄海江友硅胶G板购自烟台黄海江友化工厂,青岛鼎康硅胶G板购自青岛鼎康化工厂。
1.1.2主要仪器 奥林巴斯CX41简易偏光显微镜(日本奥林巴斯公司)及明美S60显微成像系统(广州明美光电技术有限公司),REPROSTAR3薄层数码成像系统(瑞士CAMAG公司),WP-MP-II-20实验室超纯水机(四川沃特尔水处理设备有限公司),EL204电子天平(瑞士METTLER公司),DK-98-Ⅱ型水浴锅(天津泰斯特有限公司)。
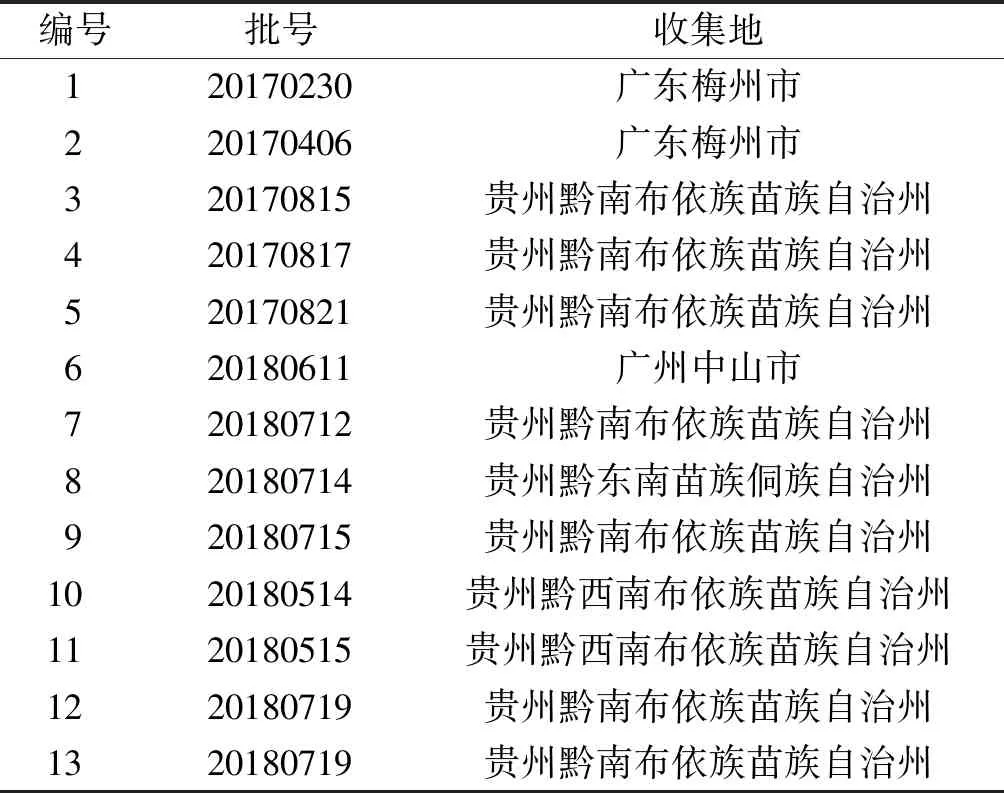
表1 不同批次玉叶金花样本Tab.1 The different batches of M. pubescens
1.2 方法
1.2.1性状鉴定 采用标尺对玉叶金花的大小进行测量,采用看、摸、闻及尝等直观方法对样品的形状、色泽、表面、质地、断面及气味进行鉴定。
1.2.2显微鉴别 表面制片系采用表皮撕离法,分别撕取玉叶金花上下表皮,置于载玻片上,滴加甘油醋酸试液,或者加水合氯醛试液加热透化,再滴加稀甘油,盖上盖玻片,在显微镜下(100×)观察上下表皮细胞的形状、气孔和毛状体等特征,拍照记录;粉末制片系挑取玉叶金花粉末(过4号筛)少许置载玻片上,滴加蒸馏水、水合氯醛试液或稀甘油试液等(必要时加热透化),盖上盖玻片,倒置显微镜下(400×)观察、测量和拍照。
1.2.3薄层色谱鉴别 取玉叶金花粉末(过3号筛)0.5 g,加乙酸乙酯5 mL,超声处理20 min,滤过,取续滤液作为供试品溶液;另取玉叶金花对照药材0.5 g,同法制得对照药材溶液。按《中国药典》2015年版四部通则0502进行薄层色谱法试验[13],吸取对照品溶液及供试品溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷 ∶甲醇 ∶水(8.5 ∶1.5 ∶1.5)为展开剂,展开、取出、晾干,喷硫酸乙醇溶液置105 ℃加热10 min,置紫外灯光365 nm检视。
1.2.4水分、总灰分和浸出物测定 取玉叶金花粉末(过2号筛)2 g,精密称定,按《中国药典》2015年版四部通则0832水分测定法(第二法 烘干法)进行水分测定[13];取本品粉末2 g,置炽灼至恒重的坩埚中,称定质量(准确0.01 g),按《中国药典》2015年版四部通则2302灰分测定法进行灰分测定[13];取本品粉末(过2号筛)2 g,精密称定,置100 mL的锥形瓶中,精密加乙醇50 mL,按《中国药典》2015年版四部通则2201浸出物测定法中醇溶性浸出物测定法进行浸出物测定[13]。
2 结果
2.1 性状鉴定
玉叶金花茎呈圆柱形,直径3~10 mm,表面棕色或棕褐色,具细纵皱纹、点状皮孔及叶柄痕,质坚硬、不易折断,断面黄白色或淡黄绿色,髓部明显、白色;叶对生或轮生、多缩皱、破碎,完整叶片展平后呈卵状矩圆形、顶端渐尖、基部楔形,上表面近无毛或被疏毛,下表面密被短柔毛,有时稍疏;气微,味淡。见图1。

图1 玉叶金花(批号20170714)药材的外观性状Fig.1 Characters of M. pubescens
2.2 显微鉴别
玉叶金花药材的叶表皮显微结构特征表现为:上表皮细胞呈类多角形,垂周壁增厚,气孔少见;下表皮细胞不规则形状,垂周壁波状弯曲;气孔为平轴式;非腺毛多见(图2)。玉叶金花药材的粉末显微结构特征表现为:粉末灰白色或灰绿色;非腺毛众多,由2~9个细胞组成,表面光滑,基部直径10~35 μm;导管主为具缘纹孔,直径20~90 μm,偶见螺纹导管;石细胞众多,长方形、方形及类圆形,直径15~70 μm;叶上表皮细胞类多角形,叶下表皮细胞不规则形状,垂周壁稍弯曲;纤维壁薄,具单纹孔,直径12~50 μm(图3)。
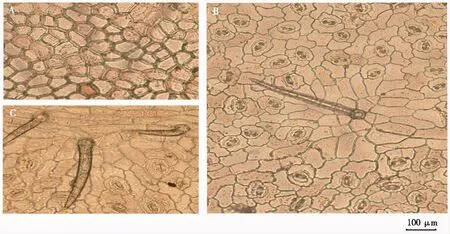
注:A为叶上表皮细胞,B、C为叶下表皮细胞。 图2 玉叶金花的叶表皮显微结构(100×)Fig.2 Microscopic features of epidermis of leaves of M. pubescens(100×)

注:(1)为叶表皮细胞,(2)为导管,(3)为石细胞,(4)为纤维,(5)为非腺毛。图3 玉叶金花药材的粉末显微结构(400×)Fig.3 Microscopic features of powder of M. pubescens(400×)
2.3 薄层色谱
2.3.1系统适用性试验 以玉叶金花对照药材作为对照品对其进行薄层鉴别,结果显示在供试品色谱中,与对照药材色谱相应的位置上显相同颜色的斑点,各斑点分离度良好。见图4。

注:1为20170230, 2为20170406,3为20180611,4为对照药材。图4 玉叶金花薄层色谱鉴别系统适用性试验Fig.4 Applicability test of the TLC identification system of M. pubescens
2.3.2耐用性试验 不同厂家薄层板展开效果显示,青岛海洋、烟台江友及青岛鼎康3种不同厂家的硅胶G板均能鉴别玉叶金花(图5);利用不同浓度硫酸调整湿度为32%、60%及72%,考察不同湿度条件下的展开效果,结果显示不同湿度下色谱图的斑点清晰,均能较好的鉴别玉叶金花(图6);分别在10 ℃、20 ℃及30 ℃下展开,考察不同温度对展开的影响,结果显示不同温度下色谱图的斑点清晰,均能较好的鉴别玉叶金花(图7);将同一批次的本品粉末于放置3 d、2 d、1 d及当日按拟定的方法制备供试品溶液,分别点于同一硅胶G板上,展开显色结果显示,各斑点无明显差异(图8)。
2.3.3不同批次样品鉴别 按拟定的薄层色谱鉴别方法,对13批样品进行测定,结果显示供试品色谱中与对照品色谱相应的位置上显相同颜色的斑点,13批玉叶金花饮片均符合要求。见图9。
2.4 水分、总灰分和醇溶性浸出物测定
13批玉叶金花的水分、总灰分和醇溶性浸出物结果显示不同产地的玉叶金花中水分、总灰分和醇溶性浸出物含量存在一定差异。见表2 。
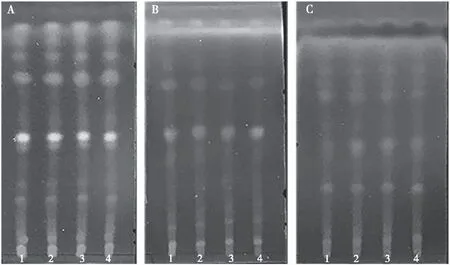
注:A为青岛海洋硅胶板,B为台江友硅胶板,C为青岛鼎康硅胶板;1为20170230,2为20170406,3为20180611,4为对照药材。图5 玉叶金花在不同厂家硅胶板的展开效果Fig.5 Investigation of M. pubescens in silica gel plates from different manufacturers

注:A为相对湿度32%,B为相对湿度60%,C为相对湿度72%;1为20170230,2为20170406,3为20180611,4为对照药材。图6 玉叶金花在不同湿度环境的展开效果Fig.6 Different developing humidity of M. pubescens

注:A为温度10 ℃,B为温度20 ℃,C为温度30 ℃;1为20170230, 2为20170406,3为20180611,4为对照药材。图7 玉叶金花在不同温度环境的展开效果Fig.7 Different developing temperature of M. pubescens

注:1为当日,2为放置1 d,3为放置2 d,4为放置3 d,5为对照药材。图8 玉叶金花供试品溶液稳定性考察Fig.8 The stability of the test sample of M. pubescens

注:1~13为不同批次(批号见表1),14为对照药材。图9 不同批次玉叶金花薄层鉴别色谱结果Fig.9 TLC of different batches of M. Pubescens

表2 玉叶金花的水分、总灰分和醇溶性浸出物测定结果 Tab.2 Determination of moisture, total ash and alcohol soluble extracts of M.
3 讨论
玉叶金花不仅可以作为药物使用,还可食用,广东等地常用玉叶金花制备凉茶[6]。玉叶金花资源丰富,使用价值广泛,具有潜在的开发和利用前景,建立完善的质量标准具有一定的必要性。性状鉴定、显微鉴定和薄层色谱鉴定是中药鉴定的常用方法[14],具有快速、直观和便捷等特点,对中药材和饮片的鉴别具有重要意义。本研究对玉叶金花地上部分入药药材的性状特征进行了描述,并对干燥药材叶表面制片的方法进行考察,采用浸泡后撕取表皮和切取表皮等方法比较,最后发现撕取表皮制片的方法较好,最终成功地观察到比较清晰和明显的玉叶金花叶表皮特征,如平轴式的气孔,垂周壁波状弯曲的下表皮细胞,呈类多角形的上皮细胞,表面光滑的非腺毛及长方形、方形及类圆形的石细胞等,这些特征均可作为玉叶金花鉴定的依据。
本研究通过考察不同溶剂(甲醇、三氯甲烷及乙酸乙酯等)、不同提取方法(超声处理与回流)和不同时间等,最终得到最佳提取条件。进一步考察不同展开条件,包括三氯甲烷 ∶甲醇(8.5 ∶8.0)、三氯甲烷 ∶甲醇 ∶水(8.5 ∶1.5 ∶1.5)、三氯甲烷 ∶甲醇 ∶水(8.5 ∶0.5 ∶0.5),确定最佳展开条件。耐用性试验考察结果表明不同厂家薄层板、不同湿度和不同温度下色谱图的斑点清晰,均能较好的鉴别玉叶金花,说明该方法适用性好,受相对湿度,温度影响不明显;稳定性试验考察结果表明同一批玉叶金花粉末在不同放置时间下色谱图无明显差异,说明样品稳定性良好,进一步说明该方法稳定、可靠。将所建立的薄层色谱法对13批玉叶金花药材进行鉴定,结果显示主斑点明显、清晰及分离度好,且主斑点颜色和位置与对照药材一致,进一步说明该方法专属性强,可以有效鉴别不同批次的玉叶金花药材,同时色谱图结果表明不同产地的药材中主斑点颜色深浅不同,提示不同产地玉叶金花中该类成分含量可能不同。
本研究对13批玉叶金花粉末进行了水分、总灰分及醇溶性浸出物的检测,结果发现13批玉叶金花中水分含量范围是9.20%~14.30%,平均含量为11.95%。总灰分含量范围是5.26%~7.88%,平均含量为6.24%。因为玉叶金花中的化学成分主要为皂苷、萜类等,且现代研究发现这些成分可能是其活性成分[9,11,15-20],故以醇溶性浸出物作为玉叶金花质量控制指标之一,13批次玉叶金花醇溶性浸出物含量范围是5.18%~8.80%,平均值含量为6.62%。不同产地的玉叶金花中水分、总灰分和醇溶性浸出物含量存在一定差异,可能与产地、气候和采收时间有关,这些因素均有待进一步深入研究。
综上所述,本研究建立的玉叶金花的质量控制研究方法专属性强、稳定性和重复性良好,为该药材的真实性鉴定和质量评价提供了参考依据。

