肺移植术后抗感染药物相互作用的药学监护要点
王晓星,李喜平,张相林(.中日友好医院药学部,北京 0009;.华中科技大学同济医学院附属同济医院药学部,湖北 武汉 430030)
药物相互作用(drug-drug interaction,DDI)是指联合应用两种或两种以上药物时,由于药代 动 力 学(pharmacokinetics,PK) 或 药 效 学(pharmacodynamics,PD)的相互影响,导致药物暴 露量、药物疗效或不良反应风险发生改变[1]。肺移 植术后因免疫抑制治疗、抗感染治疗以及药物不良反应等因素,存在诸多DDI 问题,是药学监护工作中的关注重点。
美国移植学会(American Society of Transplantation,AST)感染病学委员会已将抗感染药物与免疫抑制药物的相互作用列为实体器官移植术后抗感染指南的一部分[1]。事实上,不仅抗感染药物与免疫抑制药物存在复杂的DDI,抗感染药物之间、与移植术后其他常用药物之间的DDI 也是实践中不能忽视的问题。现将肺移植术后抗感染药物DDI 药学监护要点总结如下。
1 基于药代动力学的DDI
1.1 常用抗菌药物:大环内酯类药物红霉素、 克拉霉素显著影响免疫抑制药物的PK 过程。作为细胞色素P450 酶(cytochrome P450,CYP450, 以下简称CYP)3A4 的抑制剂,红霉素、克拉霉素能够明显升高钙调蛋白酶抑制剂(calcineurin inhibitors , CNI)、环孢素、他克莫司以及哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin, mTOR)抑制剂西罗莫司、依维莫司的血药浓度。因此在选择大环内酯类药物时,优先使用对药物代谢影响较小的阿奇霉素。当必须联用时,可以考虑将免疫抑制药物剂量减半[1],并密切监测血药浓度(表1)。由于耐药性的增加,大环内酯类抗菌药物当前并不常用,但实体器官移植受者感染非结核分枝杆菌的风险较高,在启动克拉霉素治疗时需考虑到DDI 对免疫抑制药物的影响[2]。
抗代谢药物吗替麦考酚酯的活性成分为霉酚酸,霉酚酸在肝脏代谢为无活性的葡萄糖醛酸化产物后,有一部分可经过肝肠循环,在肠道微生物的作用下再次转化为霉酚酸并被吸收,占霉酚酸体内暴露量的40%左右[3]。因此,影响肠道菌群的抗菌药物可能通过抑制二次吸收来影响霉酚酸的体内水平。有病例报道指出口服阿莫西林克拉维酸钾、环丙沙星、甲硝唑联合诺氟沙星,能够明显降低霉酚酸的体内暴露量[4]。尽管证据有限,但使用广谱抗菌药物时,需警惕霉酚酸暴露不足,可以考虑应用血药浓度监测指导吗替麦考酚酯的剂量。
1.2 抗真菌药物:肺移植术后真菌感染风险显著高于其他实体器官移植,因此三唑类抗真菌药物是肺移植患者术后常见的药物处方。然而,三唑类药物不仅是CYP3A4 的强抑制剂,有些还影响药物外排转运蛋白P-糖蛋白表达,同时其代谢还受基因多态性的影响,使得与免疫抑制药物的DDI 管理充满挑战[5]。
伏立康唑是治疗肺曲霉感染的一线用药,说明 书中指出开始与环孢素合用时需要将环孢素剂量下调50%,与他克莫司合用时需要将他克莫司剂量下调2/3。而在临床实践中,CNI 类药物的剂量有时会调整到更低,可能与亚裔人群伏立康唑代谢酶CYP2C19 突变率较高有关。虽然他克莫司主要经CYP3A4 代谢,与CYP2C19 快代谢人群相比,CYP2C19 中间代谢和慢代谢人群合用伏立康唑显著升高他克莫司的药物暴露量[6]。药品说明书中禁止西罗莫司与伏立康唑联合使用,因为伏立康唑可以使西罗莫司的体内暴露量升高10 倍以上。 然而在造血干细胞移植受者中的回顾性研究提示,可以将西罗莫司的剂量下调90%,在密切监测下合用这两种药物[7]。依维莫司相关研究较少, 但其与西罗莫司药动学特征相似,可参考西罗莫司的用法。
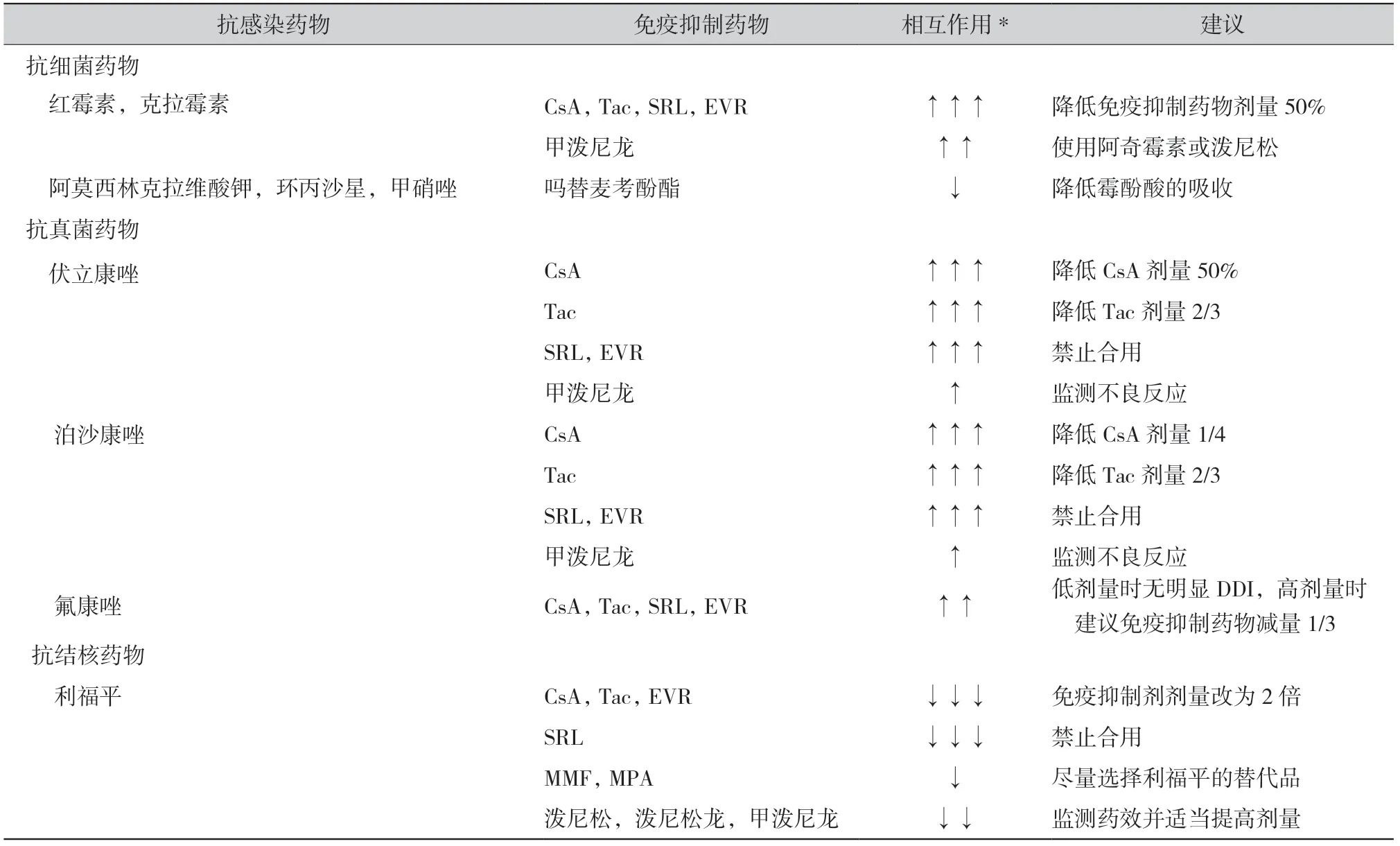
表1 基于药动学的常见药物相互作用
泊沙康唑也常用于预防肺移植术后的曲霉感染,与伏立康唑相似,泊沙康唑口服混悬液说明书中指出,开始与环孢素合用时需要将环孢素剂量下调1/4,与他克莫司合用时需要将他克莫司剂量下调2/3。此外,同时应用H2 受体拮抗剂西咪替丁、质子泵抑制剂奥美拉唑、泮托拉唑等,显著降低泊沙康唑口服混悬液的吸收。对于肺移植术后患者来说,需要考虑该DDI 导致的体内药物浓度不足的问题,通过血药浓度监测及时调整泊沙康唑的剂量。近几年上市的泊沙康唑肠溶片与口服混悬液相比,可能对CYP3A4 的抑制作用更强。虽然说明书给出了相同的剂量调整建议,但在肺移植受者的小样本研究中发现,合并使用肠溶片的患者他克莫司谷浓度-剂量比(C0/dose)显著升高,更有可能出现浓度高于目标值的情况[8]。
氟康唑的酶抑制作用相对较弱,与CNI 类药物的相互作用与剂量和给药途径相关。与口服给药相比,静脉给予氟康唑仅微弱影响CNI 类药物的浓度,尤其是CNI 类药物也通过静脉给予时[9]。口服氟康唑对DDI 的影响则随剂量增加而增加。在肾移植受者中发现,每日口服50 mg 氟康唑对他克莫司的谷浓度和体内暴露量没有明显影响[10]。但氟康唑日剂量在100 mg 时则需要将他克莫司的剂量下调40%,并且推测随着氟康唑剂量的进一步升高,相互作用影响会更强[9]。而与环孢素合用时, 日剂量在200 mg/d 以下的氟康唑对环孢素的代谢影响较小,无需调整剂量[5,9]。因此,也有专家建议,开始较高剂量的氟康唑治疗时将CNI 类药物剂量减少1/3[11]。
三唑类药物与糖皮质激素的相互作用也是不可忽视的问题。伊曲康唑在三唑类药物中酶抑制作用最强,当与静脉途径的甲泼尼龙合用时可导致后者的血药浓度-时间曲线下面积(area under concentration-time curve, AUC)增加2.6 倍,半衰期延长2.3 倍。除尽量避免两药合用外,可以考虑在联合使用时将甲泼尼龙减量50%。而泼尼松与伊曲康唑未发现有临床意义的相互作用[12]。虽然尚无数据证明伏立康唑、泊沙康唑与糖皮质激素的相互作用,但同样作为CYP3A4 抑制剂,推测其存在与伊曲康唑相似的影响,与甲泼尼龙合用时建议密切监测糖皮质激素的不良反应,必要时酌情减量。
1.3 抗结核药物:由于免疫抑制剂的长期使用,实体器官移植受者罹患结核病的风险大大提高,其中以肺移植为最,发病风险是其他器官移植的 5.6 倍[13]。而抗结核药物的毒性以及DDI 都明显增加了治疗的复杂性,对药学监护提出了较高的要求。 以利福平为代表的利福霉素类药物是强效肝药酶诱导剂,联合应用可显著增加CNI 类药物或mTOR抑制剂的清除,使后者难以维持在治疗水平,即使合用酶抑制剂也不能消除该效应。因此,建议尽可能避免利福霉素类药物在肺移植患者中的应用。 需要注意的是,与酶抑制作用的即刻起效不同,酶诱导作用需要经过1 ~ 2 周方可达到最大效应。因此,当必须合用时,如活动性肺结核病,起始治疗时应增加CNI 类药物或mTOR 抑制剂至原剂量的 2 倍,随后通过密切监测血药浓度迅速的调整免疫抑制药物剂量,至少上调2 ~ 5 倍,最高可上调 10 倍以上[1]。虽然临床证据有限,但利福布汀的酶诱导作用和DDI 风险均弱于利福平,在HIV 患者的结核病治疗上与利福平方案疗效相当,是实体器官移植受者可以优先选择的利福霉素类药物[14]。
利福平也显著影响糖皮质激素的代谢,包括甲泼尼龙、泼尼松及泼尼松龙。在联合使用泼尼松和利福平的巨细胞动脉炎患者中发现,与单独应用泼尼松相比,合用导致泼尼松龙的清除率增加了200%以上,半衰期减少40% ~ 60%。因此,该作者建议联合使用利福平时需要将泼尼松增加至原剂量的2 倍[2]。在实体器官移植受者人群中尚无明确的剂量调整建议,但联合使用利福平时需注意监测糖皮质激素的疗效,适当增加剂量以避免治疗失败。
吗替麦考酚酯药品说明书中也提示,在单心肺移植的患者合并利福平给药时,可观察到活性成分霉酚酸的暴露量(AUC0~12h)下降70%,建议尽量避免两者的联合应用。其机制可能在于肝脏、小肠的霉酚酸代谢酶水平在利福平诱导作用下显著升高。
对于同时存在真菌、结核感染的肺移植患者来说,治疗方案将会更加复杂,因为利福霉素类药物与三唑类抗真菌药也存在严重的DDI。例如,泊沙 康唑与利福布汀合用时,泊沙康唑的整体暴露量(AUC)下降49%,而利福布汀的暴露量则增加72%[12]。因此,当不能避免合用时,务必监测三唑类药物血药浓度,警惕肝毒性等利福霉素类药物的不良反应,及时调整药物剂量。
2 基于药效学的DDI
免疫抑制药物及抗感染药物均存在较高的不良反应风险,包括肾毒性、骨髓抑制、QT 间期延长等,联合使用时需尤其警惕不良反应的叠加,密切监测相关指标,及时减少或停用相关药物(表2)[1]。例如,肺移植术后需长期使用更昔洛韦或缬更昔洛韦预防巨细胞病毒感染,与霉酚酸合用存在较高的骨髓抑制风险,需密切监测血细胞水平,并根据肾功能及时调整药物剂量。
值得注意的是,肺移植受者往往需要同时使用长疗程的伏立康唑和CNI 类药物,可能导致某些罕见不良反应,如神经肌肉毒性的风险增加[15]。在一项27 例肺移植受者的研究中发现,即使他克莫司浓度处于目标水平,长期应用伏立康唑也导致30%的患者出现神经肌肉异常,表现为肌肉疼痛或无力,麻木,感觉异常等。其中两例患者既往曾接受过伏立康唑治疗而耐受良好,提示他克莫司联合伏立康唑与该不良反应的发生有相关性。停用 伏立康唑后,大部分患者在1 ~ 2 周内症状完全缓解。而将伏立康唑浓度维持在较低的水平(小于 1.5 mg/ml),也有利于降低该不良反应风险[16]。

表2 基于药效学的常见药物相互作用
3 展 望
肺移植是目前临床上肺疾病终末期治疗的唯一有效方法,然而术后各种并发症的发生极大增加了患者管理的复杂性。感染是肺移植术后的主要问题之一,抗感染药物与免疫抑制药物的相互作用也是药学监护关注的重点。该领域虽然已有相关指南,但仍缺乏足够的循证证据,需要在临床实践中不断探索和完善。

