超声波辅助/疏水性低共熔溶剂萃取-高效液相色谱法测定牛奶中的多环芳烃
何婷婷, 周 彤, 谭 婷, 万益群*
(1.江西省预防医学重点实验室,南昌大学公共卫生学院,江西南昌 330006;2.南昌大学分析测试中心,江西南昌 330047)
多环芳烃(PAHs)是一类含有两个或两个以上的芳香环或簇状的五元环组成的有机高分子化合物,主要是由煤、石油以及其它有机物在高温下不完全燃烧,或者是由自然现象例如火山喷发和森林火灾所产生的[1,2]。在目前已发现的100多种PAHs中,有16种PAHs被美国环境保护机构列为首要污染物。该类化合物具有很高的致癌性、致突变性和毒性。由于它们的性质以及形成方式,导致了PAHs及其降解产物广泛存在于水、土壤、大气等环境中,从而也造成了多种食品样品,如食用油、烤肉、蔬菜、咖啡等的污染[3 - 5]。PAHs本身具有亲脂性,易在脂肪组织中积累,并可在乳汁中排出[6],而乳制品被广泛应用于人们的饮食中,因此,建立一种简单、快速、有效的牛奶中PAHs化合物的分析新方法具有重要的现实意义。
1 实验部分
1.1 仪器与试剂
Agilent 1260高效液相色谱仪(美国,安捷伦公司),配荧光检测器;DF-101S集热式恒温水/油浴锅(河南省予华仪器有限公司);KQ-5200数控超声波清洗器(江苏省昆山市超声仪器有限公司);JY5002电子天平(上海舜禹恒平科学仪器有限公司)。
两种牛奶样品(全脂牛奶和低脂牛奶)均购于江西省南昌市天虹超市。
1.2 实验方法
1.2.1 DESs的制备采用简单加热法[13]制备DESs。按照一定化学计量比,称取氢键供体和氢键受体于500 mL圆底烧瓶中,在80~120 ℃条件下搅拌,直至形成均一透明的液体,即为DESs。本实验制备了4种不同种类的DESs,其合成的原料和配比如表1所示。
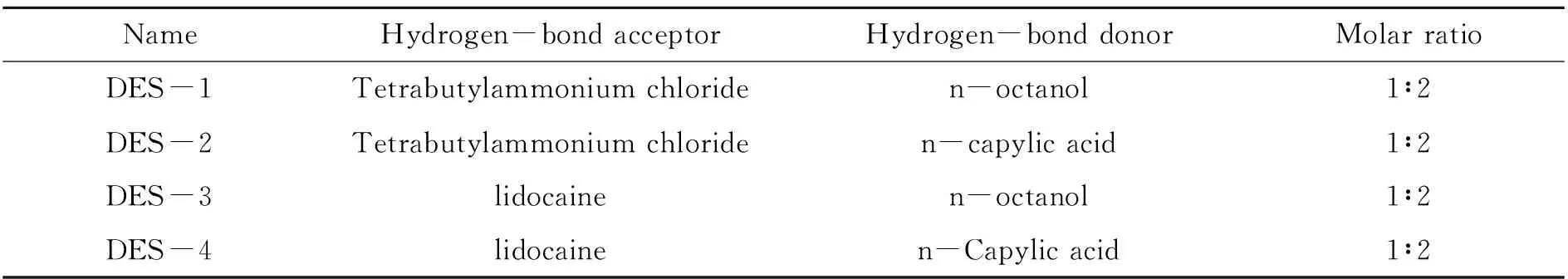
表1 不同低共熔溶剂的组成
1.2.2 样品前处理准确称取1.0000 g牛奶样品于5 mL离心管中,分别加入0.3 g NaCl和2.0 g疏水性DESs,在迷你振荡器中混合均匀后,于50 ℃超声波萃取9 min。以12 000 r/min离心8 min,分离上清液,经0.45 μm有机相滤膜过滤,采用液相色谱-荧光法进行分析。
1.2.3 液相色谱检测条件色谱柱为Dikma Spursil C18柱(150 mm×4.6 mm,5 μm);流动相为不同比例的乙腈-水(使用前经过超声脱气),采用梯度洗脱程序为:0~5 min,71%乙腈;5~15 min,71%~100%乙腈;15~20 min,100%乙腈;20~21 min,100%~71%乙腈;21~30 min,71%乙腈。流速:1.0 mL/min;进样量:5 μL;柱温:30 ℃。
由于不同多环芳烃化合物其荧光测定的最佳激发波长和发射波长的差距比较大,因此为了获得较高的响应值,对检测条件进行了优化,在不同的时间段内,选择不同的激发和发射波长对6种多环芳烃化合物进行了检测,如表2所示。
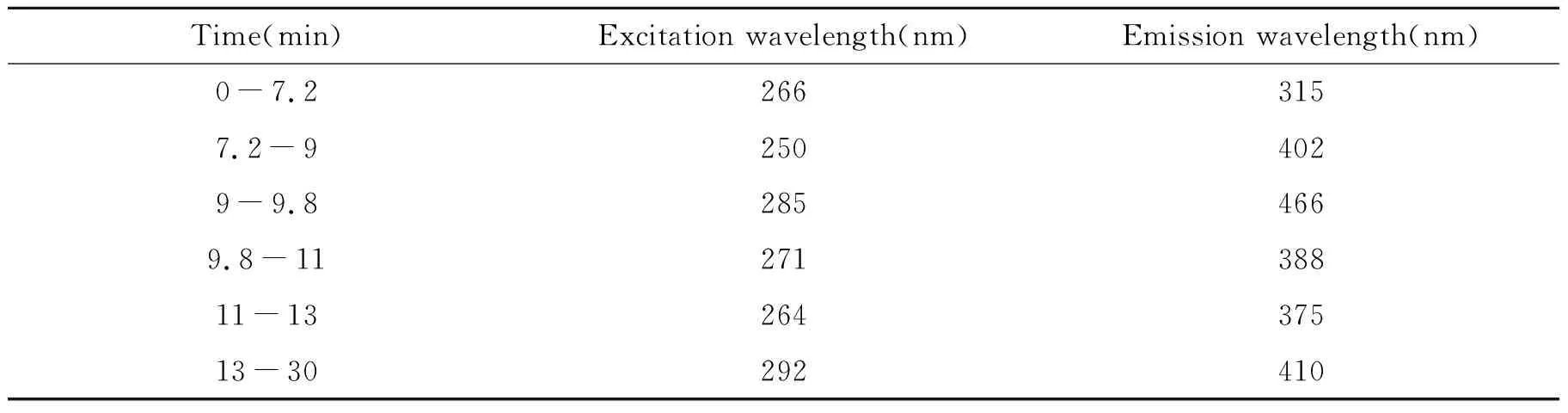
表2 激发波长和发射波长
2 结果与讨论
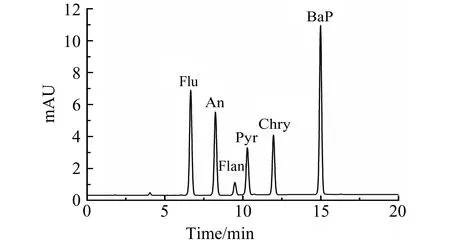
图1 标准溶液的色谱图Fig.1 Chromatogram of the standard solution
2.1 检测条件的选择
采用荧光检测器对6种多环芳烃化合物进行了波长扫描,发现不同PAHs之间的最佳激发和发射波长的差距比较大。为了提高方法的灵敏度,本研究结合液相色谱分离条件,在不同的时间段选择不同的激发和发射波长对6种多环芳烃化合物进行检测(表2)。在最佳的检测波长下,以100 μg/kg混合标准溶液进样分析的色谱分离图如图1所示,6种多环芳烃都能得到很好的分离和检测。
2.2 萃取条件的优化
2.2.1 DESs种类的选择DESs是一类具有不同物理化学性质的多组分溶剂体系,与目标物之间存在多种不同的相互作用,如静电、疏水、偶极-偶极、范德华力(分散)、氢键以及π-π作用力等,因此DESs的萃取效率与目标物之间形成的作用力大小有关[14]。本实验考察了4种不同组成的疏水性DESs体系对牛奶中6种目标物(50 μg/kg)的萃取效率的影响,萃取效果如图2所示。结果表明,相对于利多卡因,以四丁基氯化铵作为氢键受体的DESs对6种PAHs的萃取效果较好,而以四丁基氯化铵和正辛醇合成的DES -1的萃取效果最好。此外,还分别探讨了四丁基氯化铵和正辛醇对牛奶中6种PAHs的萃取效果(图2)。结果表明,与DES -1相比,正辛醇对6种多环芳烃的萃取效率较低,而四丁基氯化铵溶于水,无法对牛奶样品中多环芳烃进行有效萃取。因此本实验选择DES -1进行后续的实验。
2.2.2 DESs用量的选择采用DES -1为萃取剂,其用量是影响萃取效果的一个重要参数。一方面,通过增加萃取溶剂的用量,可以提高萃取效率;另一方面,随着萃取剂用量的增加,稀释效应会使萃取效率降低。因此,为了获得最佳萃取剂的用量,对在1.0~3.5 g范围内萃取剂的萃取效率进行了评价,结果如图3所示。结果表明,随着萃取剂用量的增加,萃取效率的影响并不显著,实验选择萃取剂用量为2.0 g。
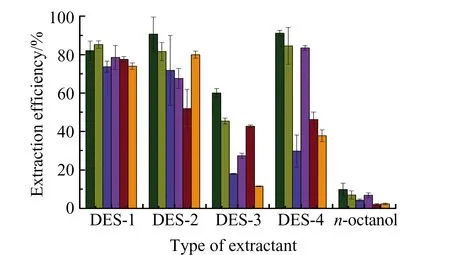
图2 萃取剂的种类对多环芳烃化合物萃取效果的影响Fig.2 Effect of the type of extractant on the extraction efficiency of PAHs
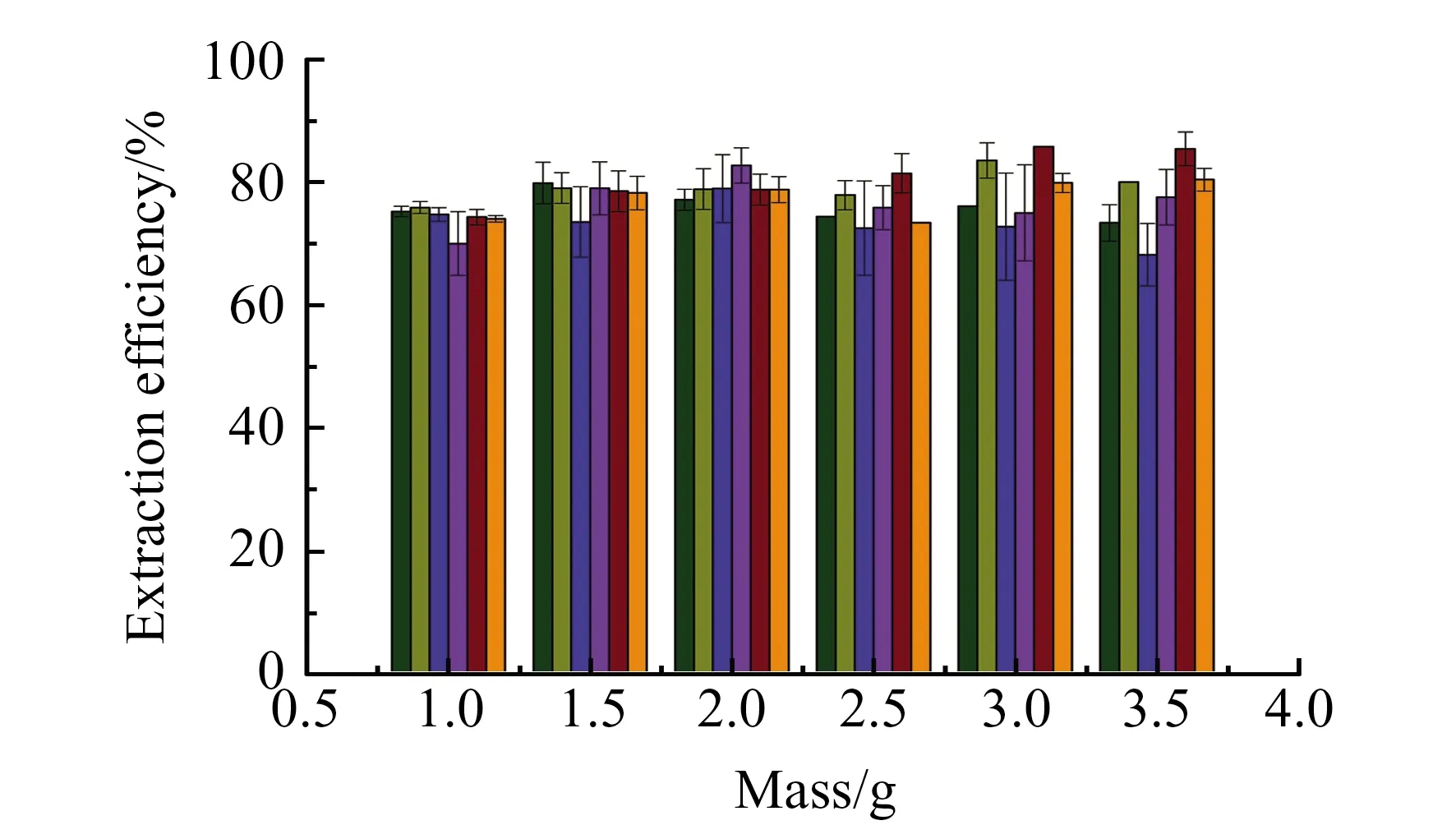
图3 萃取剂用量对多环芳烃化合物萃取效率的影响Fig.3 Effect of extractant amount on the extraction efficiency of PAHs
2.2.3 萃取时间的选择有效的超声萃取时间可以加速分析物从牛奶样品中向DESs相的转移。固定DESs用量,探讨了超声萃取时间在3~18 min范围内对萃取效果的影响(图4)。结果表明,在3~6 min范围内,6种目标物萃取效率都迅速增加,在9 min时,DESs对6种PAHs都达到了比较好的萃取效果。随着萃取时间的进一步增加,萃取效率基本不发生变化,因此实验选择萃取时间为9 min。
2.2.4 萃取温度的选择温度会影响DESs多种物理化学性质,如粘度、表面张力、扩散率、电导率和热容量[15]。升高温度通常会降低DESs的粘度和表面张力,增加溶剂的扩散率,从而促进DESs在样品基体中的渗透,增加和目标物的相互作用,提高其萃取效率。实验探讨了在20~60 ℃范围内,萃取温度的变化对多环芳烃的萃取效率的影响。从图5可以看出,在20~30 ℃范围内,各分析物的萃取效率随温度的升高而增大,当温度进一步增加,其中芴、蒽、屈和苯并[a]芘这四种目标物的萃取效果波动不大,但是荧蒽和芘这两种物质的萃取效果随着温度的增加而增加,当温度达到50 ℃时效果最好。因此,实验选择50 ℃作为最佳的萃取温度。
2.2.5 NaCl用量的选择牛奶基质比较复杂,其中蛋白会对目标物提取产生一定的影响,本实验选择使用NaCl来消除这种影响,同时探讨了NaCl的用量对萃取效果的影响。结果表明随着NaCl的用量增加,目标物的萃取效率逐渐增大,当NaCl的用量超过0.3 g时,萃取效果有下降的趋势,因此实验选择NaCl的用量为0.3 g。
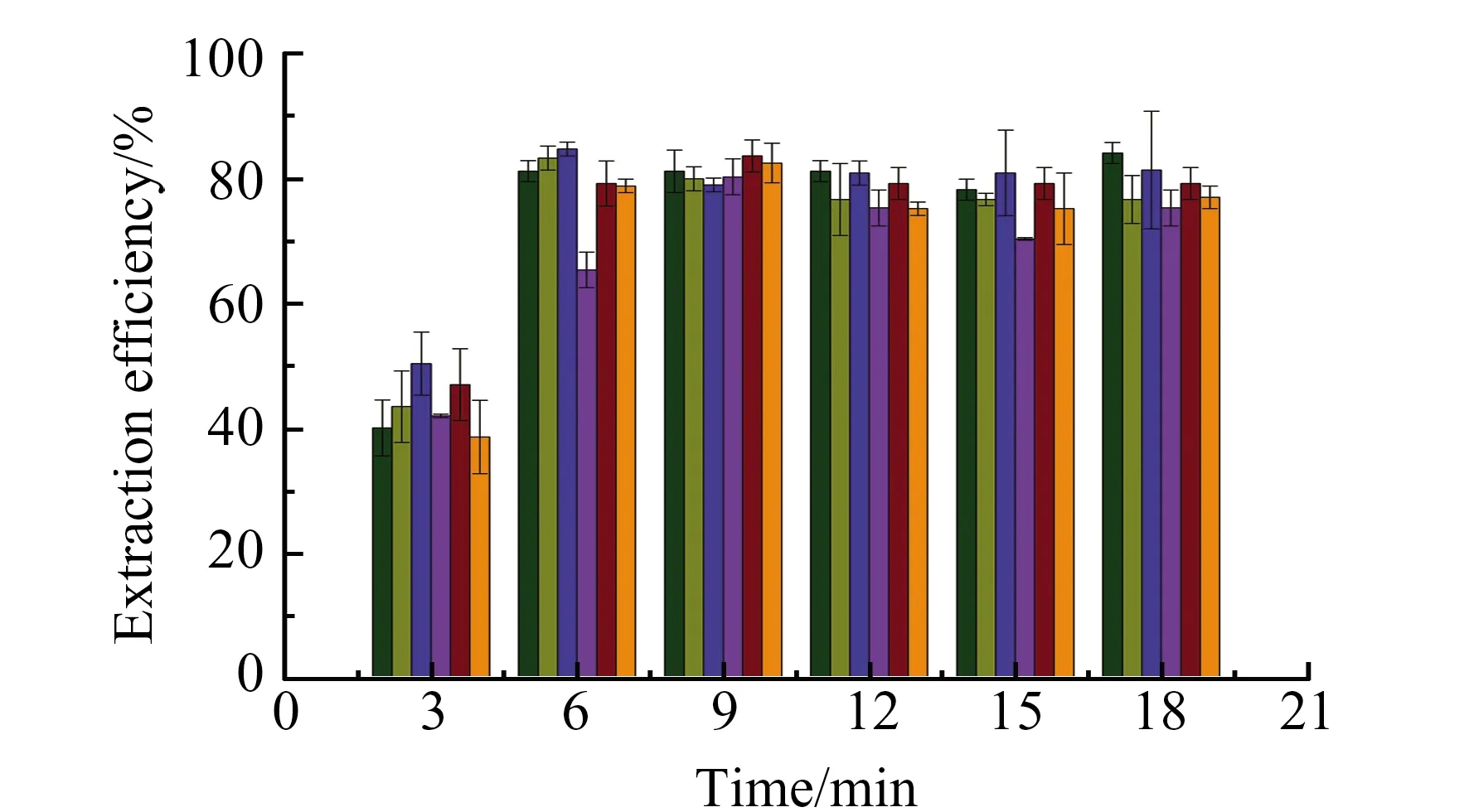
图4 萃取时间对多环芳烃化合物萃取效率的影响Fig.4 Effect of extraction time on the extraction efficiency of PAHs
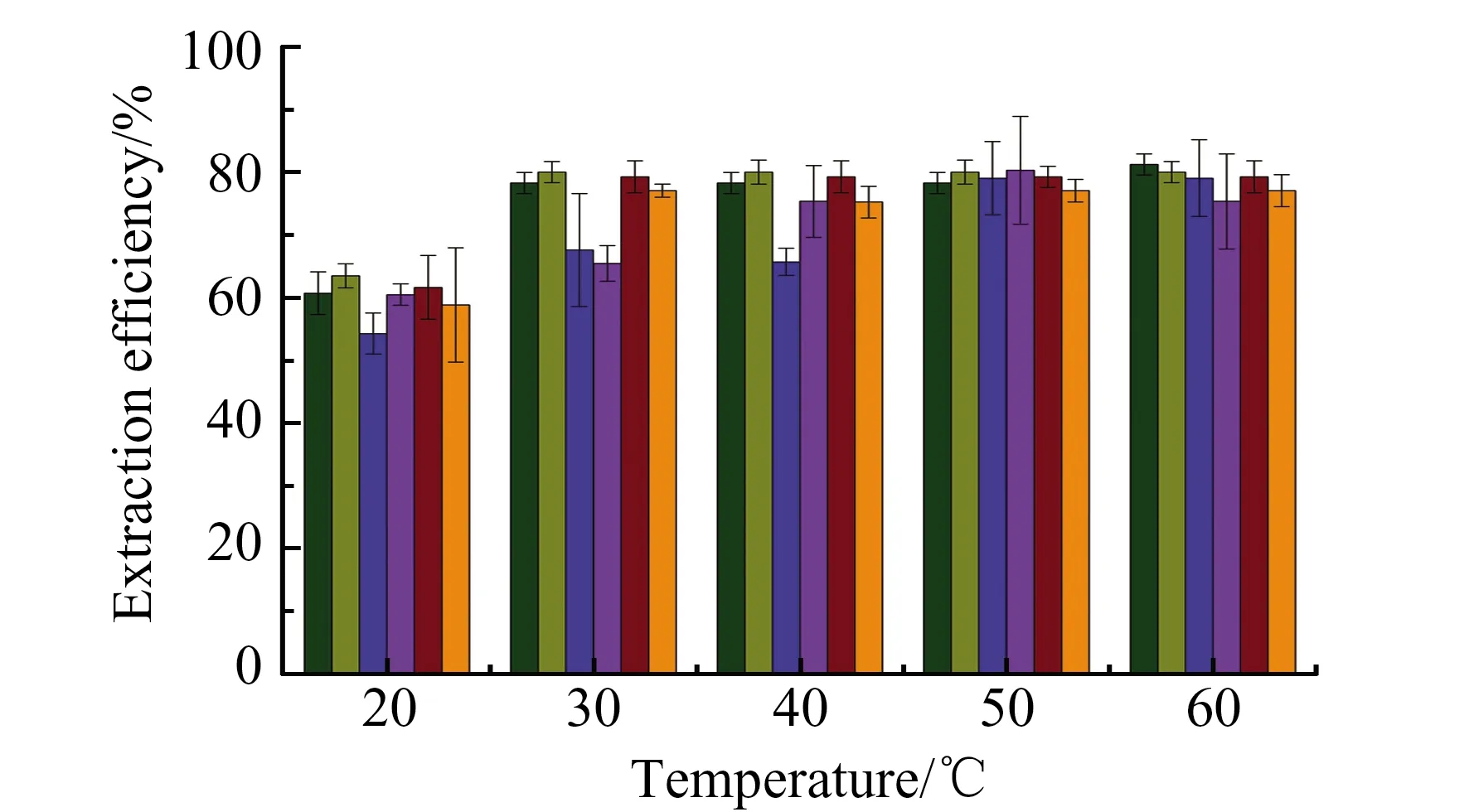
图5 萃取温度对多环芳烃化合物萃取效果的影响Fig.5 Effect of extraction temperature on the extraction efficiency of PAHs
2.3 方法的评价
2.3.1 方法的线性范围和检测限配制一系列不同浓度的6种PAHs化合物混合标准溶液,在优化的实验条件下进行测定,结果见表3。结果表明,6种分析物在一定的浓度范围内具有良好的线性关系,检测限在0.03~0.3 μg/kg之间,定量限为0.1~1 μg/kg。
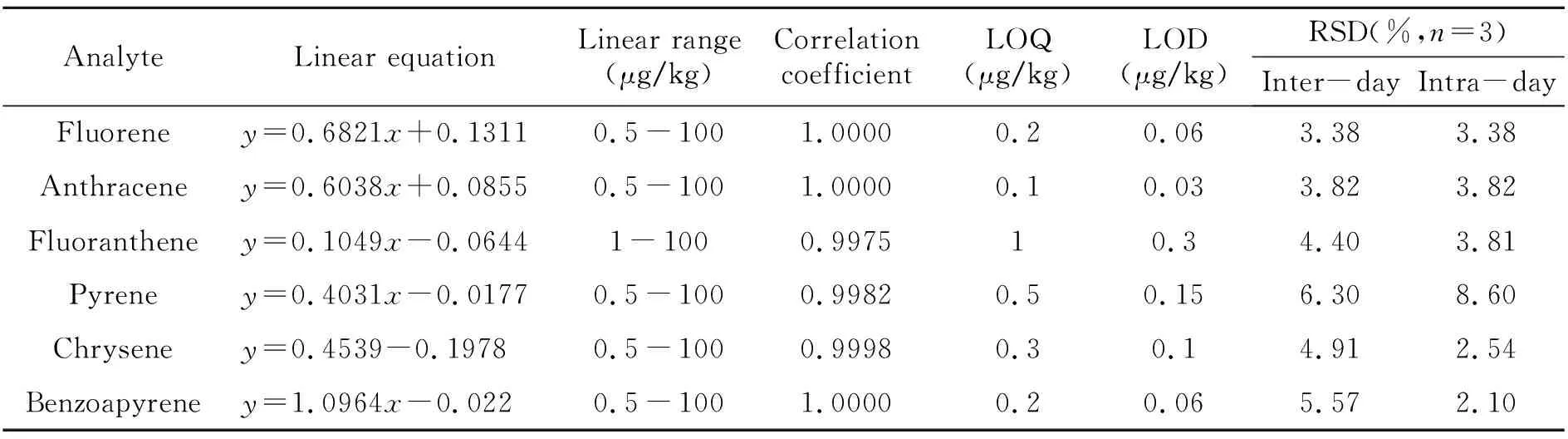
表3 分析物的线性方程、相关系数、检出限(LOD)、定量限(LOQ)和精密度(RSDs)
2.3.2 样品分析及加标回收实验应用所建立的分析方法,对当地超市的2种牛奶样品(低脂牛奶和全脂牛奶)进行检测,2种牛奶样品中均未检测出6种PAHs化合物。在牛奶样品中分别添加3个不同浓度水平的PAHs混合标准进行加标回收实验,其结果见表4。加标回收率在70.87%~100.45%之间,相对标准偏差(RSD)在1.05%~8.95%之间。日间RSD为3.38%~6.30%,日内RSD为2.10%~8.60%。说明该方法的准确性和重现性较好,适用于牛奶中PAHs的分析。
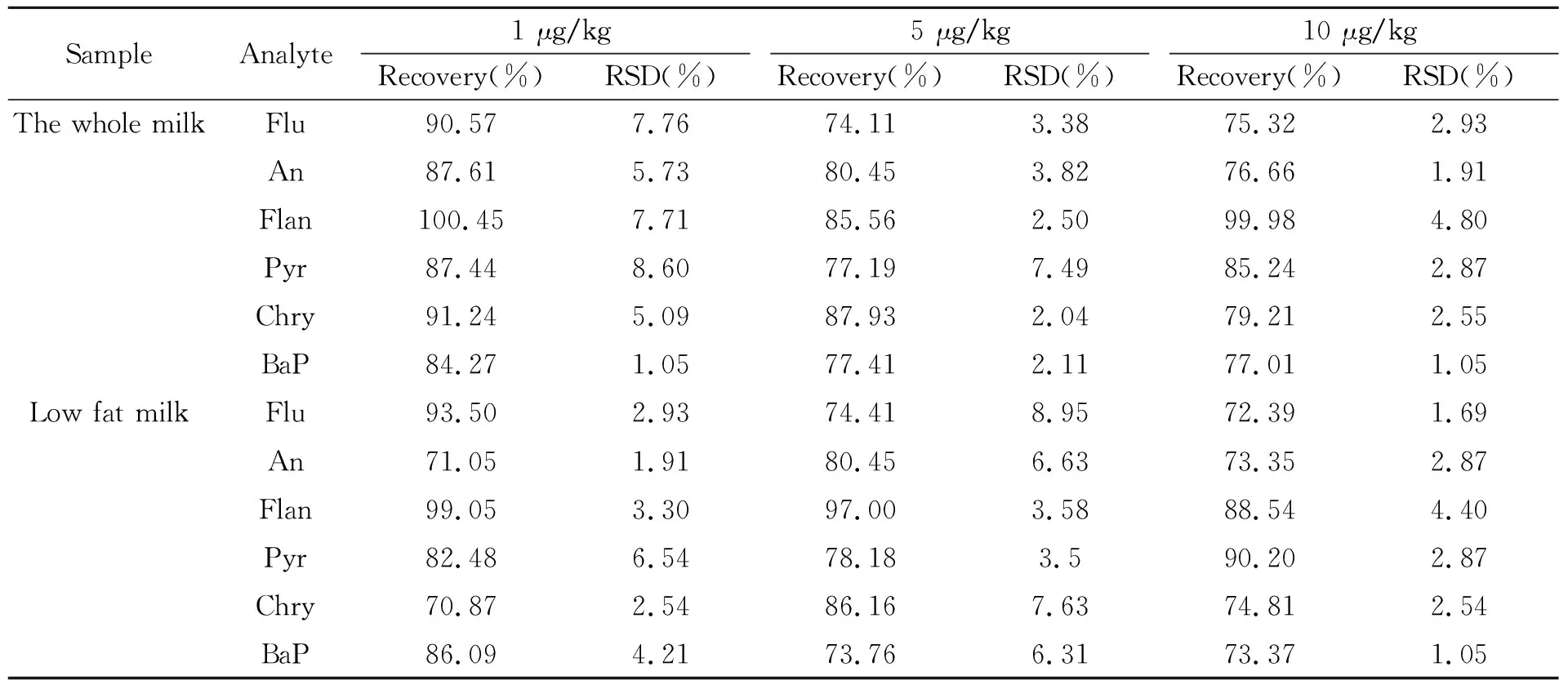
表4 牛奶样品中6种多环芳烃的加标回收结果(n=3)
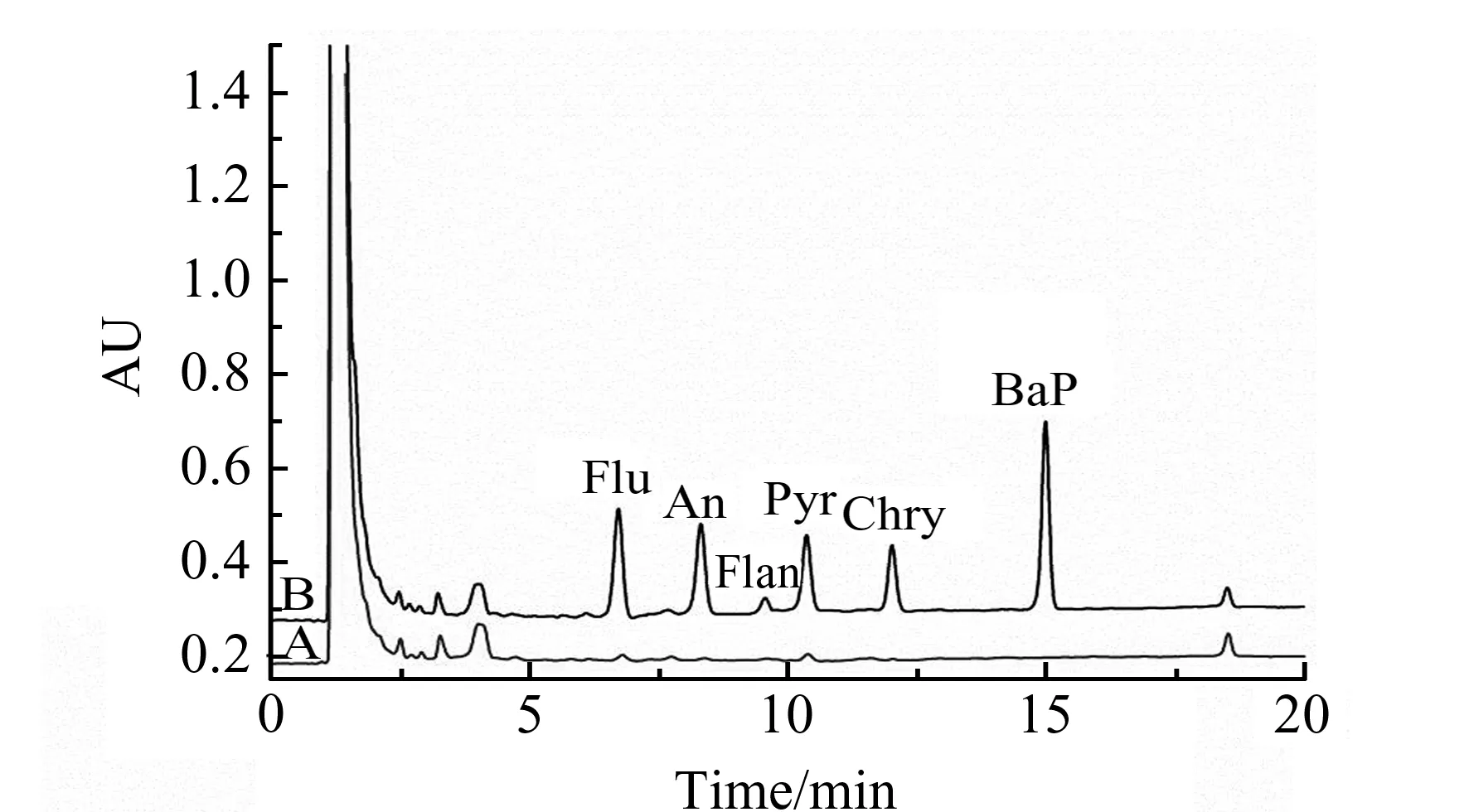
图6 牛奶样品未加标(A)和加标(5 μg/kg)(B)后的色谱图Fig.6 Chromatograms of the analyte of the non-spiked(A) and spiked(B) milk samples(5 μg/kg)
样品分析色谱图见图6。
2.4 与其他方法的比较
将本文所建立的方法与所报道的关于牛奶中PAHs的检测方法进行了对比(表5)。从表中可以看出,本方法与其他关于牛奶中PAHs的检测方法相比,具有样品前处理时间短、操作简便、灵敏度高等特点。尤其是本文采用绿色、环保的DESs对目标物进行萃取,避免了使用有机溶剂。
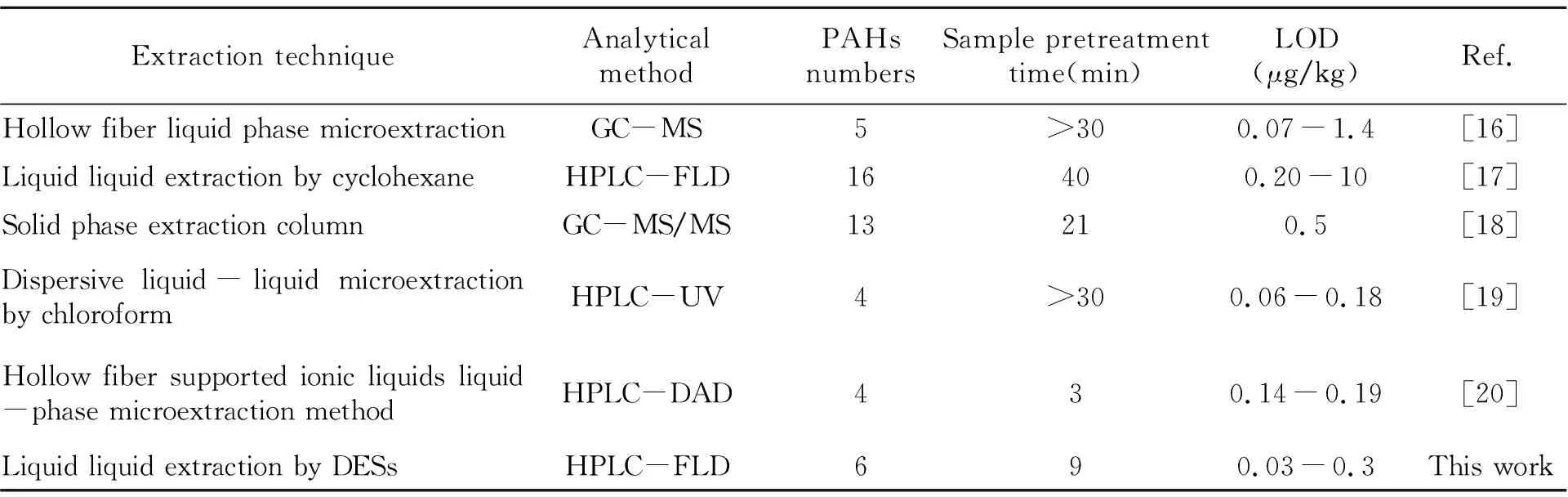
表5 分析方法的比较
3 结论
本文以四丁基氯化铵和正辛醇为原料制备了疏水性低共熔溶剂,并应用于牛奶中6种多环芳烃化合物萃取分离,结合高效液相色谱-荧光检测技术,建立了牛奶中6种多环芳烃化合物同时分析新方法。该方法具有操作简单、成本低、绿色环保等优点,能较好地满足牛奶样品中多环芳烃污染物的监测。

