新型冠状病毒疫苗研发策略分析
宋旭东,张福珍,袁毅君,王廷璞*
(1.天水师范学院 生物工程与技术学院,甘肃 天水 741001;2.兰州理工大学 生命科学与工程学院,甘肃 兰州 730000;3.江苏大学 生命科学学院,江苏 镇江 212013)
2019年末新型冠状病毒开始在全球肆意传播,对人类的健康造成极大危害,而疫苗的研发是从根本上控制病毒传播的最有效手段。本文拟从疫苗研发的不同路径以及研发中需着重注意的几个关键问题入手,分析探讨新型冠状病毒疫苗研发策略,旨在为疫苗研发提供一些参考。
1 新型冠状病毒概述
新型冠状病毒在2019年末或更早几乎同时在所有国家传播。[1]世界卫生组织(WHO)最终将其命名为COVID-19(Corona Virus Disease 2019),国际病毒学分类委员会(International Committee On⁃Taxonomy of Viruses,ICTV)冠状病毒研究小组(Coronaviridae Study Group of CSG)将其命名为“严重急性呼吸综合征(Severe acuterespiratory syn⁃dromes,SARS)冠状病毒-2”(SARS-CoV-2)。[2-3]新型冠状病毒迅速蔓延全球,导致感染者严重的肺部炎症反应和急性肺部损伤,是造成此次突发公共卫生事件的元凶。Worldometers世界实时统计数据显示,截至北京时间2020年10月20日7时30分,全球新冠肺炎累计确诊病例超过4061万例,达到40,610,267例,累计死亡病例超过112.2万例,达到1,122,192例。全球219个国家和地区受到影响。[4]
冠状病毒(coronavirus,CoV)在系统分类上属套式(又称巢式)病毒目(Nidovirales)、冠状病毒科(Coronaviri-dae)、冠状病毒亚科(Corona⁃virus)、冠状病毒属 (Coronavirus)。[5]因其在电子显微镜下呈现如日冕般外围的冠状特征,表面有形似中世纪欧洲帝王皇冠的棘突而得名。在基因型和血清学上又分为四个属,即α,β,γ和δ冠状病毒。[6-7]感染人类的第一株冠状病毒于1965年被分离出来,SARS-CoV-2是迄今为止发现的第7种可以感染人类的β属冠状病毒。[7]通过构建该病毒全基因组进化树发现,SARS-CoV-2与云南的中华菊头蝠冠状病毒Bat CoVRaTG13的基因组同源性最高,为96.2%;与BAT-SL-CoVZC45和BAT-SCoVZXC21(分别是在中国浙江2015年和2017年在蝙蝠体内分离到的类SARS样冠状病毒)的亲缘关系较近,序列同源性为88%;与SARS-Co-V的较远约79%,与中东呼吸综合症冠状病毒MERSCoV的更远,仅50%,[8-10]所以认为该病毒的原始宿主为蝙蝠。
近期研究表明,人类血管紧张素转换酶II(Angiotensin-converting enzymeII,ACE2)是SARSCoV-2与宿主细胞结合的重要受体。[11]其主要通过受体介导的内吞作用进入细胞,从而破坏纤毛支气管上皮细胞和II型肺泡细胞。
1.1 SARS-CoV-2结构特点
SARS-CoV-2是一种大型有包膜的线性单股正链RNA病毒,其基因组大小约为29.8kb,[12]是目前已知的RNA病毒中最大的。SARS-CoV-2基因组的5'端有甲基化帽子编码多种非结构蛋白,3'端有多聚腺苷酸(polyA)结构,该结构编码4种较为保守的结构蛋白,分别为表面刺突蛋白(Spike,S)、小包膜蛋白(Envelope,E)、外膜蛋白(Mem⁃brane,M)、核衣壳蛋白(Nucleocapsid,N),[13-14]其结构功能各异。对该病毒结构特点的深入研究,有助于针对其特异性疫苗的快速研发。研究证明SARS-CoV-2的宿主细胞靶受体与SARS-CoV相同为ACE2,而不是MERS-CoV受体DPP4,[15-16]ACE2在人体多种组织中都有分布。
1.1.1 SARS-CoV-2的棘突蛋白(S蛋白)
S蛋白是位于病毒表面的I类病毒融合蛋白,其编码基因用于病毒分型。冷冻电镜下可见以同源三聚体形式存在,呈典型的花瓣状囊膜突起。该蛋白含S1、S2两个亚基,其中S1主要包含有受体结合域(receptor binding domain,RBD),负责识别细胞的受体;S2含有的两个七肽重复序列HRI和HR2,参与病毒与细胞膜的融合,[17]从而导致病毒感染细胞。S蛋白的中和抗体可阻断这一过程从而防止病毒侵入,[18]同时该蛋白还可有效刺激T细胞免疫应答反应,[19]因此是疫苗设计的重要靶点。
1.1.2 SARS-CoV-2的膜蛋白(M蛋白)
M蛋白是最丰富的结构蛋白,病毒包膜的形状由该蛋白决定。[13]它有三个跨膜区,从而促进膜弯曲。另外,M蛋白与N蛋白结合,[20]同时与E蛋白一起参与病毒装配。[21]
1.1.3 SARS-CoV-2的核衣壳蛋白(N蛋白)
N蛋白在病毒内部并包裹病毒RNA基因组,它是唯一一种与病毒RNA基因组结合形成核糖核蛋白复合物的蛋白质,[22]可作为病毒检测的诊断抗原。
1.1.4 SARS-CoV-2的包膜蛋白(E蛋白)
E蛋白是一种小的、完整的膜蛋白,参与病毒生命周期的组装、出芽、包膜形成和致病等,并充当离子通道,缺乏E蛋白的冠状病毒可作为候选疫苗。[21,23]
1.1.5 SARS-CoV-2非结构蛋白
目前对SARS-CoV-2的非结构蛋白研究较少,部分非结构蛋白在病毒复制中起作用,如:NSP1~16,但还有部分更加保守的非结构蛋白的功能尚未明确,[24]结构蛋白的多样化以便病毒适应新的不同宿主。[25]
1.2 SARS-CoV-2的复制周期
SARS-CoV-2感染宿主细胞的主要过程包括:附着和进入宿主细胞、复制酶的翻译和复制转录复合体的组装、基因复制和转录、结构性蛋白的翻译和病毒粒的组装和释放等(见图1)。[26]首先SARS-CoV-2的S蛋白与宿主细胞表面受体结合诱导胞吞作用,通过蛋白受体-血管紧张素转换酶2(ACE2)的靶向识别进入细胞脱壳;以其RNA为模板,表达出病毒RNA聚合酶;再利用此酶完成负链亚基因组RNA(sub-genomic RNA)的转录合成、各种结构蛋白mRNA的合成,以及病毒基因组RNA的复制,结构蛋白和基因组RNA复制完成后;将在宿主细胞内质网、高尔基体上完成装配,经胞吐作用释放到细胞外,完成其生命周期。[27-28]
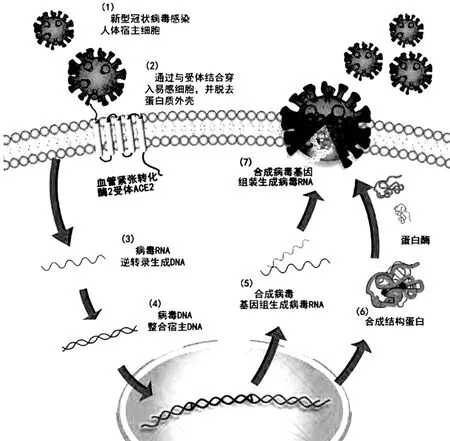
图1 SARS-CoV-2的复制周期[29]
1.3 SARS-CoV-2受体-血管紧张素转换酶2(ACE2)
ACE2是I型跨膜糖蛋白的一种,是SARS-CoV-2侵入人体的关键,体内多种组织细胞都能表达ACE2,(见表1)。研究者利用冷冻电镜技术成功解析了SARS-CoV-2受体ACE2的全长结构,总分辨率为0.29nm,并发现该病毒S蛋白上的受体结合域(RBD)与ACE2有很强的结合能力。大量抗体通过靶向S蛋白上的RBD从而破坏病毒与受体的结合。[29]因此,SARS-CoV-2的S1亚基的RBD可以作为疫苗研发的重要作用靶点。此外,最新研究表明ACE2在人体的睾丸、肺部和肾脏表达量最高,而在卵巢组织中并未检测到其表达。由此推断,睾丸可能成为病毒储存库,导致男性发病率更高。[30-34]
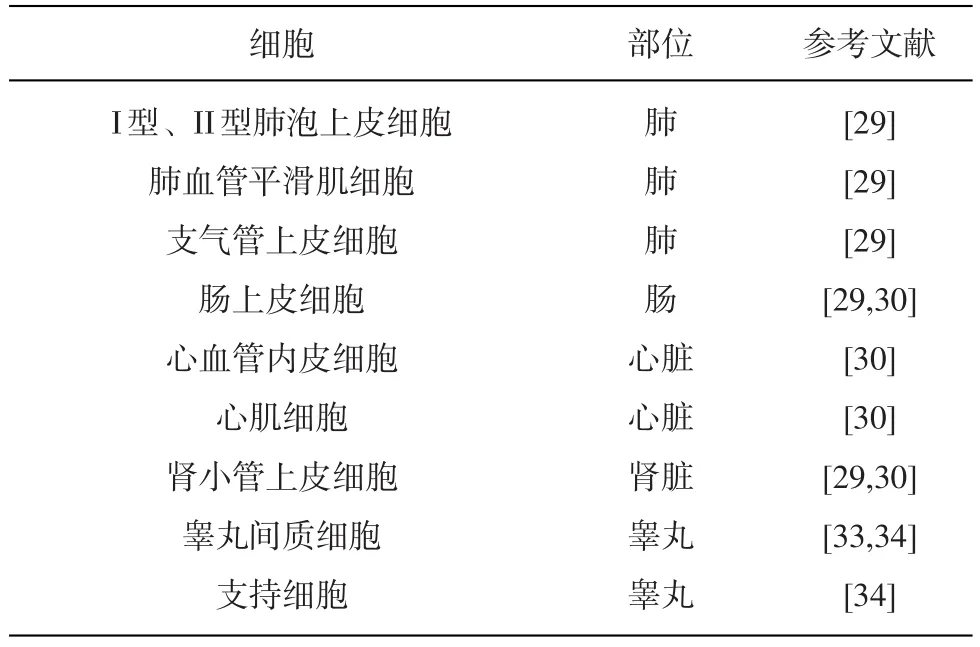
表1 表达ACE2的组织细胞
2 新冠疫苗研发的一般流程与现状
疫苗泛指一切通过注射或黏膜途径接种后,可以诱导机体产生针对特定致病原的特异性抗体或细胞免疫,从而使机体获得保护或消灭该致病原能力的生物制品,包括蛋白质、多糖、核酸、活载体或感染因子等。通过疫苗接种是保护易感人群,控制传染性疾病有效的、经济的手段。疫苗的使用使人类得以在全球范围内消灭了传染性极强的天花,控制了白喉、百日咳、脊髓灰质炎、麻疹等,显著降低了传染病的发病率和死亡率。[35]随着分子生物学、免疫学等学科的迅速发展,疫苗制备有不同策略,现代病毒性疫苗种类多种多样。疫苗研究正逐步从传统疫苗如灭活病毒疫苗、减毒病毒疫苗发展到新型疫苗,包括病毒载体疫苗、亚单位疫苗、核酸疫苗(mRNA疫苗和DNA疫苗)等。新型疫苗拓展了对疫苗组成和功能的认识,也代表着疫苗研发的方向。截至目前世界上已注册并正式投放市场能有效防控新冠疫情的新型疫苗还没有,新型冠状病毒疫苗研发迫在眉睫。[36]
2.1 SARS-CoV-2疫苗研发流程
疫苗的研发包括三个阶段(见图2):一是疫苗前期研发,包括获得免疫原、免疫反应测试、动物保护测试、免疫原生产工艺(放大)优化、临床前毒理研究等环节;二是疫苗研发及注册过程,包括临床前研究、申报临床、开展临床试验,最后疫苗注册上市。疫苗的研发过程到疫苗上市和批签发具有长周期性。[37-38]因此,SARS-CoV-2疫苗至少需要18个月才有可能研制成功。
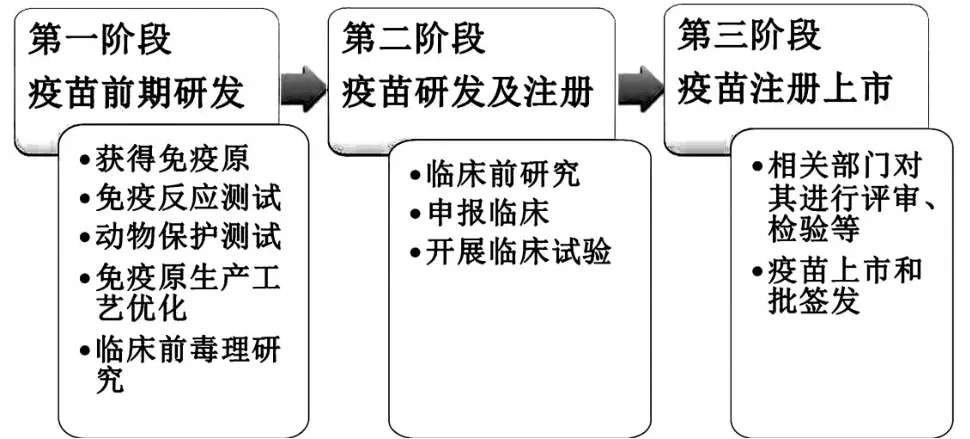
图2 SARS-CoV-2疫苗研发流程图
2.2 SARS-CoV-2疫苗研发类型
目前全球正在研发的有90多种针对SARS-CoV-2的疫苗,其中积极研制的至少有八种类型,[39]它们主要依赖于不同的病毒形式或病毒组分。这里主要对全病毒疫苗、病毒载体疫苗、核酸疫苗、基于蛋白类疫苗进行简要概述。
2.2.1 减毒活疫苗
减毒活疫苗是对病原体进行减毒处理(利用体外传代或基因重组等方法)后从而得到的致病力减弱但仍然具有良好免疫原性的疫苗制品,另外它是一种由完整的病毒组成的疫苗类型。[40-42]由于减毒活疫苗的免疫原性强,能引起更大范围的免疫反应,保护作用相对更持久。但因其含有活病原体,减毒活疫苗存在隐形感染隐患。另外不同的减毒活疫苗中病原体的致病能力各不相同,该类疫苗存在一定的毒力回升风险,安全性不是很高。
2.2.2 灭活疫苗
灭活病毒即死疫苗,通过理化方法(甲醛等)使病毒灭活,失去其感染性保留抗原性,需要进行多次试验和筛选。灭活疫苗保留了病毒原有的表面蛋白,抗原性与活病毒相似,但已经无法在宿主体内复制与引发感染,不存在毒力回升的问题。[42-44]因此,与减毒活疫苗相比,灭活疫苗的安全性更高,不会导致人体感染。灭活疫苗不能模拟自然感染,免疫原性不足,因此其效果低于减毒活疫苗,但可以通过增加剂量和接种次数弥补。目前,灭活疫苗的技术路线发展成熟,研发时间短。
2.2.3 亚单位疫苗
灭活疫苗成分复杂,含有病毒的多种结构蛋白和非结构蛋白。亚单位疫苗组成简单,一般仅含有一种或者几种病毒蛋白,不需要病毒的培养与灭活,生物安全性相对更高。
SARS-CoV-2可能包括S蛋白、M蛋白、N蛋白、E蛋白以及1ab/3/7/8/9/10b/13/14等12种结构蛋白。[44]对这些结构蛋白功能与免疫原性进一步分析,将有助于SARS-CoV-2亚单位疫苗的研发。
2.2.4 复制型病毒载体疫苗
我国新冠疫苗的5条研发路线中有1条就是流感病毒载体疫苗,这类疫苗安全性较高,但是针对载体产生超强的免疫反应可能会削弱疫苗本身的有效性。以现有的流感病毒疫苗中的减毒流感病毒作为载体,将编码SARS-CoV-2S蛋白的基因转入到流感病毒载体的基因内,让流感病毒表面表达S蛋白。[45]以流感病毒为载体的新冠病毒疫苗可以同时预防新冠肺炎和流感,且流感病毒无DNA,没有将流感病毒DNA整合进宿主基因组的风险。但流感病毒的容量较小,限制了可插入外源基因的范围,且载体的靶向性不高。
2.2.5 非复制型病毒载体疫苗
腺病毒作为常用的疫苗载体,具有结构小、安全性好、感染范围广及重组腺病毒获得方便等特点。腺病毒载体技术是以改造后无害的腺病毒为载体,将S蛋白的基因转入腺病毒的基因内(与流感病毒载体不同的是,腺病毒表面并不会表达S蛋白)。接种该疫苗后,腺病毒载体会进入细胞,由于基因缺陷,腺病毒本身无法复制,但其基因内的S蛋白基因通过转录翻译表达S蛋白,这种S蛋白从细胞内转移到细胞外,从而引动人体的免疫应答,效果较好。无法自我复制的腺病毒则会被人体免疫机制清除,不会对人体造成影响,安全性高。埃博拉疫苗(腺病毒载体疫苗)的研发经验为此次SARS-CoV-2的疫苗研发奠定了一定的基础。[46-47]
2.2.6 DNA疫苗
DNA疫苗直接将编码病毒抗原基因片段的DNA序列(常用质粒)注入宿主,使病毒的抗原蛋白在宿主体内表达,进而激活体液免疫和细胞免疫。该类疫苗能模仿活病毒感染方式合成内源性抗原。DNA疫苗的制备不需要获得病毒,研发机构可以根据中国分享的SARS-CoV-2的基因序列直接制造疫苗。[48-49]然而,DNA疫苗的缺点在于这种外来的DNA可能会与细胞自身的DNA整合,因此DNA疫苗尤其需要关注其安全性。
2.2.7 mRNA疫苗
mRNA疫苗与DNA疫苗的技术路线类似,mRNA疫苗的原理是将病毒抗原的mRNA制为疫苗,注入宿主的mRNA可以表达病毒的抗原蛋白,从而诱发机体产生免疫应答。直接用mRNA做疫苗,无须像DNA疫苗一样先进入细胞核完成转录过程再在胞浆进行蛋白质的翻译表达,mRNA疫苗可以直接在细胞浆内合成蛋白,比DNA疫苗省了一步。mRNA疫苗的步骤简化,不用担心病毒DNA整合到宿主DNA上。[49-50]但是,mRNA不如DNA或蛋白质稳定,其最大的缺陷就是容易降解,如何保证mRNA能够顺利进入宿主细胞并产生具有一定免疫原性的蛋白质是一个难点。
2.2.8 基于S蛋白的疫苗
基于蛋白质的疫苗不需要培养病毒,只需要知道病毒的基因序列,再利用现代生物技术合成病毒的蛋白质(重组蛋白)即可。由于不需要培养病毒,该类疫苗比灭活病毒疫苗开发更快,需要找到最强抗原效应的蛋白是该类疫苗成功研发的关键。S蛋白被认为是SARS-CoV-2与人体细胞上的ACE2受体的结合部位,在体外完成S蛋白的表达后再将其用于制备疫苗。这种疫苗保留了病毒的抗原性而没有病毒的致病性,不会因病毒感染而致病,安全性好。由于体外表达的蛋白通常由MHC II分子呈递,所以基于蛋白质的亚单位疫苗无法像载体疫苗一样在细胞内表达抗原进而被MHC I呈递而激活T细胞发挥杀伤作用。[39,45]
2.2.9 基于病毒外壳的疫苗
该类疫苗为病毒空外壳(Virus-like particle,VLP),不含有病毒的遗传物质。通过病毒外壳模拟冠状病毒的结构,具有抗原性而不会使宿主产生感染。安全性较高,但是生产这种VLP较为困难。[48]
2.3 SARS-CoV-2疫苗研究现状
疫苗是防控SARS-CoV-2等一系列传染病的最佳手段。面对汹涌而来的疫情,国内外研究人员争相投入到疫苗的研发工作中,开始了与病毒的时间赛跑,当前全球多种新冠肺炎疫苗正处于研发阶段,多个研发技术并行推进了疫苗开发,包括灭活疫苗、减毒活疫苗、重组蛋白疫苗、病毒载体疫苗、核酸疫苗(mRNA疫苗和DNA疫苗)等,截至2020年3月15日已有部分SARS-CoV-2疫苗进入动物试验阶段。在2020年1月26日左右,SARSCoV-2的病毒毒株相继由中国疾病预防控制中心和浙江省疾病预防控制中心分离出,这为疫苗研究奠定了基础。与SARS-CoV和MERS-CoV一样,SARS-CoV-2的S蛋白及其中所包含的RBD依旧是疫苗研发的主要靶点。[23]在流行病防范创新联盟的倡导和资助下,针对SARS-CoV-2的疫苗研制项目也相继公布。截至2020年7月20日,全球有大约250种SARS-CoV-2疫苗在研发中,其中至少有17种疫苗正处于临床试验阶段。9月9日,WHO最新数据显示,我国已有25个新冠疫苗进入到临床或者临床前阶段,在进入临床阶段的疫苗中我国有11个,占全球的31%,进入到临床三期的我国有4个,占全球三期临床试验总数的44%。[51]相关国内研究机构有中国武汉生物制品研究所与中国科学院武汉病毒研究所、北京生物制品研究所、科兴中维、厦门大学和香港大学等,国外研究机构有葛兰素史克公司(GSK)、美国Moderna和Inovio公司、德国BioNTech公司、英国牛津大学和AstraZeneca公司等。以下就国内外对SARS-CoV-2疫苗研究现状进行概述。
2.3.1 国内SARS-CoV-2疫苗研究现状
2020年1月,中国CDC病毒所开始了SARSCoV-2疫苗研发、筛选种子毒株。2020年3月初,国务院应对新型冠状病毒感染肺炎疫情联防联控机制宣布,5类疫苗研发路线同步进行,包括灭活疫苗、基因工程重组亚单位疫苗、腺病毒载体疫苗、核酸疫苗和减毒流感病毒载体疫苗。3月末,腺病毒载体重组疫苗由中国军事科学院军事医学研究院陈薇院士团队研发并完成I期临床试验阶段,成为我国首个进入临床研究的SARS-CoV-2疫苗,4月中开始II期临床试验,这也是全球第一个进入II期临床研究的新冠疫苗。此外,我国多家研究机构在4月相继进入不同时期SARS-CoV-2灭活疫苗临床试验研究阶段,其中12日中国武汉生物制品研究所与中国科学院武汉病毒研究所协同攻关的SARSCoV-2灭活疫苗率先获得全球首个临床试验批件,本月末进入II期临床试验阶段。随后科兴中维研制的SARS-CoV-2灭活疫苗被国家药品监督管理局批准并开展临床试验,16日进入I期临床试验阶段。28日,北京生物制品研究所研发的灭活疫苗获得临床批件,并于河南进行临床试验。截至4月底5月初,我国有4项针对SARS-CoV-2的疫苗处于临床试验阶段,包括1个腺病毒载体疫苗其已进入II期临床试验阶段和3个灭活病毒疫苗。[52-54]6月19日,国内首个获批开展临床试验的mRNA疫苗ARCoV由军事科学院军事医学研究院与地方企业共同研发;同日国家药品监督管理局批准了中科院微生物研究所和安徽智飞龙科马共同研发的新冠重组蛋白疫苗进入临床试验。6月28日高福等研究报道了一种针对COVID-19、MERS和SARS的β冠状病毒疫苗的通用设计。[55]8月16日,中国首个新冠疫苗(Ad5-nCoV)专利由军科院军事医学研究院陈薇院士团队及康希诺生物联合申报并被授予专利权。[56]截至9月25日,我国有11个新冠病毒疫苗进入临床试验阶段。4个疫苗进入三期临床试验,其中3个为灭活疫苗,1个为腺病毒载体疫苗。[46,51]
2.3.2 国外SARS-CoV-2疫苗研究现状
2020年2月3日,英国伦敦帝国理工学院的疫苗研发处于动物试验结果验证阶段。葛兰素史克公司(GSK)与流行病防范创新联盟(CEPI)宣布合作。美国多家企业迅速开启SARS-CoV-2疫苗研发,其中Moderna开展的mRNA疫苗经该国家过敏和传染病研究所开展了临床前评价但并未开展动物试验,其产品mRNA-1273于2020年3月16日开始I期临床注射试验。[57]次月6日,美国Inovio公司的DNA疫苗INO-4800进入I期临床注射,40位志愿者接受了该疫苗的注射;16日,Inovio宣布与国际疫苗研究所(IVI)及韩国国立卫生研究院(KNIH)将合作开启I、II期临床试验。德国生物新技术公司BioNTech与辉瑞进行合作的mRNA疫苗于4月22日获得批准并启动临床试验,其研发疫苗BNT162以四种RNA疫苗(两种核苷修饰的mRNA,一种包含尿嘧啶核苷的mRNA和另一种可自我复制的mRNA)同时启动I、II临床试验。目前在纽约的Farmingdale生物公司开展通过改变SARS-CoV-2的基因密码从而降低致病风险的减毒活疫苗的研发。5月初英国牛津大学研发的是非复制性病毒载体疫苗ChAdOx1正处于I期临床试验阶段,牛津大学与AstraZeneca公司宣称双方将共同研发、大规模生产ChAdOx1疫苗。[58]8月11日,俄罗斯注册了第一个新冠病毒疫苗——“卫星-V”(SPUTNIK V)。[59]11月9日,美国辉瑞制药公司宣布与德国生物科技公司BioNTech共同开发新冠mRNA疫苗BNT162b2能有效阻止90%的感染。[60]
3 展望
新型冠状病毒从去年年底开始在全球迅速传播,而疫苗将是对抗该病毒的重要武器。在SARSCoV-2面前,不同的研究机构有不同的疫苗研发路径,疫苗从研发到上市需要18个月到十年不等,研发周期长,这就需要加快疫苗研发的速度。因而中国香港大学医学院通过改造已有的流感疫苗,即加入SARS-CoV-2的S蛋白的表达序列从而实现缩短研发周期的目的,同样的法国巴斯德研究所也利用此方法对麻疹疫苗进行改造。为缩短疫苗研发时间,可以用已成熟的疫苗平台研发SARS-CoV-2疫苗,此外核酸疫苗的研发流程较短也可缩短研发周期。
疫苗研发需要考虑其安全性和有效性,首先对于安全性,疫苗研发需要培养SARS-CoV-2病毒,因而存在没有完全灭活的病毒,那么这些病毒的蛋白可能会引起炎症反应;细胞免疫病理反应(cel⁃lular immunopathology)也是疫苗研发潜在的风险;疫苗可能会引起抗体依赖性免疫增强作用(anti⁃body-dependent enhancement,ADE),即疫苗不仅使机体产生中和抗体而且也可使机体产生无中和抗体活性但可增强病毒感染的抗体,从而加重病毒感染。以上这些风险在疫苗研发过程必须考虑并要克服。其次对于疫苗的有效性,需考虑免疫原性即抗体水平及免疫持久性。哪一种疫苗安全性和有效性更好,目前无法下结论,针对这一问题,可以考虑两种或两种以上疫苗联合使用,从而达到更理想的效果。
另外,新型冠状病毒存在变异和进化的情况,通过改变其结构以适应新的环境。这使得疫苗研发更加困难,也使得针对其特异性疫苗的使用范围变得非常有限,如可能会出现适用于一个地区的疫苗不能适用于其他地区,也可能会出现适用于一个时间段的疫苗而不适用于别的时间段。这为疫苗研发工作带来巨大挑战,针对此难题,需要不断对其尚未认知的结构组成进行深入研究,对该病毒的检测更快速精准。另外在此基础上提前预测其变异形式,做好应对之策,也不失为一种方法,而要从根本上消灭病毒,则要考虑DNA疫苗,由于其不用分离病毒,可快速合成,从而有效应对病毒变异。因此成功研制新型冠状病毒疫苗任重而道远。即使在与病毒做斗争的路途中困难重重,坚信人类终将战胜它。

