车前子对腹泻大鼠炎性因子和结肠组织AQP8蛋白表达的影响
彪雅宁,张纳博,张睦清,郭秋红,王 月,韩 雪,张一昕*
1河北中医学院药学院 河北省高校中药组方制剂应用技术研究中心,石家庄 050200;2河北省中医院心内科,石家庄 050011
腹泻是临床常见的由多种因素所导致的肠道水液代谢紊乱的一种疾病,其临床表现多样,以大便次数频多、粪质稀薄或呈水样为主要特征,若病情急重或迁延不愈可导致脱水、电解质紊乱、酸碱失衡、影响生长发育,甚至危及患者生命[1,2]。中医学认为,泄泻的主要病因是湿,故通利小便,排泄水湿为常用治法。车前子(PlantagoasiaticaL.)为车前科植物车前PlantagoasiaticaL.或平车前PlantagodepressaWilld.的干燥成熟种子,具有利尿通淋,渗湿止泻,明目,祛痰功效,其入小肠经,善能通水道而分清浊,利小便以实大便,药理研究也表明其具有止泻之功,临床单味或随证配用治疗腹泻效果显著[3,4],但其止泻的作用机制尚不明确。
结肠具有吸收水分、电解质、浓缩食物残渣并形成粪便等功能。研究发现,水通道蛋白(aquaporins,AQPs)广泛分布在肠道上皮和内皮组织细胞膜上,是负责跨细胞转运水分子的主要蛋白,炎症反应是腹泻发生发展的病理生理基础,若因炎症反应等因素导致肠道AQPs的表达异常,使肠道对水液的吸收减少,水分大量在肠道蓄积,便会导致腹泻的发生[5,6],因此AQPs的功能状态与腹泻的发生和转归具有非常密切的关系[7-9]。本实验采用番泻叶灌胃法复制腹泻大鼠模型,通过观察其对实验大鼠血清中肿瘤坏死因子α(TNF-α)、白细胞介素-6(IL-6)和 C反应蛋白(CRP)含量和结肠组织中AQP8蛋白表达的影响,探讨车前子止泻的可能作用途径和作用机理。
1 材料
1.1 动物
清洁级SD大鼠60只,雄性,6~8周龄,体质量160~180 g,由河北省实验动物中心提供,合格证号:SCXK(冀)2013-1-003。饲养于18~22 ℃明暗各12小时的实验室,自由进食水。该实验经河北中医学院伦理委员会批准同意,编号为:DWLL2018005。
1.2 药物
车前子配方颗粒(批号:8122593,当量比为15∶1)购于四川新绿色药业有限公司,由生产厂家将车前子饮片按照成熟的工艺,采用水煎全成分提取、浓缩、干燥、干法制粒而成。实验时将其加入到100 ℃适量的蒸馏水中,加热充分搅拌使其溶解,配至所需浓度。氢氯噻嗪片(山东仁和堂药业有限公司,批号:180922),实验时以0.5%的羧甲基纤维素钠溶液配成所需浓度的混悬液。番泻叶购于石家庄同仁堂药房,称取200 g番泻叶浸入1 000 mL 100 ℃纯净水中,充分搅拌,浸渍30 min后用四层纱布过滤,滤液蒸发浓缩至600 mL,制成番泻叶药液(含生药0.3 g/mL),置4 ℃冰箱中冷藏备用。
1.3 试剂
TNF-α、IL-6试剂盒(上海森雄科技实业有限公司,批号分别为SXR032,SXR063);CRP 试剂盒(北京普尔伟业科技有限公司,批号:20170926);AQP8一抗(赛默飞世尔科技(中国)有限公司,批号PA5-77713),辣根过氧化物酶(HRP)标记二抗、DAB显色试剂盒(北京中杉金桥生物技术有限公司,批号分别为K176716J、K182410E),苏木素-伊红(HE)染色液(河北博海生物技术有限公司,批号分别为20180526,20180618),Trizol(美国Invitrogen生命技术有限公司,批号:139603),TIANScript RT KIT、SuperReal PreMix Plus(中国北京天根生化科技有限公司批号分别为KR104-02、FP205)。
1.4 仪器
ELx800型酶标仪(美国BIO-TEK公司);1-15K型高速冷冻离心机(美国Sigma公司);HMIAS-2000型显微图像分析系统(武汉千屏影像技术有限公司);15D(P)型电泳仪及28D型电泳槽(北京六一生物科技有限公司);UVP 凝胶成像系统(中国Thermo公司);AE-6687半干转膜仪系统(日本ATTO公司);RM2016型切片机(德国Leica公司)。
2 方法
2.1 分组造模及给药
将60只大鼠按体质量随机分为正常组、模型组、氢氯噻嗪组和车前子低、中、高剂量组,每组10只。除正常组外,其余各组均于上午9∶00灌胃番泻叶药液复制大鼠腹泻模型,正常组灌胃等量蒸馏水;下午3∶00各治疗组灌服相应药物,正常组和模型组灌服等量蒸馏水。参照文献[10]确定番泻叶给药剂量为20 mL/kg,各组给药剂量按照人与大鼠体表面积系数进行换算,其中车前子低、中、高剂量组的大鼠用药剂量分别为:0.95、1.9、3.8 g/kg,氢氯噻嗪组大鼠的用药剂量为9 mg/kg,给药体积均为10 mL/kg,连续用药14天。每隔3天称量1次体质量,大鼠自由饮水进食,给药期间观察大鼠粪便情况。
2.2 标本采集
实验结束后以3.5%水合氯醛(10 mL/kg)采用腹腔注射方法将大鼠麻醉,腹主动脉取血,置洁净试管中,3 500 rpm,离心15 min,分离血清,检测相关炎性因子含量。取血后迅即剖取固定位置的适宜长短的结肠组织2份,剖开,生理盐水洗净,一份固定于4%多聚甲醛液,有待HE染色法观察结肠组织病理形态学及免疫组化法观察AQP8蛋白表达;另1份置于冻存管中液氮保存,以备Western blot法观察结肠组织AQP8蛋白的表达。
2.3 检测(观察)指标
2.3.1 各组大鼠粪便变化及一般情况
实验开始后,每天观察实验大鼠的进食量、毛发色泽、活动状态,特别是粪便质地等情况。
2.3.2 各组大鼠血清炎性因子含量变化
采用酶联免疫吸附测定(ELISA)法检测血清中TNF-α和IL-6的含量,放免法检测CRP的含量,以上严格按试剂盒说明书要求操作。
2.3.3 HE染色法观察结肠黏膜病理形态学变化
取4%多聚甲醛溶液固定的结肠组织,常规脱水、包埋、切片、HE 染色,显微镜下观察。
2.3.4 免疫组化法检测结肠组织中AQP8的蛋白表达情况
将4%多聚甲醛溶液固定的结肠组织,脱水、包埋、切片,滴加3%甲醇双氧水,室温处理20 min,自来水冲洗;切片高压修复后放入PBS中,滴加一抗,4 ℃过夜,次日取出待切片恢复至室温后,PBS清洗5 min×3;滴加二抗,37 ℃避光20 min后,PBS清洗5 min×3;滴加DAB显色剂,显色5 s后,水洗终止显色;苏木素复染,梯度乙醇脱水,二甲苯透明,封片,显微镜观察。根据阳性反映的图像灰度选择合适的灰度分割阈值并予以双阈值分割,获得标本的半灰度目标图像,测定阳性免疫染色的强度和面积,每组选取6例,分别测5个视野,计算测得的阳性反应相对含量的灰度值和面积,由平均吸光度值表示。
2.3.5 Western blot法检测结肠组织中AQP8的蛋白表达
称取约100 mg的结肠组织,液氮研磨,转移到含有1 mmol/L PMSF的900 μL RIPA中性裂解液中,混匀,超声裂解,配平后4 ℃,12000 rpm离心15 min,收集上清液,测定蛋白含量。蛋白煮沸变性以后,经SDS-PAGE凝胶电泳分离,然后转移到PVDF膜上,5%的脱脂奶粉封闭,一抗4 ℃孵育过夜,PBST洗膜3次,洗净未结合的一抗。将洗涤后的一抗反应膜放入二抗工作液中,室温孵育1.5 h,PBST洗膜3次,洗去游离二抗。暗室曝光,X胶片上显影,用Tanon Gis软件扫描各条带的吸光度值并分析结果。
2.4 统计学方法
3 结果
3.1 各组大鼠粪便变化情况
除正常组以外,其余大鼠灌饲番泻叶药液2天以后,排出夹杂黏液的水样稀便,腹泻发生率为100%,同时大鼠出现不同程度的食欲减少,精神差,活动减少,毛发干枯失去光泽,肛周体毛被稀便沾染。给药治疗4天后,各用药组大鼠粪便逐渐成形,含水量降低,但车前子各剂量组与正常组相比,大便仍偏于湿软。
3.2 各组大鼠结肠黏膜病理形态学变化
正常组大鼠结肠黏膜上皮较完整,细胞排列规整,未见肠黏膜表皮细胞坏死脱落,固有层腺体亦无萎缩,黏膜下层未见明显改变;模型组大鼠结肠黏膜表皮细胞出现凋亡坏死,固有层毛细血管扩张充血,少量中性粒细胞浸润;氢氯噻嗪组大鼠结肠表皮细胞少量凋亡坏死,上皮细胞核大小排列及染色与正常组一致,固有层毛细血管扩张轻微充血,少量中性粒细胞浸润;车前子低、中剂量组结肠黏膜表皮细胞少量凋亡坏死,上皮细胞增生活跃,核大,深染,排列密集,少量中性粒细胞浸润,低剂量组毛细血管充血现象明显;车前子高剂量组大鼠结肠黏膜表皮细胞偶见凋亡与坏死,上皮细胞增生减轻,偶见核分裂,固有层充血以及中性粒细胞浸润均缓解(见图1)。

图1 车前子对各组大鼠结肠黏膜病理形态学的影响(HE,×200)
3.3 各组大鼠血清中炎性因子含量变化
模型组大鼠血清中TNF-α、IL-6和CRP的含量与正常组比较均明显增加(P<0.05或P<0.01);车前子各剂量组血清中TNF-α和CRP的含量与模型组比较,均显著减少(P<0.05或P<0.01),中、高剂量组IL-6含量有下降趋势,但无统计学意义(P>0.05)(见表1)。

表1 各组大鼠血清中TNF-α、IL-6和CRP 含量的比较
注:与正常组比较,*P<0.05,**P<0.01;与模型组相比,△P<0.05,△△P<0.01。
Note:Compared with control,*P<0.05,**P<0.01;compared with model,△P<0.05,△△P<0.01.
3.4 各组大鼠结肠组织中AQP8蛋白表达水平变化情况
Western blot法检测结果:与正常组比较,模型组大鼠AQP8蛋白的表达水平明显降低(P<0.01);与模型组比,车前子各剂量组AQP8蛋白表达水平明显升高(P<0.05或P<0.01)(见表2,图2)。
续表2(Continued Tab.2)

组别Group剂量Does(g/kg)平均吸光度AQP8蛋白AQP8protein氢氯噻嗪组Hydrochlorothiazide0.0090.068±0.037△0.71±0.06△低剂量组Lowdose0.950.059±0.029△0.64±0.09△中剂量组Middledose1.90.075±0.032△0.82±0.05△△高剂量组Highdose3.80.097±0.043△△0.97±0.08△△
注:与正常组比较,*P<0.05,**P<0.01;与模型组相比,△P<0.05,△△P<0.01。
Note:Compared with control,*P<0.05,**P<0.01;Compared with model,△P<0.05,△△P<0.01.
免疫组化结果显示:AQP8免疫阳性表达产物为棕黄色颗粒,主要表达在结肠黏膜间质中,少量表达在上皮细胞。与正常组比较,模型组大鼠结肠组织中AQP8的阳性表达染色明显变浅,各治疗组大鼠结肠组织中AQP8的阳性表达较模型组明显增多、染色加重。经软件分析,结果表明:模型组的平均吸光度值较正常组显著降低(P<0.01),各用药组平均吸光度值较模型组明显升高(P<0.05或P<0.01)(见表2、图3)。

图2 各组大鼠AQP8蛋白表达情况(Western blot法)
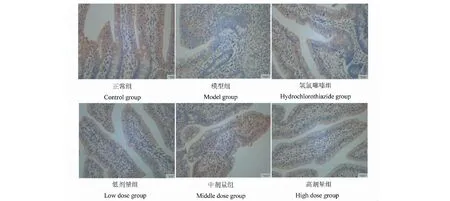
图3 各组大鼠结肠组织AQP8表达(免疫组织化学法,×200)
4 讨论
中医认为腹泻是由于饮食所伤、感受寒湿、情志失和等多种原因导致脾运失常,湿困中焦,湿浊下注于肠所致,“湿邪”为病因的关键,《素问·六元正纪大论》曰:“湿胜则濡泄”,《医宗必读》更是明确提出“无湿不成泻”的理论。故临床治疗以祛湿为第一要务,而小便为水湿排泄的主要出路,因而通利小便乃为重要治法。正如《景岳全书·泄泻》所说:“凡泄泻之病,多由水谷不分,故以利水为上策”。车前子功善渗湿利水,泌别清浊,堪称止泻的妙品,为古今医家首选的利湿止泻药。
番泻叶是腹泻模型中常用的导泻剂,番泻叶可刺激肠道,损伤肠黏膜,活化巨噬细胞及T细胞,引起炎症介质TNF-α的合成和释放[10-12],TNF-α可促进炎性因子(如IL-1、IL-6等)分泌,损伤肠黏膜,致其水肿、充血并加重炎性反应[13]。IL-6还可促进CRP释放,CRP 是急性时相反应蛋白,为炎症反应评价的关键指标,在诊断损伤、感染等非特异性炎症反应方面有极高的价值[14,15]。Wang[15]在双歧杆菌三联活菌散治疗感染性腹泻临床观察中发现患者治疗后血清中TNF-α、CRP和IL-6的水平均下降;张林美发现急性、迁延慢性腹泻患儿血清中IL-2、IL-6水平均升高[16]。由此可见,炎性因子促进的肠道炎症反应与腹泻的发生、发展有密切联系。
对于腹泻的症状而言,结肠肠腔内液体量增多、肠道蠕动加快可导致该病的发生[17]。结肠是肠道吸收水分的重要场所,但结肠的上皮细胞排列紧密,对细胞旁路这个吸收的途径有所限制。因此,跨细胞膜转运就成为其对水分吸收重要方式,在粪便的脱水成形中起到重要作用[18,19]。AQPs是负责跨细胞转运水分子的主要蛋白,对维持体内水液代谢起着重要作用。原位分子杂交技术结果显示AQP8在空肠、近端结肠、十二指肠均高表达,在胃和远端结肠微量表达[7]。杜丽东用当归治疗血虚便秘型大鼠实验中发现模型组中大鼠结肠AQP8基因和蛋白表达水平均高于正常组,表明AQP8的表达增多可促进结肠对水分的吸收,导致便秘[20];杨镛证实腹泻大鼠模型在治疗后,结肠中AQP8mRNA和蛋白表达均有所升高[17]。AQPs的表达水平受炎性细胞因子和其他多种因素的调节,有研究证实腹泻模型大鼠中炎性因子含量升高,而AQP8表达水平下降,肠道的炎症反应可进一步加重肠黏膜损伤,肠黏膜表皮细胞的凋亡与坏死,使AQP8分布部位受损,则AQP8表达减少,认为炎性因子与AQP8具有一定的相关性[21]。
本实验结果显示,大鼠灌胃番泻叶后,排出水样稀便,血清中TNF-α、IL-6、CRP含量均显著升高,结肠黏膜上皮细胞部分凋亡坏死,固有层毛细血管扩张充血,少量中性粒细胞浸润,Western blot法和免疫组化观察结果表明结肠组织中AQP8蛋白表达水平明显降低,表明番泻叶可致结肠黏膜炎性损伤,AQP8蛋白表达水平下降,水分吸收减少而致腹泻。车前子各剂量组给药治疗后,大鼠粪便基本成形,血清中TNF-α、IL-6和CRP含量均明显下降,尤以中剂量组降低趋势更为明显,说明车前子的抗炎作用并非随着用量增加而增强,中剂量乃较为适宜的浓度。结肠黏膜上皮细胞凋亡坏死、毛细血管充血及中性粒细胞浸润现象明显减轻,结肠组织中AQP8蛋白表达水平升高,提示车前子具有较好的止泻作用,其作用机制可能与改善结肠黏膜损伤、减轻炎症反应、上调AQP8蛋白的表达,进而促进结肠对水分的吸收,调节水液代谢有关。

