基于单颗粒电感耦合等离子体质谱法测定环境基质水样中纳米银颗粒
管 鹏,郭鹏然,潘佳钏,荀 合,梁维新
(广东省科学院 广东省测试分析研究所(中国广州分析测试中心) 广东省化学危害应急检测技术重点实验室,广东 广州 510070)
纳米材料因其独特的物理化学性质而具有广阔的应用前景,已成为近几十年来科学研究和产品开发的热点[1-2]。其中纳米银颗粒(AgNPs)对大量的致病微生物均具有良好的抑制和杀灭作用,被广泛用于抗菌纺织品、生活用水过滤器、化妆品、儿童玩具、食品包装材料、医疗器械产品等领域[3-9]。与此同时,含AgNPs产品的大量生产和使用致使其环境释放量不可避免地增加,成为新兴环境污染物,其中生活污水的排放是AgNPs进入生态环境的主要途径,并可通过地表和地下径流的方式污染饮用水源地,而目前饮用水的处理方法无法将AgNPs完全去除[10-12]。相关研究指出,长期接触和饮用含AgNPs的水体将可能导致AgNPs穿透细胞膜进入细胞组织内,对人体产生不利影响[6,11,13],其影响的大小与AgNPs的数量浓度和粒径等密切相关。
环境水体中AgNPs的浓度约在110 ng/L以下[14],目前针对纳米颗粒物常用的表征方法如扫描电子显微镜(SEM)、透射电子显微镜(TEM)、原子力电子显微镜(AFM)等需复杂的样品前处理步骤,无法直接对水体中AgNPs进行表征[15]。其他如体积排阻色谱(SEC)[16]、场流分级分离(FFF)[5,17]、动态光散射(DLS)[17]、拉曼光谱[18]等方法虽可直接表征测定水体中的AgNPs,但较高的检出限制约了DLS和拉曼光谱在环境水体中AgNPs表征方面的应用[19],而SEC、FFF需复杂的前处理或需要与其他技术联用方可进行定性定量分析[5]。2003年,Degueldre等[20]提出单颗粒电感耦合等离子体质谱法(Single-particle ICP-MS,SP-ICP-MS),该方法具有操作简单、灵敏度高、检出限低、分析时间短等特点,可同时实现纳米颗粒的数量浓度以及粒径分布的表征,并可直接对水体中纳米颗粒物进行分析,近年来已被应用于环境[21-22]、食品[23]、化妆品[24]、人体组织[19]等样品中纳米颗粒物的分析。环境水体样品具有基质成分复杂、干扰物质较多的特点,易对AgNPs的颗粒形态及其毒性造成影响,干扰测定结果。因此有必有对环境水体中潜在的干扰物质进行考察。
本文采用SP-ICP-MS方法同时测定水中AgNPs的粒径分布、数量浓度和质量浓度,研究了水中溶解性有机质(DOM)、pH值以及离子强度等对AgNPs的颗粒态及浓度的影响,为环境水样中AgNPs的SP-ICP-MS表征测定提供数据参考。
1 实验部分
1.1 仪器与试剂
Agilent ICP-MS/MS 8800三重四极杆电感耦合等离子体串联质谱仪(美国安捷伦公司);PB-10 pH计、BSA224S-CW型分析天平(赛多利斯科学仪器(北京)有限公司);KQ-500E超声波发生器(昆山市超声仪器有限公司)。
60 nm AgNPs标准储备液(20 mg/L,美国Sigma公司);Ag离子标准储备溶液(1 000 mg/L,国家钢铁研究院);浓硝酸(电子级,德国Merck公司);腐殖酸(上海麦克林生化科技有限公司);氯化钠、氢氧化钠(AR,广州化学试剂厂);含有Ce 、Co、Li、Tl、Y的调谐液(1 μg/L,美国安捷伦公司);实验用水为二次蒸馏水。

表1 ICP-MS仪器单颗粒测定模式工作条件Table 1 Operating conditions of ICP-MS in single particle mode
1.2 SP-ICP-MS仪器操作条件
首先对ICP-MS仪器进行等离子体点火,预热稳定30 min后采用调谐液对仪器进行调谐,使ICP-MS灵敏度达到最佳状态。同时,采用ICP-MS的“No Gas”调谐模式对1 μg/L的107Ag进行信号监测,并调节各项调谐参数使其对107Ag的监测信号值达到最高,相关仪器操作条件见表1。
1.3 标准溶液的配制
标准离子响应溶液的配制:采用0.1%硝酸将Ag离子标准储备液稀释至1 μg/L,用于ICP-MS对Ag响应灵敏度的调谐。标准参比颗粒物溶液的配制:用于计算传输效率和评价分析结果准确性,使用超纯水将AgNPs(60 nm)标准储备液稀释成100 ng/L的标准工作溶液。根据ISO/TS 19590[25],60 nm的AgNPs在2~200 ng/L质量浓度范围内标准工作溶液皆能获得准确的传输效率,本研究选择100 ng/L的标准工作溶液。
1.4 水样的采集与处理
河流水样:采集于广州市某河流,水样pH值为6.51,DOM为90 μg/L,离子强度约为0.055 mmol/L。染料废水水样:采集于广州市某印染厂,pH值为2.60,DOM为3.1 mg/L,离子强度约为0.029 mmol/L。养殖废水水样:采集于广州市某养殖场,pH值为6.41,DOM为20 mg/L,离子强度约为0.19 mmol/L。
采集的水样先经0.45 μm的滤膜过滤并分为2份,用于检测水样中总离子浓度的一份加入浓硝酸使其浓度达到2%,并密封置于阴凉处;另一份密封置于4 ℃冰箱中保存,待用。
2 结果与讨论
2.1 方法原理
SP-ICP-MS是在常规ICP-MS的基础上,采用“单颗粒”分析模式的技术。将水溶液中的颗粒引入等离子体,当液滴在等离子体中去溶剂化时,纳米颗粒经电离产生的大量离子云到达检测器后在极短的驻留时间内形成一个极强的脉冲信号,且产生的脉冲信号的数量与溶液中纳米颗粒的数量成正比,产生的脉冲信号的强度与纳米颗粒的质量以及粒径相关。如Peters等[26]通过已知颗粒浓度的标准溶液在单位时间内检测到的脉冲信号数量以及样品流速计算传输效率,并采用传输效率、标准离子响应强度以及脉冲信号强度计算纳米颗粒的质量及粒径,计算公式如下:
(1)
(2)
(3)
(4)
式中,Cp为颗粒数量浓度(particles/L);Np为在时间范围内检测到的颗粒数(particles/L);ηn为传输效率;V为样品流速(mL/min);Ip为样品中纳米粒子的信号强度(cps);mp为纳米颗粒质量(ng);RFION为离子响应强度(cps/(μg·L-1));td为停留时间(s);Mp为纳米粒子的摩尔质量;Ma为纳米粒子中待测元素的摩尔质量;dp为待测纳米粒子的粒径(nm);ρp为纳米粒子的密度(g/mL);Cm纳米粒子质量浓度(ng/L)。

图1 不同pH值条件下水中AgNPs颗粒浓度、质量浓度及粒径Fig.1 AgNPs particle concentration,mass concentration,and particle size in water at different pH value conditions
2.2 SP-ICP-MS的测定及AgNPs标准物品的确证
根据文献采用的粒度/颗粒检出限计算方法[9],本方法的粒度检出限为25 nm,颗粒浓度检出限为8×104particle/L。实验在表1的仪器条件下对100 ng/L AgNPs(60 nm)标准溶液进行测定,验证方法的准确性。结果显示,采用SP-ICP-MS法测得标准物质的颗粒浓度为8.43×107particle/L,质量浓度为100 ng/L,平均粒径为59 nm,与标准值颗粒浓度(8.43×107particle/L)、标准粒径(60 nm,TEM值)一致。

图2 不同DOM浓度下水中AgNPs颗粒浓度、质量浓度及粒径Fig.2 AgNPs particle concentration,mass concentration and particle size in water at different DOM concentrations

图3 不同NaCl浓度下水中AgNPs颗粒浓度、质量浓度及粒径Fig.3 AgNPs particle concentration,mass concentration,and particle size in water at different NaCl concentrations
2.3 pH值对AgNPs测定的影响
溶液的pH值会影响纳米颗粒的聚集和稳定性[27-30],因此需考察其对AgNPs测定的影响。配制不同pH值(1.0、2.0、3.0、4.0、5.0、7.0)的100 ng/L AgNPs(60 nm)溶液,采用SP-ICP-MS测定其中AgNPs的颗粒浓度、质量浓度及粒径(图1)。从图1中可以看出,当溶液由中性变化至酸性时,溶液中的AgNPs的颗粒浓度、质量浓度依次降低,在pH值为5.0和7.0时与标准值一致;当pH<3.0时溶液中AgNPs的颗粒浓度、质量浓度及粒径大小均降低,这是因为溶液的酸性较大,部分颗粒态的纳米银转化为离子态;pH值为3.0和4.0时颗粒浓度、质量浓度降低较少,粒径几乎不受影响,由于碱性溶液对仪器的进样系统有所损害,因此对水中AgNPs检测时的pH值应在5.0~7.0之间。
2.4 DOM对AgNPs测定的影响
溶解性有机质(DOM)[31]主要包括腐殖酸和富里酸等,广泛存在于环境水体中,其在地下水和地表水中的含量在0.02~30 mg/L范围内,能与各种纳米颗粒物结合形成稳定的悬浮液,因此实验配制100 ng/L的AgNPs(60 nm)溶液,考察了腐殖酸质量浓度(0、1、2、5、10、15、20、25、30 mg/L)对测定的影响(图2)。从图2中可以看出,当溶液中腐殖酸的质量浓度小于30 mg/L时对溶液中AgNPs颗粒浓度的测定结果无明显影响,对质量浓度及粒径测定结果影响较小。
2.5 离子强度对AgNPs测定的影响
溶液中纳米颗粒的稳定性很大程度上取决于离子强度,当离子强度大时,颗粒之间更易聚集[27,29,32-33],为此在仪器承受范围内考察了不同离子强度(NaCl浓度为0、1、5、10、20、30、50 mmol/L)对100 ng/L AgNPs(60 nm)测定的影响(图3)。结果显示,当溶液中NaCl浓度为0~1 mmol/L时,AgNPs的颗粒浓度、质量浓度及粒径的测定结果均不受影响,但当NaCl的浓度大于1 mmol/L时,AgNPs的颗粒浓度、质量浓度及粒径均随NaCl浓度的升高而下降,对测定结果影响较大,这可能是由于高离子强度增强了颗粒物的聚集作用使其迅速沉降。因此,采用SP-ICP-MS法测定水中的AgNPs时水中的离子强度浓度需低于1 mmol/L。
2.6 实际水样中AgNPs的测定
采用SP-ICP-MS方法对3种不同基质条件的环境水样(河水、染料废水、养殖废水)进行测定。由于测定时纳米颗粒产生的脉冲信号值与样品中纳米颗粒的浓度成比例,为避免样品颗粒浓度过高导致两个或多个纳米颗粒同时进入等离子体中受到激发,造成在同一驻留时间内脉冲信号发生叠加,在本次实验中,待测样品中颗粒浓度控制在106~109(particles/L)之间[9,25]。在对水样进行单颗粒检测及加标前,首先对3种水样中的总离子浓度进行测定,发现3种水样中总银离子均未检出,其他重金属离子(Mn、Fe、Zn、As、Cd、Pb)的质量浓度为0~50 μg/L;再对3种实际水样进行纳米银加标,加标浓度为100 ng/L,测定结果见表2和图4。3个水样中均未检出AgNPs,经加标后出现了明显的脉冲信号,河水、养殖废水加标样品的回收率分别为98.1%和93.3%,平均粒径分别为58.5 nm和56.6 nm,与标准粒径(60 nm,TEM值)一致;而染料废水平均粒径为52.7 nm,回收率为83.3%,这是由于染料废水pH值较低(2.6),致使水样中AgNPs部分溶解,从而影响其粒径及颗粒浓度,所得结论与前文一致。

表2 SP-ICP-MS法测定3个环境水样(n=3)Table 2 Determination of three environmental water samples by SP-ICP-MS(n=3)
-:not detected

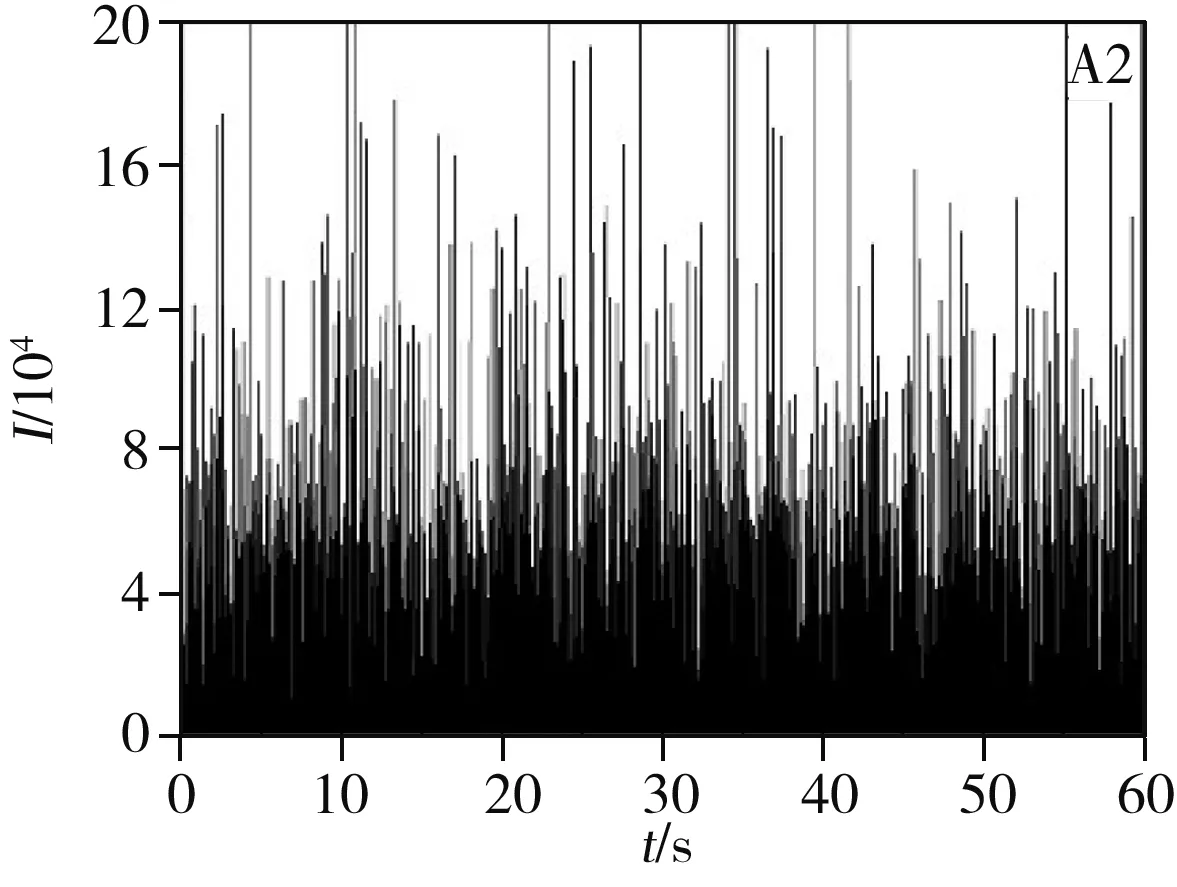




图4 加标100 ng/L的河水、染料废水和养殖废水的原始信号图(A)及粒径分布图(B)Fig.4 Original signal diagrams(A) and particle size distribution diagrams(B) of river water,dye wastewater and aquaculture wastewater spiked with 100 ng/L1.river water;2.dye wastewater;3.aquaculture wastewater
3 结 论
本文基于单颗粒电感耦合等离子体质谱法同时测定了不同环境基质水样中纳米银颗粒的粒径分布以及数量浓度,发现标准物质测定结果与标准值的相对误差小于2%,表明SP-ICP-MS方法具有很高的准确性。溶液中pH值、离子强度、DOM浓度分别在5.0~7.0、0~1 mmol/L和0~30 mg/L范围内对测定结果影响较小。当pH值小于5.0时,AgNPs的数量浓度和粒径随着pH值的减小而减小。当离子强度大于1 mmol/L时,AgNPs的数量浓度和粒径随着离子强度的增大而减小。本研究可为环境水样中纳米颗粒物的表征分析以及纳米颗粒物的环境安全性评估提供数据参考。

