铁碳微电解处理印染废水的效能及机理研究
贾艳萍,张真,佟泽为,王嵬,张兰河
(1 东北电力大学化学工程学院,吉林省吉林市132012; 2 长春工程学院能源动力工程学院,吉林长春130012)
引 言
我国每年纺织品加工总量高达5×107t,产生约2.2×109t 的废水,其中印染废水排放量占纺织行业废水总量的60%~80%[1-5]。印染废水的有机污染物含量高、难降解、色度高、组分复杂,若直接排入水体,会影响受纳水体环境和危害人类健康[6-12]。铁碳微电解工艺将铁屑与活性炭浸没于废水中,利用铁碳间的电位差形成电池电解水中污染物,提高废水可生化性,其流程简单、运行管理方便、成本低[13-20]。Vijayalakshmi 等[21]采用活性炭负载纳米零价铁处理含吡啶的印染废水,在pH 为6,铁碳投加量为15 g/L的条件下,吡啶去除率为86%;Azzam 等[22]采用零价铁处理含Pb2+、Ni2+的废水,Pb2+、Ni2+去除率接近100%;王悦[23]采用铁碳微电解工艺处理人工模拟废水,当铁碳投加量为600 g/L、进水pH 为3、气水比为3∶1、反应时间为120 min 时,COD 去除率为30.6%;余丽胜等[24]采用超声强化-铁碳微电解-Fenton 工艺处理含硝基苯废水,当pH 为4、反应时间为30 min、H2O2投加量为4 ml 时,硝基苯去除率为100%,TOC去除率为75%。这些研究主要探讨单一指标的去除,实际印染废水成分复杂,影响处理效果的因素较多,但是关于铁碳微电解工艺处理实际印染废水机理方面的研究尚少。
因此,本研究采用铁碳微电解工艺处理实际印染废水,优化工艺运行参数,通过SEM、EDS 和XRD等方法分析处理印染废水前后铁碳组成的变化,采用紫外可见光谱、傅里叶红外光谱、三维荧光光谱及气相色谱质谱联用仪等手段分析印染废水处理前后有机污染物成分结构和铁碳组成的变化,探究印染废水中有机物的降解机理。
1 材料与方法
1.1 实验用水
实际印染废水取自吉林市某毛纺厂漂洗车间,该车间主要对毛呢、毛线和精纺呢绒等纺织品进行退浆、漂洗及整理等操作,废水呈鲜红色,有刺激性酸臭味,废水pH 为4.58±1,COD 为(1288±100)mg/L,TOC 为(107.8±10) mg/L,氨氮为(10.9±4) mg/L,浊度为(112.4±3.2) NTU,色度为(345.2±15)倍,BOD5/COD为0.151。
1.2 实验试剂
铸铁屑,直径为0.050~0.074 mm,北京市有研合金材料有限公司生产;焦油活性炭,直径为1.5 mm,郑州市洛森环保有限公司生产;氢氧化钠,分析纯,沈阳市华东试剂厂生产;盐酸,分析纯,天津市北联精细化学品开发有限公司生产;二氯甲烷,分析纯,天津市永大化学试剂有限公司生产;用于分析COD、氨氮、色度和浊度的试剂,兰州市连华环保科技有限公司生产。
1.3 实验装置
实验装置见课题组前期发表文章[25]中的图1。
1.4 分析项目及检测方法
pH 采用pH 计(pHSJ-3F 型,上海仪电科学仪器有限公司)测定;COD、氨氮、色度及浊度采用紫外可见智能型多参数水质测定仪(LH-3BA 型,兰州连华环保科技有限公司)测定;TOC 采用总有机碳分析仪(liqui TOC Ⅱ型,德国Elementar 公司)测定;Zeta电位采用Zeta 电位仪(JS94K2 型,上海中晨数字技术设备有限公司)测定;SEM 采用场发射环境扫描电子显微镜(XL-30 ESEM FEG 型,美国FEI 公司)测定。
铁碳微电解工艺的进水、出水均采用0.45 μm滤膜过滤,滤液采用紫外-可见分光光度计(UV1700型,上海奥析科学仪器有限公司)分析印染废水处理前后在紫外-可见光区域物质及含量变化。取铁碳微电解工艺进水和出水各100 ml,分别采用50 ml二氯甲烷分3次萃取,将萃取液合并于50 ml容量瓶中,再利用傅里叶红外光谱仪(IRAffinity-1 型,日本岛津公司)400~2000 cm-1扫描,分析印染废水处理前后红外光区的基团变化。
采用三维荧光光谱仪(RF-5301PC 型,日本岛津公司)分析印染废水处理前后的荧光物质结构及官能团变化。设定光源为氙灯,激发光波长(Ex)及发射光波长(Em)范围均为200~600 nm,狭缝宽度为5 nm,扫描速度为6000 nm/min,扫描间隔均为5 nm,光谱带宽均为3 nm。
铁碳微电解工艺的进水、出水经二氯甲烷萃取后,采用气-质联用仪(GCMS-QP2010Ultra 型,日本岛津公司)分析印染废水处理前后的物质变化。控制柱箱温度为60℃,进口样,温度为250℃,进样时间1 min,以4.33 ml/min 速率进样,进样量2 μl,分流比20。
2 结果与分析
2.1 工艺参数的优化
2.1.1 初始pH对废水处理效果的影响 初始pH直接影响铁的溶出速度、氧化还原反应发生速率及污染物的处理效果。在铁投加量为100 g/L、铁/碳质量比为1∶1 及反应时间为60 min 的条件下,调节初始pH分别为1、2、3、4、5、6、7,考察初始pH对印染废水处理效果的影响,结果见图1。
当初始pH 为4 时,污染物去除效果最佳,COD、浊度、色度、氨氮及TOC 去除率分别为76.07%、97.42%、71.60%、91.74%及69.94%。当初始pH 小于4时,铸铁屑表面发生氧化反应,逐渐生成铁氧化物沉积于铸铁屑表面。酸性体系中铸铁屑及活性炭形成的微型原电池电势差增大,发生电解反应,较低的pH 使溶液中H+含量增多,可竞争在反应中阳极产生的电子,导致极化现象发生;同时铸铁屑表面易发生钝化现象,铸铁屑及活性炭接触面积减小,废水处理效果变差,这与Ying 等[26]、张龙龙[27]研究结果相似。当初始pH 大于4时,污染物去除率呈下降趋势,这是由于铁氧化物逐渐反应消耗体系中的H+,导致pH 上升,当铁的离子浓度积大于氢氧化物的溶度积时,便开始形成氢氧化物沉淀,生成的Fe(OH)2、Fe(OH)3絮凝体聚集于铁屑表面,影响电极反应的发生,降低铁碳微电解的反应速率,废水处理效果变差,Xu等[28]、郑敏[29]也得到了类似的研究结果。Fe3+水解形成氢氧化物沉淀的反应过程如式(1)~式(3)所示[30]。
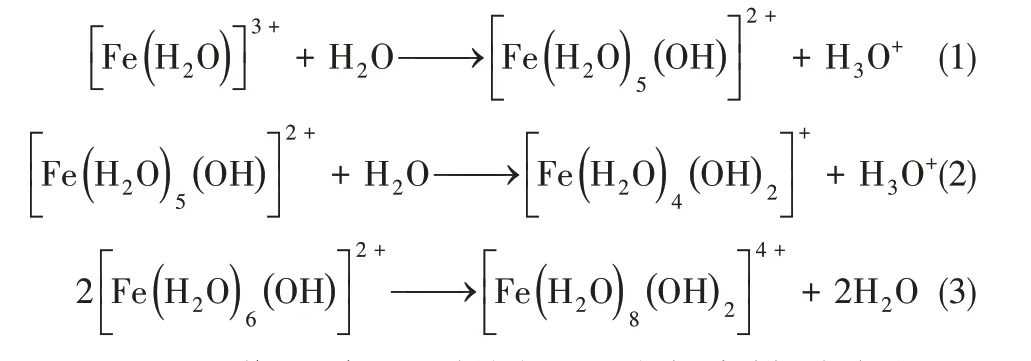
Zeta 电位可衡量颗粒间吸引力或排斥力的强度,评价反应体系的稳定性。进水、出水的Zeta 电位分别为-19.7778 mV 和-5.4238 mV,出水Zeta 电位降低,吸附沉降作用较好,主要有3 方面原因:①原电池可产生微电场,以胶体状态存在的污染物、极性分子及细小颗粒受到微电场作用后发生电泳现象,即带电胶粒向带相反电荷的电极移动,聚集沉积在电极上形成大颗粒沉淀;②形成Fe(OH)2、Fe(OH)3及少量Fe(OH)2+、Fe(OH)2
+、Fe(OH)4-等铁的氢氧化物,发挥卷扫、网捕作用,使絮凝作用增强,将悬浮物和部分不溶性污染物絮凝沉降,出水Zeta 电位降低;③可能存在铁盐水解沉淀物,产生的沉淀物迅速沉降,对胶粒产生卷扫、网捕作用,发生共沉降现象。Fe3+反应生成的二聚合体还可形成水合度更高的聚合体,产生羟基架桥作用,聚合体的生成过程如式(4)和式(5)所示。

图1 初始pH对污染物去除率的影响Fig.1 Effect of initial pH on removal efficiencies of pollutants

2.1.2 铁投加量和铁/碳质量比对废水处理效果的影响 在初始pH 为4,铁/碳质量比为1∶1,反应时间为60 min 的条件下,考察铁投加量对废水处理效果的影响,结果如图2 所示。当铁投加量为80 g/L时,污染物处理效果最佳,COD、浊度、色度、氨氮、TOC 去 除 率 分 别 为71.05%、98.21%、73.54%、90.98%、77.82%。当铁投加量低于80 g/L时,未能充分发生氧化还原反应形成微型原电池,造成电化学富集作用变弱,同时产生的新生态H+和Fe2+数量减少,使氧化还原效果变差;当铁碳微电解反应中铁含量高于80 g/L时,污染物去除率呈下降趋势,这是由于铁投加量增多,形成的微型原电池数量增加,有机物去除率提高,但同时也会使铁消耗量增加,形成的铁氧化物聚集堆积,使铁和活性炭之间相对接触面积减小。因此,随着铁投加量的增加,反应速率保持稳定,过量的铁被氧化成Fe2+和Fe3+,出水易出现“返黄”现象,Fe(OH)2、Fe(OH)3絮体增多。
在初始pH 为4、铁投加量为80 g/L、反应时间为60 min 条件下,考察铁/碳质量比对废水处理效果的影响,结果如图3 所示。当铁/碳质量比为0.8 时,COD、浊度、色度、氨氮、TOC 去除率最高,分别为75.63%、91.25%、75.56%、92.97%、31.98%。当铁/碳质量比低于0.8 时,铸铁屑被过量活性炭包裹,使宏观电池作用减弱,且新生态[H]的外部扩散位阻增大,与废水中污染物接触机会减少,处理效果降低;随着铁/碳质量比升高,铸铁屑逐渐增加,形成微型原电池数量增多,有机污染物去除率升高;当体系中铁/碳质量比大于0.8 时,污染物去除率呈下降趋势,这是由于多余铸铁屑堆积,抑制新的铁离子生成,减小了铸铁屑与活性炭之间接触面积,破坏铁碳电极的平衡电位,影响处理效果。
2.1.3 反应时间对废水处理效果的影响 反应时间直接影响铁碳微电解反应的进行程度和运行成本。在初始pH 为4、铁投加量为80 g/L、铁/碳质量比为0.8 的条件下,考察反应时间对印染废水处理效果的影响,结果见图4。当反应时间为90 min 时,COD、浊度、色度、氨氮、TOC 去除率最高,分别为75.48%、87.88%、75.34%、92.01%、81.09%。当反应时间小于90 min 时,停留时间过短,易导致氧化还原反应进行不彻底,废水处理效果差。当反应时间大于90 min 时,污染物去除率并未增加,这可能是由于反应时间过长导致铸铁屑消耗增多,生成的大量Fe2+氧化成Fe3+,造成色度增加,处理效果变差。同时,铁沉淀物增多并覆盖于电极表面,使铁电极表面发生钝化,这也是导致出水COD 增大的主要原因。

图2 铁投加量对污染物去除率的影响Fig.2 Effect of iron dosage on removal efficiencies of pollutants

图3 铁/碳质量比对污染物去除率的影响Fig.3 Effect of iron-carbon mass ratio on removal efficiencies of pollutants

图4 反应时间对污染物去除率的影响Fig.4 Effect of reaction time on removal efficiencies of pollutants
2.2 铁、碳表面特征分析
利用SEM、EDS 及XRD 分析铁碳微电解工艺反应前后铸铁屑、活性炭成分结构的变化。
2.2.1 SEM 分析 铁碳微电解工艺反应前后的铁、碳表面形貌如图5所示。
处理印染废水前,铁碳反应器中的铸铁屑主要富集在大晶粒中,表面粗糙,可增大接触面积;活性炭孔隙率高,表面形态分布较均匀,孔隙结构发达,可与铸铁屑进行充分接触,提高污染物的氧化概率,加快反应速率。
反应后铁、碳表面覆盖大量不规则絮状沉淀物、白色晶体颗粒,铁屑表面发生了氧化还原、吸附絮凝反应,生成铁的氧化物、氢氧化物及其他金属化合物等附着于铁、碳表面,呈片状、絮状等晶型结构。
2.2.2 EDS分析 采用EDS分析铁碳微电解工艺反应前后的铁、碳表面元素组成,结果如图6所示。
反应前的铸铁屑表面富含Fe、O元素,含有少量的Si、C、Al、K、Ca、Mg、Na、Ti、S 等元素,Fe 为主要成分,其他元素含量较低;反应后的铸铁屑表面含量最多的元素为O 和C,其他元素包括Si、Fe、Al、K、Ca、Mg、Na、Ti、S,铸铁屑表面形貌多呈絮状,可能为铸铁屑本身的吸附性或反应中产生的铁氢氧化物沉淀。对比图6(a)、(b)发现,铸铁屑中C、O 元素含量增加,Fe 元素含量减少。C 元素含量增加主要因为活性炭的消耗和转移;O 元素含量增加主要是反应过程中金属元素的氧化和有机物的分解;Fe 元素含量减少是由于Fe参与氧化、催化、置换等反应,造成部分Fe 转移到活性炭表面,同时生成了Fe 的氧化物、氢氧化物等被去除[31]。

图5 反应前后铁、碳表面形貌Fig.5 Topography of iron and carbon surface before and after reaction
反应前的活性炭表面含量最多的元素为活性炭自身富含的O 和C,其他元素为Fe、Si、Al、K、Mg、Na、Ca、Ti、Cl、S;反应后的活性炭表面含量最多的元素为Fe 和O,其他元素包括C、Si、S、Al、Ca。对比图6(c)、(d)发现,反应后的活性炭中部分金属元素含量降低,这可能是由于这些金属元素发生氧化、催化、置换等反应而被去除;同时Fe 元素的含量有所增加,可能是反应过程中不断生成的Fe2+被活性炭吸附。
2.2.3 XRD分析 采用XRD分析反应前后铁、碳中物质的存在形态,如图7所示。
反应前的铸铁屑主要是铁及其氧化物,如Fe、Fe2O3、Fe3O4;反应后的铸铁屑生成一些铁的氧化物、氢氧化物或羟基氧化物,衍射峰主要为含铁化合物,即FeOOH、Fe2O3、Fe3O4,反应后出现FeOOH 的衍射峰,铁的羟基氧化物的增多可使铸铁屑活性降低,该过程可能发生反应[32-33]

反应前的活性炭主要为碳,存在少量其他物质;反应后的活性炭表面含量最多的元素为Fe 和O,其他元素按照含量高低为C、Si、S、Al、Ca,主要存在碳及含铁化合物,即C和FeOOH、Fe2O3、Fe3O4。
2.3 废水成分分析
2.3.1 紫外可见光谱分析 铁碳微电解工艺进、出水经紫外可见光全波段(200~800 nm)扫描,其紫外可见吸收光谱见图8。
进水吸收峰高且数量多,吸收峰波长分别为330、360、510及530 nm;出水吸收峰波长为330 nm,波长大于400 nm时吸光度趋近于零,360~370 nm为萘环特征吸收峰[34]。与进水相比,出水吸收峰大幅度降低,这说明铁碳微电解工艺对萘环不饱和体系具有一定降解效果,可将芳香结构等大分子物质降解成小分子物质;490~530 nm 为偶氮键形成的共轭体系的强吸收峰,偶氮键为含有p 电子原子团的发色物质,可与萘环形成5-萘酚-1-磺酸大共轭发色体系,这是造成进水色度高的原因之一,其化学性质活泼,易于吸收紫外光而产生电子跃迁生成激发态电子,在铁碳微电解体系中稳定性低,使与其相连的碳原子变得不稳定,促进偶氮双键的去除。

图6 反应前后铁、碳表面EDS分析Fig.6 EDS analysis of iron and carbon surfaces before and after reaction
2.3.2 红外光谱分析 铁碳微电解工艺进、出水的红外光谱如图9所示。
3450 cm-1为水分子或有机物中羟基振动产生的强且宽的吸收峰,出水吸收峰减弱,并向低波数方向位移;2390、2350 cm-1为CO2的不对称伸缩峰,与进水相比,出水吸收峰增强,说明部分大分子有机污染物降解生成CO2、H2O 等小分子物质;1620、1590、1520 cm-1为C O、C C 等的吸收峰,出水中双键有机物断链生成含饱和甲基的物质,但出水出现较弱的芳环及杂环振动峰,这可能是由于多环类物质分解产生较多芳环、杂环及苯环等小分子物质所致;1110 cm-1为酯醚醇类C—O 伸缩振动、醚类中C—O—C伸缩振动或卤代烃C—F伸缩振动吸收峰,进、出水的吸收峰变化保持一致,说明铁碳微电解工艺对该类污染物降解能力较弱;970 cm-1为醚类C—O—C 的反对称伸缩振动吸收峰;800 cm-1为C—H面外变形振动吸收峰,即苯环邻接三氢取代吸收峰;470 cm-1为卤代烃C—I伸缩振动峰,卤代烃为难降解物质,说明铁碳微电解工艺对卤代烃的降解作用有限。
2.3.3 三维荧光光谱分析 铁碳微电解工艺进出水的三维荧光光谱图如图10所示。
荧光峰的颜色可直观反映水质受污染程度,颜色越深说明有机物浓度越高[35-36]。进水Ex/ Em=500 nm/510 nm 为类腐殖酸峰,浓度较高,腐殖酸含大量酚羟基、羰基等基团,结构复杂且难降解,这与紫外及红外检测结果吻合。出水存在2 处较明显的峰:①Ex/Em=290 nm/325 nm 和Ex/Em=290 nm/340 nm 为类蛋白物质中的类色氨酸峰,类色氨酸具有结构简单、易分解的特点,提高了出水可生化性;②Ex/Em=300 nm/400 nm为可见光区类富里酸荧光峰,富里酸具有分子量较小、芳构化程度低及分子结构简单等特点。

图7 反应前后铁、碳XRD分析Fig.7 XRD analysis of iron and carbon before and after reaction
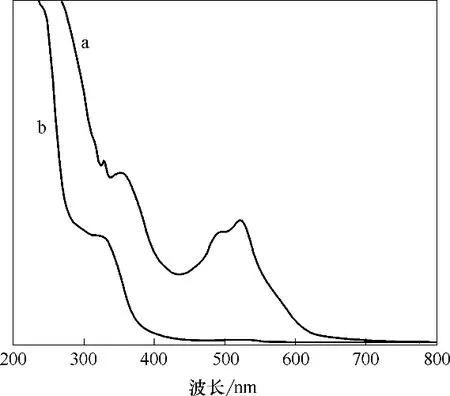
图8 紫外可见光谱图Fig.8 UV-visible spectrum of influent and effluent
与进水相比,出水激发或发射波长均出现蓝移,芳香性强的部分物质被分解成小分子结构,芳香环数量或链状共轭键减少,分子量大的物质氧化成易被生物降解的类蛋白荧光物质[37],有机污染物被大量分解、断键,向低浓度及小分子趋势发展。
2.3.4 气-质联用色谱分析 利用气相色谱质谱联用仪研究铁碳微电解处理前后的印染废水中有机物种类和含量变化,如图11所示。通过对比可明显看出,出水中有机物明显少于进水,出水主要含4种有机物,其中有3种与进水相同,1种为新生产物。

图9 进出水红外光谱图Fig.9 Infrared spectrum of influent and effluent
进水中的磷酸三乙酯、膦酸苯基-双(三甲基甲硅烷基)酯、柠檬酸三乙酯、D-甘露糖腈五乙酸酯、邻苯二甲酸二异辛酯等酯类及1-[(三甲基硅烷基)氧基]丙-2-醇、丙三醇等醇类物质经铁碳微电解反应后,被完全降解和转化。这表明铁碳微电解工艺可以降解含苯环、酯类、醇类等物质,将其开环断链,转变为小分子物质,即由难降解物质转化为易降解物质,使出水可生化性提高。但是,出水中仍存在己二酸双(2-乙基己基)酯邻苯二甲酸二异辛酯,这可能是造成部分COD残留的原因。

图10 进出水三维荧光光谱图Fig.10 Three-dimensional fluorescence spectrum of influent and effluent

图11 进出水气-质联用谱图Fig.11 Gas-mass spectrometry of influent and effluent
3 结 论
(1)铁碳微电解工艺处理实际印染废水具有处理效果好、运行费用低、操作方便等优点。在初始pH 为4、铁投加量为80 g/L、铁/碳质量比为0.8、反应时间为90 min 时,COD、浊度、色度、氨氮及TOC 去除率达到最高,分别为75.48%、87.88%、75.34%、92.01%及81.09%。
(2)通过SEM、EDS 及XRD 分析该工艺反应前后的铸铁屑、活性炭的变化。结果表明:反应前铸铁屑以Fe、C 为主,活性炭孔隙结构发达,反应后铸铁屑及活性炭表面附着其他被置换或氧化的金属物质及铁的氢氧化物絮体。
(3)通过对铁碳微电解工艺处理前后的废水Zeta 电位分析可知,铁碳微电解工艺反应过程中产生铁的氢氧化物絮体,具有较强的吸附絮凝作用。通过光谱分析和气-质联用色谱分析可知,铁碳微电解工艺能高效地分解酯类、醇类等污染物,使其转化为易于生化处理的小分子有机污染物。

