不同烟草品种接种蚜虫后NtCPI1基因表达分析
孙计平 张慧敏 陈飞 孙焕 娄亚楠 李雪君 平文丽

摘 要:半胱氨酸蛋白酶抑制剂(CPI)与植物抗病抗虫性密切相关,为了明确烟草半胱氨酸蛋白酶抑制剂基因NtCPI1功能,研究其与烟草品种抗虫性的关系,对不同蚜虫抗性烟草品种进行了接虫前后NtCPI1荧光定量表达分析。结果表明,抗蚜烟草品种接种蚜虫后,NtCPI1表达量显著增加,664-01接种蚜虫3 h后,NtCPI1表达量为对照的10.8倍,Blue River接种蚜虫6 h后,NtCPI1表达量为对照的6.28倍;而螺丝头2474、云烟97和中烟100等感蚜品种接虫后,NtCPI1表达量极显著降低。NtCPI1可以作为高效抗蚜候选基因,具有潜在的应用价值。
关键词:烟草;NtCPI;抗蚜虫;表达
Analysis of NtCPI1 Gene Expression in Different Tobacco Varieties
SUN Jiping1, ZHANG Huimin1,2, CHEN Fei1, SUN Huan1, LOU Yanan1, LI Xuejun1*, PING Wenli1,
(1. Tobacco Research Institute, Henan Academy of Agricultural Sciences, Key Laboratory for Green Preservation & Control of Tobacco Diseases and Pests in Huanghuai Growing Area, Xuchang, Henan 461000, China; 2. Pingdingshan academy of agricultural sciences, Pingdingshan, Henan 467000, China)
Abstract: Cysteine proteaseinhibitor(CPI) is closely related to plant disease and insect resistance. In order to clarify the function of tobacco CPI (NtCPI) and its relationship with tobacco resistance to aphids, the expression of NtCPI1in different tobacco varieties were analyzed by qRT-PCR before and after raphid infestation. The results of qRT-PCR showed that the expression of NtCPI1 gene in resistant tobacco varieties was significantly increased after infestation of aphids. The expression of NtCPI1in tobacco cultivar 664-01 after three hours of aphid infestation was 10.8 times higher than that in plants of control inoculation. The NtCPI1 expression in cultivar Blue River after six hours of aphid infestation was 6.28 times higher than that in plants of control inoculation. However, the expression of NtCPI1 in aphid susceptible cultivars, such as Luositou 2474, Yunyan 97 and Zhongyan 100, decreased significantly after insect infestation. NtCPI1 can be used as a highly effective anti-insect gene and has application potential.
Keywords: tobacco; NtCPI; aphid resistance; expression
煙蚜是烟草的主要害虫之一,烟蚜发生数量大,危害时间长,被危害烟叶烤后缺乏光泽,且易破碎。烟蚜分泌的“蜜露”又常导致烟叶发生“煤污病”,影响烟叶品质,同时烟蚜的迁移为害,成为烟草多种病害尤其是黄瓜花叶病毒病的传播媒介。很多半翅目、鞘翅目和同翅目蚜虫均以巯基蛋白酶作为主要的消化酶[1-4]。半胱氨酸蛋白酶抑制剂(Cysteine proteinase inhibitor, CPI)又称巯基蛋白酶抑制剂,其生理作用是与巯基蛋白酶互相作用,调节机体蛋白酶的活性[5-6],具有降解和储存蛋白、抵抗生物或非生物胁迫的作用[7-8]。CPI对鞘翅目和半翅目昆虫的消化酶有抑制作用。植物CPI通过与昆虫肠中巯基蛋白酶形成蛋白酶-抑制剂复合物,抑制巯基蛋白酶水解作用,进而降低昆虫的消化功能,降低昆虫摄食量,抑制昆虫正常的生长发育,甚至导致昆虫死亡[9-10]。水稻最早被确定含有植物同源CPI[11],近年来,CPI的研究越来越引起人们广泛关注[6],CPI基因已经在多种植物中得到了分离和鉴定,其中,大豆已经鉴定出20个半胱氨酸蛋白酶抑制剂基因,柯丹霞等[12]对其中的GmCYS2基因进行了功能验证。拟南芥受到甜菜胞囊线虫感染后半胱氨酸蛋白酶抑制剂基因AtCYS1、AtCYS5和AtCYS6表达量上升[13]。林世锋等[6]从烟草中克隆了4个CPI基因的全长cDNA序列(NtCPI1、NtCPI2、NtCPI3、NtCPI4),研究认为4个基因在根、茎、叶和芽中都有表达。王江英[9-10]等研究认为过量表达山茶花CPI基因CaCPI的烟草蚜虫抗性显著提高,并认为CaCPI与NtCPI1和NtCPI2序列比较接近。NtCPI与烟草品种蚜虫抗性的关系研究较少,本实验室前期研究发现,虽然NtCPI1和NtCPI2序列有很高的相似性,但转录组分析表明NtCPI1表达量较高,而NtCPI2几乎不表达,说明在烟草中NtCPI1发挥主要作用。因此,本研究以不同烟蚜抗性烟草品种为试验材料,利用qRT-PCR分析了NtCPI1基因在接种蚜虫后的表达量变化,进一步明确NtCPI1的基因功能,为烟草抗虫育种提供基因储备和理论参考。
1 材料与方法
1.1 试验时间、材料
试验于2019年3—5月在河南省农业科学院烟草研究所实验室和网室进行。供试烟草品种为云烟97、螺丝头2474、中烟100、三八烟、K326、Blue River和664-01,均由河南省农业科学院烟草研究所提供。
1.2 不同烟草品种蚜虫抗性鉴定
参考周婷婷等[14]的叶碟法,研究烟蚜对不同烟草品种的选择性;参考邱睿等[15]单头饲养法,研究烟蚜在不同烟草品种上的繁殖特性和存活时间。
烟草品种抗蚜性评价参考“烟草品种抗虫性评价技术规程”(YC/T509—2014):高抗(i≤0.25)、抗(0.25
1.3 烟草NtCPI1对接种蚜虫的响应
采用漂浮育苗培育烟苗,培养到4~5片真叶时移栽到花盆中,每个品种移栽12株,每盆1株。烟苗生长到6~7片真叶时,每个品种选取有代表性植株9株接种蚜虫,每株接种4龄无翅成蚜20头,接虫0,3,6,9和12 h分别取样,每次每株取1/3片叶子,3株混合样作为一个重复,锡箔纸包裹,立即投入液氮中冷冻,?80 ℃保存备用,试验3次重复。
根据NtCPI1的cDNA序列设计定量PCR引物q-F和q-R,以烟草18S RNA作為内参基因。引物序列及用途如表1所示,引物合成及测序工作由生工生物公司(武汉)完成。
以处理后各个样品的cDNA为模板,样本和内参分别设置3次重复,以不作处理的样品为对照,进行PCR扩增。按照荧光定量试剂盒QuantiNova SYBR Green PCR Kit(QIAGEN)进行荧光定量表达分析。20 ?L反应体系:依次加入SYBR Green PCR Master Mix 10 ?L,QN ROX Reference Dye 2 ?L,上下游引物各1 ?L,cDNA模板1 ?L,用ddH2O补充体系至20 ?L。反应条件:95 ℃预变性2 min;95 ℃变性60 s,55 ℃退火60 s,72 ℃延伸20 s,35个循环;72 ℃延伸10 min。反应结束后根据得到的循环阈值(CT值),用2-△△CT法计算相对表达量。每个品种以未接虫处理的对照表达量为1,每个品种基因的相对表达量为该品种接虫后表达量与对照表达量的比值。
1.4 数据处理
采用DPS 14.5软件对数据进行统计分析,LSD法对数据进行差异性检验。
2 结 果
2.1 不同烟草品种蚜虫抗性比较
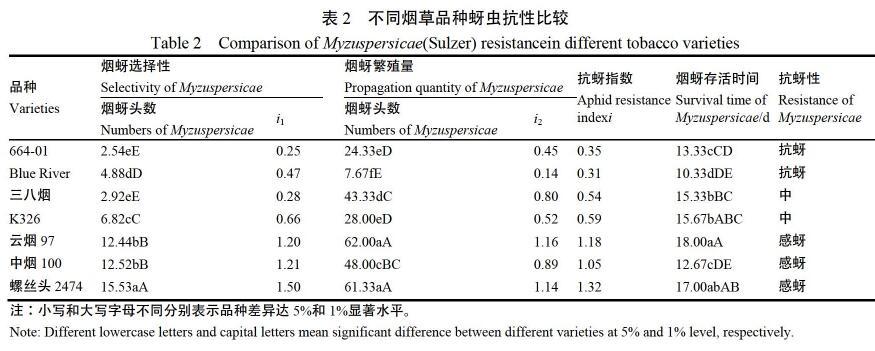
由表2可见,烟蚜成虫对不同烟草品种的选择性差异较大,664-01和三八烟,烟蚜选择性低,蚜量比分别为0.25和0.28,这2个品种烟蚜数量极显著低于其他品种;Blue River蚜量比也小于0.5;螺丝头2474烟蚜选择性最高,烟蚜数量显著高于其他品种,蚜量比为1.50,云烟97和中烟100烟蚜选择性也较高,蚜量比分别为1.20和1.21。烟蚜成虫对不同烟草品种有明显的取食选择性。
不同烟草品种烟蚜繁殖量差异较大,螺丝头2474和云烟97烟蚜繁殖量极显著高于其他品种,烟蚜繁殖量蚜量比分别为1.32和1.18;Blue River烟蚜繁殖量最少,极显著低于其他品种;其次是664-01和K326,蚜量比分别为0.45和0.52。
从不同烟草品种烟蚜存活时间比较来看,烟蚜在云烟97叶片上存活时间最长,其次为螺丝头2474,烟蚜在Blue River上存活时间最短。
根据烟草品种抗虫性评价技术规程(YC/T509—2014),参考烟蚜存活时间,初步判定Blue River和664-01为抗蚜品种,三八烟和K326烟蚜抗性为中,云烟97、螺丝头247和中烟100为感蚜品种。
2.2 接种蚜虫前后NtCPI1表达量对比分析
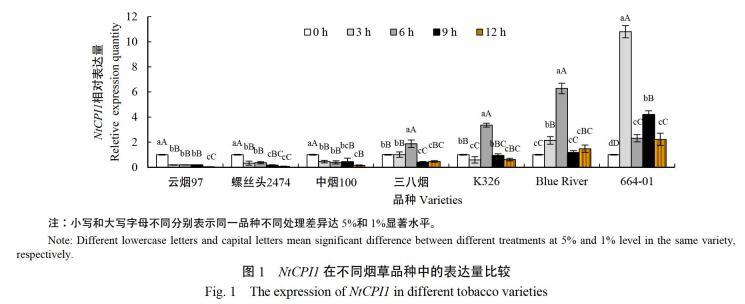
接种烟蚜后,qRT-PCR分析显示(图1),NtCPI1在不同烟草品种中的表达量差异较大。抗蚜烟草品种664-01,接蚜虫3 h后,NtCPI1表达量迅速增加,为对照的10.8倍,之后表达量下降,但在接虫后3~12 h,NtCPI1相对表达量均超过2,极显著高于对照。上述结果表明,664-01在遇到蚜虫侵袭后迅速做出应对反应,NtCPI1基因表达量迅速增加。
抗蚜烟草品种Blue River,接种烟蚜3 h后,NtCPI1基因表达量为对照的2.14倍,极显著高于对照;接种蚜虫6 h后,NtCPI1表达量提高6.28倍;之后表达量下降,接虫后9和12 h,NtCPI1相对表达量均超过1,但与对照差异不显著。与烟草品种664-01相比,Blue River在遇到蚜虫侵袭后反应延迟,但明显超过其他几个品种。
螺丝头2474、云烟97和中烟100等感蚜品种接虫后NtCPI1表达量均极显著降低。
蚜虫抗性为“中”的品种K326和三八烟接虫6 h后,NtCPI1相对表达量分别为对照的5.75倍和1.86倍,极显著高于对照。
3 讨 论
植物半胱氨酸蛋白酶抑制剂是植物体内广泛存在的一种防御蛋白,是一类可逆抑制蛋白,前人研究表明,植物CPI在抗虫方面起重要作用,作用的途径主要是被昆虫摄食后,昆虫体内蛋白酶和消化酶活性受到抑制,由于缺乏必需氨基酸的供应,进食困难,最终导致昆虫的非正常发育或死亡[9,16-21]。
CPI在多种植物中被克隆,但研究重点一直集中在生物信息学分析方面,CPI与植物抗性之间联系的研究相对较少,柯丹霞等[12]采用转基因过表达的方法,说明GmCYS2蛋白具有一定的酶活性抑制作用,并且正调控百脉根共生结瘤过程;前人将豇豆丝氨酸蛋白酶抑制剂基因转入烟草,发现转基因烟草对烟芽夜蛾和烟草天蛾有毒杀和抑制作用[22]。MASOUD等[23]将水稻半胱氨酸蛋白酶抑制剂基因转入烟草,但未报道转基因烟草是否获得了抗虫活性。林世锋等[21]进行烟草CPI基因家族的克隆,但未进一步研究基因功能及其与烟草抗虫性的关系。王江英等[9-10]研究认为转CaCPI烟草蚜虫抗性明显提高,且CaCPI与NtCPI1和NtCPI2序列比较接近。
在遇到蚜虫侵袭条件下,烟草自身CPI基因表达量变化研究较少,本研究选用不同烟草品种为试验材料,烟蚜选择性试验和繁殖量试验结果表明,云烟97、螺丝头2474和中烟100烟蚜选择性和繁殖量均较高,云烟97和中烟100抗蚜指数分别为1.18和1.05,为感蚜品种;螺丝头2474抗蚜指数为1.32,为高感品种,这与邱睿等[15]、周婷婷等[14]研究结果基本一致;Blue River和664-01为抗蚜品种,三八烟和K326烟蚜抗性鉴定结果为中。荧光定量分析结果表明,接种蚜虫后,不同烟草品种NtCPI1表达量差异较大,抗蚜烟草品种664-01接种蚜虫后NtCPI1表达量显著增加,接虫3 h后为对照的10.8倍,且在接虫6~12 h NtCPI1表达量均显著高于对照;抗蚜烟草品种Blue River接种蚜虫6 h后,NtCPI1表达量为对照的6.28倍;而高感品种螺丝头2474、感蚜品种云烟97和中烟100接虫后NtCPI1表达量极显著降低。蚜虫侵袭烟草叶片后,抗蚜品种NtCPI1基因表达量迅速增加,因此,NtCPI1可以作为高效抗蚜候选基因,具有潜在的应用价值。
植物CPI能够发挥抑制作用,有3个基本结构是必须的:N末端的甘氨酸残基G,高保守序列QVVXG以及C末端的W[9-10]。林世锋等[6]克隆了NtCPI1、NtCPI2、NtCPI3、NtCPI4等4个基因,分别编码98,98,120,123个氨基酸残基的蛋白质,都具有CPI反应位点的保守序列及植物CPI所特有的基序。本研究只对蚜虫入侵后不同烟草品种NtCPI1基因表达量进行了初步研究,烟草CPI在适应生物和非生物胁迫过程中的通路调节过程等仍需进一步的研究,通过NtCPI基因在烟草中的过表达及RNAi干扰工作,进一步证实NtCPI与烟草抗虫性之间的联系。
4 结 论
抗蚜烟草品种Blue River和664-01接种蚜虫后NtCPI1表达量显著增加;高感蚜虫烟草品种螺丝头2474、感蚜烟草品种云烟97和中烟100接种蚜虫后NtCPI1表达量显著降低;NtCPI1可以作为高效抗蚜候选基因,具有潜在的应用价值。
参考文献
[1]RYAN C A. Protease inhibitors in plants: genes for improving defenses against insects and pathogens[J]. Annual Review of Phytopathology, 1990, 28: 425-429
[2]RAHBEY, DERAISON C, BONADE-BOTTINO M, et al. Effects of the cysteine protease inhibitor of cysteine proteinases inhibitor oryzacy statin (OC-I) on different aphids and reduced performance of Myzuspersicae on OC-I expressing transgenic oilseed rape[J]. Plant Science, 2003, 164: 441-450
[3]AZZOUZ H, CAMPANE D M, CHERQUI A, et al. Potrntial effects of plant protease inhibitors, oryzacy stationI and soybean Bowman-Birk inhibitor on the aphid parasitoid Aphidiuservi Haliday (hymenoptera, Braconidae)[J]. Journal of Insect Physiology, 2005, 51: 941-951.
[4]RYAN C A. Protease inhibitors in plants: genes for improving defenses against insects and pathogens[J]. Annual Review of Phytopathology, 1990, 28: 425-449.
[5]XANIER-FILHO J. The biological roles of serine and cyste-ine proteinase inhibitors in plants[J]. RevistaBrasileira de Fisiologia Vegetal, 1992, 4(1): 1-8.
[6]林世鋒,元野,任学良,等. 烟草半胱氨酸蛋白酶抑制剂(CPI)基因家族的克隆及组织表达谱分析[J]. 中国烟草学报,2014,20(4):79-87.
LIN S F, YUAN Y, REN X L, et al. Cloning and tissue expression of cysteine proteinase inhibitor (CPI)gene family in Nicotianatabacum L. [J]. Acta Tabacaria Sinica, 2014, 20(4): 79-87.
[7]BECKER C, SENYUK V I, SHUTOV A D, et al. Proteinase A, a storage-globulin-degrading endopeptidase of vetch (Vicia Sativa, L.) seeds, is not involved in early steps of storage-protein mobilization [J]. European Journal of Biochemistry, 1997, 248(2): 304-312.
[8]GRUDKOWSKA M, ZAGDASKA B. Multifunctional role of plant cysteine proteinases[J]. Actabiochimicapolonica, 2004, 51(3): 609-624.
[9]王江英. 山茶花APX、CPI、GA20ox1基因功能研究及木糖篩选体系建立[D]. 北京:中国林业科学研究院,2015.
WANG J Y. Function analysis of APX, CPI, GA20ox1 and xylose selection system establishment of Camellia japonica[D]. Chinese Academy of Forestry, 2015.
[10]王江英,范正琪,殷恒福,等. 杜鹃红山茶CaCPI基因的克隆及过量表达提高烟草植株的抗虫性[J]. 华北农学报,2015,30(5):57-64.
WANG J Y, FAN Z Q, YIN H F, et al. Cloning CPI from camellia azalea and overexpressing to tobacco enhances insect tolerance[J]. Acta Agriculturae Boreali- sinica, 2015, 30(5): 57-64.
[11]ABE K, EMORI Y, KONDO H, et al. Molecular cloning of a cysteine proteinase inhibitor of rice (oryzacystatin). Homology with animal cystatins and transient expression in the ripening process of rice seeds
[J]. The Journal of Biological Chemistry, 1987, 262(35): 16793-16797.
[12]柯丹霞,彭昆鹏,贾妍,等. 大豆半胱氨酸蛋白酶抑制剂基因GmCYS2的功能鉴定[J]. 作物学报,2018,44(8):1159-1168.
KE D X, PENG K P, JIA Y, et al. Functional characterization of soybean cystatins gene GmCYS2[J]. Acta Agronomica Sinica, 2018, 44(8): 1159-1168.
[13]LABUDDA M, ROZANSKA E, SZEWINSKA J. et al. Protease activity and phytocystatin expression in Arabidopsis thaliana upon heteroderaschachtii infection[J]. Plant Physiology and Biochemisty, 2016, 109: 416-429.
[14]周婷婷,林华峰,王艳秋,等. 烟草对烟蚜的抗性品种筛选及抗性机制研究[J]. 应用昆虫学报,2017,54(2):198-206.
ZHOU T T, LIN H F, WANG Y Q, et al. Identifying tobacco strains resistant to Myzuspersicae(Sulzer) and investigating the mechanism responsible for resistance to this pest[J]. Chinese Journal of Applied Entomology, 2017, 54(2): 198-206.
[15]邱睿,李淑君,王海涛,等. 不同烟草品种上烟蚜的繁殖特征分析[J]. 烟草科技,2018,51(1):15-20.
QIU R, LI S J, WANG H T, et al. Reproductive characteristics of Myzuspersicae (Sulzer) in different tobacco varieties[J]. Tobacco Science & Technology, 2018, 51(1): 15-20.
[16]ARAI S, WATANABE H, KONDO H, et al.Papain inhibitory activity of oryzacystatin, a rice seed cysteine proteinase inhibitor, depends on the central Gln-Val-Val-Ala-Gly region conserved among cystatin superfamily members[J]. J Biochem, 1991, 109(2): 294-298.
[17]BELENGHI B, ACCONCIA F, TROVATO M, et al. AtCYS1, a cystatin from Arabidopsis thaliana, suppresses hypersensitive cell death [J]. European Journal of Biochemistry, 2003, 270(12): 2593-2604.
[18]杨文杰. 水稻半胱氨酸蛋白酶抑制剂基因转化甘蓝的研究[D]. 重庆:西南农业大学,2000
YANG W J. Study on transformation of cysteine proteinase inhibitor gene into cabbage (Brassica oleraceavar. Capitate L.)[D]. Chongqing: Southwest Agricultural University, 2000.
[19]EDITH B, DOMINIQUE M, CONRAD C. Molecular interactions between an insect predator and its herbivore prey on transgenic potato expressing a cysteine proteinase inhibitor from rice[J]. Molecular Ecology, 2003, 12(9): 2429-2437.
[20]GHOLIZADEH A. The possible involvement of D-amino acids or their metabolites in Arabidopsiscysteine proteinase/cystatin-dependent proteolytic pathway[J]. Cytology and Genetics, 2015, 49(2): 73-79.
[21]林世鋒,王仁刚,任学良,等. 烟草蛋白酶抑制剂基因的电子克隆及生物信息学分析[J]. 生物技术通报,2012(4):80-86.
LIN S F, WANG R G, REN X L. In silicon cloning and bioinformatic analysis of proteinase of inhibitor gene in tobacco[J]. Biotechnology Bulletin, 2012(4): 80-86.
[22]JOHNSON R, NUEVACZ J, AN G, et al. Expression of proteinase inhibitors I and II in transgenic tobacco plants: effects on natural defense against Manducasextalarvae[J]. Proceedings of the National Academy of Sciences of the United States of America, 1989,86(24): 9871-9875.
[23]MASOUD S A, JOHOSON L B. WHITE F F, et al. Expression of a cysteine proteinase inhibitor (oryzacystatin-Ι) in transgenic tobacco plantPlant[J]. Molecular Biology, 1993, 21: 655-663.
基金项目:河南省农业科学院自主创新专项基金项目“烟草抗蚜虫种质资源筛选和抗虫机理的研究”(2019ZC19,2020ZC17)
作者简介:孙计平(1978-),女,博士,助理研究员,研究方向为烟草遗传育种与分子生物学。E-mail:sunjiping2002@126.com
*通信作者,E-mail:lixuejun8373@163.com
收稿日期:2019-09-03 修回日期:2019-12-15

