旋涡提取-电感耦合等离子体发射光谱法快速测定橄榄油中9种金属元素
倪张林 喻晴 屈明华 汤富彬


摘 要 建立了旋涡提取-电感耦合等离子体光谱法(ICP-OES)准确测定橄榄油中9种金属元素的方法。采用5% (V/V)HNO3作为提取液,通过 5 min旋涡提取即可完全提取橄榄油中的待测金属元素,提取过程中加入适量二氯甲烷,将提取液置于上层,可使料液比加大至1∶1(m/V)。方法的定量限在0.01~0.05 mg/kg之间,可完全满足橄榄油中9种金属元素的测定要求。方法的加标回收率在90.2%~103.6%之间,相对标准偏差(RSD,n=6)小于5.0%,方法简单快捷、灵敏度高、稳定性好。本方法与GB 5009.268-2016的微波消解法测定结果无显著性差异(p >0.05),结果准确可靠。
关键词 橄榄油;金属元素;旋涡提取;电感耦合等离子体光谱仪
1 引 言
橄榄油是一种优质的食用油,深受消费者的喜爱。与普通植物油相比,橄榄油中含有较高含量的不饱和脂肪酸、丰富的维生素和胡萝卜素等脂溶性维生素及抗氧化物等多种成分[1,2]。橄榄油中ω3-脂肪酸能平衡人体血压,阻止血栓的形成,并具有提高人体免疫力和思维活动的作用[3]。
随着人们生活水平的提高,人们对食用植物油的健康和安全提出了更高的要求,GB 2762-2017《食品安全国家标准 食品中污染物限量》对重金属铅和总砷的限量水平为0.1 mg/kg[4];植物油中的其它微量元素尤其是过渡元素作为油脂氧化的催化剂,可大大缩短油脂的氧化诱导时间和加速油脂氧化[5,6],从而缩短油脂的储藏时间。研究表明,微量的铜和铁还能使抗氧化剂氧化成醌型化合物,从而使橄榄油中本身存在的抗氧化剂或者添加的抗氧化剂失去对油脂的抗氧化作用[7],在GB/T 23347-2009《橄榄油、油橄榄果渣油》[8]对铜和铁的限量值分别为0.1和3 mg/kg。 因此,准确、高效地测定这些元素对于橄榄油的生产加工、储存和安全食用具有重要意义。
目前,有关植物油中微量元素的含量测定已有大量文献报道,其前处理技术主要为酸消解,但是,由于植物油的高油脂的特性,前处理耗时长、试剂消耗大;另外,由于受称样量的限制,方法灵敏度较低。尽管微波技术目前已较为成熟,但仍未改变费时费力的情况。有研究者采用灰化法[9,10]、溶剂稀释直接进样法[11,12]、酸提取法[13~17]进行前处理,其中,酸提取法设备简单(一般采用振荡、超声或者旋涡等方式)、操作过程快捷,被众多研究者采用,并且效果良好,但如需测定多种元素,尤其是重金属元素,需采用高灵敏度的ICP-MS进行测定。拟在之前研究基础上,本研究采用旋涡提取法,通过加入适量的二氯甲烷,将提取液转至上层,实现加大料液比,提高灵敏度的目的,采用电感耦合等离子体发射光谱仪(ICP-OES)测定橄榄油中的3种重金属元素(Pb、As和Cd)和6种过渡金属元素(Cr、Fe、Cu、Mn、Ni和Zn)的含量。本方法具有简单、可靠、灵敏度高、运行成本低等优点,可满足橄榄油中微量元素的测定要求。
2 实验部分
2.1 仪器与试剂
iCAP 7400电感耦合等离子光谱仪(ICP-OES,美国Thermo Scientific公司);Mars 6微波消解仪(美国CEM公司);Nexion300D 电感耦合等离子体质谱仪(ICP-MS,美国PerkinElmer公司);AL104电子天平(瑞士Mettler Toledo公司);DMT2500多管旋涡振荡器(上海MULAB公司)。
HNO3(优级纯,65%,美国Thermo Scientific 公司);H2O2(优级纯,30%,国药集团化学试剂厂);二氯甲烷(色谱纯,德国Merck公司);100 mg/L多元素混合標准溶液(美国PerkinElmer公司)。
2.2 样品前处理
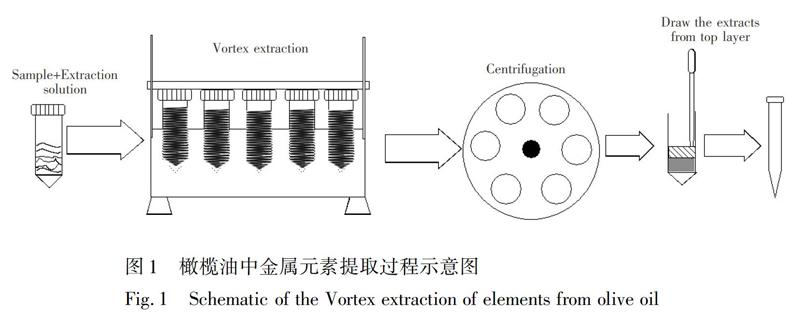
提取法:称取约6 g(精确至0.0001 g)橄榄油于50 mL离心管中,加入6 mL 5%(V/V) HNO3和4.5 mL二氯甲烷,2500 r/min旋涡振荡5 min,8000 r/min离心5 min,用5 mL巴氏吸管小心吸取上层液体于进样管中,采用ICP-OES测定,同时做加标回收和样品空白实验,过程详见示意图(图1)。
比较方法:参照GB5009.268-2016方法,采用微波消解,用ICP-MS测定待测元素。
2.3 仪器工作参数
ICP-OES仪器参数如下:入射功率为1130 W;等离子气(氩气)流量 13 L/min;辅助气流量(氩气) 0.2 L/min;载气(氩气)流量0.4 L/min;观测方式:水平观测;观测高度: 15.0 cm;泵速为1.5 mL/min。 对待测9种金属元素的谱线进行筛选,比较同一元素不同谱线的强度、峰形和谱线干扰等因素,选择灵敏度较高、干扰小的谱线作为分析线,各元素测定波长及背景扣除位置见表1。ICP-MS仪器条件参照本实验室之前研究[10]。
3 结果与讨论
3.1 提取剂的选择
研究者通常采用稀HNO3和稀HCl作为提取剂[15,17],但相比较而言,同级别的HNO3的杂质要少于HCl,也有学者采用0.05 mol/L EDTA二钠盐溶液[18]或者15%(V/V)TMAH溶液提取食用油中的多元素[19],取得了较好的效果,但是,由于EDTA二钠盐溶液的盐分含量达1.4%(m/V),TMAH溶液为有机物,这些提取剂长时间进样会导致仪器进样系统盐分堆积或者碳堆积,从而影响测定的准确性。因此,本研究选用稀HNO3溶液作为提取剂。
3.2 料/液比例的选择
料/液比例可直接影响仪器的测定灵敏度,但是,过大的料/液比会导致混合物粘度加大,难以达到旋涡的效果。为了满足ICP-OES的测定灵敏度,同时又能形成旋涡的条件下,本研究选择1∶1(m/V)的料液比;同时,为能使提取剂置于上层从而方便吸取,选择油与二氯甲烷的比例为1∶0.75(m/m),在此比例下,油与二氯甲烷的混合物密度大于提取剂的密度,离心后的液体分层明显。为了保证ICP-OES足够的进样体积,选择称样量为6 g,加入4.5 mL二氯甲烷和6 mL 5%(V/V)HNO3溶液进行提取,在此条件下,混合物能够在旋涡器中进行充分旋涡混合,离心后可得到4 mL以上的清液用于直接上机测定。
3.3 提取剂浓度和提取时间的选择
为了在较少酸使用量情况下得到最佳的提取效果,选择了一个本底元素含量相对较高的初榨橄榄油作为提取实验的样品,分别选取了不同浓度(0%、2%、5%和10%(V/V))酸溶液作为提取剂,进行提取平衡实验。由于个别元素(如Pb、Cd和As等)在实验样品中含量较低,为了得到更为准确的结果,采用ICP-MS测定提取液。
由图2可知,在纯水条件下(即0% HNO3),元素Fe、Cu、Mn、Ni和Cr的提取平衡时间较长,甚至可能无法平衡;采用2% HNO3(V/V)溶液时,除了Fe和Ni提取平衡时间需要10 min,其它元素的提取平衡时间都在10 min以内;当HNO3大于5%(V/V)时,待测元素的提取平衡时间在5 min以内,元素Cd、Zn、As和Pb在2 min达到提取平衡,其余元素在3 min时趋于提取平衡。图3为不同浓度的HNO3溶液条件下,提取平衡后实际样品中待测元素的含量,在酸环境下,随着酸浓度增大,待测元素的含量并没有显著变化。综上,橄榄油中的金属元素是以较容易被提取的游离态为主,少部分结合态元素在稀酸性条件下也很容易得到释放。最终选择5%HNO3作为提取剂,提取时间为5 min。
3.4 方法性能评价
根据橄榄油中9种待测元素的含量以及ICP-OES条件下各元素的响应情况确定线性范围(表2),线性相关系数均大于0.9990。 制备11个独立的空白溶液,采用优化后的条件进行测定,计算标准偏差,以3倍和10倍的标准偏差确定检出限和定量限 (表2),通过折算称样量和提取剂体积可知各元素的方法检出限和定量限,对照现行的标准,针对Cu、Fe、Pb和As的限量要求,开发的方法可完全满足这些元素测定。
选择初榨橄榄油作为加标基质,选择低、中、高3个加标水平,进行加标回收实验。由表3可知,各元素的加标回收率在90.2%~103.6%之间,RSD结果均小于5%(n=6),由此可见,整个提取过程基本不存在待测元素损失,检测方法稳定、可靠。
由于未找到含有这些元素准确定值的植物油标准物质,为了验证方法的准确性,本研究选择2个油样,一个为初榨橄榄油(元素含量相对较高),另一个为果渣油(元素含量相对较低),同时采用优化后的方法和目前现行的GB 5009.268-2016方法(ICP-MS法)进行比较测定,结果见表4,2种方法测定结果基本一致。
3.5 实际样品的测定
测定了22个来于当地大型超市和网络电商的橄榄油样品,包括18个初榨橄榄油和4个果渣油,Fe和Zn元素在所有的橄榄油样品中均检出,其中1个产自希腊的初榨橄榄油中Fe含量为3.97 mg/kg,超过了GB/T 23347-2009《橄榄油、油橄榄果渣油》中的限量要求,所有样品中重金属含量均较低,远低于食品安全限量标准。
4 结 论
建立了一种适合于橄榄油中金属元素的快速前处理方法,样品经旋涡提取,离心分离后的提取液采用ICP-OES测定9种金属元素。旋涡提取法与食品安全标准方法GB 5009.268-2016微波消解ICP-MS法相比,结果无显著性差异(p>0.05)。与标准方法相比,本方法简单快捷、灵敏度高,并且采用了运行成本更低的旋涡提取仪和ICP-OES,此方法的定量限可完全可以满足目前现有橄榄油金属元素限量标准的检测要求。本前处理方法通过适当的方法优化和验证,也可用于其它植物油中金属元素的测定。本研究对市售的22个橄榄油样品进行了测定和评价,所有样品中重金属含量均较低,远低于食品安全限量标准,1个产自希腊的初榨橄榄油样品Fe含量超过标准限量值。
References
1 Buckland G,Travier N,Barricarte A,Ardanaz E,Morenoiribas C,Sánchez M J,Molinamontes E,Chirlaque M D,Huerta J M,Navarro C. J. Br. J Nutr.,2012,108(11): 2075-2082
2 Tuck K L,Hayball P J. J. Nutr. Biochem.,2002,13(11): 636-644
3 GUO Chang-Jiang. Food and Nutrition in China,2002,6: 48-49
郭長江. 中国食物与营养,2002,6: 48-49
4 GB 2762-2017,Contaminant Limit in Food,National Standards of the People's Republic of China
食品中污染物限量. 中华人民共和国国家标准,GB 2762-2017
5 Andersson K,Lingnert H. J. Am. Oil Chem. Soc.,1998,75(8): 1041-1046
6 Shiota M,Uchida T,Oda T,Kawakami H. Jpn. J. Cancer Res.,2010,71(3): 120-123
7 De Leonardis A,Macciola V. Eur. J. Lipid Sci. Tech.,2015,104(3): 156-160
8 GB/T 23347-200,Olive Oil,Olive Pomace Oil,National Standards of the People's Republic of China
橄欖油、油橄榄果渣油,中华人民共和国国家标准,GB/T 23347-2009
9 SUN Jian-Gang. Spectroscopy and Spectral Analysis,2003,23(4): 793-796
孙建刚. 光谱学与光谱分析,2003,23(4): 793-796
10 Ni Z L,Liu Y H,Shen D Y,Mo R H. Anal. Lett,2015,48(11): 1777-1786
11 ZHAO Jin-Wei,CHENG Wei,FENG Ya-Hui. Spectroscopy and Spectral Analysis,2004,24(6): 733-736
赵金伟,程 薇,封亚辉. 光谱学与光谱分析,2004,24(6): 733-736
12 Souza J R D,Duyck C B,Fonseca T C O,Saint P. J. Anal. Atom. Spectrom.,2012,27(8): 1280-1286
13 LI Peng,SHAO Zhi-Ying,PEI Fei,LIU Qin,HU Qiu-Hui,FANG Yong. Chinese Journal of Analysis Laboratory,2018,37(12): 1472-1477
李 彭,邵志颖,裴 斐,刘 琴,胡秋辉,方 勇. 分析试验室,2018,37(12): 1472-1477
14 Trindade A S N,Dantas A F,Lima D C,Ferreira S L C,Teixeira L S. Food Chem.,2015,185: 145-150
15 Ni Z,Tang F,Yu Q,Wang Z. Environ. Qual. Saf.,2016,9(5): 1134-1141
16 Nash A M,Mounts T L,Kwolek W F. J. Geophys. Res. C,1983,60(4): 811-814
17 Sun H J. J. Am. Oil Chem. Soc.,1989,66(4): 549-552
18 Kara D,Fisher A,Hill S. Food Chem.,2015,188 143-148
19 Savio M,Ortiz M S,Almeida C A,Olsina R A,Martinez L D,Gil R A. Environ. Sci. Res. Rep.,2014,159(6): 433-438

