儿童急性播散性脑脊髓炎临床分析
曾向东,胡文广,刘平,邓佳,徐洋
急性播散性脑脊髓炎(ADEM)是一种免疫介导的广泛累及CNS白质的特发性炎症脱髓鞘疾病[1],常见于儿童与青少年[2],常与感染、疫苗接种有关。临床特征以脑病、多灶性神经系统症状和体征为主,伴多灶性脱髓鞘病灶。国外一项多中心研究发现,在免疫介导的CNS炎症中,ADEM排首位[3]。ADEM与多发性硬化(MS)及其变异型、视神经脊髓炎谱系疾病(NMOSD)等免疫脱髓鞘疾病的临床鉴别有一定困难,因此有必要对ADEM的临床特点进行深入探讨。本研究收集66例ADEM患儿临床资料并进行总结,以期提高对本病的认识。
1 临床资料
1.1 对象 系2013年12月至2015年12月我科收治的66例ADEM患儿。纳入标准:(1)符合国际儿童MS研究小组的儿童ADEM诊断标准[4];(2)年龄≤18岁。排除标准:(1)患儿起病前有脱髓鞘病史或/和合并有神经系统基础疾病者;(2)随访符合MS、视神经脊髓炎(NMO)或系统性红斑狼疮(SLE)的患者;(3)不同意随访的患者。其中男33例,女33例;年龄0.5~13岁,平均(4.27±3.14)岁;病程6~30 d,平均(19.25±5.71)d。入组者呈四季散发趋势(图1)。42例(63.6%)起病前2~30 d有呼吸道或消化道感染史,38例(90.5%)继发于病毒感染,4例(9.5%)继发于细菌感染,5例(7.6%)继发于疫苗接种(流感疫苗、乙肝疫苗、百白破疫苗、狂犬疫苗及肺炎链球菌疫苗各1 例)。本研究征得患儿监护人同意,并由患儿监护人签署知情同意书。
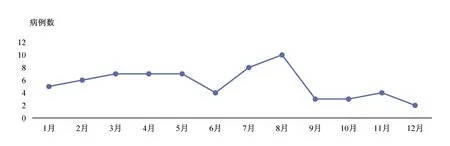
图1 ADEM患儿各月份无明显差别,呈四季散发趋势
1.2 临床表现 见表1。所有患儿均有脑病表现,其中意识障碍50例(75.8%),认知减退9例(13.6%),精神症状6例(9.1%),认知障碍合并精神症状1例(1.5%)。其他临床症状包括发热46例(69.7%),锥体束征33例(50.0%),惊厥32例(48.5%),头痛27例(40.1%),共济失调26例(39.4%),言语障碍14例(21.2%),颅神经受累11例(16.7%)(面神经受累7例,展神经受累1例,视神经受累2例,面神经合并视神经1例),锥体外系症状9例(13.6%),感觉异常7例(10.6%)。
1.3 实验室检查 39例行血清AQP4-IgG及髓鞘少突胶质细胞糖蛋白(MOG)-IgG检测,均阴性。66例行CSF常规、生化、培养及寡克隆区带检测,其中25例(37.9%)白细胞轻中度升高(15×106/L~255×106/L),以单核为主;27例(40.1%)蛋白升高(>400 mg/L),最高达1 962 mg/L;寡克隆区带(OCB)检查均阴性。66例患儿均行MRI检查,MRI病灶以皮质下白质(56例,84.8%)、深部核团(24例,36.4%)、脑干(11例,16.7%)及小脑(10例,15.2%)多见,脊髓受累相对较少(5例,7.6%)。65例患儿行EEG检查,其中45例(69.2%)提示背景慢波增多;7例(10.8%)提示有癫痫放电(表1)。
1.4 不同神经功能损伤组临床资料的比较 根据入院时Kurtzke扩展残疾状况量表(EDSS)评分,将患者分为轻症组(≤2.5分)41例(81.2%)、中症组(3~6分)15例(22.7%)及重症组(≥6.5分)10例(15.2%)[5]。三组间临床资料差异无统计学意义(均P>0.05)(表2)。
1.5 治疗方法 66例患儿均给予糖皮质激素治疗。56例采用甲泼尼龙冲击治疗,给予甲泼尼龙15~30 mg/(kg·d),每日1次,静脉滴注3 d后改用泼尼松龙1.5~2 mg/(kg·d)晨起顿服4 d为1疗程。其中3例治疗1疗程,34例治疗2疗程,19例治疗3疗程。另外10例患儿采用地塞米松0.5 mg/(kg·d)静脉滴注5~7 d。所有患儿于静脉糖皮质激素滴注结束后继续口服泼尼松龙片1.5~2 mg/(kg·d),每日1次,晨起顿服,3~6个月内减停。甲泼尼龙冲击治疗患儿最后一次随访时mRS评分[(0.81±1.29)分]与地塞米松静脉滴注治疗患儿[(1.50±1.78)分]差异无统计学意义(t=1.47,P=0.15)。
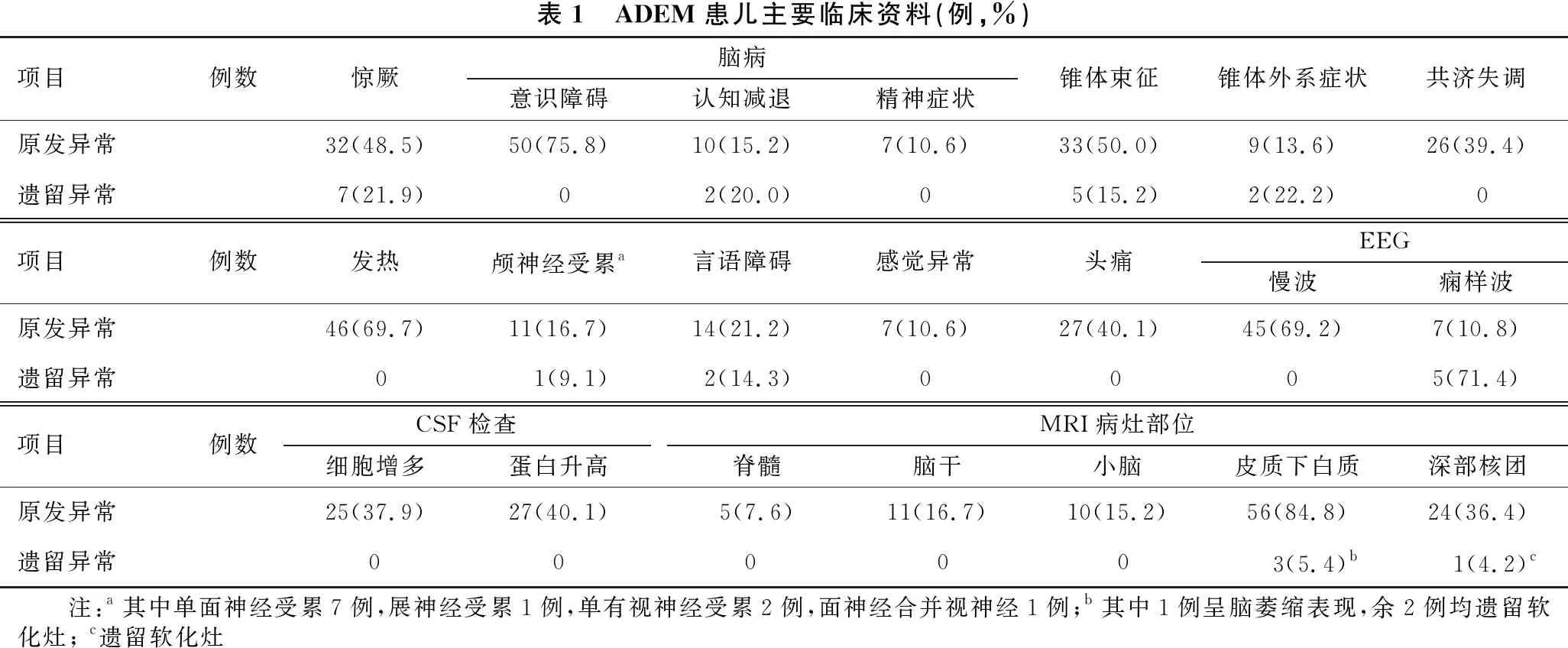
表1 ADEM患儿主要临床资料(例,%)项目例数惊厥脑病意识障碍认知减退精神症状锥体束征锥体外系症状共济失调原发异常32(48.5)50(75.8)10(15.2)7(10.6)33(50.0)9(13.6)26(39.4)遗留异常7(21.9)02(20.0)05(15.2)2(22.2)0项目例数发热颅神经受累a言语障碍感觉异常头痛EEG慢波痫样波原发异常46(69.7)11(16.7)14(21.2)7(10.6)27(40.1)45(69.2)7(10.8)遗留异常01(9.1)2(14.3)0005(71.4)项目例数CSF检查细胞增多蛋白升高MRI病灶部位脊髓脑干小脑皮质下白质深部核团原发异常25(37.9)27(40.1)5(7.6)11(16.7)10(15.2)56(84.8)24(36.4)遗留异常000003(5.4)b1(4.2)c 注:a其中单面神经受累7例,展神经受累1例,单有视神经受累2例,面神经合并视神经1例;b其中1例呈脑萎缩表现,余2例均遗留软化灶; c遗留软化灶
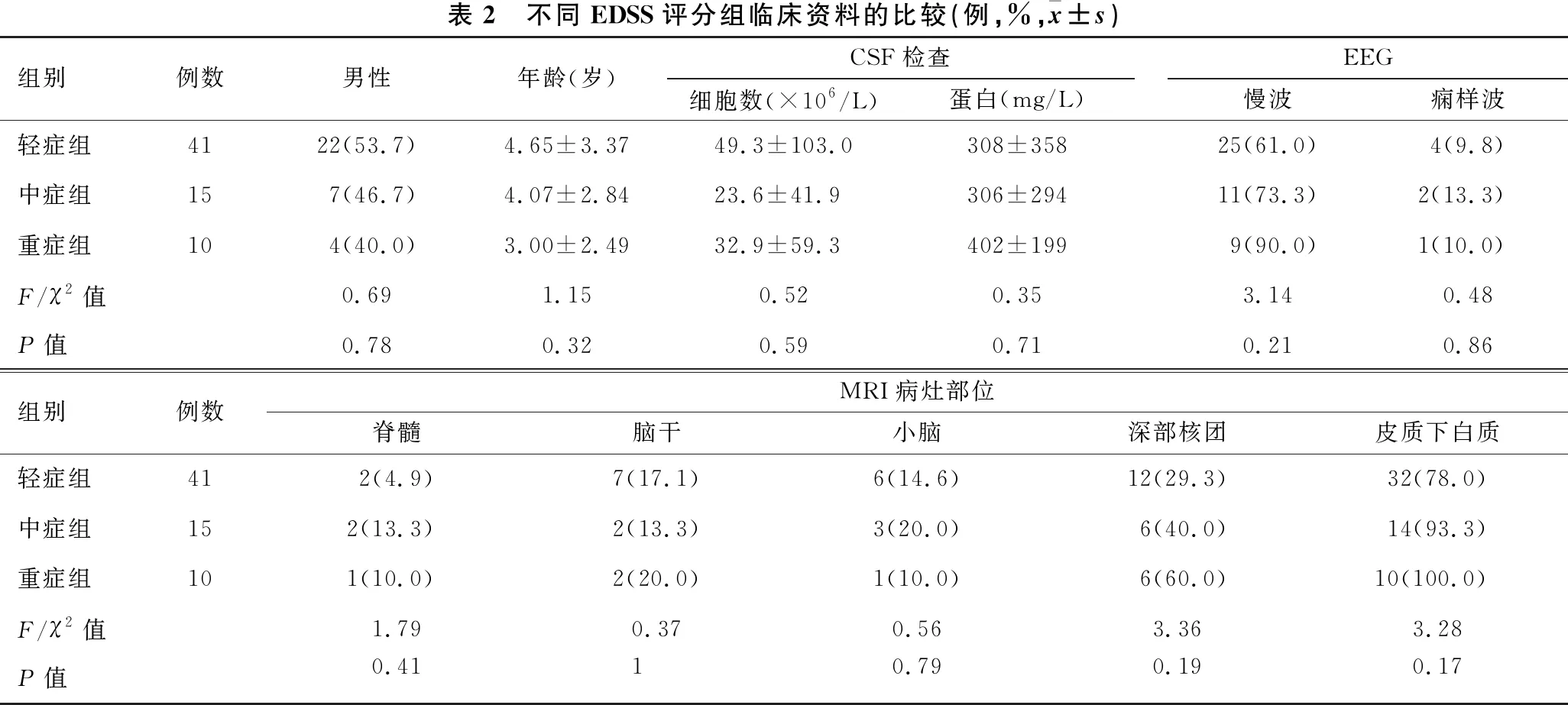
表2 不同EDSS评分组临床资料的比较(例,%,x±s)组别例数男性年龄(岁)CSF检查细胞数(×106/L)蛋白(mg/L)EEG慢波痫样波轻症组4122(53.7)4.65±3.3749.3±103.0308±35825(61.0)4(9.8)中症组157(46.7)4.07±2.8423.6±41.9306±29411(73.3)2(13.3)重症组104(40.0)3.00±2.4932.9±59.3402±1999(90.0)1(10.0)F/χ2值0.691.150.52 0.35 3.140.48P值0.780.320.590.710.210.86组别例数MRI病灶部位脊髓脑干小脑深部核团皮质下白质轻症组412(4.9)7(17.1)6(14.6)12(29.3)32(78.0)中症组152(13.3)2(13.3)3(20.0)6(40.0)14(93.3)重症组101(10.0)2(20.0)1(10.0)6(60.0)10(100.0)F/χ2值1.790.370.563.363.28P值0.4110.790.190.17
1.6 随访情况 截至2018年12月,66例患儿于门诊进行了3~5年的定期(6~12个月)随访。主要遗留症状包括反复癫痫发作(7例)、肢体运动障碍(7例)、认知减退(2例)、语言障碍(2例)、颅神经受累(1例)。根据患者最后一次随访时的mRS评分将患者分为康复组(0分)39例(59.1%)、好转组(1~2分)16例(24.2%)及恢复不佳组(≥3分)11例(16.7%)[3]。三组间年龄(F=4.47,P=0.02)、入院EDSS评分(F=38.62,P<0.01)及惊厥(χ2=9.64,P=0.01)、言语障碍(χ2=17.64,P<0.01)、认知减退(χ2=24.15,P<0.01)的比率差异有统计学意义(表3)。
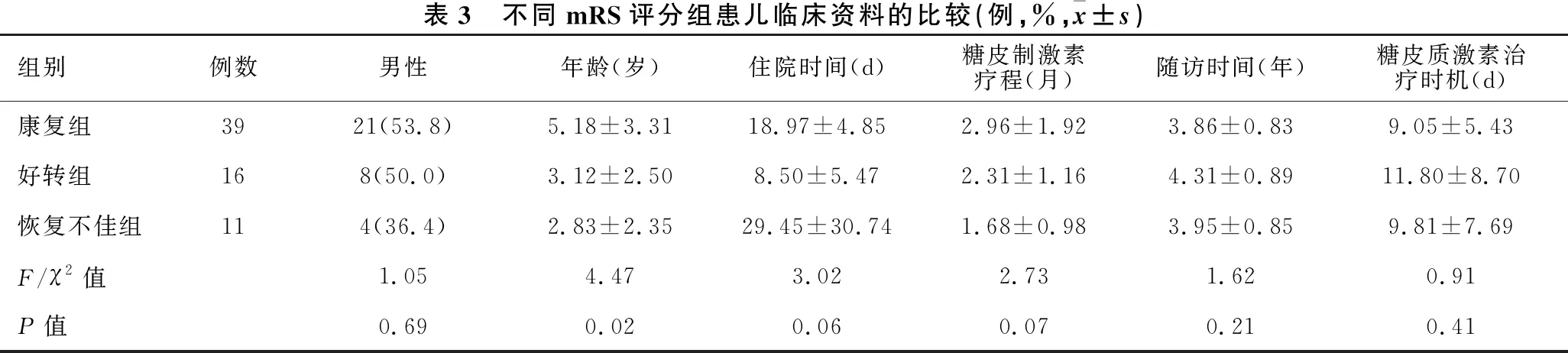
表3 不同mRS评分组患儿临床资料的比较(例,%,x±s)组别例数男性年龄(岁)住院时间(d)糖皮制激素疗程(月)随访时间(年)糖皮质激素治疗时机(d)康复组3921(53.8)5.18±3.3118.97±4.852.96±1.923.86±0.839.05±5.43好转组168(50.0)3.12±2.508.50±5.472.31±1.164.31±0.8911.80±8.70恢复不佳组114(36.4)2.83±2.3529.45±30.741.68±0.983.95±0.859.81±7.69F/χ2值1.054.473.022.731.62 0.91P值0.690.020.060.070.210.41
续表
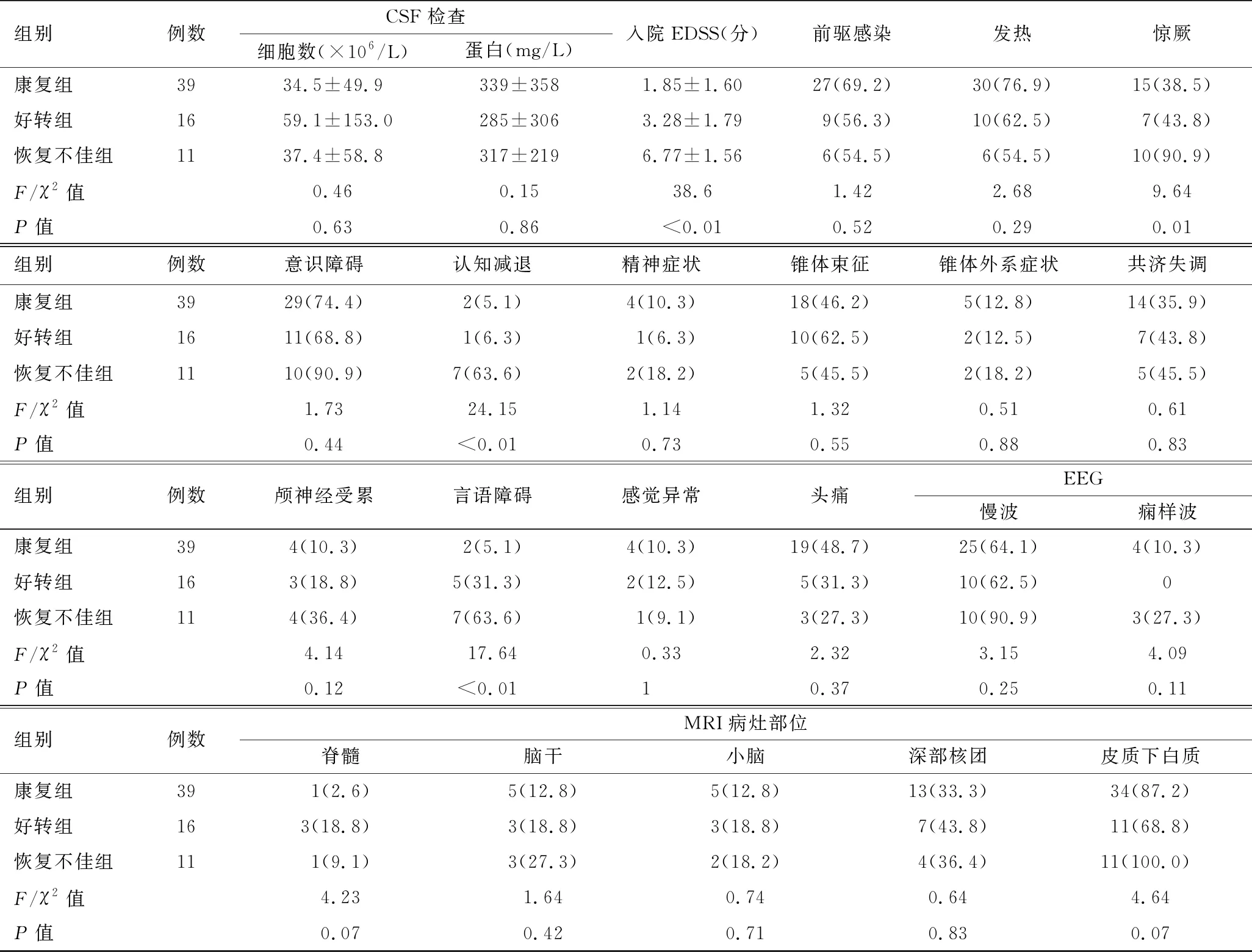
组别例数CSF检查细胞数(×106/L)蛋白(mg/L)入院EDSS(分)前驱感染发热惊厥康复组3934.5±49.9339±3581.85±1.6027(69.2)30(76.9)15(38.5)好转组1659.1±153.0285±3063.28±1.799(56.3)10(62.5)7(43.8)恢复不佳组1137.4±58.8317±2196.77±1.566(54.5)6(54.5)10(90.9)F/χ2值0.460.1538.61.422.689.64P值0.630.86<0.010.520.290.01组别例数意识障碍认知减退精神症状锥体束征锥体外系症状共济失调康复组3929(74.4)2(5.1)4(10.3)18(46.2)5(12.8)14(35.9)好转组1611(68.8)1(6.3)1(6.3)10(62.5)2(12.5)7(43.8)恢复不佳组1110(90.9)7(63.6)2(18.2)5(45.5)2(18.2)5(45.5)F/χ2值1.7324.151.141.320.510.61P值0.44<0.010.730.550.880.83组别例数颅神经受累言语障碍感觉异常头痛EEG慢波痫样波康复组394(10.3)2(5.1)4(10.3)19(48.7)25(64.1)4(10.3)好转组163(18.8)5(31.3)2(12.5)5(31.3)10(62.5)0恢复不佳组114(36.4)7(63.6)1(9.1)3(27.3)10(90.9)3(27.3)F/χ2值4.1417.640.332.323.154.09P值0.12<0.0110.370.250.11组别例数MRI病灶部位脊髓脑干小脑深部核团皮质下白质康复组391(2.6)5(12.8)5(12.8)13(33.3)34(87.2)好转组163(18.8)3(18.8)3(18.8)7(43.8)11(68.8)恢复不佳组111(9.1)3(27.3)2(18.2)4(36.4)11(100.0)F/χ2值4.231.640.740.644.64P值0.070.420.710.830.07
2 讨 论
ADEM是常见的CNS脱髓鞘疾病之一[3]。国内报道,ADEM的年发病率为0.3/100 000[6]。ADEM发病高峰为5~9岁,男女发病率无显著差异[6-7]。发病前常有前驱感染或疫苗接种史,以前驱病毒感染较多见,但并不是所有ADEM患儿都有前驱事件。前驱事件不是诊断ADEM的特异指标[8]。本研究纳入的患儿男女比例相当,发病年龄为(4.27±3.14)岁,63.6%的患儿有前驱感染,7.6%的患儿有疫苗接种史。
ADEM临床表现复杂多样,且轻重不一。本研究根据入院时EDSS评分,将患儿神经功能损伤分为轻、中、重症组,试探讨CSF、EEG及MRI等指标与病情轻重的相关性,结果并无阳性发现。因此,评价ADEM患者病情轻重需结合临床综合分析,不推荐根据单一实验室指标做出判断。有研究发现,ADEM患者病情轻重与炎症脱髓鞘累及部位有关[9]。本研究提示,不同神经功能损伤患儿的病灶部位差异无统计学意义,考虑与各部位受损严重程度不一有关。ADEM以急性脑病伴多灶性神经功能障碍为主要临床特征,病初常有发热、头痛、呕吐等非特异性表现。随着病情进展,患者逐渐出现神经系统症状,如锥体束征、共济失调、急性偏瘫、颅神经损害、惊厥及言语障碍等[10-11]。脑病(意识障碍、精神行为异常)是ADEM诊断的必要条件,本研究所有患儿均具有脑病表现。但近年来对于ADEM是否必须具有脑病表现及脑病表现如何明确界定的争议越来越多。国外研究发现,无脑病但有其他ADEM典型表现患儿的国际儿童MS研究小组ADEM诊断符合率仅70%,因此认为国际儿童MS研究小组的ADEM诊断标准过于严格[12]。本组患儿除脑病外,以发热、锥体束征、惊厥、头痛、共济失调及言语障碍症状多见。
ADEM缺乏特异性实验室指标,但近年来越来越多的研究探讨MOG抗体在ADEM的作用。研究表明,儿童持续性血清MOG-IgG抗体阳性患者,其炎症性脱髓鞘障碍的复发率较高,MOG-IgG血清评估对估计患儿预后具有重要的临床意义[13]。有报道称,64.3%的ADEM患儿血清MOG抗体阳性,ADEM复发患儿的血清MOG抗体阳性率高达96%[14]。本组39例患儿的血清MOG抗体均为阴性,可能系部分患儿病程中存在MOG-IgG抗体阳性,但为一过性,而本研究中无复发患者,故未对MOG-IgG抗体进行持续动态监测。
MRI检查对诊断具有重要意义。典型的头颅MRI表现为双侧多灶性、非对称性长T1、长T2异常信号影,病变主要累及皮质下白质、脑干、小脑、丘脑及深部核团[9-10]。本组患者上述部位均累及,与报道一致。有文献报道,脊髓受累率为11%~28%[15]。而本研究脊髓病变率约为7%,较以往报道偏低,可能是因为部分患者临床脊髓受累症状不重,未完善脊髓检查。
目前尚无ADEM药物治疗的大样本多中心随机对照临床试验。糖皮质激素被认为是本病的一线治疗药物[10],但药物种类、剂量和减量方法至今尚未统一。一项回顾性临床研究显示,静脉滴注甲泼尼龙优于地塞米松[16]。本研究结果显示,甲泼尼龙冲击治疗患者最后一次随访时mRS评分(0.81±1.29)与地塞米松静脉滴注治疗患者(1.50±1.78)差异无统计学意义(t=1.47,P=0.15)。可能的原因为医生更倾向于予临床病情较轻者地塞米松治疗(分组未随机化)。因此,针对ADEM的不同治疗方案的随机试验可能更有助于进一步明确不同治疗方案的疗效。丙种球蛋白是本病的二线用药。但临床中,特别是未除外糖皮质激素禁忌证时,可采用丙种球蛋白早期冲击治疗,能够迅速减轻免疫反应,改善预后[17]。其他二线治疗还包括血浆置换、免疫抑制剂等。
儿童ADEM患者预后良好。研究表明,57%~94%的患儿可完全康复,少数遗留神经功能缺损症状,主要遗留症状包括运动障碍、认知及言语功能减退、癫痫发作等[18]。本组59.1%的患者完全康复,余患儿均有不同程度的遗留症状,主要包括癫痫发作、肢体运动障碍、认知减退、语言较同龄儿落后等。本研究结果显示,入院时EDSS评分越低,预后越好。患儿起病年龄越大,预后越好,可能因为患儿年龄越大自身免疫状态越完善。发病时伴有惊厥、言语障碍及认知减退(皮质受损)的患儿,预后相对较差,提示起病时伴有皮质受损的患儿预后可能相对较差。但本研究样本量相对较小,未来还需通过随机大样本的研究进一步验证。
综上所述,ADEM并不是一种罕见的脱髓鞘疾病,发病前多有前驱史,临床表现多样,MRI对诊断具有重要意义,多数患者经积极糖皮质激素治疗后预后良好,少数遗留后遗症。本研究比较分析发现,起病年龄、发病时EDSS评分、发病时是否伴有惊厥、言语障碍及认知减退,可能与预后结局有关。

