HPLC法测定参麦地黄丸中毛蕊花糖苷含量的研究
佘雪花 潘 馨
福建中医药大学药学院,福建 福州 350122
参麦地黄丸始载于清代张秉成《成方便读》,是补益剂中补阴剂的代表方,由熟地黄、山药、山茱萸、泽泻、茯苓、牡丹皮、麦冬、北沙参八味中药组成[1]。参麦地黄丸具有养阴润肺之功效,临床上主要用于肺肾两虚、咳嗽气喘、咽干口燥[2-3]。其中,熟地黄滋肾填精为主药,毛蕊花糖苷常被作为熟地黄质量控制的指标性成分,具有抗氧化、增强免疫功能等作用[4-5]。目前参麦地黄丸质量标准仅有丸剂的常规制剂检查项,缺少有效成分的含量控制[1]。为更好控制参麦地黄丸的质量,本研究建立了HPLC法测定其毛蕊花糖苷含量,以期进一步提高参麦地黄丸的质量标准。
1 仪器与材料
1.1 仪器 日本岛晶LC-20AT高效液相色谱仪;在线脱气机、四元泵、自动进样器、柱温箱、DAD检测器、LCsolution工作站(岛晶制造);数控超声波清洗器KQ-500DE型(昆山市超声仪器有限公司);OHAUS型万分之一电子分析天平(奥豪斯仪器(常州)有限公司);Milli-Q超纯水系统(美国,Millipore公司)。
1.2 材料 参麦地黄丸由福州海王金象中药制药有限公司生产提供(批号:1905071、1905072、1904162、1905081、1904152);毛蕊花糖苷对照品(批号:AF8051802),购自成都埃法生物科技有限公司;乙腈为色谱纯(天津市福晨化学试剂厂),冰醋酸为分析纯(天津市福晨化学试剂厂),水为自制超纯水,其余试剂均为分析纯(天津市福晨化学试剂厂)。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液的制备 精密称取毛蕊花糖苷2.66 mg,置于25 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,即得对照品储备液。再精密量取1 mL置10 mL容量瓶中,加流动相定容至刻度,配制成10.64 μg/mL对照品溶液。
2.1.2 供试品溶液的制备 取本品细粉约10 g,精密称定,置圆底烧瓶中,精密加入甲醇100 mL,称定重量,加热回流30min,放冷,用甲醇定容,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液50 mL,减压回收溶剂近干,残渣用流动相溶解,转移至10 ml量瓶中,加流动相至刻度,摇匀,滤过,取续滤液,即得。
2.1.3 阴性对照溶液的制备 按处方比例称取参麦地黄丸处方饮片(除熟地外),按照制备工艺制成参麦地黄丸缺熟地的阴性样品,并按上述供试品溶液制备方法,制成阴性对照溶液。
2.2 色谱条件与系统适用性试验 色谱柱:Chrom CoreTMC18 (5 μm,4.6×250 mm);流动相:乙腈-0.1%冰醋酸溶液 (14∶86);流速:1.0 mL/min;柱温:30 ℃。检测波长:334 nm;进样量:20 μL。理论塔板数按毛蕊花糖苷峰计算应不低于5000[6]。
2.3 专属性试验 分别取对照品溶液、供试品溶液、阴性对照溶液按“2.2”项下方法进样分析,在该色谱条件下,供试品中毛蕊花糖苷与对照品色谱峰保留时间一致,与相邻峰的分离度大于1.5,阴性对照品溶液未见该峰,说明阴性无干扰。色谱图见图1。
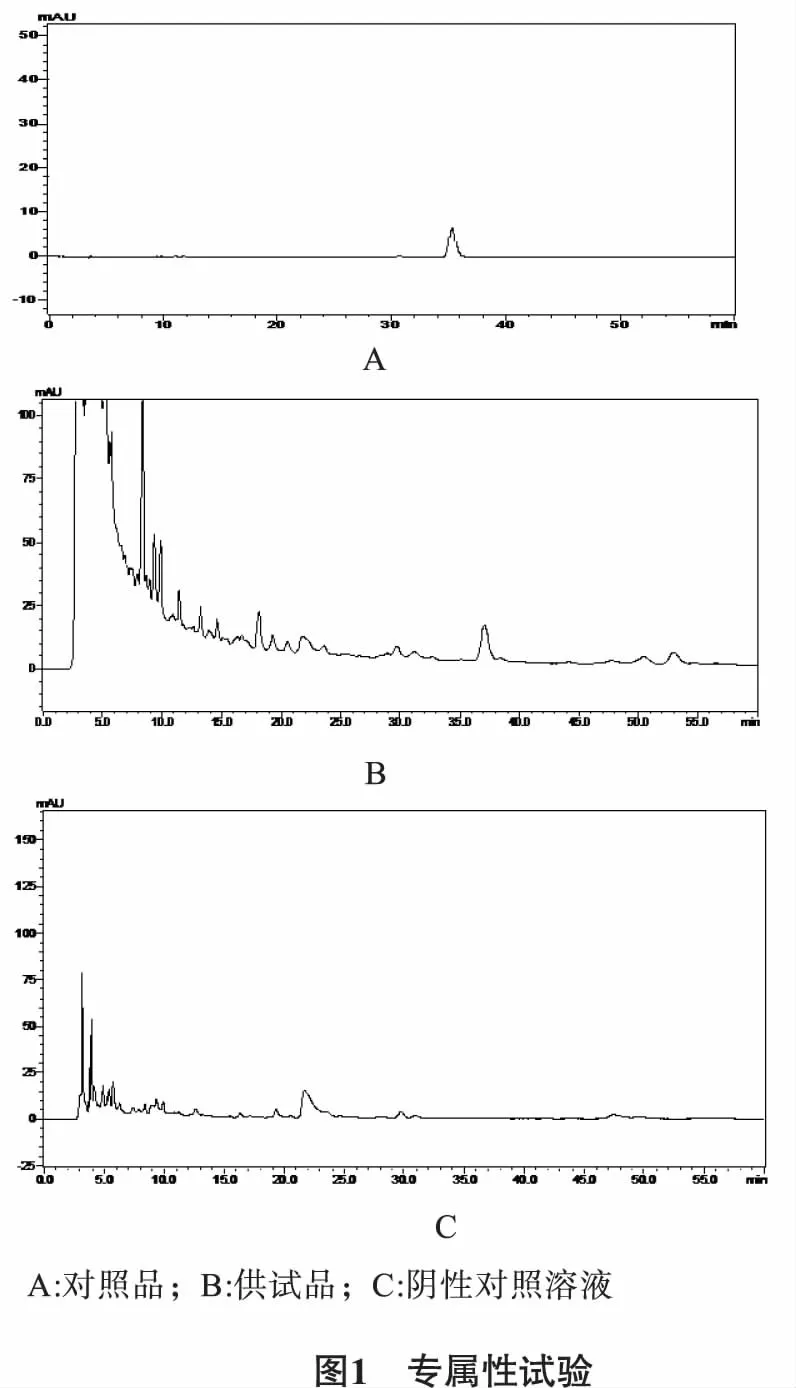
2.4 线性关系考察 分别精密量取“2.1.1”项下对照品储备液0.2 mL、1 mL、4 mL、6 mL、8 mL置10 mL容量瓶,用流动相稀释至刻度,配制成2.13 μg/mL、10.64 μg/mL、42.56 μg/mL、63.84 μg/mL、85.12 μg/mL的浓度。按“2.2”项下方法测定,以峰面积(mAU)为纵坐标,相应的毛蕊花糖苷对照品浓度(μg/mL)为横坐标进行线性回归,得回归方程:y=30347x+135606,r=0.9992。毛蕊花糖苷在2.13~106.4 μg/mL范围呈线性关系。
2.5 精密度试验 取对照品溶液,连续进样6次,按“2.2”项下色谱条件测定,测得毛蕊花糖苷峰面积的RSD为1.47%,表明仪器精密度良好。
2.6 稳定性试验 取同一批号参麦地黄丸供试品溶液室温下放置,分别于0,2,4,8,12,24 h,按“2.2”项下色谱条件进样,测定毛蕊花糖苷峰面积,计算RSD为1.77%。表明供试品溶液中毛蕊花糖苷在24 h内稳定。
2.7 重复性试验 取同一批号参麦地黄丸(201904152),称取5份,每份约10 g,精密称定,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进样。测得毛蕊花糖苷平均含量为0.0474 mg/g,RSD为1.56%。表明该方法重复性良好。
2.8 加样回收率试验 取已知含量的同一批号参麦地黄丸(201904152),采用加样回收试验,精密加入一定量毛蕊花糖苷对照品,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进样测定,计算回收率。结果毛蕊花糖苷平均回收率(n=6)为97.63%,RSD为0.63%。表明本法具有较好的加样回收率。见表1。
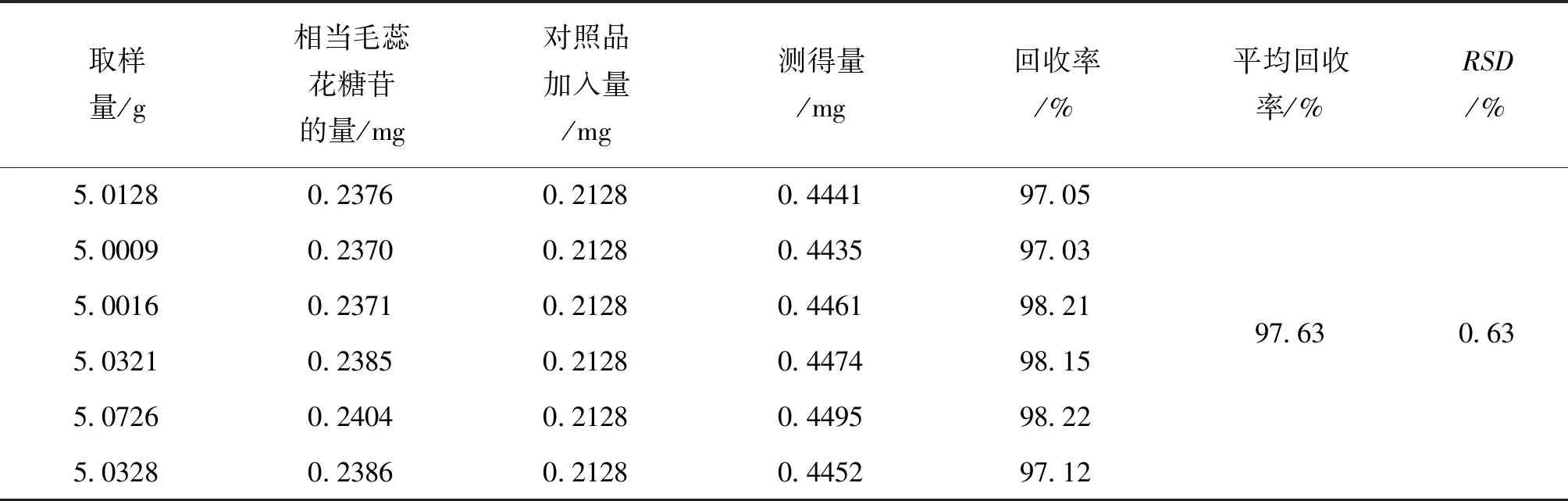
表1 回收率试验结果
2.9 样品含量测定 取5批样品(批号:1905071、1905072、1904162、1905081、1904152),按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进样测定,并计算含量,样品含量测定结果见表2。

表2 参麦地黄丸样品测定结果
3 讨论
熟地黄为参麦地黄丸的主药,熟地黄中有效成分含量直接关系到药品的疗效。2015版《中国药典》将毛蕊花糖苷作为评价熟地黄的指标性成分,规定其含量不少于0.020%[7]。故本实验通过建立HPLC法测定参麦地黄丸中毛蕊花糖苷含量。在对毛蕊花糖苷的分离试验中,考察了乙腈—水、乙腈-磷酸溶液、乙腈-冰醋酸溶液为流动相进行测定,发现流动相为乙腈-0.1%冰醋酸溶液(14∶86),分离效果较好。对毛蕊花糖苷对照品溶液进行扫描,在334 nm波长处有最大吸收,故以334 nm为检测波长。本研究通过测定参麦地黄丸中毛蕊花糖苷的含量,为本制剂的质量控制提供依据,后期课题组将继续研究其他成分含量测定,以不断提高参麦地黄不同制剂的质量标准。

