aVR与aVL导联QS波振幅比鉴别右室流出道室性心律失常起源前后侧的价值
张海青,张玉霄,史成龙,周叶,卢才义*
(1解放军总医院第一医学中心心血管内科,北京100853;2解放军联勤保障部队第九六〇医院第一派驻门诊部,济南 250031;3解放军联勤保障部队第九八三医院心血管内科,天津 300142;4首都医科大学附属北京友谊医院医疗保健中心心血管内科,北京 100050)
右室流出道(right ventricular outflow tract,RVOT)是无器质性心脏病的室性心律失常最常见的起源部位,通过导管射频消融手术治疗效果好,安全性高[1]。术前通过心电图预判室性心律失常的具体起源部位,可以减少标测时间,增加手术成功率[2]。起源于RVOT的室性心律失常(ventricular arrhythmias,VAs)心电图通常表现为特征性的左束支传导阻滞及下壁导联高大R波等特征,但由于RVOT解剖部位复杂,常常需要与毗邻结构如主动脉窦部起源的室性心律失常相鉴别[3]。目前关于鉴别RVOT-VAs与心脏其他部位起源VAs的心电图方法研究较多,且灵敏度及特异度均较高[4-9],但对于RVOT内部消融靶点的三维定位尚缺少准确度高的心电图指标。根据Kamakura等提出的RVOT三维解剖分区[10],在右前斜30°透视下,RVOT可分为前侧和后侧,根据其解剖方位与心电向量方向的关系,有学者提出使用I导联QRS波的正负或aVL和aVR导联的QS波振幅来鉴别其前后侧[11,12],但目前尚无统一标准。本研究旨在探讨aVR与aVL导联QS波振幅及比值对鉴别RVOT室性心律失常起源点前、后侧的价值。
1 对象与方法
1.1 研究对象
回顾性分析2009年至2019年在解放军总医院第一医学中心行导管射频消融且靶点在RVOT的87例室性心律失常患者的临床资料。纳入标准:(1)单形性室性早搏或室性心动过速;(2)有至少1份室性心律及窦性心律下的12导联体表心电图;(3)VAs引起明显临床症状或动态心电图提示室性心律失常负荷≥10%或超过8 000次/24 h;(4)心电图aVR与aVL导联呈QS型。排除标准:(1)多形性VAs;(2)成功消融靶点不在RVOT或存在多个消融靶点;(3)术中消融失败或术后6个月内复发症状性的室性心律失常。依据Kamakura等提出的RVOT解剖分区,消融靶点在左侧1/2为RVOT前侧,在右侧1/2为RVOT后侧,将手术患者划分为2组:前侧组(n=52)和后侧组(n=35)。患者术前均签署知情同意书,且停用抗心律失常药物至少5个半衰期。
1.2 方法
收集患者性别、年龄等一般资料。采用数字心电图机记录患者室性心律及窦性心律下的12导联心电图特征,心电图纸速25.0 mm/s,振幅10 mm/mv。对于已经出院的患者通过电子病历系统获取院内12导联心电图扫描图像,采用DESKTOP-RULER电子卡尺软件,检测患者心电图aVR与aVL导联QS波的振幅,分别记为QSaVR和QSaVL,计算二者比值,记为QSaVR/QSaVL。
采用CARTO或ENSITE三维标测系统进行RVOT三维电解剖立体构型,予起搏联合激动标测,找到最早激动点或起搏图形与发病时室性心律心电图相同的位点作为消融靶点。消融后给予异丙肾静脉滴注及右室程控刺激,不再诱发室性心律失常则结束手术。术后全部患者接受电话随访,如有心悸不适则接受12导联心电图及24小时动态心电图检查以明确。消融成功定义为术后6个月以内不出现症状性VAs。保存右前斜30°时消融靶点位置的影像。
1.3 统计学处理

2 结 果
2.1 2组患者一般资料比较
2组患者在性别、年龄等基线资料间差异无统计学意义(P>0.05;表1),具有可比性。
2.2 2组患者心电图指标比较
消融靶点在RVOT前侧组相对于RVOT后侧组表现为更小的QSaVR[(0.88±0.25)和(1.03±0.32)mV],更大的QSaVL[(0.87±0.37)和(0.61±0.38)mV],从而表现为更小的振幅比QSaVR/QSaVL[(1.25±0.81)和(2.13±1.16)]。2组患者QSaVR、QSaVL、QSaVR/QSaVL间差异均具有统计学意义(P<0.05;表2)。
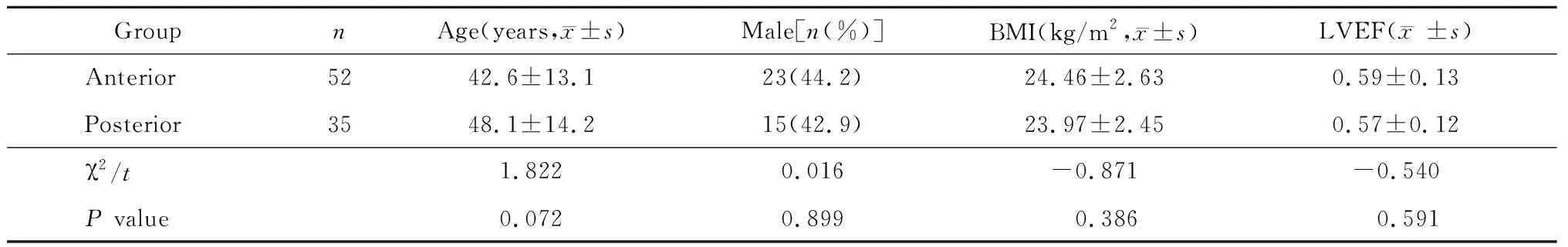
表1 2组患者一般临床资料对比
BMI: body mass index; LVEF: left ventricular ejection fraction.
表2 2组患者心电图特征比较
QSaVR: QS-wave amplitude in lead aVR;QSaVL: QS-wave amplitude in lead aVL; ECG: electrocardiogram.
2.3 ROC曲线
ROC曲线结果显示,QSaVR/QSaVL、QSaVL和QSaVR的AUC分别为0.786、0.724和0.649,可见QSaVR/QSaVL的AUC大于QSaVL和QSaVR,当QSaVR/QSaVL截断点取1.48时,约登指数最大(0.54),此时预测RVOT前侧靶点的灵敏度为0.83,特异度为0.71;当截断点取1.12时,约登指数为0.52,此时预测RVOT前侧靶点的灵敏度为0.67,特异度0.86(图1)。
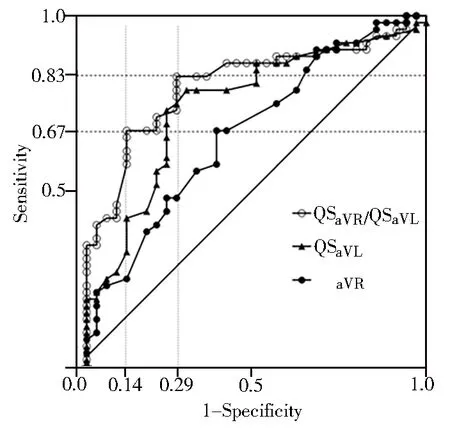
图1 QSaVR、QSaVL和QSaVR/QSaVL估测RVOT室性心律失常起源点前后侧的ROC曲线
QSaVR: QS-wave amplitude in lead aVR; QSaVL: QS-wave amplitude in lead aVL;RVOT: right ventricular outflow tract;ROC:receiver operating characteristic.
3 讨 论
RVOT,又称右室漏斗部,下界位于室上嵴,上界达肺动脉瓣,是右室解剖结构移行集中的部位,也是右室血流动力学变化大的部位,这可能是该部位心律失常发生率高的原因[13]。RVOT毗邻主动脉窦,位于心底高位,故其起源的室性心律失常在心室内除极方向向下,在aVR和aVL导联表现为倒立的QS波,在Ⅱ、Ⅲ和 aVF导联则表现为高大直立的R波[14]。对RVOT起源的室性心律失常精确定位,可以避免射频消融手术中不必要的穿刺和标测,减少手术时间及射线暴露。虽然随着计算机技术的进步,远程心电监测、心电标测背心等新技术不断涌现[15,16],但常规体表心电图作为简单且无创的检查手段仍有其不可替代的地位。体表心电图指标预判RVOT-VAs消融靶点位置的研究不断推陈出新:比如Yoshida等提出的胸导移行区积分指数[5],Betensky等提出的V2转换比率[6],以及Yoshida等后来提出的V2S/V3R指数[7],用于RVOT-VAs靶点定位的准确性不断提高。近年来,Kaypakli等[8]提出的V1-V2导联S-R差,Cheng等[9]提出的V3R/V7指数,对于鉴别左、右流出道室早的准确性甚至优于V2S/V3R指标,V3R/V7鉴别左右室流出道室性心律失常起源点的灵敏度可达87%,特异度可达96%。但RVOT内部的消融靶点三维定位尚缺少公认的心电图诊断特征[17]。
本研究依据Kamakura等提出的RVOT解剖分区,其前侧起源的室性心律失常除极扩布方向偏右下,故aVL导联可能表现为更深的QS波;同理,后侧起源的除极偏左下,在aVR导联可能表现为更深的QS波,因此推测通过aVR与aVL导联QS波振幅进行前后侧鉴别可能会有不错的效果。目前针对该指标相关的研究不多,且缺乏统一标准。本研究在前期研究基础上,对QSaVR、QSaVL和QSaVR/QSaVL3个指标进行了验证,发现QSaVR/QSaVL对于预测RVOT室性心律失常前、后侧有一定意义(AUC=0.786),当QSaVR/QSaVL截断点取1.48时,约登指数最大(0.54),此时预测室性心律失常起源点位于RVOT前壁的灵敏度为0.83,特异度为0.71。
本研究结果表明,aVR/aVL导联QS波振幅比可基本实现对RVOT室性心律失常起源点前、后侧的鉴别,对于术前精确定位消融靶点有一定的指导意义。本研究的局限性在于:(1)回顾性分析,缺少进一步前瞻性验证;(2)部分采用的心电图为病历扫描所得,扫描后通过电子标尺软件计算,可能存在测量偏倚。

