基于GC-TOFMS技术对痰浊壅肺型COPD急性加重期血清代谢组学研究
张瑞,张凤云,黄雪元
(上海市嘉定区中医医院,上海 201800)
慢性阻塞型肺病 (COPD)是一种慢性非特异性炎症性疾病[1],“痰浊壅肺证”是COPD急性加重期(AECOPD)的最主要证型之一。中医证候传统研究手段缺乏客观的诊断标准,使方剂疗效难以正确评价。目前代谢组学广泛应用于中医药证本质科研研究,本研究运用气相色谱-飞行时间质谱联用(GC-TOFMS)技术寻找中医AECOPD“痰浊壅肺证”的生物学物质基础,以期从系统生物学水平探讨中医“证”的本质,为临床诊断、治疗疾病提供客观依据,现报道如下。
1 资料与方法
1.1 临床资料
选取2017年4月—2019年4月上海市嘉定区中医医院门诊及住院确诊为COPD急性加重期,经中医辨证为痰浊壅肺证的60例患者作为疾病组。其中男性患者30例,女性患者30例;年龄(65.83±7.75)岁;病情严重程度GOLD 2级36例,GOLD 3级24例;病程(16.88±6.09)年;BMI(22.13±3.21)kg/m2;合并高血压者32例,2型糖尿病者33例,冠心病者21例。
本研究共纳入同期在我院体检中心的体检的健康受试者30例作为对照,年龄60~80岁,男性15例,女性15例。
1.2 诊断标准
疾病组:西医诊断标准及病情严重程度分级参照2016年GOLD诊断标准[2];中医诊断标准参照《中医病证诊断疗效标准》[3]。主证:咳嗽,喘息气促,咳痰黏稠量多,色白或成泡沫状;次证:喉间痰鸣,喘息不能平卧,胸部膨满,憋闷如塞,纳呆,脘腹胀满,肢体困重,大便秘结或不畅;舌脉:舌暗,苔薄腻或浊腻,脉小滑。具备主症及次症中≥2项者,结合舌象、脉象,即可诊断。健康组:参照《中医体质分类与判定》中平和质的判定标准[4]。
1.3 纳入标准
符合上述西医诊断标准同时符合肺胀病痰浊壅肺证中医诊断标准的患者,患者气流受限程度根据2016年慢性阻塞性肺疾病全球倡议[2](GOLD)纳入GOLD2级、GOLD3级患者,能够完成肺功能检测,第1秒用力呼气量(FEV1)%为30%~80%,吸入支气管舒张剂后FEV1/用力肺活量(FVC)%<70%,年龄60~80岁,且病情属于1周之内急性加重期,所有受试者均签署知情同意书并经上海市嘉定区中医医院伦理委员会审查批准。
1.4 排除标准
COPD伴有呼吸衰竭同时需要机械通气者;因肺部肿瘤、肺结核、支气管哮喘、支气管扩张、间质性肺病等原因导致的慢性喘咳患者;发病时有严重的心功能不全,肝、肾功能不全等诸脏器功能不全,造血系统疾病和精神疾病患者。
1.5 标本采集和制备
疾病组治疗前24 h内于清晨6:00左右在室温下釆取静脉4 mL,血液样本在室温下自然凝固1 h,收集血清,留置于EDTA管中,3 000 r/min离心10 min后收集血浆置于1.5 mL Eppendorf管中,置于液氮萃取后转运至-80 ℃冰箱中保存备用。
1.6 代谢物检测和分析
代谢组学的检测和分析与上海百趣生物科技有限公司共同完成,包括样品的处理、GC-TOFMS测试和数据处理分析部分。
1.6.1 实验仪器与试剂
仪器:Agilent 7890A GC-MS色谱仪(Agilent);PEGASUS HT质谱仪(LECO);DB-5MS色谱柱(Agilent);Heraeus Fresco17冷冻离心机(Thermo Fisher Scientific);Forma 900 series超低温冰箱(Thermo Fisher Scientific)。
试剂:甲醇(CNW Technologies);氯仿、吡啶、甲氧胺盐、L-2-氯苯丙氨酸、BSTFA及各化合物标准品(Adamas);FAMEs(REGIS Technologies);纯水由Merck Millipore系统制备。
1.6.2 样品处理
100 μL血清加入4倍体积冷甲醇及再加入10 μL L-2-氯苯丙氨酸沉淀蛋白,离心取上清液低温减压干燥;各样本分别取40 μL混合制备混合血清进行质量控制(quality control,QC),按相同方法进行前处理;提取物用30 μL甲氧胺盐试剂, 80 ℃孵育30 min后向每个样品中加入40 μL BSTFA溶解,70 ℃孵育90 min;之后加入5 μL FAMEs(溶于氯仿),随机顺序上机检测。
1.6.3 分析条件
色谱条件:DB-5MS(30 m×0.25 mm,0.25 μm)色谱柱;进样口温度280 ℃,不分流模式,进样量 1 μL,载气(高纯氦)流速为3 mL/min;柱箱升温程序为50 ℃保持1 min后,以10 ℃/min升至310 ℃,保持8 min。
质谱条件:标准EI离子源,电离电压-70 eV,离子源温度250 ℃,在全扫描模式下采集数据,质量范围(m/z)50~500,扫描速率12.5 spectr/s。
1.6.4 数据处理与分析
使用ChromaTOF软件(V 4.3x,LECO)对质谱数据进行了分析,使用LECO-Fiehn Rtx5数据库对物质定性,匹配质谱及保留时间指数,将QC样本中检出率50%以下或RSD>30%的峰去除。得到的峰表输入Simca 15.0.2件进行主成分分析(PCA)、正交偏最小二乘法分析(OPLS-DA)。然后进行置换检验对模型有效性做进一步检验,即随机改变变量Y的顺序得到不同的随机Q2值。按照VIP(variable importance projection,VIP)>1,T检验(T-Test)P<0.05的条件进行筛选后,通过检索在线数据库(KEGG、HMDB、PubChem)定性可能的差异性代谢物。
2 结果
2.1 疾病组与健康组的PCA结果
比较样本基本处于95%置信区间,疾病组与健康组主要成分得到了完全的分离,说明两组间代谢物存在显著差异;该模型主成分累计解释率为R2X(cum)=0.473,说明建立的PCA模型可靠。详见图1。
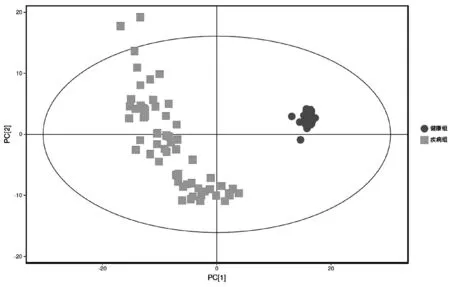
注:R2X=0.473图1 疾病组与健康组的PCA得分散点图
2.2 疾病组与健康组OPLS-DA及对模型的验证比较
疾病组和健康组的血清样品OPLS-DA图中,样本处于95%置信区间,两组样本区分非常显著,R2Y非常接近1,Q2非常接近1,表明当前模型较为真实可靠,可以解释两组之间的差异代谢物。置换检验建立对应的OPLS-DA模型获得随机模型的Q2值均小于原模型的Q2值;置换的Y变量比例增大,表面模型具有良好的稳健性,拟合良好。结果见图2。
2.3 潜在证候标记物
对疾病组和健康组分组贡献较大的重要变量因子VIP值进行提取,保留VIP>1的代谢物进行统计t检验,差异有统计学意义(P<0.05)的代谢物作为差异代谢物。利用KEGG、HMDB、PubChem等相关数据库进行检索,结果对代谢物鉴定和代谢通路分析后找到主要17种差异代谢物与本研究有重要贡献,其升级趋势等相关信息如表1所示,其中牛磺酸、苏氨酸2种在疾病组中呈下降趋势,其余15种呈上升趋势,代谢差异物热图见图3。
3 讨论
慢性阻塞型肺病(COPD)归属“肺胀”范畴,古代众多医家认为COPD的发生多由久病肺虚,痰浊潴留,每因再感外邪诱使病情发作加重,病机以痰为根本。痰浊壅肺为急性加重期最常见证型之一,临床表现上患者咳、痰、喘症明显加重,此阶段患者咳吐痰浊较多。笔者前期基于“痰浊壅肺证”进行了一系列药物疗效观察和药物作用机制研究方面的研究[5],但中医证候缺乏明确统一的客观化、量化指标,对临床证型的统一造成了一定的障碍,也对临床治疗造成一定的困扰。
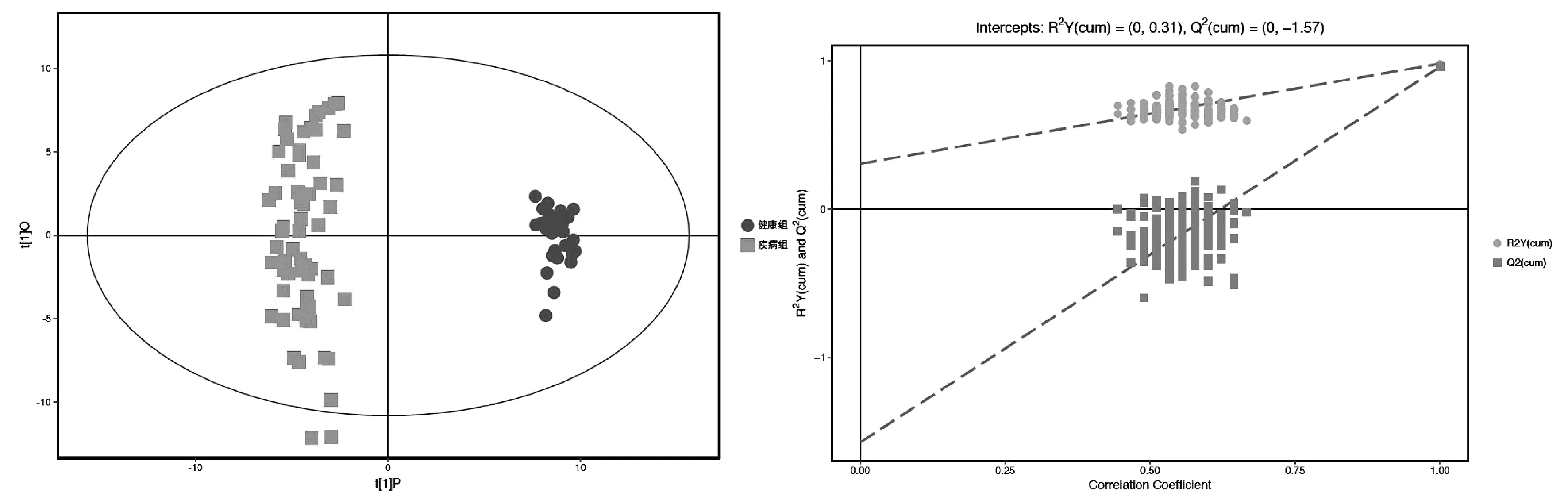
注:R2X=0.15,R2Y=0.98,Q2=0.958;截距:R2=(0,0.31),Q2=(0,-1.57)图2 两组血清样品OPLS-DA得分散点图(左)和置换检验图(右)

图3 两组代谢物的热图
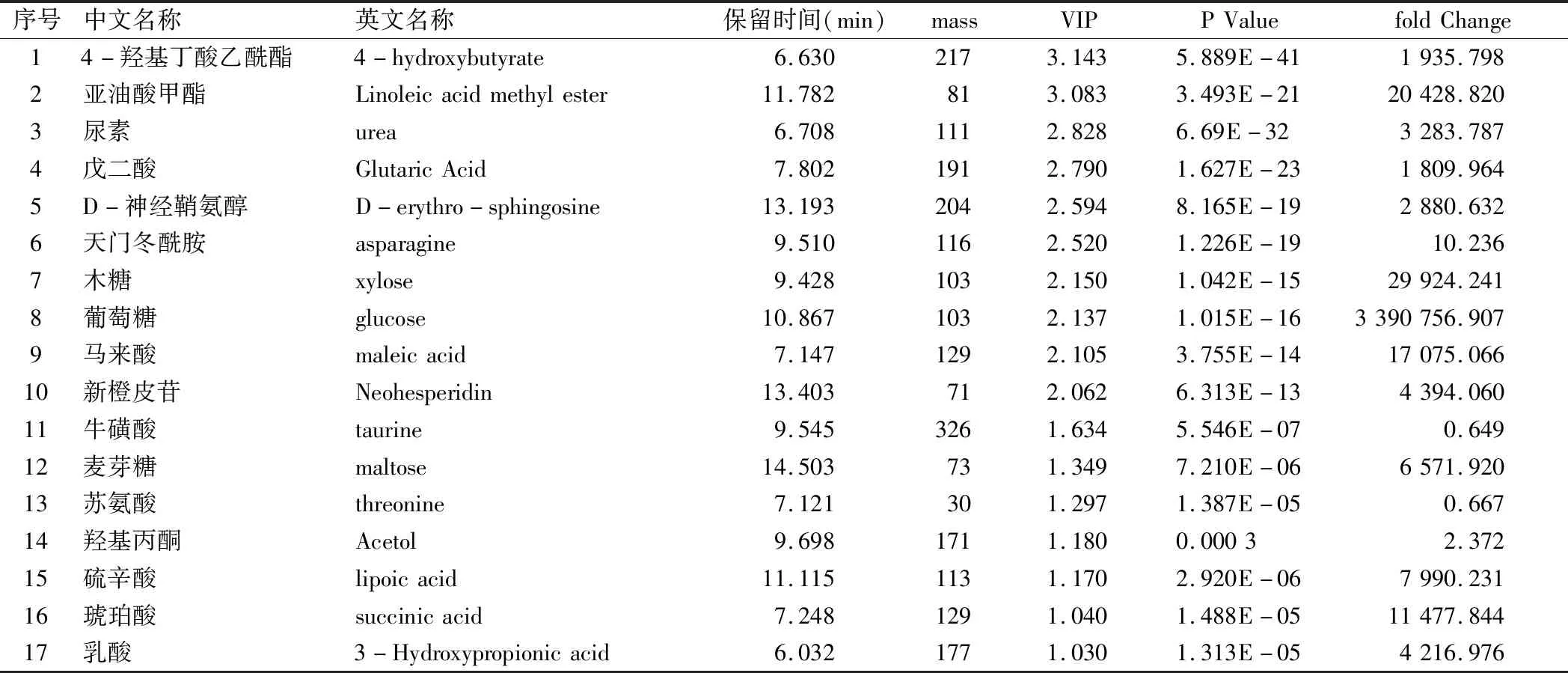
表1 COPD急性加重期痰浊壅肺证潜在有重要贡献的证候标志物及变化趋势
注:mass表示物质特征离子的质荷比,VIP表示OPLS模型中代谢物变量的影响因子,fold Change表示该物质在该组对比两组实验间的倍数关系。
中医证候反映了机体整体某一时刻的外在宏观表现,而代谢组学从整体水平阐明了机体的内在微观变化,更能揭示中医证候的本质。在“精准医学”的时代,众多学者从代谢组学层面研究中医证型实质研究上做出了大量有益的探索,取得了很多研究成果。痰热壅肺型AECOPD主要和能量代谢和蛋白质代谢紊乱有关,患者血清中丙酮酸、3-羟基丁酸、赖氨酸、谷氨酸等明显升高,而缬氨酸、亮氨酸、异亮氨酸等水平明显下降[6]。COPD肺气虚证检测出13种物质存在变化,其中胆酸、羊毛固醇、脂肪酸等下降,2-羟基已二酸、甲羟戊酸、硬脂酰肉碱明显升高[7]。多囊卵巢综合征(PCOS)痰湿证患者和健康人的血清代谢物存在差异,13 种代谢物可能是 PCOS 痰湿证潜在的生物标志物,主要表现为三羧酸循环障碍、糖代谢缓慢、脂肪动员加强[8]。肿瘤患者体内脂肪代谢加强,多种氨基酸下降和脂肪代谢有关的代谢含量增加在痰瘀证肿瘤患者体内比非痰瘀证肿瘤患者严重[9]。中医证候痰证较非痰证患者代谢组学检测结果在糖代谢、脂肪代谢、氨基酸代谢等各方面均存在不同差异,在不同的疾病中亦各有侧重。
基于GC-TOFMS技术对AECOPD痰浊壅肺证患者血浆样本进行代谢组学研究,本研究结果筛选出17种有意义差异代谢物(包括氨基酸、脂肪酸、糖等)。血清中上调代谢物比较有意义的是乳酸、琥珀酸、硫辛酸、新橙皮苷、D-神经鞘氨醇、葡萄糖、亚油酸甲酯、天门冬酰胺、尿素等;下调物质中比较有意义的是牛磺酸、苏氨酸。
目前普遍认为,AECOPD不仅与气道炎症有关,还是一个全身系统性炎症,笔者前期的研究结果已证明AECOPD患者血液中某些炎症因子水平显著升高[5]。炎症反应部位使物质分解加速,加重组织耗氧,同时炎症反应部位微循环障碍影响氧供,引起无氧酵解产生乳酸量增多。同时COPD 病人因长期处于氧供不足的状态,糖酵解亦产生乳酸增多。琥珀酸是TCA中的中间代谢产物,在线粒体生成ATP的过程中起关键作用,亦可作为炎症中的一种物质代谢信号, 促进炎症[10]。硫辛酸属于B族维生素中的一类化合物,在催化α-酮戊二酸氧化脱羧成琥珀酸的反应重起转酰基作用,能增强AECOPD患者抗氧化能力, 减轻氧化应激水平, 降低相关炎症因子水平, 起到抗炎、抗氧化作用, 从而改善肺功能[11]。新橙皮苷在是一种天然的强抗氧化剂,具有抗炎的作用[12]。D-神经鞘氨醇是神经鞘磷脂类成分,是形成生物膜的重要脂类成分。神经鞘氨醇相关物质可结合肿瘤细胞或炎症细胞表面的受体,增强其下游的IL-6表达,增强炎症反应,含量增高可能导致炎症反应风险增大[13]。以上物质水平增高均提示炎症反应增强及其导致机体自身抗炎能力得到发挥。牛磺酸是一种抑制性神经递质,具有抗炎、抗氧化应激、调节胞内钙、调节渗透压以维持细胞膜的稳态[14]。氧化应激与炎症高度相关,AECOPD患者牛磺酸含量降低,可能与 COPD病人氧化应激增强,牛磺酸消耗程度较高相关。
基于代谢组学方面,机体的能量代谢过程是伴随着物质的彻底氧化分解过程。天冬酰胺可以与天冬氨酸相互转化,天冬氨酸是合成延胡索酸(三羧酸循环中间体)的前体物质[15],并可作为底物生成的谷胱甘肽和草酰乙酸,具有抗氧化功能并与琥珀酸参与三羧酸循环,提供能量。机体主要是利用血液提供的葡萄糖供能,葡萄糖、木糖、麦芽糖等葡萄糖代谢物增多及琥珀酸等三羧酸循环代谢中间体的上调表明了COPD急性加重期急性炎症反应和氧化应激使机体能量代谢处于比较旺盛的状态。同时随着炎症反应产生机体能量代谢需求增加,脂肪的代谢增加。D-神经鞘氨醇、亚油酸甲酯、4-羟基丁酸乙酰酯等脂质及分解产物呈现出显著的上调,提示脂肪酸代谢发生紊乱。氨基酸的代谢紊乱主要体现在尿素生成增加及苏氨酸的下调。尿素是蛋白质代谢的主要产物,炎症反应时尿素水平的升高可认为是炎症状态下蛋白质的分解代谢增强所致。苏氨酸是一种必需的氨基酸,参与动物的免疫调节和增强肠道黏膜屏障功能[16]。苏氨酸的含量相对减少, 说明AECOPD患者免疫力相对较低下, 正是COPD患者因为免疫下降才导致病情反复加重。
本研究证明伴随着体内炎症反应,AECOPD痰浊壅肺证患者血清代谢谱发生了特异性变化,能量代谢、脂肪代谢、氨基酸代谢发生了紊乱,鉴定出的差异代谢物及相关代谢通路可以为更深入的研究中医证本质提供参考依据。

