新型冠状病毒肺炎疫情下治疗药物监测实验室气溶胶产生风险及应对*
熊 歆,张现化,李晓娜,赵荣生,杨 丽△
(1.北京大学第三医院药剂科,北京100191;2.北京大学治疗药物监测与临床毒理中心,北京100191)
自2019年12月武汉出现首例新型冠状病毒肺炎(COVID-19)以来,疫情迅速蔓延至全国。截至2020年2月27日9:00,全国(含港、澳、台)累计报告确诊病例78 211例,累计死亡病例2 720例。目前发现,人群对严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)普遍易感。传染源主要是COVID-19患者,包括无症状感染者[1-2]。除呼吸道飞沫传播和密切接触传播外,在相对封闭环境中长时间暴露于气溶胶也有感染可能[1]。医疗机构中从事治疗药物监测(TDM)工作的药学实验室,尤其是本次疫情定点医院的TDM实验室工作中,体液标本前处理、检测分析相关操作步骤可能产生气溶胶,工作人员面临微生物、化学试剂气溶胶的职业暴露风险与个人防护压力,需防范和降低其危害[3]。目前,人们对气溶胶的认识尚待完善,现就气溶胶的定义、分类、产生、操作控制及个人防护等方面进行总结,以期为一线TDM工作人员防控气溶胶危害提供参考。
1 气溶胶的定义及分类
气溶胶是固体微粒或液体小质点分散并悬浮在空气介质中形成的相对稳定的胶体分散体系。气溶胶颗粒的动力学直径为0.001~100 μm,其分类依据成因、物理状态、颗粒大小及来源的不同而不同[4],详见表1。不同粒径气溶胶颗粒传播特点[5]见表2。

表1 气溶胶分类

表2 不同粒径气溶胶的传播特点
TDM实验室样本操作过程中容易产生微生物气溶胶、化学气溶胶,其中微生物气溶胶的危害主要来源于微生物本身的感染力、致病力、毒害力、存活力等[4]。据报道,流感病毒在各种相对湿度范围内的气溶胶中于一定时间内保持稳定,并具有传染性(部分亚型如H1N1为1 h)[6-7],严重急性呼吸综合征(SARS)、中东呼吸综合征(MERS)和埃博拉病毒在患者一定距离(1 m)范围内存在气溶胶传播可能[8-10]。对于SARS-COV-2,目前证实部分患者(尤其是危重症患者)出现病毒血症时,其血液标本具有传染性[11]。对于TDM实验室,实验人员在相对封闭的环境中有暴露于高浓度气溶胶并经气溶胶感染的风险[1]。因此,建议开展TDM检测工作的实验室,将所有确诊和疑似患者标本按照急性传染性疾病防护措施进行管理,以保护工作人员的安全。
2TDM实验室气溶胶的产生途径
TDM实验室样本接收、处理过程中,若操作不慎均可能产生气溶胶。易产生气溶胶的操作包括但不限于以下操作[4,12-13]。
微量移液器吹吸:样本吸取、转移等操作中,使用微量移液器的枪头向外排液时,如力量过大会造成液滴飞溅,可能伴随气溶胶产生。
样本混匀:使用振荡器、涡旋仪及超声清洗仪时,由于剧烈振荡,本身可产生大量气溶胶。若操作不当,容器密封不严或电压不稳等情况,可能发生溶液飞溅、溢洒或混匀时容器内液流紊乱等形成气溶胶。
离心:离心机停止转动后打开机盖易产生气溶胶,会飘散于在地板和台面上,造成室内空气污染,增加室内工作人员的感染风险。
意外:若离心过程中样本管破裂,会造成液体飞溅,在离心管管壁及离心机内产生气溶胶,可能发生感染性污染。
3TDM实验室气溶胶的控制
3.1 实验技术操作的控制
3.1.1 血液样本接收操作
确认样本标识:鉴于SARS-CoV-2传染性强,用于确诊或疑似患者标本转运的转运箱应有统一特殊标识。实验人员接收时需确认转运者和转运箱的特殊标识,没有标识时应拒收标本。
消毒样本外包装:确认装箱前有消毒环节,开箱前用75%乙醇喷雾消毒,取出生物安全罐。在生物安全柜中再取出标本密封袋,用75%乙醇喷雾消毒。打开密封袋后,用75%乙醇消毒,再取出血液标本。
信息记录:该类标本属于高风险标本,应有采集、转运、接收环节的签字,以便回溯。
运送标本转运箱:运送确诊或疑似患者标本的转运箱,需用含1 000 mg/L有效氯的消毒液进行表面擦拭[14]。
3.1.2 离心血液样本操作
1)推荐使用塑料离心管,离心前应检查离心管管盖密闭性,有无破损。
2)离心时,操作者不能离开离心机。
3)离心时若使用套管,应将管内残留物清理干净。离心前可在套管中加入适当的消毒液,这样即便离心管破裂,也可减少感染性气溶胶的产生[15]。
4)若离心过程中有异常声响或警报,停止离心30 min以上,小心开盖,75%乙醇喷雾消毒后处理。
5)离心过程若无意外,停止离心10 min以上,开盖喷雾消毒后进行后续处理。
6)由于离心后离心管内会产生大量的气溶胶,离心管的开盖操作应在生物安全柜中进行,打开离心管盖时动作应轻柔缓慢,并缩短打开管盖的持续时间。
3.1.3 血液样本的灭活操作
血清或血浆样本:离心分离出血清或血浆样本后,在保证待测药物的稳定性不受加热影响的情况下,推荐采用60~65℃加热20~30 min灭活处理。
热不稳定样本:若加热影响检测结果,则未灭活的血液样本应按未经培养的感染性材料处理,可在生物安全二级实验室开展,加三级生物安全防护。3.1.4超声血液样本操作
建议超声过程加盖(因该过程会产生大量气溶胶);超声结束后,样本应静置10 min以上;打开样品瓶盖操作应在生物安全柜中进行,动作应轻柔缓慢。
3.1.5 移液操作
血液样本前处理过程中会涉及多步移液操作,移液器的吹吸过程易产生气溶胶。建议对血液样本进行的所有移液操作均应在生物安全柜中进行;使用移液器移液时,生物安全柜台面上应铺一层浸有消毒液的一次性吸水材料,以免样本滴落台面造成污染;向样本处理管中加入血液样本时,枪头应贴壁缓慢吹出,避免产生气溶胶;不使用移液器吹打混匀血液样本。
3.1.6 混匀血液样本操作
振荡前,应检查样本处理管盖的密闭性、有无破损,确保高速振荡时不会漏液;血样振荡完成后,静置10 min以上;打开样品盖操作在生物安全柜中进行。
3.1.7 意外洒落处理操作
在实验操作过程中,样本发生意外洒落时会产生气溶胶污染,可使用高质量浓度(5 500 mg/L)含氯消毒液的毛巾或纸巾覆盖污染区,消毒30 min以上,并进行实验室通风换气。如果有玻璃,用镊子夹取,置锐器盒中,脱掉污染的外层手套,更换新手套。处理后的污染物也应按照医疗废物的相关规定进行规范处置。
3.1.8 检测后样本处理操作
SARS-CoV-2致病性高、风险高,确诊或疑似患者标本不适宜长期保存。检测剩余血液标本应在生物安全柜中重新加盖管帽,当日高压消毒后再按医疗废物处理。如果实验室没有高压消毒条件,则建议双层包装袋密封后由专人运送到指定地点集中高压消毒后按医疗废物处理。标本及包装袋应有特殊标识,并单独放置。严格按《医疗废物管理条例》《医疗卫生机构医疗废物管理办法》有关规定进行规范处置。
3.2 设备的安全使用
3.2.1 移液器
TDM实验室通常使用的是内置活塞式移液器,液体与活塞间有一段空气隔离,活塞与液体不接触,但在移液过程中,样本与空气接触可能会发生气雾交叉污染,不仅造成样品的交叉污染,还会威胁实验室人员的健康。因此,推荐使用滤芯吸头,可有效屏蔽气溶胶对移液器的潜在污染,保护实验人员健康;对于存在气溶胶污染的移液器,使用完毕用75%乙醇擦拭彻底消毒,可放置于紫外灯下消毒0.5 h;建议移液器专用,不与其他移液器混用,放置生物安全柜中专用。
3.2.2 涡旋振荡仪
使用时可能产生气溶胶,建议所有进行涡流搅拌的样本应放置一段时间后,置生物安全柜内再进行开盖操作;使用完毕后用75%乙醇彻底消毒,小型涡旋振荡仪可放置于紫外灯下消毒0.5 h。
3.2.3 离心机
离心机在高速运转的过程中,周围的空气流动很快,会从离心机周围和下方吸收污染物,并扩散到实验室的空气中形成气溶胶。而离心的患者标本或含有提取液的标本,含有病原微生物、生物分子和前处理过程加入的有机试剂,同样也会产生气溶胶,对实验人员健康造成危害。因此,推荐使用带有防生物污染密封盖的离心机,确保高速运转过程中产生的气溶胶能被安全隔离;且离心机能快速装卸转头,方便把转头和样本整体卸下,搬运至生物安全柜中进行操作;离心机使用完毕后用75%乙醇彻底消毒,如有条件,可置紫外灯下消毒0.5 h。
3.2.4 生物安全柜
生物安全柜是用于提供防护感染性材料溅出或微生物气溶胶的主要装置。建议使用二级生物安全柜,有保护工作人员的定向气流,保护实验材料的垂直层流和保护环境的排气系统,A2,B1,B2型均可[11,16];需年检合格、性能验证通过、运行指标符合规范要求,并执行每日功能监测、清洁消毒等;每次开机时要用烟雾法或丝线检测操作口的气流方向;用75%乙醇擦拭消毒,作用30 min后,紫外线消毒30 min,风机运行5 min后方可开始使用;使用时,最好一次性把需要的物品全部放入,不能在柜内进行剧烈的实验操作,不能在柜内点酒精灯,操作时不能说话、咳嗽等,避免可能引发火灾事故和感染;使用完毕后风机运行5 min,擦拭掉表面可见污物,并用75%乙醇擦拭,再用清水擦拭,然后打开紫外灯消毒0.5 h。
4 工作环境的防护
4.1 分区管理
TDM实验室必须划分出污染区、半污染区(缓冲区)和清洁区,以保护实验人员的安全。对于基于体液标本进行处理、测定分析的TDM实验室,样本接收、保存、前处理及分析检测等工作区域均属于污染区,走廊属于缓冲区,而试剂耗材储存区、办公室、会议室以及文件室等属于清洁区。对于污染区,负压环境最理想[17]。
4.2 医疗垃圾管理
被污染的一次性手套、帽子、一次性口罩、鞋套、一次性隔离衣、接触过标本的医疗废物如移液枪枪头、离心管等需要放入专门的双层医用垃圾袋并标注,实验结束后进行高压消毒[17]。高压消毒后医疗废弃物需用专门的医疗垃圾转运箱及转运车转运,每日对医疗垃圾桶、转运箱及转运车消毒。高压洗消间要设立窗户,安装紫外灯、防虫灯,必要时安装防鼠等设施[17]。
4.3 环境消毒管理
样本接收及制备室实验台面采用含1 000 mg/L有效氯的消毒剂擦拭,地面采用同样的消毒剂进行消毒。实验完毕后,打开窗户及机械通风装置进行通风,以降低气溶胶的残留,或进行空气消毒,如紫外线、空气过滤或空气消毒剂的方式。
在靠近样本前处理的区域设立高压洗消间,配备高压灭菌器或其他清除污染的工具,要有应急喷淋装置。此外,所用的含氯消毒剂要新鲜配制,24 h内使用完毕。紫外灯要符合国家标准[11],定期检测性能、完整记录使用时间,不能超时使用。
5 实验人员的个人防护
5.1 操作人员分级防护
操作人员可根据工作内容的不同进行分级防护[3]。相关要求见表3。
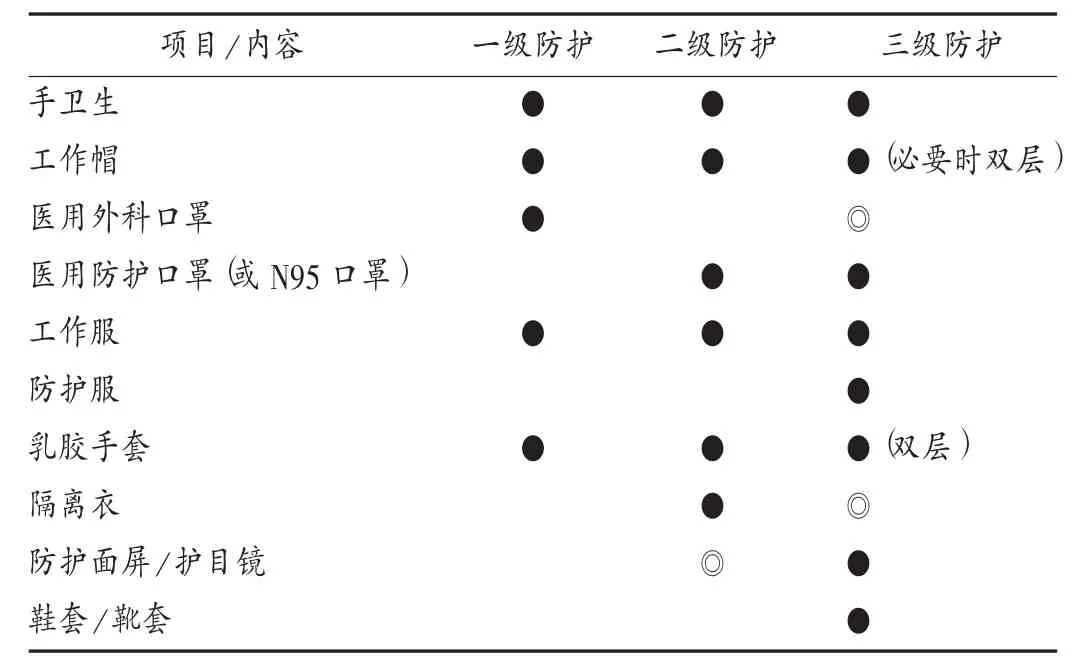
表3 不同级别生物安全防护要求
5.2 人员培训
实验室工作人员必须接受SARS-CoV-2相关微生物学、感染病学、流行病学、感染控制学等方面的培训,掌握相应技术规范、标准操作规程、生物安全防护知识和实际操作技能,经考核合格后方可上岗。此外,从业人员还要接受相关的心理疏导及培训,使工作人员保持良好的精神状态。针对患者隐私保护方面,工作人员也需进行相关的培训及考核,确保不会泄漏患者隐私。
5.3 不同岗位人员防护要求
样本接收人员:确诊或疑似患者样本运送到实验室之前,应进行表面消毒及塑料袋封口、置转运箱的生物安全罐内保存,接收到的样本应保持原塑料包装并单独分开。因此,样本接收人员受到气溶胶的影响较小,在样本接收室操作时可按二级防护要求执行[3]。
样本前处理人员:其可能接触到因离心、取样、涡旋、超声及意外洒落等步骤产生的气溶胶,风险较高,人员必须具备相应的工作资质、岗位认可能力,需接受专业培训并考核合格。工作时按照生物安全三级防护[3]。如需离开样本前处理区域进入其他操作区进行操作,必须在缓冲区进行手卫生防护后摘掉面屏及护目镜,二次手卫生防护后脱掉防护服和外层手套,第3次手卫生防护后脱掉内层手套并直接进行手卫生防护,再更换新手套后方进入其他操作区域,如有化学污染,还须佩戴化学防喷溅眼镜。此外,由于样本前处理可能涉及化学气溶胶污染,因此涉及有机溶剂移取、吹干等过程的,必须在通风橱进行,且打开实验室机械通风系统,以降低对操作人员的伤害。工作人员一定要掌握正确的手卫生时机及方式,工作期间禁止随意触碰皮肤、眼睛、鼻等黏膜相关部位。疫情期间,建议剪短长发,禁止佩戴首饰。
溶液配制及试剂保存人员:不涉及生物污染,但可能受到化学气溶胶的影响,因此需佩戴防喷溅眼镜,根据需要佩戴一次性口罩或防毒口罩、聚酯手套。
上机检测人员:通常仅涉及提取灭活后的样本,生物危险性较低,但仍可能涉及化学气溶胶,因此需佩戴防喷溅眼镜,可根据需要选择佩戴一次性医用口罩或防毒口罩、一次性乳胶手套或聚酯手套等防护用品,在工作站电脑上进行操作前必须脱掉手套并进行正确的手卫生防护。
5.4人员消毒
所有人员一定要掌握正确的手卫生时机及方式,在穿脱防护装备时根据需要随时用速干消毒剂进行手卫生。检测确诊或疑似患者样本时,实验结束后或遇紧急情况时必须正确脱掉相关防护装备且手卫生后,采用实验室的洗眼器进行眼部及鼻部清洗,必要时采用应急喷淋装置进行喷淋。佩戴过的防护面屏及护目镜采用75%乙醇擦拭后置紫外灯下彻底消毒。
6 小结
作为存在暴露风险的人群,TDM相关工作人员每天会接触临床患者的血液或其他样本,应高度重视COVID-19疫情防控和职业暴露保护。对于进行体液标本处理、测定分析的TDM实验室,血液样本前处理步骤中涉及高速离心、开盖、振荡混匀、移液、超声等易产生生物气溶胶的操作时需采取有效措施进行防范。从该类实验室产生气溶胶的途径、操作控制策略、人员防护和消毒等方面进行分析,提出的相应措施和建议,可供此次疫情下TDM实验室工作的安全开展参考。

