咪唑苯脲注射液特殊安全性试验研究
刘欣彤,王玉凤,陈孝杰,刘义明,徐 飞,王宏磊,张志博,张向阳,李 存,李秀波*
(1.中国农业科学院饲料研究所,国家饲料药物基准实验室,北京 100081;2.天津农学院动物科学与动物医学学院,天津 300384)
咪唑苯脲注射液(imidocarb,IM)又称双脒苯脲或咪多卡,是一种动物专用二苯基脲衍生物类新型抗原虫的化学药物[1]。该药是由Schmidt应用鼠骆巴贝西虫筛选均二苯脲类化合物时发现的,由Beveridge研究证实该药的半数致死量低于其他抗巴贝西虫药物,已上市产品由瑞士Monbijoustrasse公司研发[2]。我国在1985年首次成功合成了咪唑苯脲的二丙酸盐和双盐酸盐形式。由于双盐酸盐对局部组织具有较强刺激性,临床上一般常用二丙酸盐做成制剂[3],通过肌肉或皮下注射的方式给药[4]。在抗犬[5]、牛[6]、羊[7]、羔羊[8]、马[9]巴贝西虫病方面具有良好的治疗和预防效果,也可用于抗牛泰勒虫病[10]、抗牛边虫病[11]、抗小鼠利什曼病[12]、抗犬埃立克体病[13]、抗羊/猪附红细胞体病[14-15]、抗梨形虫病[16]、抗锥虫病[17]等[18]。注射后迅速吸收并分布于全身组织,1 h后即可达到血药峰浓度,在肾脏中浓缩并以原型再吸收,在肝脏中解毒。本品毒副作用较小,但静脉注射毒性大,且内服无效[19]。作为兽用专用药,咪唑苯脲具有用量小、药效持久、疗程短、刺激小、耐药性低、使用方便等特点。该药已广泛应用于世界各地,是当今国际公认的最佳抗原虫药[20]。鉴于国内当前没有咪唑苯脲注射液临床使用有关全部特殊安全性方面的资料,且我国已批准进口该药,根据农业部公告要求,在国内生产此产品,须进行特殊安全性试验。因此,本研究通过豚鼠、新西兰大白兔的皮肤致敏、皮肤刺激、肌肉刺激、红细胞溶血试验,全面考察咪唑苯脲注射液的特殊安全性,为其临床用药提供参考。
1 材料与方法
1.1 受试药物 咪唑苯脲注射液,1211.5 mg/mL,由齐鲁动物保健品有限公司提供,批号:1503003。阳性对照药物:1-氯-2,4-二硝基苯(含量99%),购自北京百灵威科技有限公司。
1.2 试验动物 新西兰大白兔(体重2.5~3 kg) 16只,雌雄各半,单笼、常规饲料喂养,自由饮水,由北京市海淀兴隆实验动物养殖厂提供,动物质量合格证编号为:SLB112018122420091788和SLB112018122420091780;豚鼠系Hartley种白化豚鼠26只(一级,体重260~320 g),雌雄各半,常规饲料喂养,自由饮水,由北京市海淀兴旺动物养殖场提供,动物生产许可证编号:SCXK(京)2016-0003。
1.3 试验方法及判定原则
1.3.1 皮肤刺激试验 采用新西兰大白兔进行,分组及剂量见表1。取咪唑苯脲注射剂,直接涂布于左侧已去毛的皮肤上,然后用二层纱布(2.5 cm×2.5 cm) 和一层无刺激塑料膜覆盖,再用无刺激胶布固定,家兔的右侧去毛皮肤涂布赋形剂(生理盐水) 作对照。贴敷4 h后,除去受试物并用温水清洁给药部位。每天一次,连续7 d,每次给药时间相同。每次去除药物后1 h以及再次贴敷前观察去毛部位皮肤是否有红斑、水肿及其他异常表现,并在末次给药后1、24、48、72 h肉眼观察去毛部位皮肤局部反应,按照《药物刺激性、过敏性和溶血性研究技术指导原则》[21](以下简称《原则》)进行刺激反应评分。按表2判定受试动物评分积分的平均值进行综合评价,最高积分均值<0.50,无刺激性;0.50~2.99,轻度刺激性;3.00~5.99,中度刺激性;6.00~8.0,强刺激性。
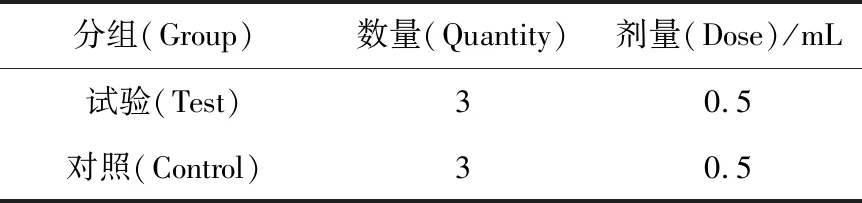
表1 皮肤刺激试验分组、剂量
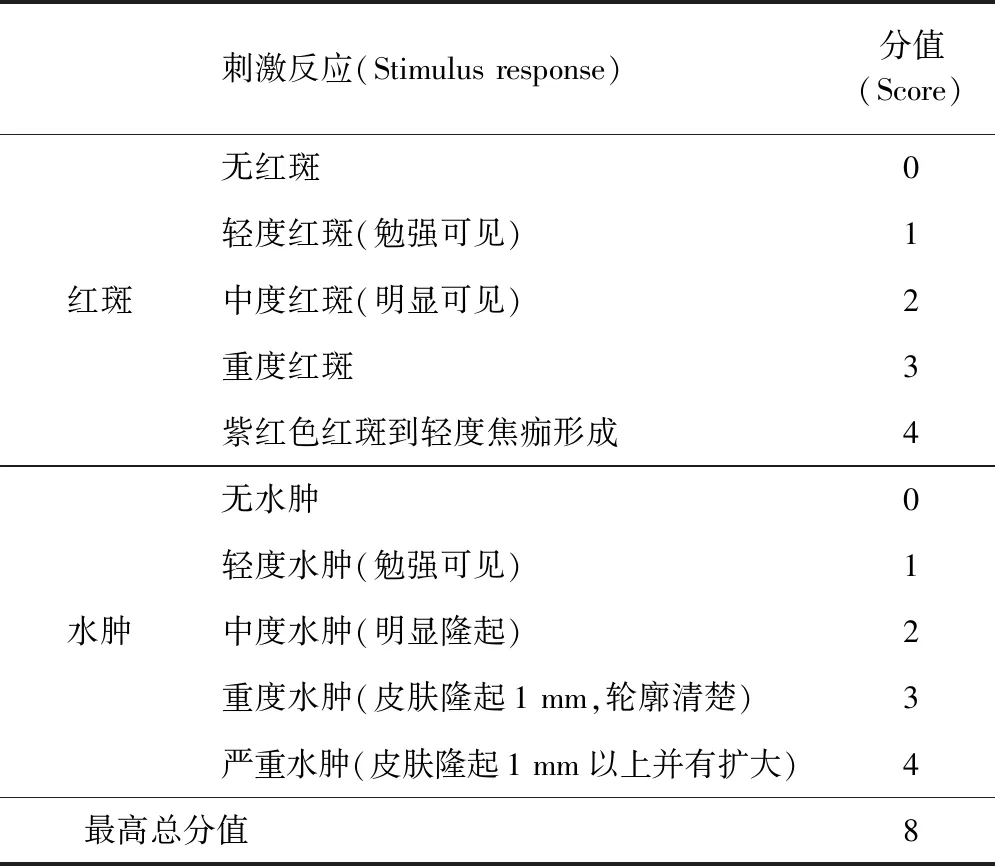
表2 皮肤刺激反应评分标准
1.3.2 皮肤致敏试验 采用白化豚鼠进行,分组及剂量见表3,以豚鼠背部左侧皮肤进行染毒。先进行诱导接触,分别在试验0、7、14 d 时,在试验组豚鼠左侧备皮处涂敷咪唑苯脲注射液,在阳性对照组动物相同部位涂敷2,4-二硝基氯苯。末次诱导后14 d进行激发接触,实验组和阴性对照组涂敷咪唑苯脲注射液,阳性对照组动物涂敷2,4-二硝基氯苯。激发接触实验染毒后24、48、72 h,根据表4和表5评判是否出现皮肤致敏反应并判定致敏强度。

表3 皮肤致敏试验分组、剂量

表4 皮肤过敏反应程度的评分标准
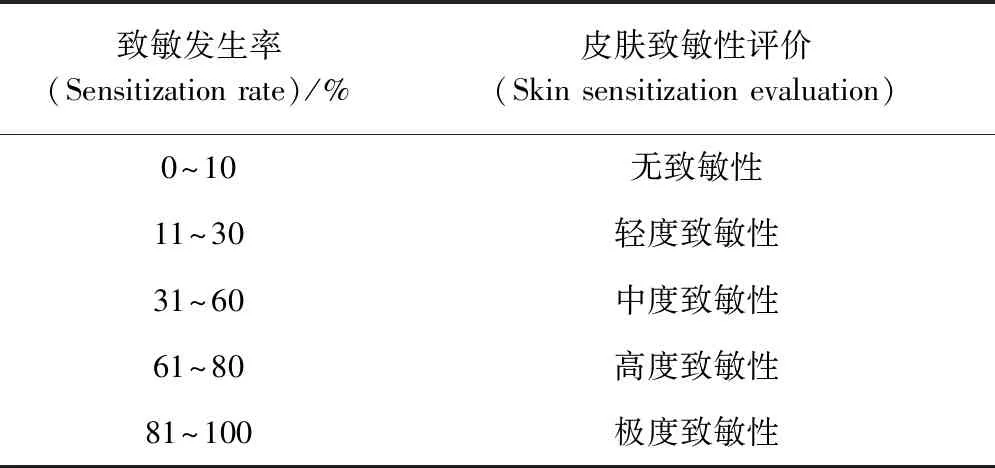
表5 皮肤致敏性评价标准
1.3.3 肌肉刺激试验 采用新西兰大白兔进行,分组及剂量见表6。试验前24 h剪去两侧股四头肌部位的兔毛,碘酊和乙醇消毒后分别在右侧股四头肌注入受试药物(对照组注入0.9%氯化钠溶液),左侧股四头肌注入同样体积的灭菌0.9%氯化钠溶液作为右侧的对照。给予受试物后4、12、24、48 h观察皮肤表面的反应及变化情况。观察48 h后将家兔处死,剖开股四头肌,肉眼观察注射部位肌肉组织的药液吸收情况,检查注射局部是否产生刺激性反应;并将高、中、低剂量组和对照组各2只(雌雄各1只) 注射部位肌肉标本用10%中性福尔马林固定液浸泡固定,做组织切片进行病理学检验。根据《原则》进行刺激反应评分。根据表7计算肌肉刺激性总反应级,计算平均值,按表8判定刺激等级。若各股四头肌反应级的最高与最低之差大于2,应另取动物重新试验。

表6 肌肉刺激试验分组和剂量

表7 肌肉刺激反应分级标准
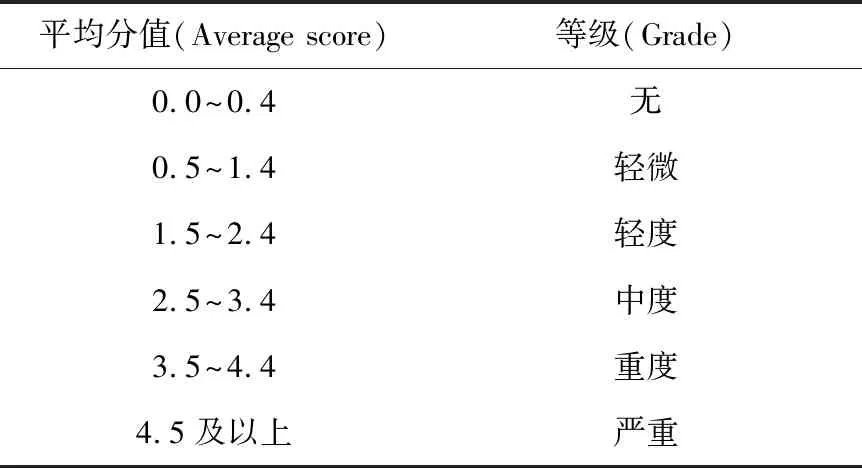
表8 平均分值和等级
1.3.4 溶血试验 试验动物为新西兰大白兔2只,采用体外试管法,即肉眼观察法进行,分组及剂量见表9。采心脏血50 mL,制成脱纤血液,处理后置37 ± 0.5 ℃的恒温箱中进行温育。15 min、1 h、2 h、3 h各观察1次,若试验中的溶液呈澄明红色,管底无细胞残留或有少量红细胞残留,表明有溶血发生;如红细胞全部下沉,上清液体无色澄明,表明无溶血发生。若溶液中有棕红色或红棕色絮状沉淀,振摇后不分散,表明有红细胞凝聚发生。如有红细胞凝聚的现象,进一步判定是真凝聚还是假凝聚。

表9 红细胞溶血试验分组、剂量
2 结果与分析
2.1 皮肤刺激试验 6只受试新西兰大白兔连续给药7 d期间,在其去毛部位均未观察到皮肤红斑、水肿及其他异常表现,且在停药后观察期限内的各个时间点均未出现红斑和水肿等刺激反应,见图1;根据《原则》判定受试物咪唑苯脲注射液各个时间点的刺激反应积分均值为0,与阴性对照组比较无显著差异,详见表10,表明受试物咪唑苯脲注射液对新西兰大白兔无皮肤刺激性。

图1 新西兰大白兔皮肤刺激结果
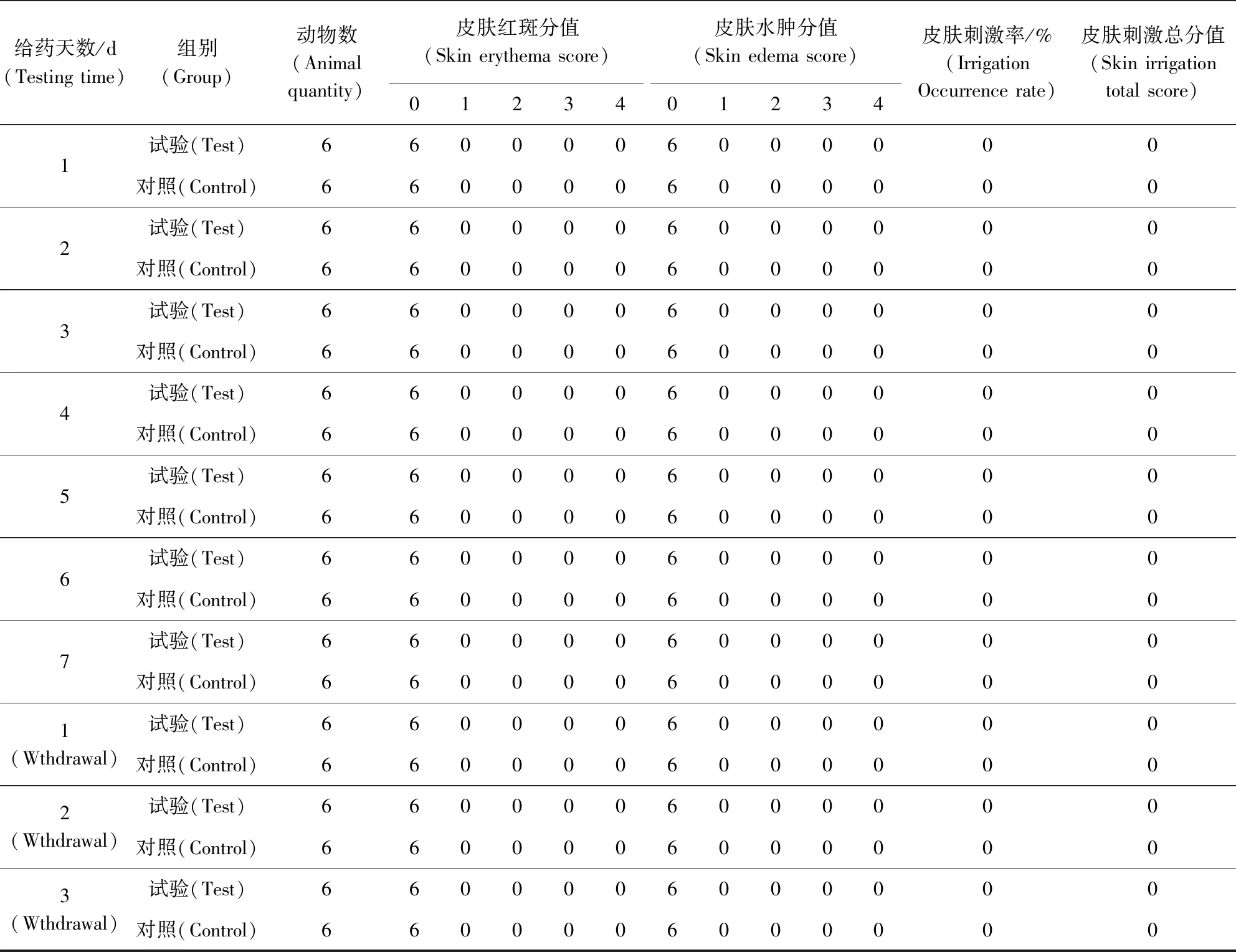
表10 皮肤刺激分值
2.2 皮肤致敏试验 受试药物组和阴性对照组豚鼠的皮肤在激发给药24、48、72 h 后,皮肤均未见红斑和水肿现象(图2);根据《原则》判定受试药物组和阴性对照过敏反应率为0,而阳性对照组豚鼠均出现严重或中度红斑和水肿,过敏反应发生率为100%(表11)表明受试药物咪唑苯脲注射液对豚鼠皮肤进行诱导后不出现过敏反应,试验结果为阴性。

图2 豚鼠给药后 72 h 皮肤致敏结果

表11 皮肤致敏率
2.3 肌肉刺激试验 给予受试物后4、12、24、48 h均未观察到注射部位充血、瘙痒、起包。给予受试物后48 h 处死各剂量组和对照组各2只(雌雄各1只) 家兔,病理显示其组织注射部位血管未见出血、血栓、血管扩张充血、间质炎细胞浸润及血管壁周围组织坏死等异常改变,详见图3。判定各个时间点的刺激反应分值均为0,与阴性对照组比较无显著差异,详见表12,由此表明受试物咪唑苯脲注射液对新西兰大白兔无皮肤刺激性。
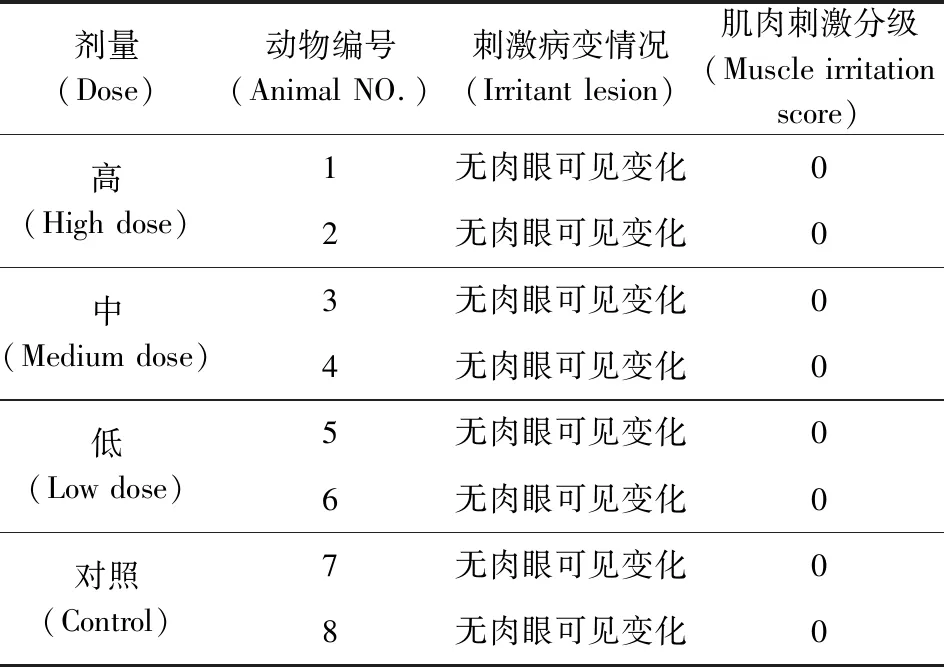
表12 刺激性反应分值
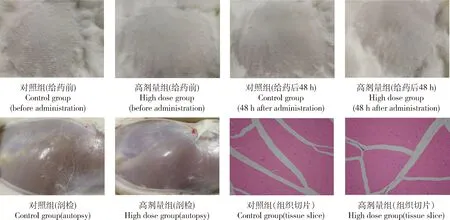
图3 新西兰大白兔给药后48 h 皮肤致敏及病理结果
2.4 溶血试验 图4结果显示,1~6号试管在3 h内红细胞全部下沉,上清液体均为澄明,溶液中未见有棕红色或红棕色絮状沉淀;7号试管中的溶液呈澄明红色,管底无细胞残留或有少量红细胞残留。结果可判定受试药物及阴性对照未发生溶血和凝聚,阳性对照组发生溶血,表明咪唑苯脲注射液对兔红细胞无溶血和凝聚作用,可以注射使用。

图4 新西兰大白兔红细胞溶血性结果
3 讨论与结论
药物特殊安全性试验是注射剂临床前安全性评价的重要组成部分,主要由体外溶血性试验、过敏性试验、局部刺激性试验等组成。任何一项试验结果出现阳性,则表明该药安全性评价不符合标准,不宜通过注射途径给药[21]。药物刺激性是指药物制剂经非口服途径给药,对用药局部产生刺激性。通过药物在给药部位使用后是否引起局部或全身毒性,以揭示临床应用时可能出现的毒性反应、安全范围等指标,并为临床提供参考[22]。
咪唑苯脲注射液涂敷部位的皮肤刺激试验,给药剂量为0.5 mL。试验中同时进行了生理盐水的阴性对照试验。结果表明,受试兔在给药后的1 h内和每次去除药物后1 h以及再次贴敷前去毛部位皮肤均未出现异常表现;在试验的第7天及停药后3天内受试兔外观及病理观察均正常。由此可见,咪唑苯脲注射液经皮肤涂敷连续给药7天及停药后对受试兔是安全的。
咪唑苯脲注射液注射部位的肌肉刺激试验,给药剂量为0.1 mL/kg,约为临床正常剂量(1倍剂量)。试验中同时进行了2倍剂量组、5倍剂量组和0.9%氯化钠溶液的对照组试验。结果表明,每组受试兔的刺激反应分值均为0,与阴性对照组比较无显著差异;剖检股四头肌,肉眼观察注射部位肌肉组织的药液吸收良好,注射局部未产生刺激性反应;病理组织注射部位肌肉切片的血管未见异常改变,病理学检验正常。由此可见,咪唑苯脲注射液以5倍剂量经肌肉注射对受试兔是安全的。
随着上市新药的增多,尤其是注射途径药物的广泛应用,药物致敏反应的发生率大大提高[21]。因此,临床前致敏反应评价非常关键。皮肤致敏是将具有致敏作用的化学物质经一定途径进入机体,与组织蛋白结合形成完全抗体,刺激免疫活性细胞产生致敏淋巴细胞或体液抗体;经1~2周致敏期,使体内免疫反应得到充分发展,形成一定数量的致敏淋巴细胞或特异抗体;当再次接触(激发)时使机体对该化学物质产生感受性增高的状态,以一定的异常形式表现出来的反应。
咪唑苯脲注射液涂抹部位的皮肤致敏试验,给药剂量为0.5 mL/kg。试验中同时进行了涂抹0.2 mL 2,4-二硝基氯苯的阳性对照和末次诱导后14 d再涂敷咪唑苯脲注射液的阴性对照。结果表明,激发接触实验染毒后受试药物组和阴性对照组受试豚鼠,无肉眼可见的病理变化,受试物咪唑苯脲注射液无过敏反应;阳性对照组豚鼠均出现过敏反应。由此可见,咪唑苯脲注射液以0.5 mL/kg的剂量经皮肤涂敷给药对受试豚鼠是安全的。
药物制剂引起体内溶血可分为免疫性溶血和非免疫性溶血两类,都通过药物引发溶血反应。因此,凡是注射液和可能引起溶血反应的其他药物制剂均应进行溶血性试验。
本研究对咪唑苯脲注射液进行了溶血性试验,结果表明咪唑苯脲注射液对受试兔红细胞无溶血和凝聚现象,可供临床注射使用。
近年来,动物原虫病的发病率逐年上升,部分病已呈局部流行的趋势。因此,在畜牧养殖过程中,抗原虫药对于动物原虫病的预防及治疗尤为重要。抗原虫药主要包括抗球虫药、抗锥虫药、抗梨形虫药、抗滴虫药四大类。抗球虫药主要分为三类。三嗪类的地克珠利和妥曲珠利,缺点为半衰期短且易产生耐药性[23]。二硝基类的二硝托胺为产蛋期禁用的药物;尼卡巴嗪的副作用较大,在体内蓄积时间长,因此在长休药期期间可复发其他疾病,甚至造成死亡[24]。磺胺类药物不适用于肾脏有疾病的畜禽,且不可长期连用;磺胺氯吡嗪的毒性较大,抗虫谱较窄[24]。锥虫病的主要传播体是自然界的蜱虫,喹嘧胺作为抗锥虫药物在家禽中应用较少[24]。巴贝西虫病经蜱传播,治疗药物有黄色素、贝尼尔、硫酸喹啉脲和咪唑苯脲。病牛服用黄色素后对光较敏感,强光照射易灼伤[25];贝尼尔的副反应较大[26];使用硫酸喹啉脲需特别注意妊娠奶牛可能发生流产。滴虫为单细胞原虫,火鸡、鸽子、犊牛均可感染滴虫病。抗滴虫的药物甲硝唑,在一些国家只允许用作治疗药物,不允许用作添加剂长期使用[27]。
1986年,Vos A J D的研究结果表明,咪唑苯脲作为一种有效预防牛巴贝斯虫感染的药物,对牛痘苗的传染性有明显的抑制作用,是一种有效的牛分枝杆菌化疗药物[28]。2019年,Ehimiyein A M的研究结果表明,犬巴贝斯虫引起的行为和临床血液学损伤的实验感染,如口干、眼内有分泌物、脾肿大、贫血和血小板减少症,在联合应用咪唑苯脲和丙氨酸丙咪唑的情况下得到了最佳的改善,是治疗犬巴贝斯虫病的有效药物[29]。但国内外当前没有关于咪唑苯脲注射液临床使用有关全部特殊安全性研究报告。
本研究通过豚鼠和新西兰大白兔进行的皮肤致敏、皮肤刺激、肌肉刺激、红细胞溶血试验结果表明,咪唑苯脲注射剂无皮肤刺激性、不出现过敏反应(致敏率为0)、无肌肉刺激性、无溶血和凝聚作用,未对受试动物产生明显的不良影响,受试动物未见异常行为,临床上可以肌肉注射使用,具有良好的应用前景。

