氧化铝负载高锰酸钾氧化甲醛的实验研究
文 力 蒋 昊 牛立科 王丽娟
氧化铝负载高锰酸钾氧化甲醛的实验研究
文 力1蒋 昊1牛立科2王丽娟1
(1.西安工程大学城市规划与市政工程学院 西安 710048;2.烟台宝源净化有限公司 烟台 264003)
采用蜂窝板式反应器与管状式反应器考察了氧化铝负载高锰酸钾(简写PM球)在模拟空间内氧化气态甲醛的效果,研究PM球降解甲醛的动力学规律。结果表明:PM球对甲醛的氧化反应过程符合一级反应动力学方程;当风量相同且PM球用量在1.25kg以上时,管状式反应器结构有利于氧化反应的进行。经处理后,模拟空间中的甲醛含量最快30min可以降至国家标准(0.1mg/m3)以下。通过分析可知反应器的净化效果除了取决于氧化剂之外还与风机的风压有关。
氧化铝;高锰酸钾;降解;甲醛;反应器;反应动力学;风压
0 引言
调查显示,现代人的一生中有80~90%的时间是在建筑中度过的[1]。近年来伴随着建筑装修热潮,我国室内空气环境品质(Indoor Air Quality,IAQ)急剧恶化,其中一个重要原因就是装修材料中会释放出来甲醛、苯系化合物等有机物[2]。人若长期处于挥发性有机化合物(Volatile Organic Compounds,VOCs)超标的室内环境将会出现以下3种病症:病态建筑综合症(Sick Building Syndrome,SBS)、与建筑有关的疾病(Building Related Illness,BRI)以及多种化学污染物过敏症(Multiple Chemical Sensitivity,MCS)[3-5]。
锰系化合物易获取,其强氧化性可以高效氧化甲醛[6],因而被国内外学者广泛研究。近年来也常被用于去除水中的微量有机物及某些重金属[7,8]。其中,高锰酸钾(Potassium Permanganate,PM)的使用pH范围较广、稳定性较强[9,10]。有学者研究发现不同基体材料经高锰酸钾改性后,甲醛穿透时间均有不同程度的延长,提高了材料本身吸附降解甲醛的能力[11]。此外,还有相关学者研究发现MnO2对甲醛亦有一定的催化降解作用[12],其对甲醛降解的性能高低与MnO2的晶型有关[13-16],在室内VOCs的降解方面具有较大的潜力[17,18]。
现阶段研究人员更关注于高锰酸钾去除水中污染物,而对用其去除室内气态污染物的效果以及动力学规律的研究偏少。本文主要从氧化气态甲醛出发,对在不同反应器中氧化铝负载高锰酸钾氧化甲醛的能力进行实验与反应动力学研究;同时将高锰酸钾技术与其他技术相结合,研究分析其降解甲醛的效果。
1 实验
1.1 高锰酸钾氧化原理
由于高锰酸钾具有强氧化性,在中性下可与室内气态甲醛发生化学反应,理论上可以生成CO2、H2O以及MnO2,因此选用高锰酸钾作为氧化剂理论上具备长期去除甲醛的功能。反应方程式如 下[11]:
8KMnO4+12HCHO=7MnO2+8HCO2K+
Mn(HCO2)4+6H2O (1)
3HCHO+4KMnO4=4MnO2+3CO2+4KOH+H2O (2)
在反应初期,高锰酸钾处在中性环境中,按照式(1)发生反应,Mn7+只能还原到Mn4+。由于MnO4-/MnO2的反应电位势为0.588V[19]并不能将甲醛完全氧化成二氧化碳和水。随着反应的进行,虽然化学平衡会逐渐向弱碱性方向改变,但KMnO4在弱碱性环境中的氧化能力仍然较弱,因此也只能被还原成MnO2。只有当氢氧化钠浓度大于2mol/L时,高锰酸钾才能还被原成MnO42-[20]。实际中由于高锰酸钾过量,有相当一部分的甲醛会按照式(2)发生反应被氧化成CO2和H2O。
在实验初期,实验用载体选择有活性炭、分子筛、活性氧化铝、炭毡以及膨胀珍珠岩等材料,经测试发现载体选用活性氧化铝时对甲醛的降解效果最显著;且由于活性氧化铝(Al2O3)颗粒具有较大比表面积、化学性质稳定以及吸水性较好等特性,因此经常作为脱水吸附剂和色谱吸附剂使用,更重要的是可作为氧化剂和氧化剂载体[21]。为实现快速且长期去除甲醛的效果,本文以活性氧化铝颗粒为基材、高锰酸钾为氧化剂,将高锰酸钾负载于活性氧化铝颗粒进行改性测试与分析研究,在有一定物理吸附性能的前提下,实现对甲醛的最大去除率。
1.2 材料与仪器
高锰酸钾晶体(天津科密欧化学试剂有限公司,分析纯AR,KMnO4含量≥99.5%),甲醛(天津科密欧化学试剂有限公司,分析纯AR),活性氧化铝(烟台宝源净化有限公司,粒径3~5mm,堆积密度≥0.63g/cm3,Al2O3含量≥92%),ES02B电化学式甲醛检测仪(深圳市普利通电子科技有限公司)。
1.3 氧化剂的合成与制备
由前文可知,氧化剂选择高锰酸钾,为保证实验用载体较大的比表面积,因而实验用载体选择粒径为3~5mm的活性氧化铝。之后用去离子水配置0.4mol/L的高锰酸钾溶液,然后将一定量洗净并烘干的活性氧化铝浸泡于上述溶液一定时间,最后取出并烘干即可制得高锰酸钾氧化铝颗粒,简写为PM球。
1.4 高锰酸钾空气净化设备降解VOCs的实验设计
本节主要研究目前市场上常见反应器结构对氧化效果的影响,以期提供一种能较快去除甲醛、且对氧化剂用量敏感的反应器结构,同时研究高锰酸钾降解甲醛的动力学规律,给出反应器中PM球的合理用量,以便在实际应用中最大限度地发挥氧化剂的性能与反应器的优势。
1.4.1 反应器结构
借鉴目前市场上常见反应器与滤芯结构,设计了两款反应器进行测试,反应器的结构原理如图1与图2所示。
蜂窝板式反应器的填料装填部分类似于蜂窝型,其两侧均由无纺布粘结,空气先通过一侧无纺布,再通过氧化剂完成氧化反应,最后通过另一侧无纺布送入室内。
管状式反应器的截面则类似于圆环,可以提供比蜂窝板式反应器更大的氧化剂反应接触面积,空气在进入内部圆环后,由于右端截面被封闭无法流通,故向四周挤压,先经过内壁,再通过氧化剂发生反应,最后通过外壁送入室内。
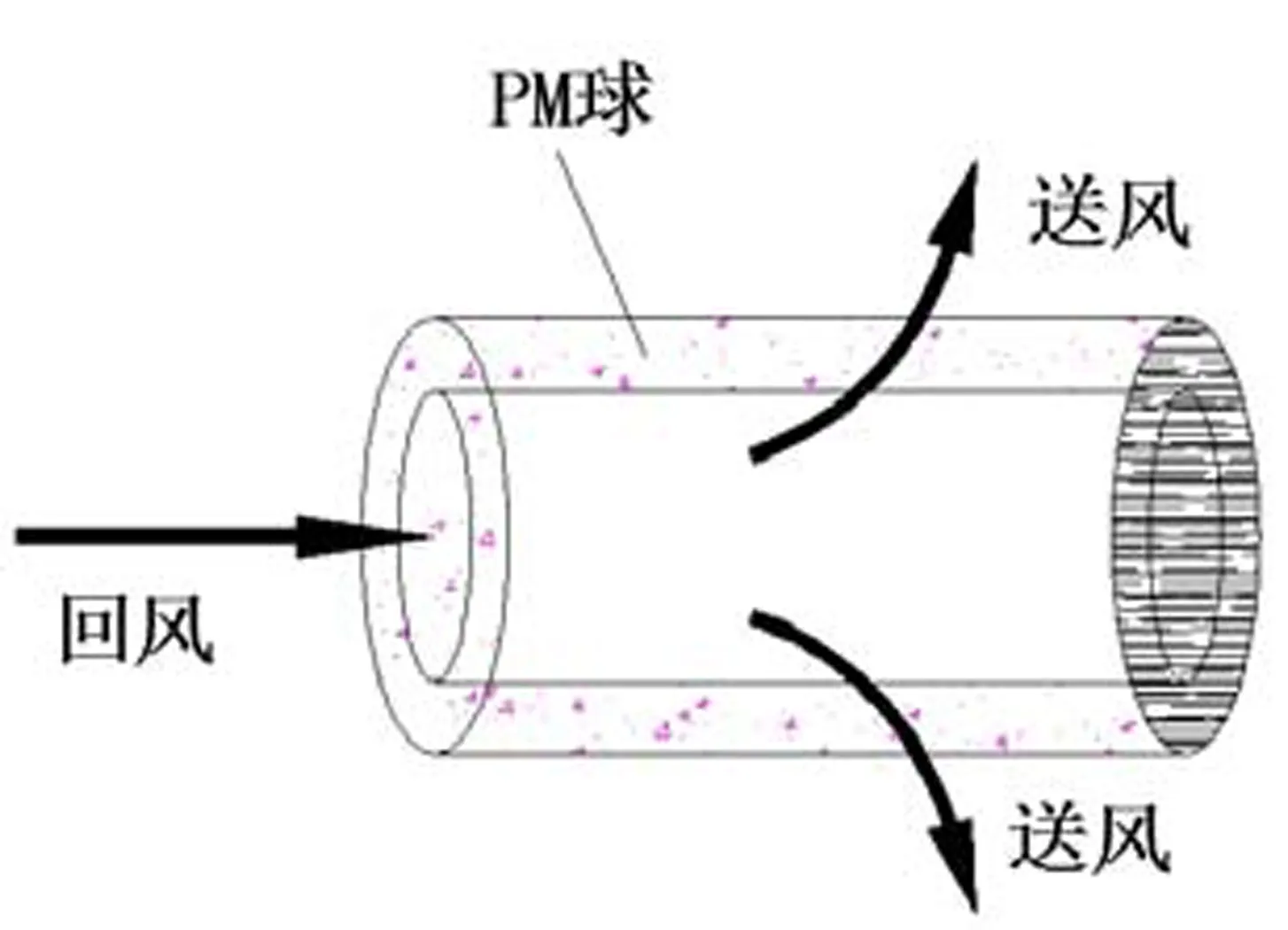
图2 管状式反应器
1.4.2 实验系统设计
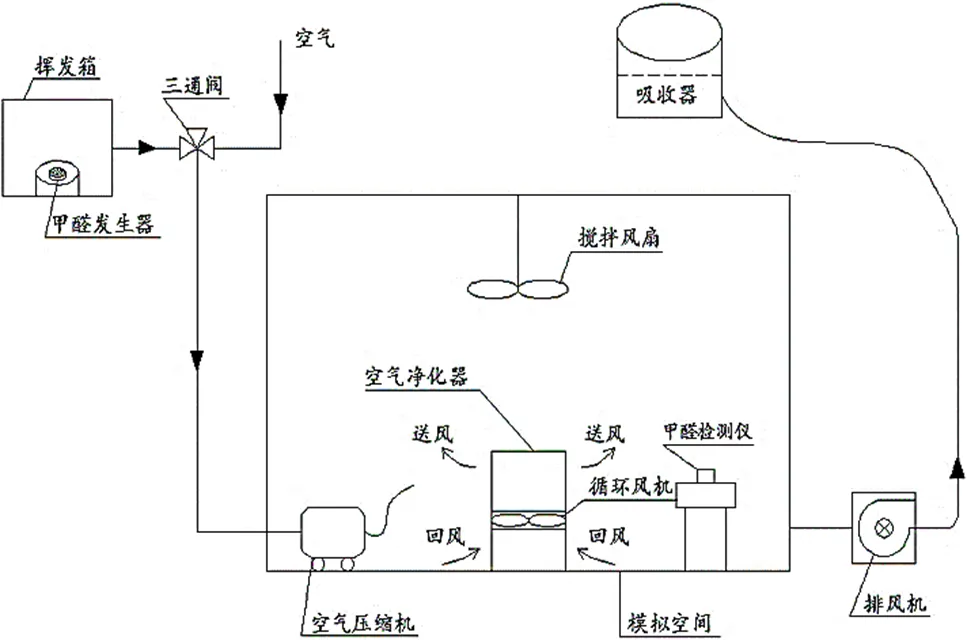
图3 模拟空间示意图
本文在模拟空间内利用上述两种反应器测试PM球对甲醛的降解效果,模拟空间由环氧树脂自流平地面、一面玻璃壁面、顶棚以及三面乳胶漆墙面构成,示意图如图3所示,尺寸3m×5m×2.8m。甲醛通过设置在房间内的电化学传感器实时监测房间内的浓度变化,并每隔5min记录一次数据。为保持氧化剂测试过程的可对比性,模拟空间中甲醛的初始浓度控制在1.0±0.2mg/m3,且风量采用风机功率进行限制,均设定为300m3/h。
2 结果与分析
2.1 仅放入PM球的蜂窝板式反应器测试结果与分析
选用蜂窝板式反应器分别测试3种PM球用量下对甲醛的降解率,其中甲醛的初始浓度控制在1.0±0.2mg/m3,且风机风量设定为300m3/h。得出对于蜂窝板式反应器而言,在300m3/h时500g PM球为最佳用量。
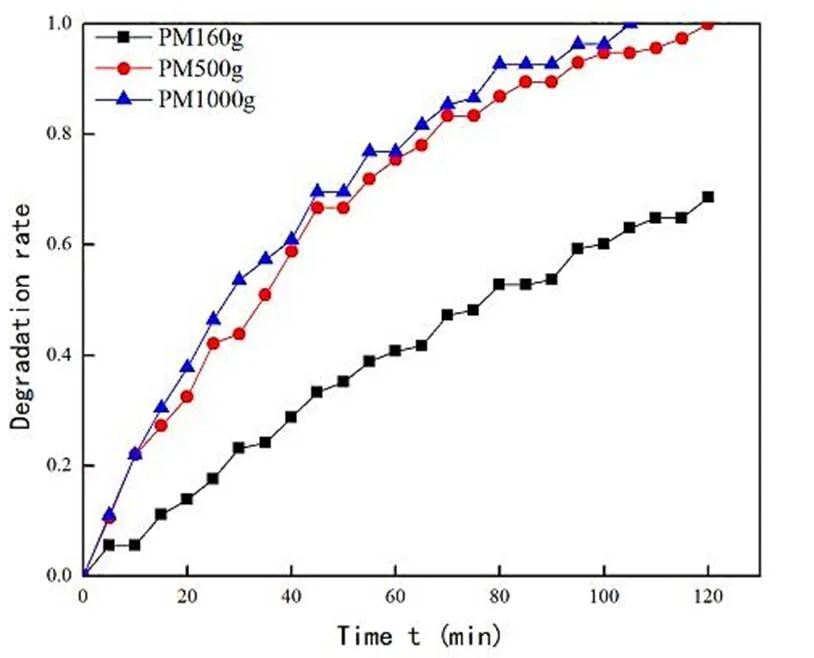
图4 蜂窝板式反应器中不同PM球用量对甲醛降解率的影响
由图4可知,PM球用量为160g时经过120min反应仍未降至国标(0.1mg/m3),500g、1000g条件下甲醛浓度降至国标所需时长分别为95min以及80min。在相同时间内PM球用量为500g时的净化效果比160g有明显的提升,降解速度快30%左右;但是当用量达到1kg时仅比500g的降解速度快5%,降解率基本没有提升。由此可以得出此时制约氧化效果的因素不再是氧化剂的用量,而是氧化剂的阻力。考虑到空气净化器中其余模块的阻力,对于蜂窝板式反应器而言,在300m3/h时500g PM球为最佳用量。
2.2 仅放入PM球的管状式反应器测试结果与分析
根据蜂窝板式反应器的最佳用量,选用管状式反应器首先测试PM球用量在500g时对甲醛的降解率;由于受到容积的限制,管状式反应器的最大装填量为5kg,故之后分别测试PM球用量为1.25kg、2.5kg与5kg时对甲醛的降解率,其中甲醛的初始浓度控制在1.0±0.2mg/m³,且风机风量设定为300m3/h。得出管状式反应器对氧化剂的用量十分敏感,在300m3/h时5kg PM球的降解速度最快,为管状式的最佳用量。

图5 管状式反应器中不同PM球用量对甲醛降解率的影响
由图4和图5以及测试对比发现PM球用量在500g时管状式反应器比蜂窝板式反应器的降解速度快5%左右,甲醛浓度降至国标(0.1mg/m3)所需时长分别为85min与95min,因而后续测试的反应器结构均选用管状式反应器。
由图5可知,在相同时间内当PM球用量为5kg时降解速度最快,比2.5kg与1.25kg的用量分别快15%与25%左右,其中甲醛浓度降至国标(0.1mg/m3)所需时长分别为30min、55min以及70min。同时测试发现管状式反应器对氧化剂的用量十分敏感,在此次测试条件下5kg PM球为管状式的最佳用量。
2.3 夹活性炭HEPA(ACF)+光触媒(PCO)+PM球的净化器测试数据与研究分析
由上述两类实验可知,采用管状式反应器填充PM球可以有效增大其反应面积,通过降低氧化剂表面的风速来达到降低阻力的作用,故改装空气净化器,将夹活性炭HEPA滤网、光触媒以及PM球组合成管状式反应器来测试其降解效率。改装后PM球的填充量为430g。此时净化器的风量为300m3/h。
由图6可知,采用ACF+PCO技术时降解速度比ACF+PCO+PM球技术快15%左右,仅需60min就可将甲醛浓度降至国标。
从技术层面分析,理论上采用ACF+PCO+ PM球的组合技术会比采用ACF+PCO时的反应速度更快,但实际测试结果相反,原因在于ACF+PCO+PM球的阻力大于ACF+PCO的阻力,超过了风机提供的风压,以至于降低了气流通过净化材料的风速,从而影响整体的甲醛在氧化剂表面的传质速率,导致反应速率下降。
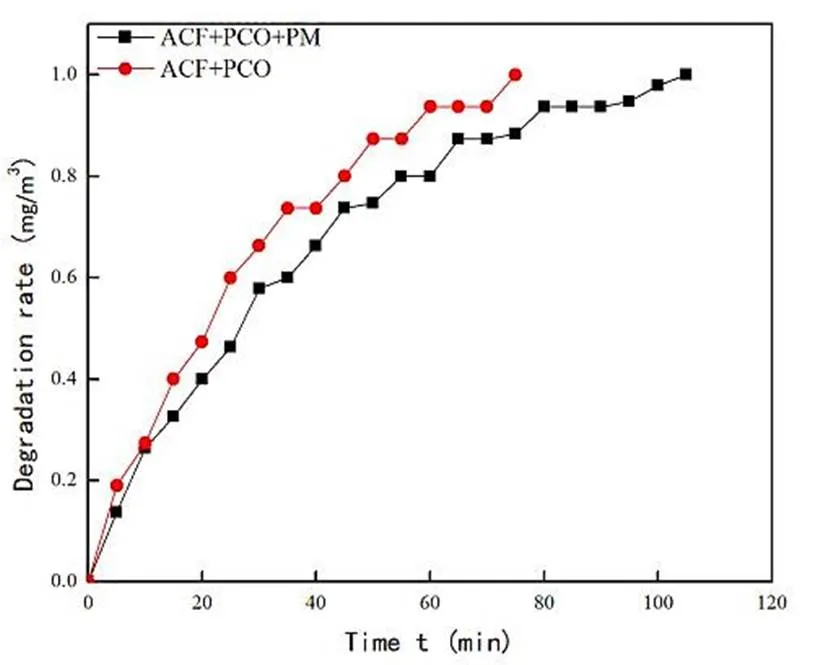
图6 添加PM球对甲醛降解率的影响
2.4 高锰酸钾降解甲醛的反应动力学研究
2.4.1 PM球降解甲醛的反应动力学研究
在不同PM球用量下确定氧化反应的动力学级数的方法是,首先分别假设反应符合零级反应和一级反应,然后根据线性拟合的方差接近1的程度确定反应的级数。
零级反应动力学方程:
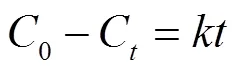
一级反应动力学方程:

式中,0为模拟空间内甲醛的初始浓度,C为时刻时模拟空间内甲醛的浓度,为反应速率常数。
首先,假设符合零级反应动力学方程,如方程(3)所示,此时氧化反应与甲醛初始浓度基本无关[22]板式反应器测试过程中的(0-C)~作图,并对曲线进行拟合,测试结果如图7与表1所示。
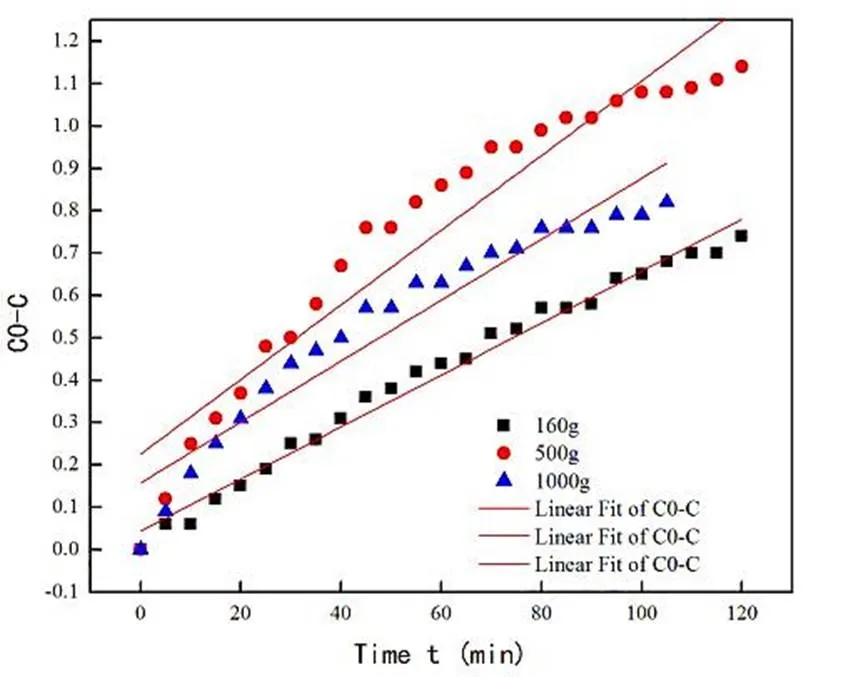
图7 不同PM球用量下的(C0-Ct)~t关系

表1 蜂窝板式反应器中甲醛在不同PM球用量下的零级反应动力学参数
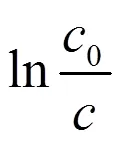
由表2、表3中相关数据综合考虑,两种反应器内的PM球对甲醛的降解均符合一级反应动力学方程,也就是说该反应与甲醛的初始浓度相关,在其余条件不变的情况下甲醛浓度越高则反应速度越快,同样氧化剂用量越大则反应速率越大。同时表中数据说明反应速率常数与氧化剂用量呈正相关。

表2 蜂窝板式反应器中甲醛在不同PM球用量下的一级反应动力学参数
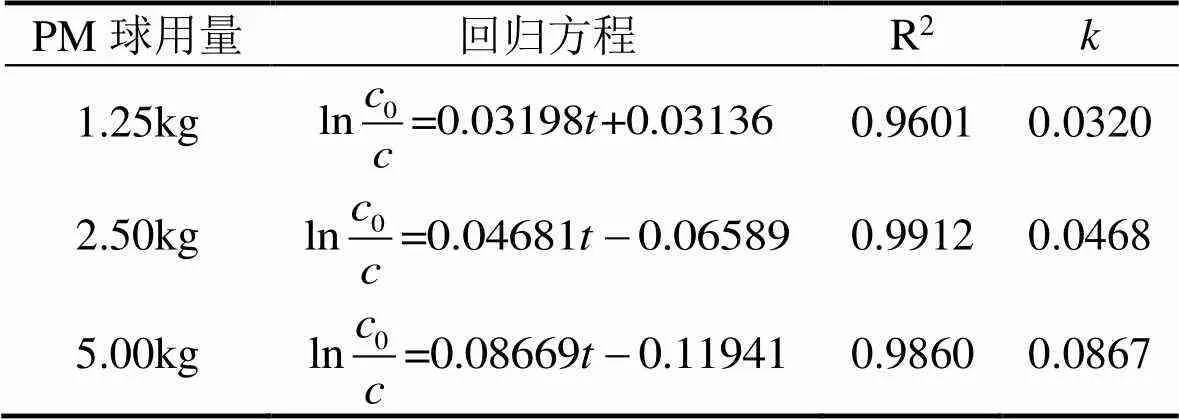
表3 管状式反应器中甲醛在不同PM球用量下的一级反应动力学参数
从反应速率常数的大小可以看出PM球用量从160g增加到500g时反应速率增幅要明显大于从500g增加到1000g,该结论也基本符合图3所示的甲醛降解率变化趋势。
2.4.2 PM球在不同反应器中降解甲醛的反应动力学对比分析
为了确定合适的反应器结构,故将相同质量的PM球置于不同反应器中进行甲醛降解的对比测试,并将测试所得数据按照一级反应动力学方程进行线性拟合,拟合参数如表4所示。

表4 PM球在不同反应器中降解甲醛的反应动力学对比
由表4数据分析可得,当PM球用量从1.25kg增加到2.5kg时,蜂窝板式反应器的反应速率常数的增幅小于管状式反应器值的增幅,且在2.5kg时管状式反应器的值大于蜂窝板式的值,造成这个现象的原因是蜂窝板中的PM球用量不断增加,导致氧化剂阻力增大,气流每次在通过氧化剂表面时的滞留时间延长,降低了整体气流循环次数。
从理论上也可知,材料的阻力与氧化剂表面的风速呈正相关性,在氧化剂用量相同的情况下,管状式反应器能够提供比蜂窝板式反应器更大的反应面积,达到降低PM球表面风速的目的,从而降低了氧化剂的阻力,提升了净化效率。由此可知管状式结构对氧化剂用量的增加更加敏感,当PM球用量在1.25kg以上时管状式结构更有利于氧化反应的进行。
3 结论
根据上述各实验结果与分析研究可得如下结论:
(1)高锰酸钾去除气态甲醛的效果显著,其反应过程符合一级反应动力学方程,且管状式反应器降解甲醛的速度更快;
(2)高锰酸钾与其他净化技术相结合,测试其降解效果,分析发现净化效果除了取决于氧化剂之外,还与风机所能提供的风压相关,只有风压满足并能克服氧化剂阻力才能达到更好的效果;
(3)PM球用量从1.25kg增加到2.5kg时,蜂窝板式反应器的反应速率常数的增幅小于管状式反应器的增幅;PM球用量为2.5kg时管状式反应器的反应速率常数要大于蜂窝板式。由此可知当PM球用量在1.25kg以上管状式结构更有利于氧化反应的进行。
[1] 陈金花,卢军.室内空气污染治理的研究进展[J].重庆建筑大学学报,2007,29(6):108-112.
[2] DU Jing. LI Nianping. Study on indoor air quality of ceiling radiant cooling panel system integrated with displac; ement ventilation[C]. Proceedings of the 8th International Symposium on Heating, Ventilation and Air Conditioning, 2014: 497-505.
[3] ZHANG X, ZHAO Z, NORDQUIST T, et al. The prevalence and incidence of sick building syndrome in Chinese pupils in relation to the school environment: A two-year follow-up study[J]. Indoor Air, 2011,21(6): 462-471.
[4] 孙宏娟,王彦君,汤跃庆.板式儿童家具中挥发性有机物(TVOC)对室内空气质量影响的研究[J].中国建材科技,2012,21(1):1-7.
[5] LU Yuanwei, WANG Dinghui, MA Chongfang, et al. The effect of activated carbon adsorption on the photocatalytic removal of formaldehyde. Building and Environment, 2010,45(3):615-621.
[6] Y Sekine. Oxidative decomposition of formaldehyde by metal oxides at room temperature[J]. Atmos. Environ., 2002,36(35):5543-5547.
[7] HE D, GUAN X H, MA J, et al. Influence of different nominal molecular weight fractions of humic acids on phenol oxidation by permanganate[J]. Environmental Science&Technology, 2009,43(21):8332-8337.
[8] 杨威,刘灿波,余敏,等.微污染水源水中重金属镉的去除[J].化工学报,2014,65(3):1076-1083.
[9] SUN B, ZHANG J, DU J S, et al. Reinvestigation of the role of humic acid in the oxidation of phenols by permanganate[J]. Environmental Science&Technology, 2013,47(24):14332-14340.
[10] DU J S, SUN B, ZHANG J, et al. Parabola-like shaped p H-rate profile for phenols oxidation by aqueous permanganate[J]. Environmental Science&Technology, 2012,46(16):8860-8867.
[11] 徐海云.室内空气中甲醛清除材料的研制及评测[D].天津:天津大学,2008.
[12] 于学华.负载型MnO2催化剂的合成和催化降解甲醛的性能研究[D].烟台:鲁东大学,2012.
[13] P Delano. Classification of manganese dioxides[J]. Ind. Eng. Chem., 1950,42(3):523-527.
[14] S L Brock, N G Duan, Z R Tian, et al. A review of porous manganese oxide materials[J]. Chem. Mater, 1998,10(10):2619-2628.
[15] C L Xu, Y Q Zhao, G W Yang, et al. Mesoporous nanowire array architecture of manganese dioxide for electrochemical capacitor applications[J]. Chem. Commun., 2009:7575-7577.
[16] P Strobel, F Thiery, C Darie, et al. Structural and electrochemical properties of new nanospherical manganese oxides for lithium batteries[J]. J. Mater Chem., 2005,15:4799-4808.
[17] Q Feng, H Kanohb, K Ooib. Manganese oxide porous crystals[J]. J. Mater Chem., 1999,9:319-333.
[18] L Jin, C H Chen, V M B Crisostomo, et al. γ-MnO2octahedral molecular sieve: Preparation, characteriz- ation, and catalytic activity in the atmospheric oxidation of toluene[J]. Appl. Catal., A: Gen., 2009, 355(1-2):169- 175.
[19] 于忠贵,刘连香.浅析高锰酸钾的氧化性[J].天津化工,1997,(3):47.
[20] 陈建国.高锰酸钾与有机物的氧化反应[J].南都学坛(自然科学专号),1994,14(3):30-33.
[21] 朱慧琴.氧化剂载体三氧化二铝制备工艺条件优化[J].广东化工,2014,41(7):58-59.
[22] 林友红.吸附与氧化协同净化室内甲醛研究[D].西安:西安科技大学,2013.
Experimental Research on Oxidation of Formaldehyde by Potassium Permanganate Supported on Alumina
Wen Li1Jiang Hao1Niu Like2Wang Lijuan1
( 1.Xi'an Polytechnic University, School of urban planning and municipal engineering, Xi'an, 710048; 2.Yantai Baoyuan purification Co., Ltd, Yantai, 264003 )
In this paper, two kinds of reactors, namely honeycomb plate reactor and tubular reactor respectively, in a simulated space with alumina-supported potassium permanganate (PM balls) were investigated, in order to evaluate their effects on oxidation of gaseous formaldehyde and the kinetics of how the PM balls can degrade formaldehyde. The experimental results showed that the oxidation reaction of formaldehyde with PM balls followed the first-order reaction kinetics equation. When the air volume was the same and the amount of PM balls was more than 1.25 kg, the tubular reactor structure facilitated the oxidation reaction. The formaldehyde content of the simulated environment could be reduced to 0.1mg/m3in the fastest 30 minutes after the reaction. It could be found with the analysis that the purification effect of the reactor was related to the wind pressure of the fan in addition to the catalyst.
Alumina;Potassium permanganate; Degradation; Formaldehyde; Reactor; Reactionkinetics; Wind pressure
TM172
A
1671-6612(2020)01-015-06
国家自然科学基金(51508434)
文 力(1972.12-),女,硕士,副教授,E-mail:14195507@qq.com
蒋 昊(1992.02-),男,硕士,在读研究生,E-mail:378943894@qq.com
2019-03-28

