11C/18F-乙酸盐在CFN-MPS200上的自动合成
程 亮,陈尚东,崔夫新,刘 丹,何 爽,朴永男
(1.沈阳化工大学 应用化学学院,沈阳 110142;2.北京安迪科电子有限责任公司,北京 100021;3.延边大学附属医院 核医学科, 延吉 133000)
11C-乙酸盐(11C-Acetate)作为正电子发射断层(postiron emission tomography, PET)显像剂,在肺癌、前列腺癌特别是肾癌和肝细胞癌的显像上可弥补18F-FDG的不足,具有很好的临床价值[1]。由于11C-乙酸盐的半衰期短(20.4 min),只能在配备医用回旋加速器的医疗机构使用,临床应用具有局限性。Sykes等[2-4]最先报道了11C-乙酸盐的类似物—18F-乙酸盐,并证实两种化合物生物学分布类似,已经应用在测定心肌氧化代谢和诊断前列腺癌、肝细胞癌的PET研究中。11C-乙酸盐的合成采用强反应活性的CH3MgBr为反应物,对该反应物的保存、添加操作及反应容器的干燥和洁净度都有很高要求,稍有不慎即造成合成失败[5]。而18F-乙酸盐的制备反应温和[6],所有试剂容易保存,合成效率稳定。国内报道中,多采用改造18F-FDG专用合成仪的方法进行18F-乙酸盐的标记合成,如邓怀福等[7]报道了改造IBA公司18F-FDG合成仪、张锦明等[8]报道了改造国产商用18F-FDG模块、张勇平等[9]报道了利用改造后的Explora FDG4合成仪合成18F-乙酸盐。这样不仅容易导致合成18F-FDG和18F-乙酸盐发生冲突,而且存在不同药物的交叉污染,不符合药品生产质量管理规范(GMP)要求。本研究在CFN-MPS200合成仪上探索实验条件,合成符合GMP要求的18F-乙酸盐,并将11C/18F-乙酸盐两种化合物进行质控对照分析,不仅直观体现了两种化合物的理化性质,也拓展了乙酸盐类化合物的临床应用。
1 实验材料
1.1 仪器
HM-10HC回旋加速器、CFN-MPS200型合成仪:日本住友重工业株式会社;高效液相色谱仪:日本岛津制作所分析计测事业部;气相色谱:上海天美公司; 放射性薄层色谱仪:美国BIOSCAN公司。
1.2 试剂
1 mol/L甲基溴化镁四氢呋喃溶液:日本KANTO公司产品;分子筛13X:日本GL公司;H218O(丰度97%):上海化工研究院;溴代乙酸苄酯、无水乙腈、碳酸钾:美国Sigma公司;Kryptofix2.2.2(K2.2.2):德国ABX公司; QMA柱、CM柱、PS-2柱、N-氧化铝柱:美国Waters公司;ON Grad-Ag、ON Grad-H:美国DIONEX公司;PS-OH柱:Macherery-Nagel公司;可裁硅胶板、乙醇(95%分析纯)、盐酸、氢氧化钠:北京化学试剂厂;注射用水、生理盐水:日本大冢公司;抗坏血酸溶液:1.0 g抗坏血酸与10 mL水配制成溶液,过无菌滤膜备用。
2 实验方法
2.1 11C-乙酸盐的合成
① 启动HM-10HC回旋加速器生产11CO2,设置打靶束流45 μA,由离子源电离氢气生产的H-在交变电场中加速,经碳膜剥离后轰击到填充0.80 MPa氮氧混合气(VN2∶VO2=99.5∶0.5)的碳靶上,发生14N(p,α)11C反应,轰击15 min后传靶。② 用加热到70 ℃的13X分子筛吸附11CO2,待13X分子筛的RI-U放射性测量探头示数不再增长时,加热13X分子筛到220 ℃,释放11CO2至0.5 mL 1 mol/L甲基溴化镁的四氢呋喃溶液中,当RI1示数不再增大并开始有下降趋势时,被分子筛吸附的11CO2释放已经完成。③ 加热反应液到30 ℃并反应120 s,然后加入0.5 mL 1 mol/L的HCl进行水解,此步骤反应剧烈,反应液为上下两层。④ 将反应液依次通过ON Guard Ag柱、ON Guard H柱和PS-OH柱。⑤ 分别用酒精和水淋洗PS-OH柱,洗脱杂质。最后用10 mL生理盐水淋洗PS-OH柱,用Cl-将11CH3COO-置换下来,再过CM柱去除可能存在的Mg2+,经过无菌滤膜得到产品。
2.2 18F-乙酸盐的合成


图1 18F-乙酸盐在CFN-MPS200模块上的合成路线
2.3 质量控制分析
2.3.1产物澄明度和pH
目测通过无菌滤膜后的产品为无色澄清溶液,用pH试纸测量pH。
2.3.2薄层色谱法
用毛细管蘸取微量的11C-乙酸盐和18F-乙酸盐的生理盐水溶液,在2 cm×10 cm的硅胶板上点样,以95%的乙腈水溶液做为展开剂(V∶V),在密闭的试管或者展开缸里进行展开,用放射性薄层色谱仪检测放化纯度。
2.3.3高效液相色谱法
配制0. 1 mol/L的乙酸钠标准品溶液,抽取此标准品溶液1 mL稀释至20 mL并摇匀,用微量注射器抽取20 μL,注入到岛津高效液相色谱进样器内,以乙腈(A泵)∶水(B泵)=6∶4(V∶V)做为流动相,C-18(5 μm,4.6 mm×250 mm)为分离柱,流速1 mL/min,紫外检测(UV)波长214 nm。
在相同的条件下,对11C-乙酸盐和18F-乙酸盐进行HPLC分析,采用UV和FC-3600放射性检测器(RI)同时进行检测。
2.3.4K2.2.2的含量检测
18F-乙酸盐的K2.2.2的含量测定,参考《中华人民共和国药典》2015年版第二部氟[18F]脱氧葡糖注射液中氨基聚醚(K2.2.2)的检测方法[11]。
2.3.5细菌内毒素的检测
参考《中华人民共和国药典》2015年版第四部通则1143[12],进行细菌内毒素检测。
2.3.6溶剂残留检测
参考《中华人民共和国药典》2015年版第四部通则0861残留溶剂测定法[13],用水定量稀释制成1 mL中约含乙腈0.4 mg、乙醇5 mg、丙酮5 mg的溶液,作为对照品溶液。以硝基对苯二酸改性的聚乙二醇为固定液的毛细管柱为色谱柱,柱温70 ℃,进样温度200 ℃,检测器温度为250 ℃,顶空瓶温度为85 ℃,平衡时间10 min,取0.5 mL样品进样进行检测。
3 结果与讨论
3.1 合成
使用CFN-MPS200合成仪进行11C-乙酸盐和18F-乙酸盐的合成,合成结束时(end of synthesis,即EOS%)不校正放化合成产率分别为(53.5±5)%和(20.2±5)%,与国内文献报道的合成产率基本吻合[8,14]。
11C-乙酸盐虽然合成时间短、成本低,但甲基溴化镁的高活性对反应器的洁净度、干燥度有较高的要求,甲基溴化镁最好用干燥的1 mL玻璃注射器抽取,带胶塞的塑料注射器遇四氢呋喃后体积会膨胀,注射试剂的阻力很大。前体甲基溴化镁的加入量不需要过多,如甲基溴化镁过多,在反应液通过ON Guard Ag柱时,生成的AgBr沉淀可能堵塞该处理柱,导致反应液无法转移出来。
11CO2从回旋加速器传出,靶气体为氮氧混合气N2∶O2=99.5∶0.5(V∶V),为避免载气中微量的O2对甲基溴化镁造成破坏,在混合气体通入反应管前必须先富集11CO2,然后用高纯N2将11CO2载入到甲基溴化镁溶液中。本研究采用150 mg 13X分子筛吸附11CO2,合成前先将分子筛加热到220 ℃进行活化,15 min后停止加热,再让分子筛自然冷却到70 ℃备用,13X 分子筛在低温70 ℃吸附11CO2,高温220 ℃时释放11CO2。传统方法中使用液氮富集11CO2,当11CO2通过浸入液氮的Loop环时即被凝固成干冰,也有很好的捕获效率,但液氮不容易长期保存,且在倾倒液氮时容易被冻伤,而分子筛可以多次使用,方便安全。
18F-乙酸盐的合成虽然耗时较长,但反应各个步骤容易控制,18F-半衰期较长,有着很好的应用前景。合成18F-乙酸盐的关键在于用水溶解氟化后的反应液。此处操作不宜将溶剂乙腈蒸发过于完全,否则加水转移中间体时,会造成大量的活度粘附于1号反应管内无法转移出来,造成大量活度损失,从而使标记率降低。
3.2 质量控制
以95%的乙腈水溶液为展开剂(V∶V),在可裁硅胶板上点样进行展开,TLC分析得到18F-乙酸盐和11C-乙酸盐的谱图示于图2。从图2结果可以看出,18F-乙酸盐的Rf约为0.31 min,而11C-乙酸盐的比移值Rf约为0.60 min,18F-乙酸盐的极性大于11C-乙酸盐。
用HPLC检测乙酸钠标准品,采用紫外检测器,检测波长214 nm,得到出峰时间为2.40 min(图3)。

图2 18F-乙酸盐(a)与11C-乙酸盐(b)TLC图谱
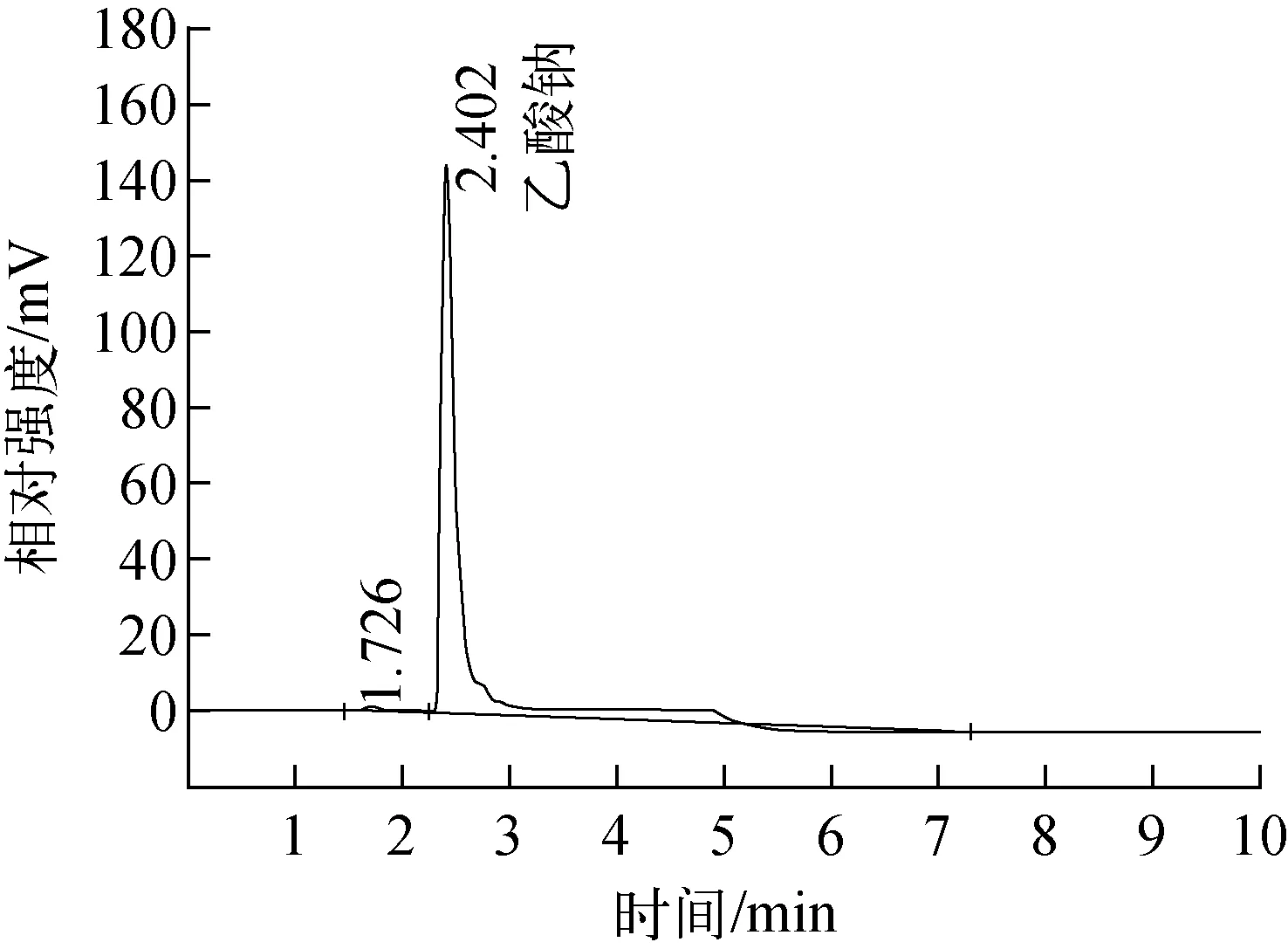
图3 乙酸钠标准品溶液HPLC的UV检测器图谱
在相同的质控条件下对11C-乙酸盐和18F-乙酸盐进行HPLC分析,采用紫外检测器和放射性检测器同时检测。18F-乙酸盐的紫外检测和放射性检测图谱(图4)均为单峰,保留时间分别为2.25 min和2.33 min。11C-乙酸盐的紫外检测图谱和放射性检测图谱(图5)也为单峰,保留时间分别为2.39 min和2.71 min,11C-乙酸盐与标准品的保留时间2.40 min基本一致,证明产物为目标产品。
用广泛pH试纸检测11C-乙酸盐和18F-乙酸盐的pH,pH约为9,偏碱性。可以用微量的抗坏血酸调节pH。用注射器抽取0.1 mL抗坏血酸溶液加入到产品瓶中,即可将pH调整到7~8之间。
细菌内毒素的检测,用内毒素检测用水稀释样品50倍,采用凝胶法进行测定,结果每1 mL细菌内毒素的含量小于15 EU,符合规定。
2.5 μL18F-乙酸盐产品滴在氯铂酸和碘化钾溶液处理的硅胶G板上,产生的蓝色颜色浅于25 μg/mL的K2.2.2标准品溶液,证明18F-乙酸盐产品中K2.2.2的含量小于25 μg/mL。

图4 18F-乙酸盐的UV(a)与RI HPLC(b)图谱

图5 11C-乙酸盐UV(a)与RI HPLC(b)图谱
气相色谱测得18F-乙酸盐产品中丙酮、乙醇、乙腈的溶剂残留(图6),其残留浓度分别为1.99 mg/L、3.34 mg/L、4.94 mg/L,符合临床使用要求。

图6 GC测定18F-乙酸盐中有机溶剂残留图谱
4 结论
11C-乙酸盐和18F-乙酸盐已用于PET/CT临床显像,11C-乙酸盐和18F-乙酸盐体内生物学分布类似,但其化学结构、合成工艺完全不同。11C-乙酸盐合成时间短、成本低、不校正合成产率高,但半衰期短,试剂不容易保存、不当的操作容易导致合成失败。18F-乙酸盐半衰期长、反应温和、各个反应步骤容易控制,但成本高,合成时间长,不校正合成产率低。实际应用中可根据临床患者数量、合成模块的稳定性、操作者的熟悉程度进行选择。
对照两种目标产物TLC图谱,11C-乙酸盐的Rf值略大于18F-乙酸盐的Rf值。18F-乙酸盐的合成工艺与固相水解法制备18F-FDG类似,本研究是首次用住友CFN-MPS200多功能合成仪,全自动合成18F-乙酸盐,并在相同的质控条件下对11C-乙酸盐和18F-乙酸盐进行质量分析,结果证明产物纯度较高,效率稳定,各项指标均符合要求。国内尚未检索到用CFN-MPS200多功能合成仪全自动合成18F-乙酸盐的文献,可为使用CFN-MPS200的医院科室提供参考,为11C/18F-乙酸盐的临床应用提供便利。

