2010~2018 年我国医疗器械召回情况分析
张 焕 洪 源 何宇卿 张 雷 陈 其 姚 雯 刘利萍
1.南京医科大学康达学院药学部,江苏连云港 222000;2.南京医科大学药学院临床药学系,江苏南京 211166;3.江苏恒瑞医药股份有限公司,江苏无锡 214000;4.三江学院财务处,江苏南京 210012;5.南京医科大学康达学院人文与管理学系,江苏连云港 222000
2017 年5 月1 日新颁布的《医疗器械召回管理办法》(以下简称“《召回办法》”)规定,医疗器械召回是指医疗器械生产企业按照规定的程序对已上市销售的某一类别、型号或者批次存在缺陷的医疗器械产品,采取警示、检查、修理、重新标签、修改并完善说明书、软件更新、替换、收回、销毁等方式进行处理的行为[1]。对缺陷医疗器械产品实施召回是国际通行的上市后监管手段,目的是确保使用安全性并消除对公共健康安全的威胁[2]。我国自2011 年7 月1 日开始实行医疗器械召回管理,本文收集原国家食品药品监督管理总局(CFDA)和国家药品监督管理局(NMPA)官网2010 年5 月~2018 年12 月“医疗器械召回”栏公布信息,在召回事件数量、原因、级别、方式、器械分类、所属国和生产企业等方面进行统计分析,以了解我国医疗器械召回现状及存在问题并提出探讨性建议。
1 资料与方法
2010 年5 月18 日~2018 年12 月30 日CFDA 和NMPA 官网“医疗器械召回”栏中召回信息共1551 例,剔除重复无效信息,得完整有效信息共1533 例。在召回事件数量、原因、级别、方式、器械分类、所属国与生产企业等方面,运用Excel 进行归类统计并分析讨论。
2 结果
2.1 召回数量
我国从2016 年年底开始逐渐加强了医疗器械飞行检查监督检查的力度,陆续开展多次国家医疗器械质量监督抽检行动[3],从2017 年开始召回数量大幅提升。见表1。

表1 各年份医疗器械召回事件数量[例(%)]
2.2 召回原因
将1533 例召回医疗器械分:设备、器械、材料、试剂试纸、软件和其他6 大类[4]。参照美国产品责任法中对产品缺陷的分类[5],将召回原因分为:设计缺陷、制造缺陷、警示缺陷和其他(界定模糊,无法归入)。见表2。
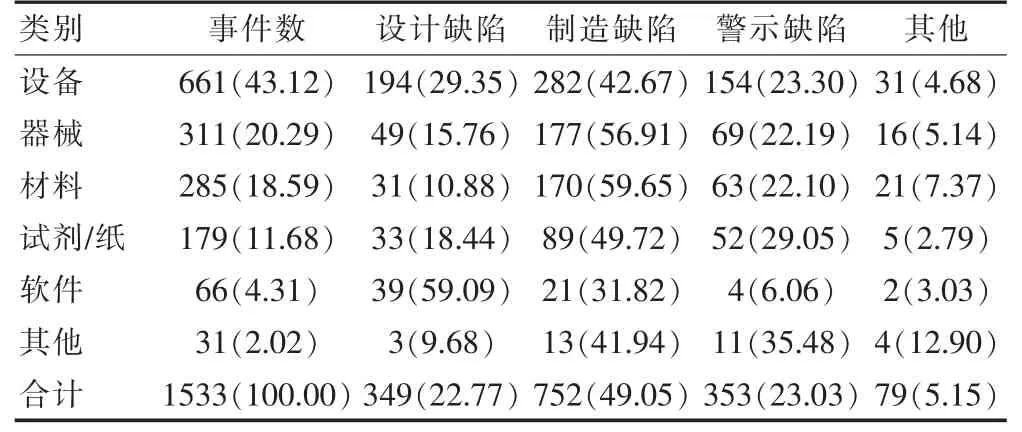
表2 不同类别医疗器械产品召回原因情况[例(%)]
2.3 召回级别
2010~2018 年涉及三级召回最多,其次为二级召回,一级召回数量最少。另据统计2010~2016 年总召回事件数量为626 例,其中未标明召回级别有340 例,占比高达54.31%。这一情况自2017 年开始好转,2017 年未标明召回级别21 例,而2018 年仅有5 例,与2016 年之前比较大幅下降。见表3。

表3 2010~2018 年医疗器械召回级别
2.4 召回方式
1533 例召回事件均为主动召回,2010~2017 年国产召回72 例仅占比4.70%,2018 年国产召回数量大幅增加至210 例。见表4。

表4 1533 例医疗器械召回方式[例(%)]
2.5 召回医疗器械分类
将1533 例事件中医疗器械按我国《医疗器械分类目录》分类分为临床检验分析仪器、植入材料和人工器官等28 种[6]进行归类统计,排名前5 位见表5。临床检验分析仪器、手术室/急救室/诊疗室设备及器具召回数量位居前列,植入材料和人工器官、医用电子仪器设备、矫形外科(骨科)手术器械排在其后,一定程度反映了当前医疗器械的市场分布情况。

表5 1533 例召回医疗器械产品种类分布情况(前5 位)
2.6 召回医疗器械所属国分布情况
召回企业共涉及18 个国家,其中美国、中国、德国、荷兰、日本居前5 位。见表6。另将产品所属公司按召回事件数进行排序,排名前4 位见表7。
3 讨论
3.1 召回事件一般情况分析
2010 年5 月18 日~2018 年12 月30 日 我 国 原CFDA 以及NMPA 官网公布的医疗器械召回事件数共1533 例,8 年间数量逐年上升,至2015~2018 年现增长态势,提示我国自2011 年实行医疗器械召回管理制度已显成效。其中进口器械1251 例占81.60%、国产器械282 例占18.40%。因制造缺陷752 例占49.05%,设计缺陷召回349 例占22.77%,主要集中在设备、器械方面,二者比例高达63.40%,制造(质量问题[7])和设计缺陷依然是导致召回的主因。在美国设计和系统缺陷也是医疗器械召回主要原因(比例达56%)[4],提示医疗器械企业应重视研究与投入,保证产品质量与水平,以减少有安全隐患产品进入市场。召回级别上,一级召回48 例仅占3.13%,二、三级召回居多,共1119 例占比72.99%,约为一级召回23.32 倍。而未标注召回级别比例达23.87%,我国《召回办法》规定医疗器械召回评估报告必须包括召回分级,召回级别缺失意味着召回产品安全隐患程度被模糊,影响召回时效性,应予以规范重视。
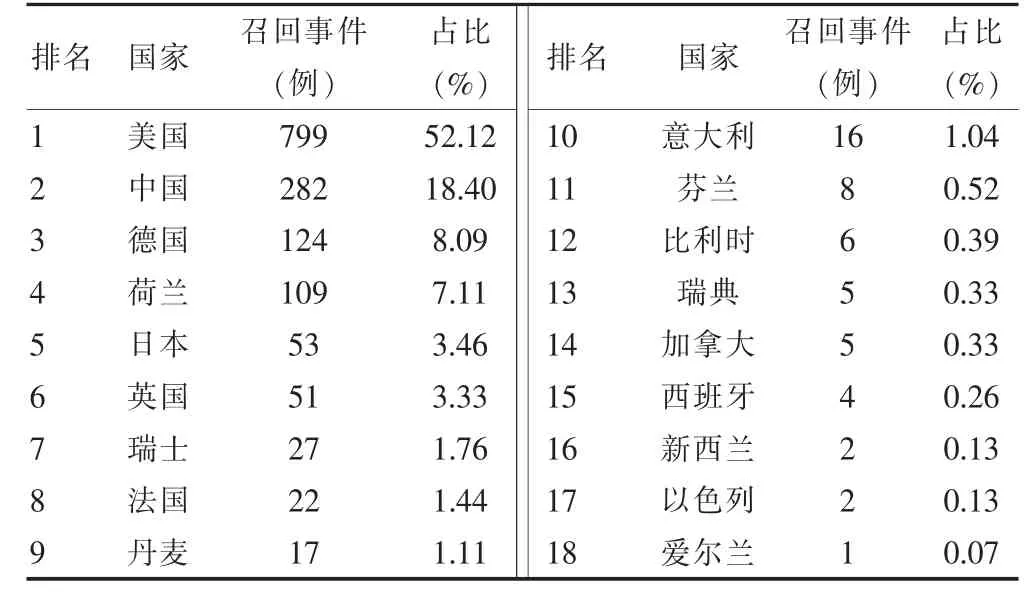
表6 1533 例召回医疗器械生产商所属国分布情况

表7 召回事件数排名前4 位公司排名
1533 例召回事件均为主动召回,国外产品召回共1252 例占比高达81.67%。经统计,目前我国批准上市国产医疗器械是进口的2.83 倍[8],但多集中于中低端市场,高端市场多被国外公司进口所垄断且市场占有率为80%以上[9]。
召回产品分类上,临床检验分析仪器、手术/急救/诊疗设备、植入材料和人工器官召回居多,后二类由于与患者接触密切或进入人体发挥作用,多属于我国规定第二、三类产品,其质量与安全要求严格,因安全隐患而召回比例较高。作为医疗诊断主要手段的临床检验分析仪器,随着精准化医疗的推进,我国对设备及组件安全性监管将继续加强。
所属国方面,美国799 例占52.12%、中国282 例占18.40%、德国124 例占8.09%、荷兰109 例占7.11%、日本53 例占3.46%;产品所属公司召回数排前4 位分别是强生120 例、飞利浦108 例、美敦力71 例、通用61 例,占总召回数23.48%,除飞利浦外其他均为美国公司。近几年国产医疗器械的市场规模年均复合增长率高于15%,然而进口医疗器械的竞争优势依旧明显。尤其是以大型医学影像设备等高精尖体外诊断设备等高、中端医疗器械市场差异最为显著[10],这些国家产品在我国市场占有率高同时因存在安全隐患问题而召回数量也多。
3.2 规范召回信息公布
《召回办法》第9 条规定,监管部门应当按照医疗器械召回信息通报和信息公开有关制度,采取有效途径向社会公布缺陷产品信息和召回信息[1]。1533 例事件中23.87%未标注召回级别。另在召回原因归类上,由于我国目前尚无统一的归类原则与标准,本文参考相关文献[4-5]按缺陷问题对照产品标准进行分类。部分产品召回原因因信息表述模糊或有交叉重叠等现象,导致归类困难,同时还存在信息遗漏、格式不标准等问题。建议监管部门强化召回信息公告制度、规范信息发布的形式与内容,制订科学合理召回原因归类标准,并进行持续反馈与评估机制以确保召回效果。
3.3 完善上市后监测数据来源
实施医疗器械召回离不开健全的医疗器械不良事件(MDAE)监测报告系统。我国自2002 年执行“关于开展医疗器械不良事件监测试点工作的通知”(药监械[2002]400 号文)以来,MDAE 数增长迅速,但相对于国际5‰的报告率,我国各省报告率最高仅1‰[11],差距较大。2012 年江苏省药品不良反应(ADR)监测中心收集的16 706 例可疑MDAE 按报告来源分析,使用单位占53.46%、经营企业占39.17%、生产企业占7.37%,报告主体为医疗机构和代理商。另外,存在报告表漏填、误填、错填等现象[12]。而美国报告主体为生产商,报告数占比90%[13],食品药品监督管理局(FDA)会利用医疗器械报告系统(MDR)对产品风险利益评估后,根据实际情况要求报告人提供更多信息以决定是否实施召回,MDAE 监测更科学透明全面[14]。建议我国可借鉴FDA 经验,建立我国医疗器械上市后监管体系(MDS)[15],拓宽MDAE 信息上报渠道,加强医企间、部门间沟通和共同评价机制,各环节联动、多数据来源,及时发现隐患医疗器械。2014 年的新《医疗器械监督管理条例》将医疗器械再评价、不良事件报告和召回制度作为上市后监管手段,以期扭转我国“重产品审批,轻过程监管”局面[16-17]。
3.4 提高主动召回意识,适时建立召回责任保险制度
2010~2017 年,960 例召回事件中我国虽仅有72 例。然而截至2018 年,在1533 例召回事件中上升为282 例,提示国内生产企业不断提高主动召回意识,市场占有率也在不断提高。由于我国缺少类似美国产品责任保险制度[18-19]以及对召回涉及成本、企业形象与社会舆论等方面顾虑,相对于国内医疗器械的生产企业总数来说,国产企业召回主动性总体还是不足。建议监管部门发挥技术指导职能,在舆论上引导企业和公众对召回正确认识,运用大数据识别与防控风险,采取主动与被动行动和基于质量体系检查的上市后监管[20],并适时建立我国产品召回保险制度,多举措促进企业对问题产品召回。
综上所述,我国自2011 年实行医疗器械召回管理制度,于2016 年建立全生命周期的医疗器械管理体系[21-23],医疗器械召回管理已初显成效。尤其是伴随2017 年新《召回办法》的实行,2018 年召回数据显示企业召回主动性越来越高,召回数量增多,我国医疗器械上市后监管在制度化和规范化上得到很大提升,相信通过不断借鉴改进,未来我国召回监管将更加科学有效。

