肝泰舒预防抗结核药物所致肝损伤的临床效果观察
曾云龙
江西省胸科医院,南昌 330006
结核病是由结核杆菌感染引起的慢性传染病。肺部是结核菌主要侵犯器官,具有传播性强等特点,常见症状为低热、盗汗、咳嗽等,严重者甚至出现呼吸功能障碍,不及时治疗可导致呼吸衰竭[1]。虽然近年来江西省结核病发病率和死亡率出现下降趋势[2],但是发病人数依旧众多,结核病仍然危害着大众的身体健康。临床治疗肺结核一线药物包括异烟肼、利福平、吡嗪酰胺、乙胺丁醇、左氧氟沙星等抗结核药物,此方案虽可有效杀灭结核杆菌,但一线抗结核药物很多都通过肝脏代谢,均可能会对患者肝功能造成严重损害。据相关文献报道[3,4],国内患者在治疗过程中因抗结核药物导致的药物性肝损害发生率最高可达30%。大多数患者因肝功能损伤导致治疗依从性变差、治疗中断、更改方案、疗效降低甚至发生耐药。虽然多数患者停用相关抗结核药物后,使用护肝药物肝功能可完全恢复,但仍然有部分患者可进展至肝衰竭甚至死亡。故治疗期间给予及时恰当的保肝药物进行预防肝损伤尤为重要[5,6]。国内治疗药物性肝损伤常用药物包括抗炎类、肝细胞膜修复保护剂、解毒类、抗氧化类、利胆类,其中很多药物主要成分来源于中药。因此在本研究中,回顾性分析采用肝泰舒胶囊作为预防肝损伤用药治疗肺结核且肝功能正常的患者,密切观察患者肝功能变化情况主要包括谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆红素(TBIL)、谷氨酰转肽酶(GGT)等指标,以及肝损伤发生情况,为临床提供治疗依据。
1 资料与方法
1.1 一般资料回顾性分析本院2019年1月—2019年12月确诊为肺结核且肝功能情况正常的患者200例。按随机数字表法分为对照组和观察组,每组100例。对照组:男47例,女53例;年龄23~58岁,平均(43.2±11.2)岁;病程4~8周,平均(6.03±2.03)周。观察组:男56例,女44例;年龄20~60岁,平均年龄(45.4±13.5)岁;病程4~8周,平均(5.67±1.98)周。两组患者一般资料比较,差异无统计学意义(P>0.05)。
1.2 纳入及排除标准(1)纳入标准:①年龄20~65岁;② 符合肺结核诊断标准[2](痰培养:影像学支持肺结核,且结核分枝杆菌培养呈阳性;分子生物学检查:影像学支持肺结核,且结核分枝杆菌核酸检测呈阳性;病理:影像学支持肺结核,且病理检查亦支持肺结核);③肝功能各项检查无异常;④初治患者;(2)排除标准:①合并病毒性肝炎、肝硬化、肝癌等原发性肝脏疾病者;②妊娠或哺乳期女性;③合并其他严重基础疾病者;④个人原因,没有完成疗程者。
1.3 治疗方法两组抗结核治疗方案相同。遵循抗结核常规用药原则,联合用药治疗。(1)异烟肼片(杭州民生制药有限公司,国药准字H33021636,规格:0.1 g),0.3 g/次,1次/d,饭后2 h口服;(2)利福平胶囊(沈阳红旗药业有限公司,国药准字H21021905,规格:0.15 g),0.45 g/次,1次/d,饭后2 h口服;(3)盐酸乙胺丁醇胶囊(沈阳红旗药业有限公司,国药准字HH21021909,规格:0.25 g),0.75 g/次,1次/d,饭后2 h口服;(4)吡嗪酰胺胶囊(沈阳红旗制药药有限公司,国药准字H20122352,规格:0.25 g),0.5 g/次,3次/d,饭后2 h口服。观察组在此基础上,全程加用肝泰舒胶囊(青海晶珠藏药高新技术产业股份有限公司,国药准字Z20025143,规格:0.4 g),1.6 g/ 次,3次/d,饭后2 h口服。两组均连续治疗8周。
1.4 观察指标观察患者治疗前后的症状变化,定期抽血检查患者的肝功能,主要包括ALT、AST、TBIL、GGT等指标,同时检测治疗前后的血常规、肾功能等,记录药物不良反应。
1.5 疗效评定指标药物性肝损伤程度分为轻度、中度、重度3个等级[3]。(1)轻度肝损伤:ALT <3倍正常值,或者TBIL <2倍正常值;(2)中度肝损伤:3倍正常值≤ALT ≤正常值10倍,或者2倍正常值≤TBIL ≤正常值5倍;(3)重度肝损伤:ALT>10倍正常值,或者TBIL >5倍正常值。
1.6 统计学方法采用SPSS 25.0统计分析数据,计量资料以()表示,进行t检验;计数资料以n、%表示,进行χ2检验,当P<0.05时,差异有统计学意义。
2 结果
2.1 两组治疗前后肝功能指标比较治疗前,两组肝功能ALT、AST、TBIL、GGT指标比较,差异无统计学意义(P>0.05);治疗后,观察组肝功能上述指标均优于对照组,两组比较差异有统计学意义(P<0.05),见表1。
表1 两组治疗前后肝功能指标比较(,n=100)
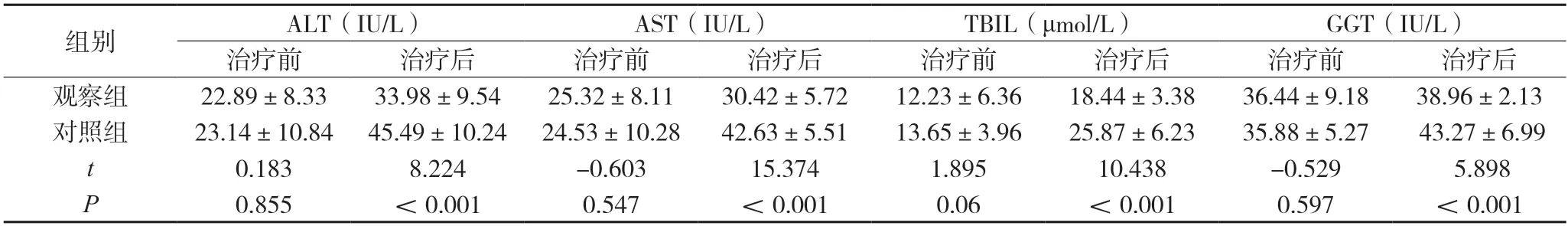
表1 两组治疗前后肝功能指标比较(,n=100)
2.2 两组肝损伤发生情况比较观察组肝损伤发生率明显低于对照组,且肝损伤程度较对照组轻,两组比较差异有统计学意义(P<0.05),见表2。
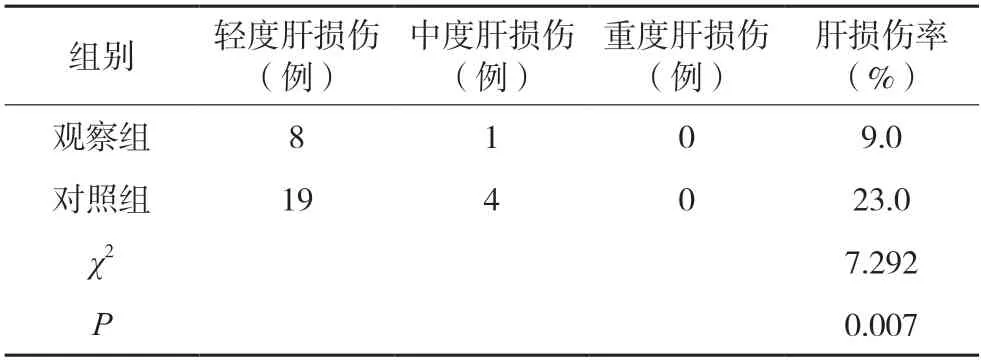
表2 两组肝损伤发生情况比较(n=100)
2.3 两组不良反应发生情况比较比较两组治疗过程中发生白细胞降低、血小板降低、肾功能异常以及恶心呕吐等毒性反应情况,差异无统计学意义(P>0.05),见表3。

表3 两组不良反应发生情况比较(n=100)例
3 讨论
药物性肝损伤(DILI)是指在治疗过程中,由于药物的毒性损害或对药物的过敏反应所导致的肝脏疾病,也称为药物性肝炎。其损害机制主要包括药物的代谢产物对肝胆系统直接的毒性作用,以及代谢过程及产物诱发的变态反应性肝损害[7]。抗结核药物与其他具有肝损害药物对肝脏的损伤机制无明显差别。具体分为:(1)中毒性肝损害:抗结核药物在肝内经过细胞色素酶P450作用,代谢产物比如亲电子基、自由基和氧基等与蛋白质、核酸和脂质等分子结合,对肝胆细胞产生毒性作用,导致细胞受损甚至死亡。这种类型的DILI往往与给药的剂量有关,呈现剂量依赖性,并且会出现蓄积效应[8,9]。(2)变态反应性肝损害:抗结核药物本身或其代谢产物作为半抗原与肝的特异蛋白质结合成为抗原,经巨噬细胞加工后,被人体免疫活性细胞识别,导致变态反应。这种类型的DILI也很常见,与药物的剂量无关,主要受机体的致敏状态、个体遗传差异等影响,并且常常伴有全身或局部的超敏表现[10,11]。由于多种抗结核药物的同时使用,具有潜在肝细胞毒性,DILI是最常见发生的情况。不少患者因肝功能损伤导致治疗依从性降低,从而影响治疗效果,这些都需要临床医生提前采取措施进行干预。因此,治疗期间应科学地给予药物保护肝脏,预防药物性肝损伤发生显得十分必要。中医学强调辨证施治的整体观念和复方配伍用药,通过多种有效成分对人体多环节、多层次、多靶点的整合调节作用,既符合人体多样性的特点,又符合肝炎病变的多症候性、整体性和复杂性,因此,中医药在防治药物性肝损害方面具有独特的优势[12,13]。
肝泰舒胶囊是根据藏医药传统经典名方制成的藏药制剂,主要成分包括青藏高原的獐牙菜、唐古特乌头、苦荬菜、节裂角茴香、黄芪等八味藏药材,其中主要成分獐牙菜[14]为藏茵陈基原植物之一,含有环烯醚萜类、酮类、黄酮类及三萜类化合物,具有清肝利胆、退诸热功效,可用于治疗黄疸型肝炎、病毒型肝炎、血病等症,还能减轻动物模型肝损伤、炎症和胆管结扎大鼠胆汁淤积,使血清中丙氨酸转氨酶(ATL)、天冬氨酸转氨酶(AST)水平显著降低,降低血清中肿瘤坏死因子(TNF-α)、白细胞介素-1(IL-1)和白细胞介素-6(IL-6)水平,还可以降低胆汁淤积大鼠体内鹅去氧胆酸(CDCA)和脱氧胆酸(DCA)的含量[15]。有研究表明,肝泰舒胶囊可以有效阻止肝细胞空泡的产生及脂肪滴的凝聚,防止肝细胞的变性坏死,促进肝细胞的再生和修复,增强机体免疫功能[16]。动物实验也证明了肝泰舒胶囊可降低小鼠因TAA所致的ALT和AST升高[17]。
在抗结核治疗过程中,护肝药物被广泛应用,然而至今尚无关于肝泰舒胶囊用于预防抗结核药物所致肝损伤的研究。本研究结果显示,治疗8周后,观察组肝功能ALT、AST、TBIL、GGT等指标和肝损伤发生率均优于对照组(P<0.05),说明肝泰舒胶囊与抗结核药物联合使用能够起到预防性保护肝功能的作用,且不良反应发生率没有明显差异。笔者推测其机制可能与中药复方具有多成分、多层次、多靶标等特点,具有全面修复药物性肝损伤的作用有关。本研究存在的不足主要是样本量较小,随访时间仅为抗结核治疗初期,以后可进行多中心大样本量研究,观察药物的中长期疗效。另外,药物作用的具体机制尚待继续深入研究。
综上所述,对接受抗结核药物治疗方案的肺结核患者,在开始抗结核药物治疗的同时加服足疗程的肝泰舒胶囊,能明显降低药物性肝损伤发生程度和概率,且安全性较好,值得临床推广。

