芦笋茎尖遗传转化体系的建立与优化
张 园,刘正杰,林 春,闫亚泽, 袁加红,王 入,毛自朝,杨焕文
(1.云南农业大学 农学与生物技术学院,昆明 650201; 2.云南农业大学 特色小宗作物研究中心, 昆明 650201; 3.云南农业大学 烟草学院,昆明 650201)
芦笋(AsparagusofficinalisL.)是多年生宿根性草本植物,百合科天门冬属,学名石刁柏,属国宴常用蔬菜,常有“蔬菜之王”美誉[1]。芦笋除具备很高食用价值之外,还能对人体多种疾病有预防和治疗效果,如降血糖、降血脂、抗癌等[2]。目前,国际芦笋市场需求量正在日益增长,其中中国芦笋约占国际芦笋消耗量40%,芦笋产业已成为芦笋栽培产地农民增收致富重要来源[3-4]。目前,市场上所用芦笋栽培品种虽然产量和品质较好,但多易感病害,特别是茎枯病、褐斑病和炭疽病等,因此筛选高产、高质和抗病品种是芦笋育种工作的重点[5]。芦笋品种以杂交育种和系统选育等常规选育方法为主,但常规选育过程长,育种流程繁琐,可控性较差且育种效率较低;与之相比,转基因育种能克服常规育种手段许多弊端,如可以定向遗传改良、育种周期短且可控性较高等,因此,越来越受到育种者的重视与广泛利用[6]。
目前,国内外对于芦笋的研究主要集中在常规育种[5]、种植栽培与管理[7]、采后生理及贮藏技术[8]、化学成分与药理[9]、组织培养[1]等方面,而对于芦笋转基因育种等相关研究较少,且不够深入。Hernalsteens等[10]将不带外源质粒的根癌农杆菌侵染芦笋茎,并在转化材料检测到了胭脂碱和农杆菌素碱的存在,证实了应用农杆菌侵染法在转化芦笋中的可能性,但该研究并没有进行含有外源质粒农杆菌的遗传转化,也未对转基因材料农杆菌基因表达情况以及遗传转化影响因素做深入研究;Limanton-Grevet等[11]用农杆菌AGL1将uidA和nptⅡ基因转入芦笋胚性系。虽然上述研究实现了芦笋转基因,但其遗传转化体系效率较低且研究不够系统。鹿志伟等[6]在前人研究基础上,开展了农杆菌介导的芦笋遗传转化影响因素研究,但该研究受体材料仍是以组织培养过程中形成的数量较少的芦笋胚状体为外植体,导致获得遗传转化植株的群体不够大。为解决上述芦笋转基因研究中存在的问题,本研究以芦笋组织培养过程中得到的茎尖为外植体,基于瞬时表达体系分析影响农杆菌转化的诸多参数,包括农杆菌侵染浓度、侵染时间、乙酰丁香酮(AS)浓度、共培养时间、分化筛选培养基中卡那霉素浓度及抑菌抗生素种类等。在优化的遗传转化参数基础上,获得转基因植株,并进行PCR、GUS组织化学染色检测和qRT-PCR分析,初步建立芦笋茎尖遗传转化体系,为后续遗传转化研究奠定基础。
1 材料与方法
1.1 供试材料与试剂
供试受体材料为芦笋品种‘达宝利’在MS培养基上扩繁得到的新的幼嫩茎尖。挑选状态良好的芦笋茎尖至预培养基(1/2 MS培养基),置于26 ℃光照培养2 d,作为后续转化受体材料。农杆菌EHA105菌株以及质粒载体pBI121由云南农业大学特色小宗作物研究中心保存。
卡那霉素、羧苄青霉素、乙酰丁香酮(AS)、DNA提取试剂盒、反转录试剂盒等药品均购自上海生物工程有限公司,DNA聚合酶、dNTPs等生化试剂购自全式金生物公司,基本培养基等购自昆明云科生物技术有限公司。
培养农杆菌的培养基为YEP(每升培养基含10 g酵母提取液、5 g胰蛋白胨、10 g NaCl和0.5 g MgSO4·7H2O,pH为7.0)。共培养基[12]为1/2 MS+ IBA 0.5 mg·L-1+ KT 0.1 mg·L-1+ 嘧啶醇 0.5 mg·L-1+ AS 150 μmol·L-1;筛选培养基[12]为1/2MS + IBA 0.5 mg·L-1+ KT 0.1 mg·L-1+ 嘧啶醇 0.5 mg·L-1+ Carb 200 mg·L-1+Kan 50 mg·L-1。茎尖抗性筛选、抗性芽的生长及生根均在上述筛选培养基中完成。
1.2 试验方法
1.2.1 转化菌液的制备 将质粒pBI121(含GUS基因)经冻融法转化至感受态农杆菌EHA105,涂布于YEP固体培养基,挑取单克隆进行PCR阳性鉴定,接种于5 mL的YEP液体培养基(含利福平50 mg·L-1+卡那霉素50 mg·L-1),28 ℃ 220 r·min-1振荡培养16~18 h,再取50 μL该菌液接种至50 mL新鲜的YEP液体培养基(含利福平50 mg·L-1+卡那霉素50 mg·L-1),28 ℃ 220 r·min-1振荡培养培养8 h后,6 000 r·min-1离心5 min收集菌体,用重悬培养基(MS+AS 150 μmol·L-1+30 g·L-1蔗糖)调节OD600值形成侵染液备用。
1.2.2 遗传转化参数的确定 在超净工作台上,切取0.1~0.3 cm芦笋茎尖,置于50 mL离心管中,然后加入侵染液(含AS)浸泡芦笋茎尖,在恒温摇床慢速摇5~40 min,再去除菌液,在无菌滤纸上吸干茎尖表面残留菌液,接种于共培养基,于20 ℃暗处共培养,选取部分经共培养的茎尖,进行GUS瞬时表达率统计,以确定最佳转化 条件。
农杆菌浓度:用活化好的不同OD600值根癌农杆菌菌液(OD600分别为0.2、0.4、0.6、0.8和1.0)侵染芦笋茎尖,再接种至共培养基,置于 20 ℃暗处培养3 d。取共培养结束后的茎尖进行组织化学染色,统计GUS瞬时表达率。
农杆菌侵染时间:将根癌农杆菌调节至OD600值为0.6,侵染外植体的时间分别设定为5、10、15、20、30和40 min,侵染完成后,将受体材料接种至共培养基上置于20 ℃暗处培养3 d。取共培养结束后的茎尖进行GUS组织化学染色,统计GUS瞬时表达率。
AS浓度:向活化好的根癌农杆菌以及共培养基中分别添加AS,使AS的浓度分别为0、50、100、150和200 μmol·L-1,将农杆菌液侵染芦笋茎尖后,再接种至共培养基并置于20 ℃暗处培养3 d。取共培养结束后的茎尖进行组织化学染色,统计GUS瞬时表达率。
共培养时间的确定:调节根癌农杆菌菌液,侵染外植体,转移至添加AS的共培养基中分别培养2、3、4、5和6 d,取共培养结束后的茎尖进行组织化学染色,统计GUS瞬时表达率。
卡那霉素浓度:芦笋离体茎尖经农杆菌侵染后,20 ℃黑暗处共培养3 d,然后接种于添加卡那霉素0、12.5、25、50、75及100 mg·L-1的筛选培养基,26 ℃培养15 d。每个处理培养约50个茎尖,每个处理重复3次。经筛选后统计外植体的存活率,以确定适宜的卡那霉素浓度。
抗生素类型及浓度:将根癌农杆菌在含有不同类型(头孢霉素和羧苄青霉素)及浓度抗生素(0、50、100、150、200、250和300 mg·L-1)的YEP培养基活化培养,通过统计其OD600值并观察其抑菌效果。
1.2.3 GUS组织化学染色 共培养后,每个处理随机取10~20个茎尖,无菌水清洗5~6次,用无菌滤纸吸干材料表面水分,放入1.5 mL离心管中,加入GUS组织化学染色液(成分为: 1 mg·L-1X-Gluc+0.5 mmol·L-1铁氰化钾+0.5 mmol·L-1亚铁氰化钾+50 mmol·L-1Na2HPO4,30 mmol·L-1NaH2PO4+8 mmol·L-1EDTA+0.5% Triton X-100),37 ℃恒温过夜,再用φ=70%乙醇浸泡脱色,直到色素脱去后观测染色情况,统计GUS瞬时表达率,以无菌水处理的未侵染的茎尖为阴性对照。GUS瞬时表达率的计算公式为:GUS瞬时表达率=显色的组织数/检测总组织数×100%,每个处理均重复3次。
1.2.4 转基因抗性植株的获得 将共培养后的茎尖,经含有羧苄青霉素(200 mg·L-1)的无菌水清洗5~6遍,用无菌滤纸吸干茎尖表面水分,置于筛选培养基(1/2 MS + IBA 0.5 mg·L-1+ KT 0.1 mg·L-1+ 嘧啶醇0.5 mg·L-1+ 羧苄青霉素200 mg·L-1+ 卡那霉素50 mg·L-1)上筛选抗性茎尖,然后将抗性茎尖继续在筛选培养基上长芽与诱导生根,获得转基因抗性植株。选取部分转基因抗性植株茎尖、茎部和根部组织,进行GUS组织化学染色的初步鉴定,方法参照“1.2.3”。
1.2.5 转基因植株的分子鉴定 取GUS组织化学染色呈阳性的转基因植株样品,用CTAB法提取其DNA[13]。以质粒pBI121的DNA为阳性对照,以未转基因芦笋植株为阴性对照。设计新霉素磷酸转移酶编码基因(NPTⅡ)特异引物KanF1: 5′-CACTGAAGCGGGAAGGGACT-3′,KanR1:5′-CGATACCGTAAAGCACGAGGAA-3′,扩增片段512 bp,扩增程序:94 ℃ 5 min; 94 ℃ 30 s,52 ℃ 30 s,72 ℃ 1 min,30个循环; 72 ℃ 10 min。扩增产物经10 g·L-1琼脂糖凝胶电泳,在凝胶成像系统下观察拍照。其中,阳性率的计算公式为:阳性率=PCR阳性数目/PCR样品总数×100%。提取转基因与非转基因芦笋植株茎部的RNA,用试剂盒反转录成cDNA,设计引物qTUB4F1:5′-CCGATAACTTTGTC TTTGGC-3′、qTUB4R1:5′-GCAAGGATTCCA AGTATGTC -3′和qKanF1:GCAGGATCTCCTGTCATCTCAC、qKanR1:CCATGGGTCAC- GACGAGATCAT,进行上述处理样品的定量Real-time PCR分析,每个反应设置3 次重复,目的基因的相对表达量采用2-△△Ct法进行计算。
1.3 数据处理
用Excel 2016进行数据处理与分析。 数据以“平均数±标准差”表示。
2 结果与分析
2.1 芦笋茎尖遗传转化效率的影响因素
2.1.1 芦笋茎尖对卡那霉素抗性 由表1可知,在筛选培养过程中,随着卡那霉素质量浓度提高,茎尖变白直至死亡,且其存活率也逐渐减小,当质量浓度超过50 mg·L-1时,存活率在8%以下。因此,设定固体筛选培养基中卡那霉素筛选最佳质量浓度为50 mg·L-1。

表1 固体筛选培养基中卡那霉素质量浓度的确定Table 1 Determination of kanamycin mass concentration in solid screening medium
2.1.2 抑菌抗生素类型及浓度的确定 通过检测YEP液体培养基中农杆菌EHA105的OD600值来检测头孢霉素(Cef)和羧苄青霉素(Carb)对农杆菌的抑制效果,由图1可知,头孢霉素和羧苄青霉素都有较好抑菌效果,羧苄青霉素对农杆菌EHA105生长抑制作用稍好。两种抗生素在质量浓度200 mg·L-1以上时,基本可以完全抑制农杆菌生长,因此在农杆菌EHA105侵染芦笋茎尖后,培养基中添加羧苄青霉素200 mg·L-1。
2.1.3 农杆菌浓度和侵染时间 由图2可知,农杆菌EHA105浓度对芦笋茎尖的GUS瞬时表达率影响较大。研究发现,随着侵染液浓度升高,GUS瞬时表达率呈现先升后降的变化趋势,当菌液浓度为OD600=0.6时,GUS瞬时表达率最高,达18.05%,之后随着菌液浓度升高,GUS瞬时表达率反而下降,而且菌液浓度OD600=1.0时,农杆菌生长过盛,污染率过高。因此,确定侵染液最佳的根癌农杆菌浓度为OD600=0.6。侵染时间过短,农杆菌不能充分与受体材料接触从而影响转化率,时间过长则受体材料会附着过多农杆菌而不易脱菌。为了确定侵染时间对芦笋茎尖GUS瞬时表达率的影响,设置了5、10、15、20、30和40 min的侵染时间。由图3可知,随着侵染时间的延长,GUS瞬时表达率呈现先上升而后趋于相对稳定状态,其中在侵染时间为15 min时,GUS瞬时表达率最高,为17.14%。
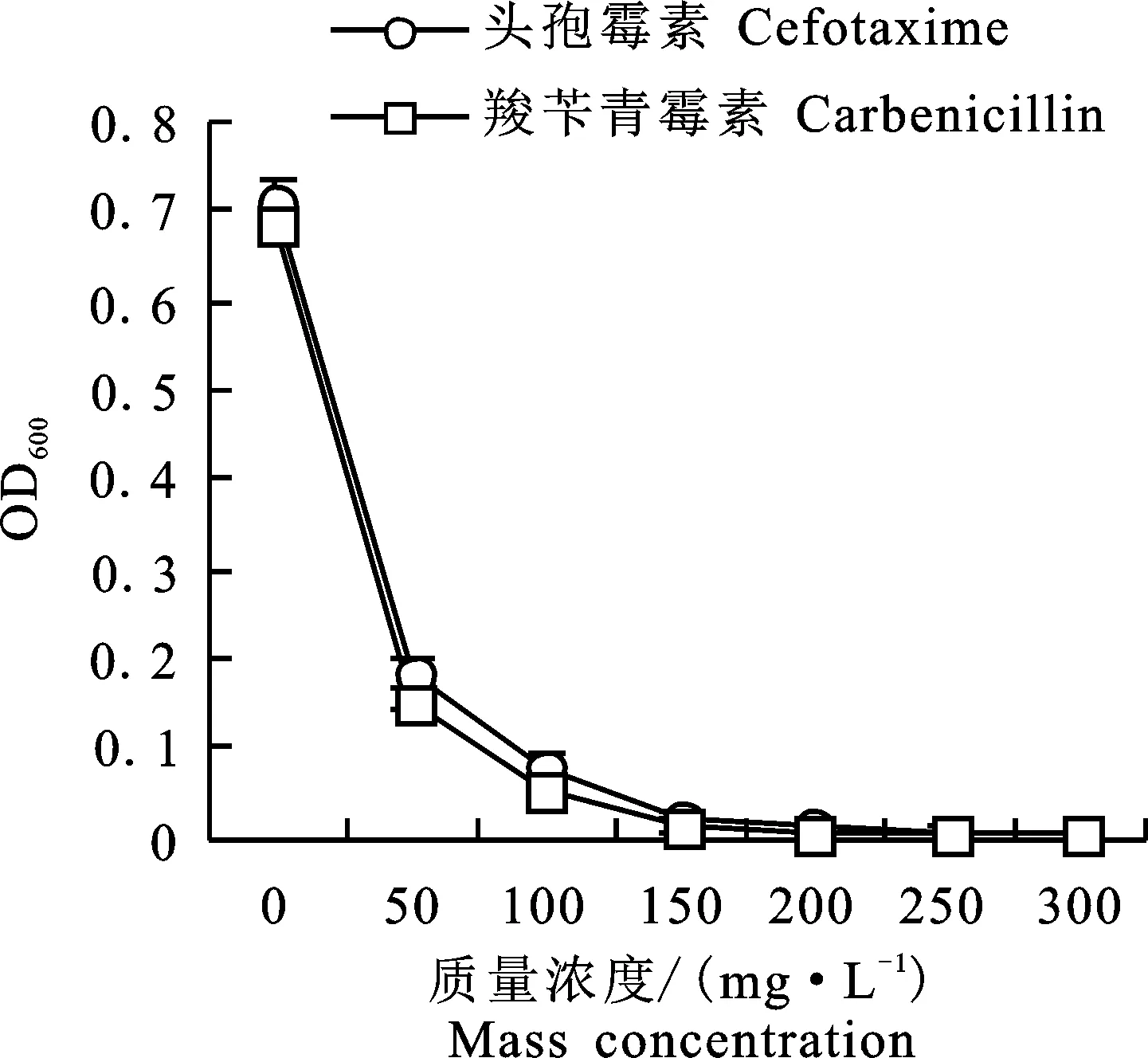
图1 头孢霉素和羧苄青霉素对 农杆菌 EHA105生长的影响Fig.1 Effects of cefotaxime and carbenicillin on the growth of Agrobacterium tumefaciens EHA105

图2 农杆菌菌液浓度对GUS瞬时表达率的影响Fig.2 Effects of Agrobacterium tumefaciens concentration on the rate of GUS transient expression
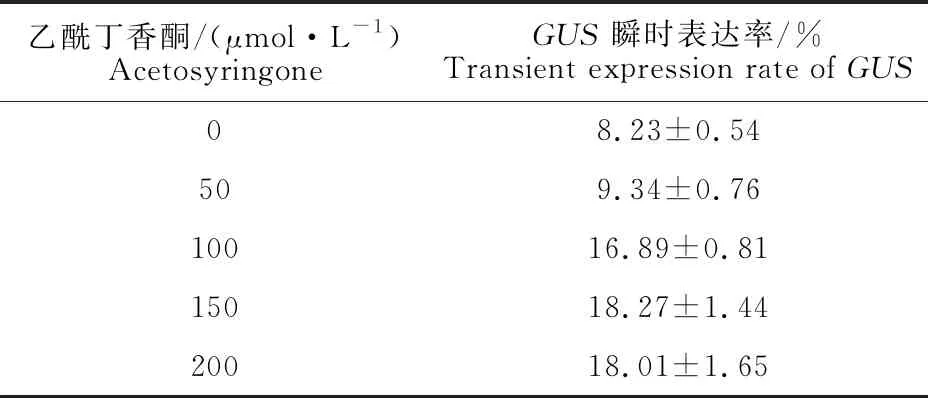
2.1.4 乙酰丁香酮(AS)浓度和共培养时间 乙酰丁香酮(AS)的添加对于农杆菌侵染受体材料至关重要,观察不同AS浓度对GUS瞬时表达率的影响,结果如表2所示,当AS浓度分别为50 μmol·L-1和100 μmol·L-1时差异最明显,当AS浓度为150 μmol·L-1时,GUS瞬时表达率最高,之后提高AS浓度反而略有下降,故AS取最适浓度为150 μmol·L-1。将受体材料芦笋茎

图3 农杆菌侵染时间对GUS瞬时表达的影响Fig.3 Effects of Agrobacterium tumefaciens infecting time on the rate of GUS transient expression
表2 AS浓度对茎尖GUS瞬时表达阳性率的影响
Table 2 Effects of AS concentration on therate ofGUStransient expression
乙酰丁香酮/(μmol·L-1)AcetosyringoneGUS瞬时表达率/%Transient expression rate of GUS08.23±0.54509.34±0.7610016.89±0.8115018.27±1.4420018.01±1.65
尖与根癌农杆菌共培养,观察不同的共培养时间(2~6 d)对GUS瞬时表达率的影响,结果如图4所示:随着共培养时间的延长,GUS瞬时表达率呈现先升高后略有降低的趋势,其中在共培养5 d时,GUS瞬时表达率达最高,为17.89%,其次是4 d时的 17.45%。由于共培养时间过长可能造成后续农杆菌污染,因此确定共培养时间为4 d。
2.2 转基因植株检测
2.2.1 转基因体系的建立 经影响因素研究,优化芦笋遗传转化体系参数:将质粒载体转化至农杆菌EHA105,挑取经PCR鉴定的重组农杆菌单菌落摇菌,配制OD600为0.6的农杆菌侵染液(含150 μmol·L-1AS),以芦笋茎尖为外植体,农杆菌侵染15 min(图5-A),共培养4 d(图5-B),然后置于筛选培养基进行抗性筛选,获得抗性茎尖(图5-C),抗性茎尖继续在筛选培养基进行长芽和生根培养(图5-D~图5-E),最终获得抗性转基因植株(图5-F)。
2.2.2 转基因植株GUS组织化学染色与PCR检测 待获得抗性转基因植株后,进行GUS组织化学染色。结果显示,在抗性植株茎尖、茎部、根等组织部位都能不同程度地被染成蓝色(图6-A),而非转基因对照不能被染色,初步说明GUS基因在抗性植株中可以稳定表达。提取抗性转基因再生植株DNA,以非转基因野生型材料为对照进行nptⅡ基因的PCR检测,结果发现只有抗性转基因植株中能扩增出目的条带(图6-B),说明获得的抗性再生材料初步鉴定为转基因阳性植株。统计PCR初步检测结果,发现PCR阳性率达到12.4%以上。

图4 共培养时间对GUS瞬时表达率的影响Fig.4 Effects of co-culturetime on the rate of GUS transient expression
2.2.3 转基因植株 qRT-PCR检测提取转基因植株与对照茎部组织的RNA,并反转录成cDNA,进行qRT-pCR鉴定,结果发现,非转基因材料中没有nptⅡ基因的表达,而在转基因材料中有不同程度的表达(图7),说明目的基因已经成功在转基因芦笋中稳定表达。

A.茎尖侵染 Stem tip infection; B.共培养 Co-culture; C.抗性筛选 Resistance screening; D.抗性芽 Resistant buds; E.抗性植株生根 Rooting of resistant plants; F.抗性植株 Resistant plants
图5 ‘达宝利’茎尖遗传转化体系的建立
Fig.5 Establishment of the genetic transformation system for stem tip of ‘Daboli’
3 讨 论
农杆菌介导的遗传是目前转化效果最好的植物转化方式之一[14-15],因此,基于芦笋再生体系和芦笋茎尖的结构特点,以及遗传转化成本与技术等因素,本研究选择应用较为普遍的根癌农杆菌介导的遗传转化。Bytebier等[16]采用农杆菌侵染愈伤组织等方式,经抗性筛选与再生获得转基因芦笋,但需较长转化周期。Bruno等[17]对3种基因型芦笋体细胞进行农杆菌介导的遗传转化,获得阳性转基因植株,但其转化率仅为0.6%~4%。Limanton-Grevet等[11]利用AGL1Gin农杆菌侵染5个芦笋胚性系,建立了转化率为 0.8%~12.8%的芦笋转基因体系。鹿志伟等[6]在以芦笋胚状体为受体材料的遗传转化研究中,分析了菌液浓度、AS浓度、侵染时间和共培养时间等4个因素对芦笋转基因效率的影响,转化率可达18%以上。与鹿志伟等[6]相关研究相比,本研究中农杆菌侵染过程的共培养时间相同,均为4 d;但采用的农杆菌侵染最佳浓度为OD600= 0.6,最佳的AS浓度为150 μmol·L-1,侵染时间为15 min,这些差异可能是由于受体材料不同而造成的。

A:转基因植株GUS组织化学染色 GUS histochemical staining of transgenic resistant plants.a.对照茎部 Stem of CK; b.转基因植株茎部 Stem of transgenic plants; c.对照茎尖 Stem tip of CK; d.转基因植株茎尖 Stem tip of transgenic plants;B:转基因植株PCR检测 PCR detection of transgenic plants;P.质粒阳性对照 Plasmid positive control; WT.非转基因植株 Non-transgenic plants;T103~T109.转基因抗性植株 Transgenic resistant plants; M.D2000 DNA ladder
图6 转基因抗性植株GUS组织化学染色与PCR检测
Fig.6 GUS histochemical staining and PCR detection of transgenic resistant plants

WT.非转基因植株 Non-transgenic plants;T103~T109.转基因抗性植株 Transgenic plants
图7 转基因植株qRT-PCR检测
Fig.7 qRT-PCR detection of transgenic plants
在共培养结束后,需将受体材料转移至筛选培养基进行抗性筛选,从而获得具有抗性的转化材料,因此需要确定抗性植株的抗生素浓度[18-20]。培养基中添加的抗生素浓度过高则很难获得转基因植株,给遗传转化体系的建立带来困难;抗生素浓度过低,则会造成假阳性率过高,增加后续筛选鉴定工作,本研究通过比较茎尖在含不同浓度卡那霉素培养室上的存活率及GUS瞬时表达率发现,筛选最佳浓度为50 mg·L-1。此外,在农杆菌侵染茎尖后续抗性筛选过程中,抑制农杆菌过度生长是建立转基因体系的关键因素之一,需要选择合适的抗生素和使用浓度,本研究选择羧苄青霉素200 mg·L-1,虽然更高的浓度对抑菌效果会更好,但也会影响茎尖的存活与生长,因此抑菌抗生素需要选择比较适中的浓度。
由于芦笋遗传转化方面的研究报道相对较少,且芦笋遗传转化的效率与其他物种一样,受多个因素的影响[21-22],因此建立芦笋稳定的遗传转化体系并不容易。本研究尝试以芦笋再生体系建立过程中较为常见且数量较多的茎尖为外植体,探讨影响芦笋茎尖遗传转化的不同影响因素,建立了稳定的遗传转化体系,拓展了芦笋遗传转化受体类型,为后续芦笋功能基因验证提供研究 平台。

