粪菌移植治疗肠易激综合征疗效的Meta分析
余思芸,何 平,房殿亮,任宁川,田文广
重庆医科大学附属永川医院1.消化内科; 2.感染科,重庆 402160
粪菌移植(fecal microbiota transplantation,FMT),又称粪便细菌治疗或肠道菌群移植,是指将健康供体的粪便微生物通过上消化道或下消化道途径转移至患病个体的胃肠道[1],从而达到调节肠道菌群的作用。近年来FMT在治疗艰难梭菌感染(Clostridium difficile infection,CDI)方面的成就有目共睹[2-3],其治愈率为80%~90%[4]。因其对肠道微生态具有强大的调节作用,在肠道菌群异常相关疾病,如溃疡性结肠炎、克罗恩病、代谢综合征、肠易激综合征(irritable bowel syndrome,IBS)等的治疗中,FMT可能是一种有效的治疗方法。
IBS是一种常见的功能性胃肠疾病,以反复发作的腹痛、腹胀、排便习惯改变为主要临床表现[5],在发达国家,10%~15%的成年人受其困扰,并严重影响生活质量和工作效率[6]。虽然目前有大量临床证据显示,多种药物能够改善IBS的临床症状,但却无法治愈。IBS的发病机制至今尚未完全明确。近年来,关于FMT治疗IBS的临床研究时有报道。HALKJAER等[7]的一项系统评价纳入48例接受FMT治疗的IBS患者,结果显示有58%的病例总体症状得到缓解。因此,FMT在临床的广泛应用或可使IBS患者受益。但上述研究纳入的患者数量较少,且以个案报道、会议摘要形式为主,临床论证不足。综上所述,本研究拟通过检索近年来国内外公开发表的关于FMT治疗IBS的随机对照试验(randomized controlled trials, RCTs),系统评价FMT治疗IBS的疗效和安全性,为今后的临床实践提供循证医学证据。
1 材料与方法
1.1 检索策略计算机检索PubMed、Embase、Cochrane Library、中国知网、万方数据库、维普数据库、中国生物医学文献数据库,收集2019年3月1日前国内外公开发表的关于FMT治疗IBS的RCTs。中文检索词:粪菌移植、肠道菌群移植、粪便细菌治疗、肠易激综合征。英文检索词:fecal microbiota transplantation、fecal microbiota transfusion、stool microbiota transplantation、stool microbiota transfusion、gut flora、intestinal flora、FMT、irritable bowel syndrome、IBS。语种限制为中、英文。同时手工检索其他相关资源及纳入文献的参考文献。以PubMed为例,具体检索策略如下:#1 fecal microbiota transplantation OR fecal microbiota transfusion OR stool microbiota transplantation OR stool microbiota transfusion OR gut flora OR intestinal flora OR FMT,#2 irritable bowel syndrome OR IBS,#3 #1 AND #2。
1.2 纳入和排除标准纳入标准:(1)研究设计:公开发表的RCTs,无论是否采用盲法,样本量≥10例;(2)研究对象:接受FMT治疗的IBS患者,同时不伴有严重的危及生命的并发症及合并症(如患有严重心肺疾病的患者);(3)干预措施:包括任何形式的FMT治疗,如口服FMT胶囊,鼻胃管、鼻空肠管、结肠镜灌注等,不限制FMT次数和粪便剂型;(4)结局指标:以总体IBS症状改善为主要结局指标,随访时间≥4周。排除标准:(1)非随机对照试验;(2)无法获取全文且无法提取数据的研究;(3)个案报道、文献综述、系统评价及重复文献。
1.3 资料提取和文献质量评价由2名研究者独立进行检索、筛选、资料提取、文献质量评价,出现争议时寻求第三位研究者意见。RCTs采用Cochrane协作网推荐的“偏倚风险评估”工具进行评估[8],并根据上述评估结果进行分级:完全满足上述标准,发生偏倚可能性最小,为低风险;任意一项或多项标准未描述则为不清楚或部分满足,为中等风险;任意一项或多项完全不满足,为高风险。
1.4 统计学分析采用RevMan 5.3软件进行Meta分析。二分类变量采用相对危险度(relative risk,RR)及其95%置信区间(confident interval,CI)进行疗效分析统计量,以P<0.05为差异具有统计学意义。采用I2值评价结果异质性,I2<50%选择固定效应模型;若I2≥50%则采用随机效应模型,资料允许情况下可进行亚组分析,探讨异质性来源。
2 结果
2.1 文献检索结果初步检索后共获得相关文献730篇,经阅读题目、摘要及全文后,最终纳入5篇RCTs[9-13](英文4篇,中文1篇),共包括288例患者,其中FMT治疗组161例,对照组127例。文献检索、筛选流程见图1。特别说明:其中有2篇[10-11]为已完成的临床试验尚未以完整的原稿发表。但为了扩大样本量,我们仍将其纳入,并且收集了以摘要形式发表的数据。纳入研究的基本特征见表1。
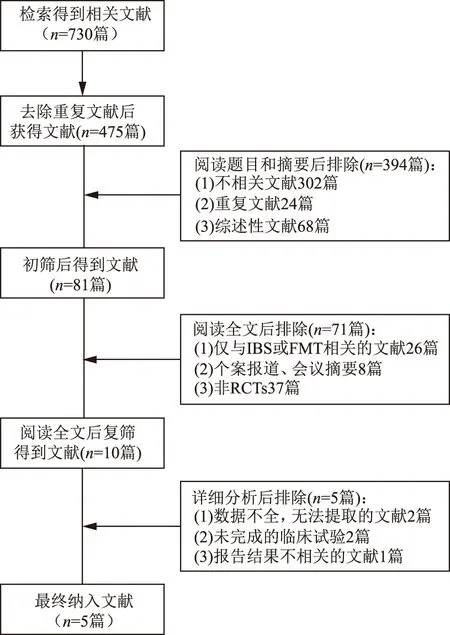
图1 文献检索、筛选流程图
2.2 纳入研究的方法学质量评价纳入的5篇文献中,仅有2篇文献[9,12]完全满足上述标准,为低风险偏倚。其余文献[10-11,13]主要在随机分配、盲法及分配隐藏等方面的描述欠缺(见表2)。
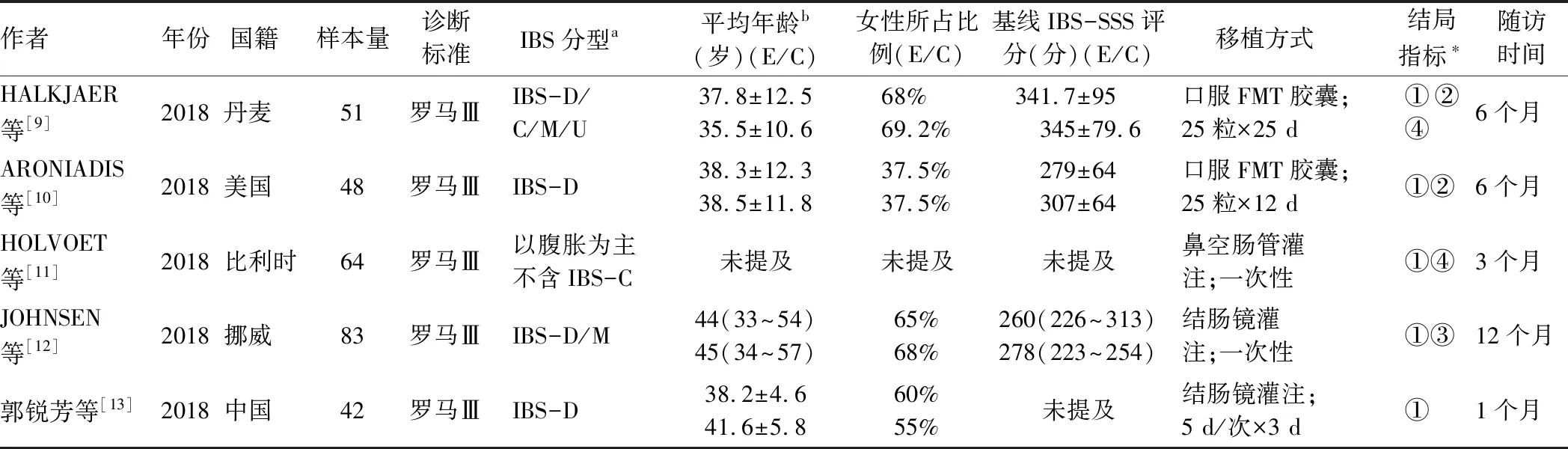
表1 纳入文献的一般特征
注: a:IBS患者根据罗马Ⅲ标准并基于大便性状可分为4种亚型:腹泻型IBS(IBS-D)、便秘型IBS(IBS-C)、混合型IBS(IBS-M)、不定型(IBS-U)。b:E代表FMT组(FMT group),C代表对照组(control group)。*:① 总体临床症状改善;② IBS严重程度评分(IBS-SSS)下降>50分;③ IBS-SSS评分下降>75分;④ IBS生活质量评分(IBS-QOL)上升。

表2 纳入文献方法学质量评价(Cochrane偏倚风险评估)
2.3Meta分析结果
2.3.1 FMT组和对照组IBS症状改善情况比较:各研究之间存在显著异质性(I2=76%),故采用随机效应模型进行合并。结果显示:IBS症状改善率在FMT组为54.0%(87/161),对照组为52.8%(67/127),组间差异无统计学意义(RR=1.04, 95%CI:0.63~1.72,P=0.88)(见图2)。进行敏感性分析显示HALKJAER等[9]的研究存在较大异质性,若剔除此研究异质性下降,但仍存在一定异质性(I2=56%,P=0.24),需进一步行亚组分析。
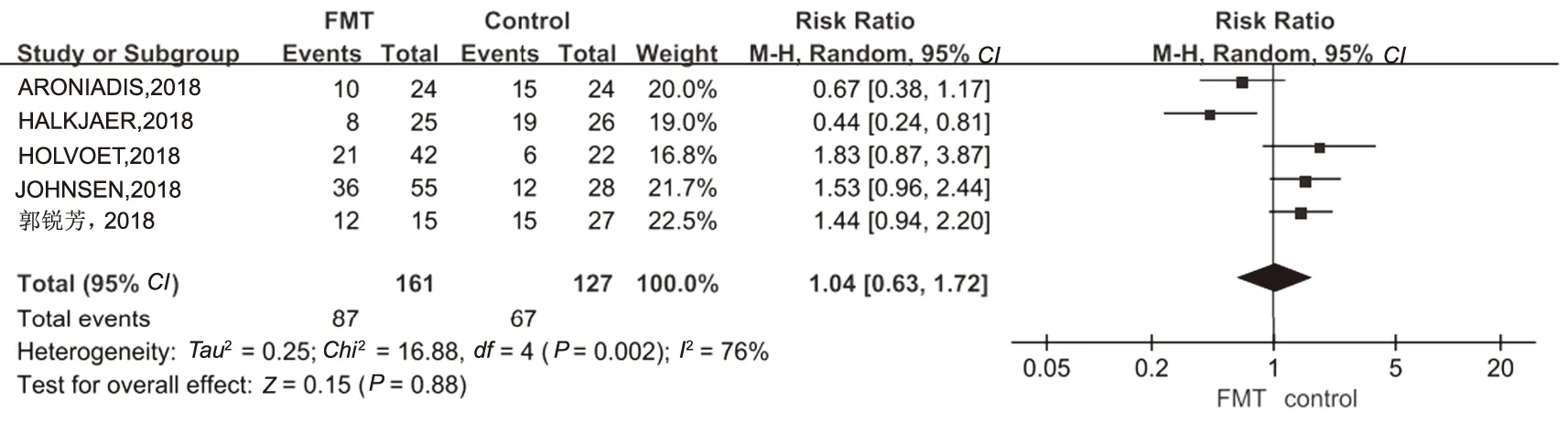
图2 FMT组和对照组IBS症状改善森林图
2.3.2 亚组分析:(1)按移植方式分 2篇文献采用口服FMT胶囊[9-10]进行FMT,各文献间无异质性(I2=0),合并后结果显示:总体IBS症状改善率FMT组与对照组存在显著差异(分别为36.7%和68.0%,P=0.004),与口服FMT胶囊相比,安慰剂组疗效更显著。有2篇[12-13]文献经结肠镜灌注、1篇[11]经鼻空肠管灌注,各文献间无异质性(I2=0),合并后结果显示:总体IBS症状改善率FMT组与对照组比较,差异有统计学意义(分别为61.6%和42.9%,P=0.004),提示采用鼻空肠管或结肠镜等途径将供体粪便微生物移植至空肠、回盲肠等下消化道区域时,FMT治疗IBS的疗效优于对照组(RR=1.57,95%CI:1.15~2.14,P<0.05)(见图3)。
(2)其他:分别按照文献质量高低、随访时间长短、移植频次等进行亚组分析,均无法显著降低异质性。
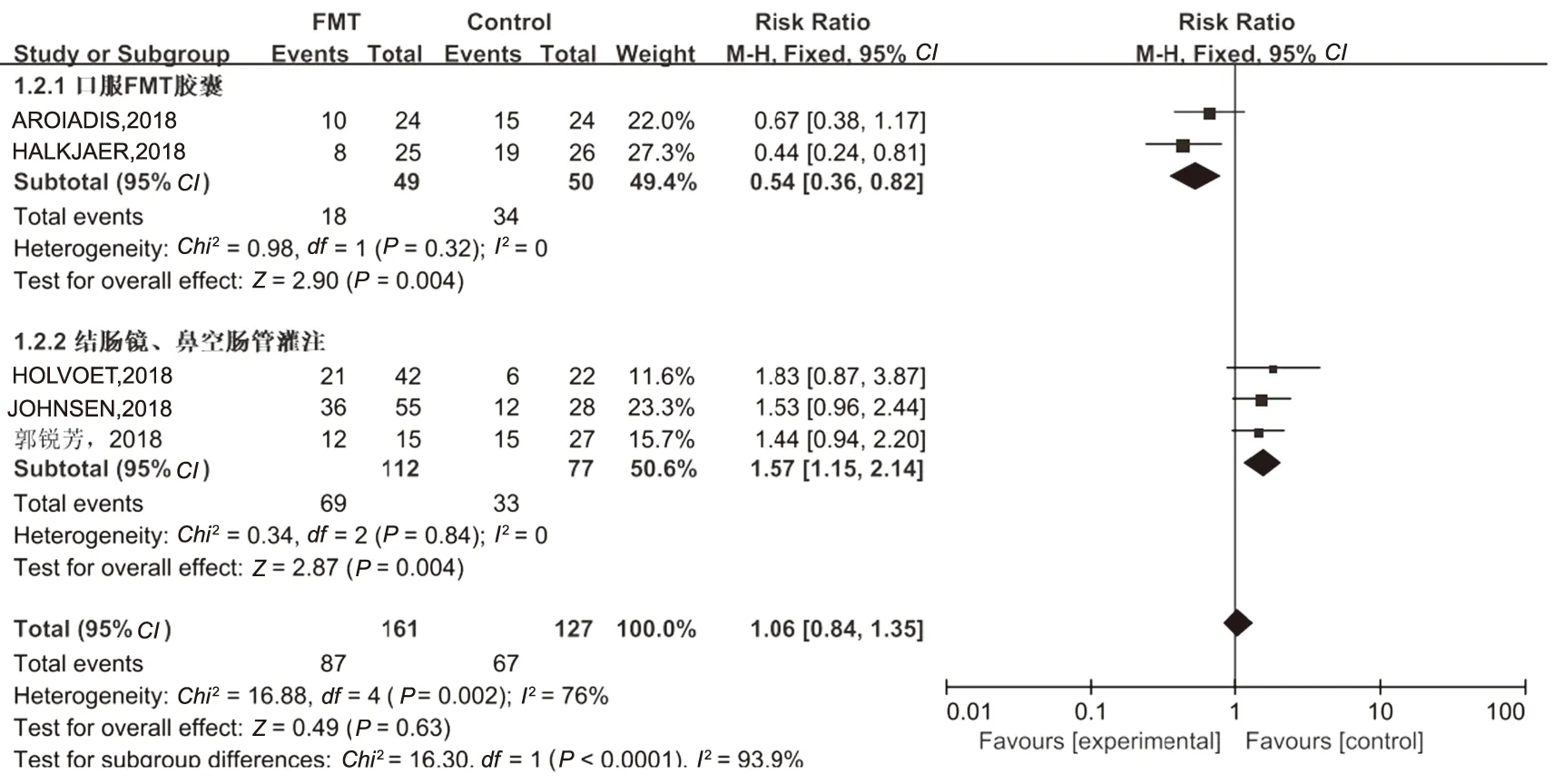
图3 不同给药途径治疗IBS症状改善森林图
2.4 肠道菌群变化郭锐芳等[13]研究了腹泻型肠易激综合征(IBS-D)患者治疗前后肠道菌群的变化,发现治疗后FMT组乳酸杆菌及双歧杆菌等有益菌群数量明显高于对照组。而HALKJAER 等[9]的研究也证明了接受FMT治疗后,受体的肠道微生物群受到持久的影响,且受体的丰度(α-多样性)增加,并向供体微生物菌群(β-多样性)转变。但这些微生物群的变化并未改善受体的预后。这可能与研究纳入了所有IBS亚型有关。
2.5 不良反应有4篇文献关于不良反应进行了报道[9-10, 12-13],在随访期间,均无严重不良反应发生,具体情况见表3。

表3 FMT组和对照组不良反应情况
3 讨论
由于“粪菌银行”(fecal microbiota transplantation bank)的建立[14],FMT已成为一种更易获得和更有用的治疗手段。一项纳入596例炎症性肠病患者的Meta分析发现,FMT对溃疡性结肠炎、克罗恩病均有一定疗效,且对中-重症患者症状缓解率显著高于轻症患者(P=0.037)[15]。近年来关于FMT治疗IBS也有所报道[16-17],但结果却不尽相同。
本研究发现FMT组IBS总体症状改善率为54.0%,与以往的研究结果基本一致[7]。但总体症状改善情况FMT组并不优于对照组。亚组分析发现:通过结肠镜、鼻空肠管等,将供体的粪便菌群直接移植入下消化道(如空肠、回肠、肓肠等)可显著改善临床症状(RR=1.57,95%CI:1.15~2.14,P<0.05);而与安慰剂组相比,口服FMT胶囊组却并不占优势(RR=0.54,95%CI:0.36~0.82,P<0.05)。表明不同移植途径对IBS的疗效可能完全不同,甚至是相反的结果。众所周知,肠道微生物群在上消化道与下消化道之间有明显的差异[18]。不同的移植途径可能影响有益菌群在肠道内的定植,从而产生不同的结局。而使用结肠镜行粪便微生物移植前,往往需要肠道清洁准备,这可能会改变肠道微生物群[19-20]。但无论是有益或有害菌群的流失,一次性植入大量正常微生物菌群,都将更有利于肠道菌群的调节,从而改善临床症状。相比而言,口服FMT胶囊更易受到胃酸及胰酶的影响,使移植菌群遭到破坏[21]。通过口服制剂一次性获得的菌量有限,需反复多次服用,这可能降低疗效及患者的依从性。且FMT胶囊的制作与储存条件较为苛刻,若保存不当可能会影响疗效[22]。同时我们发现,口服安慰剂胶囊具有较高的应答率(68.0%,34/50),这可能与不同的安慰剂治疗方法有关[9-10]。目前还无临床试验比较FMT移植方式对IBS疗效的影响,需要进一步的RCTs予以证实。此外,以往FMT治疗CDI与IBD的研究发现,不同的移植途径(如经上消化道或下消化道)及移植方式(口服胶囊、鼻肠管、内镜灌注甚至是保留灌肠等)各有优缺点,应针对疾病发病特点进行合理选择,才能使更多患者受益[1, 23-25]。
目前研究发现,不同IBS亚型中肠道菌群存在显著差异,尤其是腹泻型与便秘型IBS中,肠道菌群失调的比例、程度均不同[26-28]。而本研究纳入了所有IBS亚型,这可能是导致最终治疗结果不佳的原因之一。而进一步的敏感性分析证实了上述观点。HALKJAER等[9]因纳入便秘型IBS患者成为部分异质性的来源。但因纳入研究中对IBS亚型相关数据描述有限,无法进一步提取分析。而影响FMT疗效的因素还有很多,如使用单一供体还是混合供体、FMT的治疗时间、移植粪便微生物的剂量、频次等,都有待进一步研究证实。
一项纳入50篇关于FMT不良反应的原始文献的Meta分析发现[29]:其总发生率为28.5%,腹部不适为FMT最常见的不良反应。而本研究中FMT治疗IBS的不良反应发生率较低,且纳入研究中均未出现严重不良反应,这说明FMT在治疗IBS方面是安全可行的。
本研究的局限性:(1)本研究纳入的文献以外文为主,仅有1篇为中文[13],且文献质量偏低,研究人群以欧美居多,使研究结论在我国患者的推广受到限制;(2)本文纳入文献均为RCTs,但因目前有限的文献资料,有2篇研究中盲法及分配隐藏的情况无法获取,在一定程度上降低了研究论证强度,且纳入的RCTs较少,无法进行发表偏倚分析,可能存在发表偏倚。但本文纳入文献的研究对象均大于10例,减少个案报道存在的偏倚,是目前样本量最大的研究FMT治疗IBS疗效的Meta分析。同时,首次对不同移植方式在FMT治疗IBS疗效方面的影响进行分析。
综上所述,当前证据不足以证明FMT对所有亚型IBS患者有效。但亚组分析发现采用结肠镜、鼻空肠管灌注等方式进行粪菌移植可显著改善结局,且试验实施过程中,无严重不良反应发生,证实FMT治疗方案本身是安全可行的。同时本研究发现,FMT治疗不同的IBS亚型在疗效方面存在差异,这也为进一步研究FMT治疗IBS提供了思路。

