硼替佐米联合环磷酰胺对多发性骨髓瘤患者免疫因子、免疫细胞水平的影响
高红秀
(河南省驻马店市中心医院,河南 驻马店 463000)
多发性骨髓瘤(multiple myeloma,MM)是一种恶性浆细胞病,病因目前尚不明确,多认为与电离辐射、免疫疾病、病毒感染等因素有关。MM多见于老年群体,且随着我国人口老龄化的加重,发病率逐年增加,约占恶性造血系统疾病总数的15%左右,迫切需要明确该病的病因,对症治疗[1]。作为全球第一个被批准上市的蛋白酶体抑制剂,硼替佐米是治疗MM的首选药物,亦是当前临床公认的能有效延长患者生命周期的方法。环磷酰胺在MM患者中的应用已得到认可,且有相关文献证实,该药的近期疗效较佳[2],但对于具体治疗机制的研究却鲜有报道。本研究采用联合用药方案治疗MM,探讨该方案的疗效及对患者免疫抑制因子、免疫细胞水平的影响,旨在为临床治疗提供理论依据:
1 资料与方法
1.1 一般资料
选取2016年5月—2017年12月我院收治的MM患者76例,纳入标准:①临床诊断符合《中国医师协会血液科医师分会·中国多发性骨髓瘤诊治指南(2015年修订)》中MM的诊断标准[3];②卡氏评分>70分;③预计生存期1个月以上;④患者及家属自愿参与本研究。排除标准:①合并严重肝肾功能、凝血功能障碍者;②合并严重免疫系统疾病或感染者;③对本研究所用药物过敏或不耐受者;④合并糖尿病、肾功能损伤、肾炎等肾功能相关疾病或肾功能不全者。本研究经我院伦理委员会批准。将所有纳入对象按照随机数字表法分为对照组和研究组,各38例。研究组男16例,女22例;年龄45~81岁,平均年龄(67.09±7.37)岁;病情分期:Ⅰ期7例,Ⅱ期14例,Ⅲ期17例。对照组男17例,女21例;年龄46~82岁,平均年龄(67.14±7.52)岁;病情分期:Ⅰ期8例,Ⅱ期15例,Ⅲ期15例。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
两组均给予利尿等常规治疗,并于第1,4,8,11 d快速静注或皮下注射硼替佐米(西安杨森制药有限公司,国药准字:J20160071,规格:3.5 mg/瓶)1.75 mg,第1,2,4,5,8,9,11,12 d静注地塞米松(上海北杰集团关东药业有限公司,国药准字:H22022648,规格:1 ml∶5 mg*10支)40 mg(>75岁者减至20 mg)。在此基础上,对照组给予沙利度胺(常州制药厂有限公司,国药准字:H32026128,规格:50 mg*20片/盒)75~150 mg/d,po。研究组第1~4 d、第8~11 d静注环磷酰胺(通化茂祥制药有限公司,国药准字:H22022234,0.2 g/支)0.2 g。两组均以21 d为1个疗程,治疗3个疗程以上。于第8 d常规口服伐昔洛韦(湖北省益康制药厂,国药准字:H20083699,规格:0.15 g*6片*2板/盒),直至疗程结束。
1.3 观察指标及疗效标准
①参考相关文献报道以临床改善症状及依据《血液病诊断及治疗标准》评价治疗效果作为疗效评估标准[4]:分为完全缓解(CR):临床症状完全消失,骨髓中浆细胞<5%;部分缓解(PR);临床症状改善,血清M蛋白降低≥50%;疾病稳定(NC):临床症状明显好转,血清M蛋白降低≥25%;进展(PD):临床症状无变化,血清M蛋白降低<25%。
临床有效率=(CR+PR)/总例数×100%。
②两组患者均于治疗前后采集静脉血5 mL,以3000 r/min离心6 min,分离血清,检查并比较血清中转化生长因子(TGF)-β、白细胞介素(IL)-6、IL-17,采用双抗夹心酶联免疫法检测试剂盒(上海恒远生物科技有限公司)。采用贝克曼CytoFLEX流式细胞仪检测血清中CD4+、CD8+水平,并计算CD4+/CD8+比值。
③于治疗开始后对患者进行12个月随访,观察不良反应发生情况。
1.4 统计学方法
采用SPSS 22.0软件分析数据,计量资料以“±s”表示,采用t检验;计数资料以百分数(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
研究组临床有效率高于对照组,差异有统计学意义(P<0.05)。见表1。
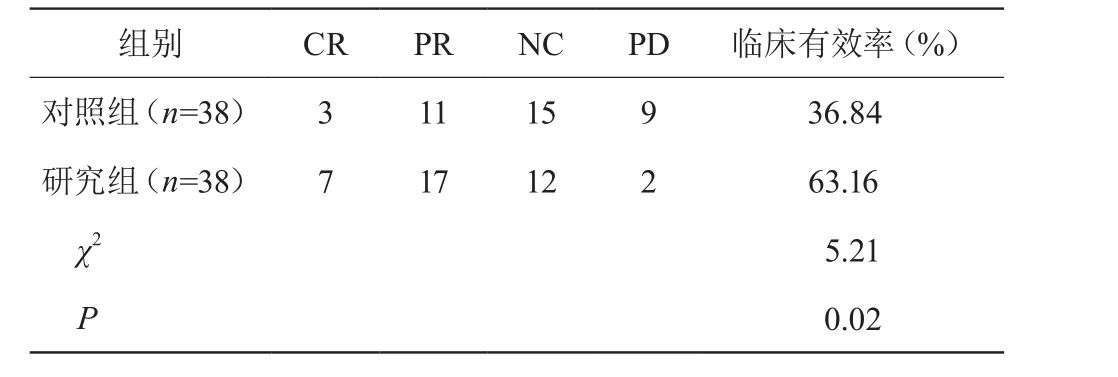
表1 两组临床疗效比较
2.2 两组免疫因子比较
治疗前,两组TGF-β、IL-6、IL-17比较差异无统计学意义(P>0.05);治疗后,两组TGF-β、IL-6、IL-17均下降,且研究组低于对照组,差异有统计学意义(P<0.01)。见表2。
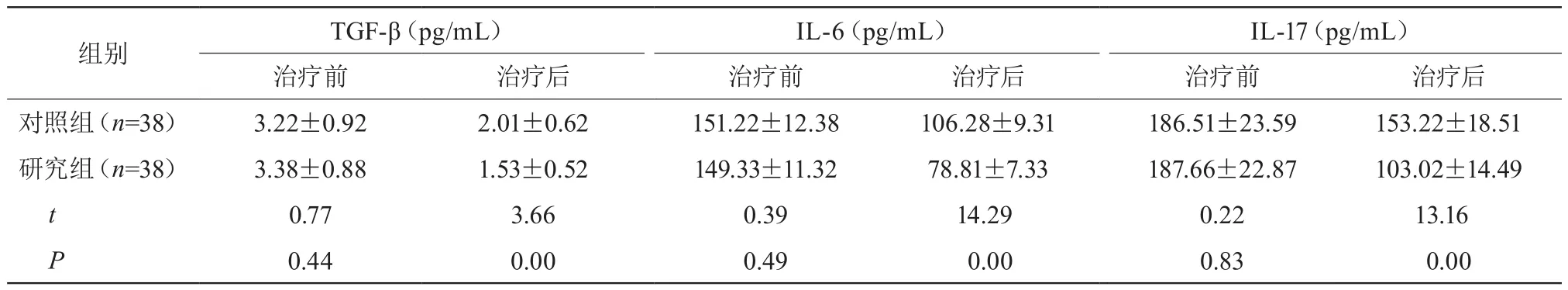
表2 两组免疫因子比较
2.3 两组免疫细胞比较
治疗前,两组CD4+、CD8+、CD4+/CD8+比较差异无统计学意义(P>0.05);治疗后,研究组CD4+、CD4+/CD8+均较治疗前增加,且研究组高于对照组,CD8+均较治疗前降低,且研究组低于对照组,差异有统计学意义(P<0.05)。见表3。
2.4 两组不良反应比较
两组乏力、恶心腹胀、白细胞减少、血小板减少发生率比较,差异无统计学意义(P>0.05)。见表4。

表4 两组不良反应比较
3 讨论
目前临床上尚缺乏治疗MM的有效手段,主要治疗方式仍以药物或药物辅助化疗为主[5]。进入新药时代后,无论是初治或复发难治MM,硼替佐米治疗极大延长了患者的生存期,该药的具体作用机制包括[6]:①结合泛素蛋白酶体系统位点,进而降低其活性;②降低癌细胞DNA修复能力,降低其耐药性;③抑制细胞凋亡蛋白及细胞周期调控蛋白降解,调节正常细胞周期;④减少IL-6等合成及分泌,调节机体内环境,抑制肿瘤生长;⑤促进集体p53基因表达,降低NF-kb活性,加快肿瘤细胞凋亡。虽然硼替佐米疗效显著,但绝大多数患者在经过一段平台期后复发,预后不佳,因此需要联合其它药物治疗。环磷酰胺为功能烷化剂及细胞周期非特异性药物,不仅可提高对MM细胞的杀伤率,降低瘤负荷,亦能够抑制特异性抗原刺激淋巴细胞的母细胞转化和补体活性,打破体内的免疫抑制环境,逆转免疫耐受或免疫低下的状态[7]。环磷酰胺在国外被推荐与硼替佐米联合应用治疗MM,可提升疗效。本研究结果显示,研究组临床有效率高于对照组(P<0.05),且未增加不良反应,证实硼替佐米联合环磷酰胺治疗MM的优越性,这一研究结果与前人的结论[8]是一致的。
免疫抑制因子表达水平与MM病情的发展有很密切关系[9]。TGF-β是由癌细胞和调节性T细胞联合分泌的免疫抑制因子,在抗肿瘤免疫方面起重要作用。IL-6属于调节免疫活性的细胞因子,主要由骨髓基质细胞分泌,可有效促使T细胞及活化B细胞的增殖,同时分泌抗体,刺激炎症因子、趋化因子和造血因子产生,从而引发促炎症反应功能。IL-17由Th17 细胞分泌,具有很强的致炎性,能通过受体对基质细胞的黏附来促进瘤细胞生长,故血清IL-17水平能够反映肿瘤对免疫应答的抑制程度。本研究结果显示,治疗后研究组TGF-β、IL-6、IL-17均明显低于对照组,提示硼替佐米联合环磷酰胺治疗在抑制肿瘤生长方面的效果更明显。既往研究表明[10],在肿瘤发生、发展过程中,机体细胞免疫功能起着重要作用,故而监测患者细胞免疫功能可在一定程度上反映病情转归情况。本研究中,治疗后观察组CD4+、CD4+/CD8+均明显高于对照组,CD8+明显低于对照组,证实该治疗方案可改善患者细胞免疫功能。
综上所述,硼替佐米联合环磷酰胺治疗MM的疗效显著,且安全性好。但本研究亦存在不足之处,即受时间和人力的限制,所纳入样本有限,需进一步扩大样本,探索加用环磷酰胺对于MM的最终实效性。

