EGFR-TKIs和培美曲塞序贯联合治疗与单药治疗EGFR-TKIs后缓慢进展晚期肺腺癌的疗效比较
汤志谋 童 波 王 凌
肺癌发病率和死亡率逐年升高,是对人类生命危害最大的恶性肿瘤,其中25%~30%为肺腺癌。培美曲塞+铂类是肺腺癌的一线方案。而对于驱动基因阳性的晚期NSCLC,靶向治疗已作为一线选择。但不久也会出现耐药。耐药后有更新一代靶向药物出现,但因为价格昂贵,许多患者会选择换化疗。耐药后是马上换化疗还是继续使用靶向药物及靶向药物是否能联合化疗,仍有很大争议。
本文选择晚期肺腺癌,驱动基因EGFR阳性的患者,给予EGFR-TKIs一线治疗,出现病情缓慢进展后,再分别接受继续单药EGFR-TKIs、单药培美曲塞和EGFR-TKIs序贯培美曲塞3种不同的治疗方式,对比在不同治疗方式下患者的临床疗效和无进展生存时间(PFS)和总生存时间(OS),期待对患者实施更有效的个体化治疗。
1 资料与方法
1.1 临床资料
选择我院2014年1月至2016年12月经病理学确诊的不能手术的晚期肺腺癌伴EGFR突变阳性的患者,经EGFR-TKIs一线治疗后缓慢进展,共90例,符合以下条件:①有至少1个影像学可测量的病灶,该病灶未接受过任何局部治疗;②年龄≤75岁,ECOG≤1;③预计生存期内可以接受到二线的治疗;④骨髓、心、肾等重要器官功能正常,血常规及肝肾功能正常,心电图正常;⑤均签署知情同意书。缓慢进展:患者服用TKIs疾病控制时间≥6个月,肿瘤负荷轻微增加(原肿瘤病变略增大或出现1~2处新病灶),ECOG评分PS≤1。患者耐药前TKI使用时间为6~31个月,中位时间为12个月。患者基本资料见表1。
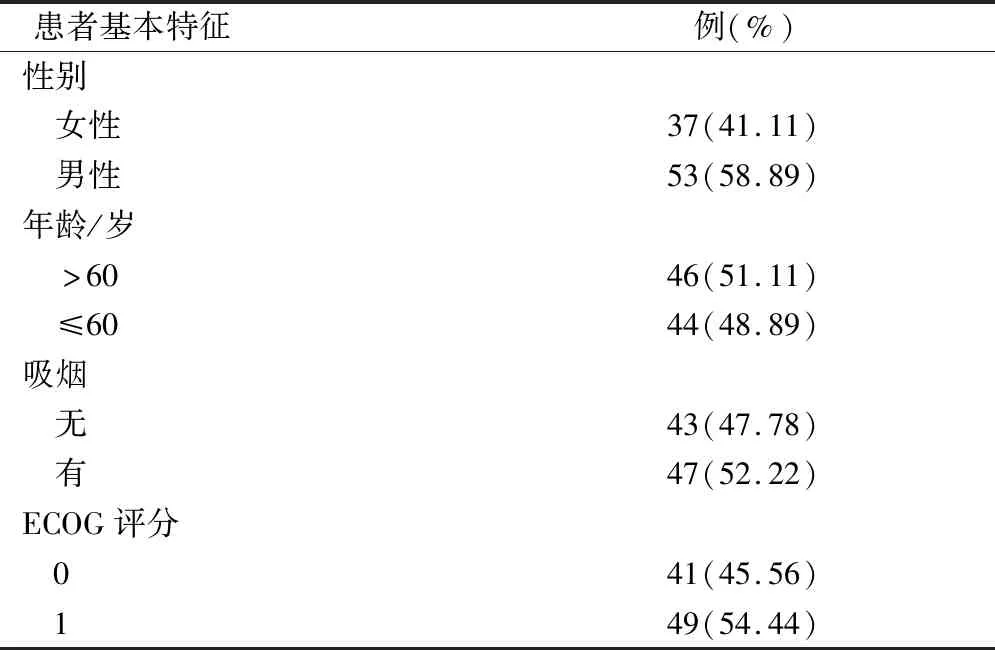
表1 患者基本资料
1.2 方法
随机分为3组,A组,B组和C组,每组30例。A组:EGFR-TKIs口服一线治疗,疾病缓慢进展后,改培美曲塞单药化疗。B组:EGFR-TKIs口服一线治疗,疾病缓慢进展后,仍继续EGFR-TKIs单药治疗。C组:EGFR-TKIs口服一线治疗,疾病缓慢进展后,改EGFR-TKIs序贯培美曲塞联合治疗。
TKIs药物:吉非替尼 250 mg/次,每天1次,空腹或与食物同服;或厄洛替尼150 mg/次,每天1次,饭前1 h或饭后2 h服用;或埃克替尼125 mg/次,每天3次,空腹或与食物同服。500 mg/m2,静脉输注,第1天,每21天重复。首次培美曲塞给药前7天肌肉注射维生素B12一次,每次1 000 μg,以后每3个周期肌注一次。给药前5天开始每天口服叶酸400 μg,一直服用整个治疗周期,在最后1次培美曲塞给药后21天停服。给药前1天、当天和给药后1日每天口服地塞米松片2次,每次4 mg。
EGFR-TKIs序贯培美曲塞:培美曲塞 500 mg/m2,静脉输注,第1天;EGFR-TKIs,d8~20,每21天重复。参考宋正波等[1]的《化疗间期序贯应用厄洛替尼治疗晚期非小细胞肺癌的临床观察》中的方案。直至肿瘤进展或不良反应不能耐受。
化疗期间常规使用5-羟色胺受体拮抗剂预防呕吐,定期复查血常规及肝肾功能。治疗过程中每2个周期全身复查1次,进行疗效评估,包括体格检查、血常规、生化常规、CT/MRI检查等。
每接受2个周期治疗后评价临床疗效和不良反应。根据1999年RECIST的实体肿瘤疗效评价方法评定疗效并记录。近期疗效分为完全缓解CR、部分缓解PR、疾病稳定SD、疾病进展PD。客观有效率ORR=(CR+PR)/(CR+PR+SD+PD)×100%, 疾病控制率DCR=(CR+PR+SD)/(CR+PR+SD+PD)×100%。药物毒性不良反应评定采用WHO抗癌药物不良反应5级标准,处理并记录。
所有患者在治疗前都已经接受活检取得标本进行EGFR基因检测,病情进展后再取组织标本、细胞学标本(外周血、胸腔积液)等方法再进行EGFR及EGFR T790M等基因检测,观察其变化。
定期随访,每月1次至少电话随访,直至死亡。记录患者的无进展生存时间(PFS)和总生存时间(OS)。失访者以末次随访日计算。末次随访日期2018年1月。无进展生存期(PFS)定义为治疗开始至肿瘤进展的时间,总生存期(OS)定义为治疗开始至任何原因患者死亡的时间。
1.3 统计方法
应用SPSS 17.0统计软件进行统计分析,三组一般情况比较采用χ2检验,三组之间的PFS和OS比较采用Kaplan-Meier检验,多因素分析采用Cox回归模型。检验水准α=0.05。三组的客观有效率、疾病控制率及PFS,OS及不良反应进行统计比较,P<0.05为有差异。并筛选出有影响的预后因素。
2 结果
2.1 近期疗效
所有患者均得到随访和疗效评价,C组客观有效率46.67%,疾病控制率86.67%,优于A组和B组(χ2=9.579,P=0.008),A、B组疗效无明显差异(χ2=0.353,P=0.553),见表2。

表2 三组患者近期疗效比较(例,%)
2.2 生存分析
A组患者的中位无进展生存时间为4.3个月,B组的中位无进展生存时间为4.5个月,C组的中位无进展生存时间为5.2个月,三组患者的无进展生存时间比较,差异无统计学意义(χ2=4.671,P=0.097 ),见图1。
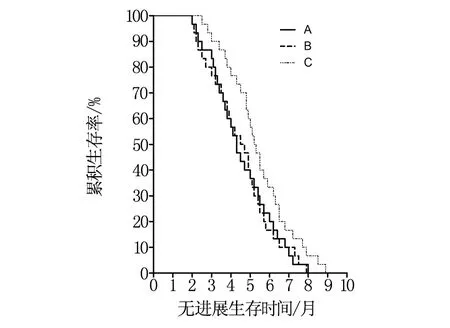
图1 三组无进展生存时间(PFS)比较
A组患者的中位生存时间为 8.5个月,B组的中位生存时间为8.0个月,C组的中位生存时间为9.0个月。三组患者的生存时间比较,差异无统计学意义(χ2=2.687,P=0.261),见图2。

图2 三组生存时间(OS)比较
2.3 不良反应
主要不良反应为骨髓抑制,多为轻中度白细胞下降,经对症处理后经缓解,两组均未出现Ⅳ度不良反应,未出现治疗相关性死亡病例,见表2。
3 讨论
表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitors,EGFR-TKIs )已经成为EGFR基因突变阳性肺腺癌患者一线治疗的最佳选择[2-3]。其通过选择抑制 ATp与 EGFR-TK 的ATp结合位点结合,从而抑制 EGFR-TK的活性,阻断 EGFR的信号传导,起到抗肿瘤的作用[4]。大约60%~80%的非小细胞肺癌存在EGFR的过度表达和突变。EGFR-TKIs类的小分子靶向抗癌药主要包括吉非替尼(gefitinib),厄洛替尼(erlotinib)和盐酸埃克替尼(icotinib hydrochloride)。多个临床研究表明,三者的核心化学结构类似,对肺腺癌的治疗,三者疗效基本一致[5]。
然而EGFR-TKIs药物的有效维持时间仅为10~16个月[6],多数患者易出现耐药进展。对EGFR-TKIs治疗后进展的患者,再次活检找出耐药原因并有针对性地选择耐药后续治疗的药物是最为理想的治疗方法。耐药机制主要有T790M突变、c-Met癌基因的扩增、PIK3CA突变等,其中50%是由于T790M突变[7]。耐药后选择新一代EGFR-TKI药物或c-Met基因扩增抑制剂是合理选择之一[8]。但因经济原因,临床上解决耐药的方法,常常停留在如何利用现有的资源进行尝试。既往有关EGFR-TKIs重复治疗的文献[3]表明,患者在疾病缓慢或局部进展后仍可以从TKIs治疗中受益,停止其治疗可能导致疾病更快地进展或死亡。Yang等[9]将EGFR-TKIs治疗失败的患者根据其EGFR-TKIs对疾病控制的持续时间及治疗进展后肿瘤负荷、患者的临床症状将其分为爆发式进展、缓慢进展及局部进展,研究结果表明对于EGFR-TKIs耐药模式为缓慢进展的人群中继续EGFR-TKIs联合化疗的OS似乎长于单纯化疗。
EGFR-TKIs药物可诱导细胞停滞在G0期,然后通过细胞本身的凋亡而将肿瘤细胞杀死,而常规化疗药物主要是对处于S期的细胞有杀伤作用。所以,化疗药物后序贯EGFR-TKIs得当可能有协同作用。 FAST-ACT-2研究表明[10],化疗间插厄洛替尼一线治疗可显著延长EGFR突变晚期肺癌患者PFS和OS。
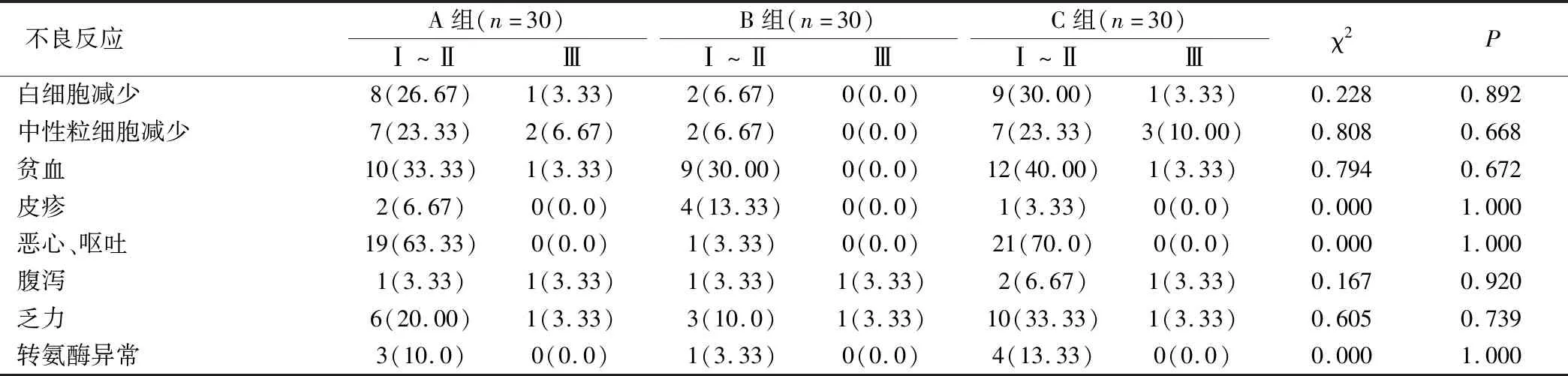
表2 三组患者的不良反应比较(例,%)
培美曲塞为抗代谢类抗癌药物,其主要通过影响肿瘤细胞中DNA和RNA合成,使细胞分裂停止于S期,从而抑制肿瘤细胞的生长。其作用于与叶酸合成有关的多种酶,是1种新型的多靶点抗叶酸制剂。许多相关临床研究已经证实培美曲塞对肺腺癌疗效优于其他第三代化疗药物[11],目前是肺腺癌的一线药物。
晚期复发进展的肺腺癌治疗目标是改善生活质量,延长生存期,治疗的毒副反应要在可耐受范围。本研究中,对于一线EGFR-TKIs治疗后耐药缓慢进展的患者,二线应用EGFR-TKIs序贯培美曲塞,客观有效率达到46.67%,疾病控制率86.67%,而单药培美曲塞的客观有效率16.67%,疾病控制率73.33%,继续EGFR-TKIs治疗的客观有效率13.33%,疾病控制率66.67%,提示序贯联合治疗比单药治疗可获得很好的近期疗效。但序贯治疗组中位无进展生存时间5.2个月,中位生存时间9.0个月,单药培美曲塞组中位PFS和中位OS分别是4.3个月和8.5个月,继续EGFR-TKIs组中位PFS和中位OS分别是4.5个月和8.0个月,三组比较未见明显差异,序贯组未有生存获益。3种治疗方式的不良反应大多在Ⅰ~Ⅱ期,患者均能很好耐受。化疗药的胃肠道反应及骨髓毒性反应较靶向药明显,而靶向药的皮疹也要引起临床关注。
有研究显示[12],EGFR-TKI耐药的患者,其EGFR T790M突变率为62%,且90% T790M突变的患者,疾病进展多表现为局部进展和缓慢进展,少数出现新的转移灶,这类患者继续应用TKI,中位生存时间也较无T790M突变的患者要长,预后更好。本研究中进展后患者均再行EGFR T790M等基因检测,和性别、吸烟史等作为多因素分析,原本期望筛选出有影响的预后因素,但因各样本数尚不够大,或因技术问题,EGFR T790M检测率不高,EGFR T790M阳性与否、EGFR其他靶点阳性与否对3种治疗的影响,未能做出分层分析,未能得出有意义的分析结果,有待于后续的更多研究来完善。
综上所述,本文结论是,EGER突变肺腺癌患者,TKIs治疗后耐药且缓慢进展,继续使用TKIs仍可获益,换培美曲塞化疗也是目前治疗选择,两者无论在近期疗效方面还是在生存方面,均未见明显差异。而换培美曲塞序贯TKIs联合治疗,疾病控制率高,但是否能进一步获益尚有争议。治疗的选择要根据耐药后EGFR及其他驱动基因的突变情况综合分析。耐药后再次做基因检测,找出耐药原因并有针对性地选择耐药后续治疗,如EGFR无突变,换化疗治疗,EGFR T790M阳性换三代TKI治疗,出现其他驱动基因阳性换其它靶向药物治疗、换免疫治疗等等,是今后研究的趋势。

