益肾降糖胶囊水提液澄清工艺的优选
黄燕,潘旭东,林雄,单丽
益肾降糖饮是福建中医药大学附属人民医院的院内制剂(批准文号闽药制字Z061060503),由制何首乌、赤芍、黄芩、玄参、地黄、黄芪等14味中药组成,具有滋阴养血、益肾通络之功效,用于糖尿病之肾虚气弱、阴血亏损、脉络瘀阻证。本品临床使用二十几年,经临床验证本方对于糖尿病肾病之蛋白尿,延缓糖尿病肾病的进展有较好的疗效[1]。因益肾降糖饮为合剂,未经任何澄清工艺,久置易产生大量沉淀,外观差,且药品体积大不易携带,液体制剂稳定性较差,容易酸败;故本试验拟将其剂型改为胶囊剂。相比其他固体制剂,胶囊剂具有掩盖药物不良气味和口味、服用方便、崩解快、溶出度高、吸收好、生物利用度高等优点,成为临床常用的剂型之一[2]。因胶囊填充剂量有限,服用量不可过大,故需对提取液进行澄清处理,尽可能去除杂质,保留适量的浸膏,要求较低的浸膏得率。处方中何首乌、赤芍为主要成分,二者的主要活性成分为二苯乙烯苷和芍药苷[3-5],因此,本试验于2018年4—6月以二苯乙烯苷、芍药苷含量及干浸膏得率为澄清工艺优选的评价指标,比较壳聚糖澄清与醇沉的澄清效果,优选较佳的澄清工艺,为益肾降糖胶囊的工业化生产提供依据。
1 仪器与试剂
1.1 仪器 Ulit Mate-3000型高效液相色谱仪(戴安中国有限公司);赛多利斯CPA-225D型电子分析天平(赛多利斯科学仪器有限公司);中佳SC-3614型低速离心机(安徽中科中佳科学仪器有限公司);KQ-500DE型数控超声波清洗机(昆山市超声仪器有限公司);电热恒温水浴锅(上海医疗器械五厂);RW20.DZM.n型悬臂式搅拌机(广州仪科实验室技术有限公司),DZF-6050型真空干燥箱(上海精宏实验设备有限公司)。
1.2 试剂芍药苷对照品(中国食品药品检定研究院,批号110736—200629);2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷对照品(中国食品药品检定研究院,批号110844—201512,含量以91.0%计);甲醇、乙腈为色谱纯,其余试剂为分析纯。制何首乌、赤芍、黄芩、山药等中药饮片均购自福建承创堂有限公司,经该院副主任中药师陈豪鉴定,均符合2015年版《中国药典》一部各饮片项下的规定。
2 方法与结果
2.1 芍药苷含量测定
2.1.1 对照品溶液的制备 精密称取芍药苷对照品适量,置25 mL容量瓶中,用甲醇稀释至刻度,摇匀,制成每1毫升含芍药苷0.392 mg的对照品贮备液。精密吸取上述溶液3 mL置25 mL容量瓶中,加甲醇稀释至刻度,摇匀,配制成每1毫升含芍药苷47.04 μg的溶液
2.1.2 供试品溶液的制备 精密吸取益肾降糖胶囊内容物制成的澄清液2 mL,置25 mL容量瓶中,加50%甲醇稀释至刻度,摇匀,即得供试品溶液。
2.1.3 阴性供试品溶液的制备 精密吸取缺赤芍的供试品澄清液2 mL,置25 mL容量瓶,加50%甲醇稀释至刻度,摇匀,即得阴性供试品溶液。
2.1.4 色谱条件与系统适用性试验[6-8]色谱柱:AccLaim 120 C18柱(4.6 mm×150 mm,5 m);流动相:乙腈-水(19∶81);流速:0.8 mL/min;检测波长:230 nm;柱温:30 ℃,进样量:10 μL。理论板数按芍药苷峰计算应不低于3 000。分别取对照品溶液、供试品溶液、阴性供试品溶液,按上述色谱条件进样10 μL,记录色谱图,结果表明,在与对照品溶液色谱相应位置上,供试品溶液中芍药苷与其它组分分离度良好,阴性供试品溶液无干扰,见图1。
2.1.5 线性关系考察 取2.1.1项下配制的对照品贮备液,分别配制成浓度为31.36、47.04、62.72、78.40、94.08 μg/mL对照品溶液,按上述色谱条件,依次进样,分别测定两次,记录芍药苷的峰面积,以芍药苷浓度(X)为横坐标,峰面积(Y)为纵坐标绘制标准曲线,得回归方程Y̑=0.257 1X+1.156 0(r=0.999 6),表明芍药苷在31.36~94.08 μg/mL范围内与峰面积成良好的线性关系。
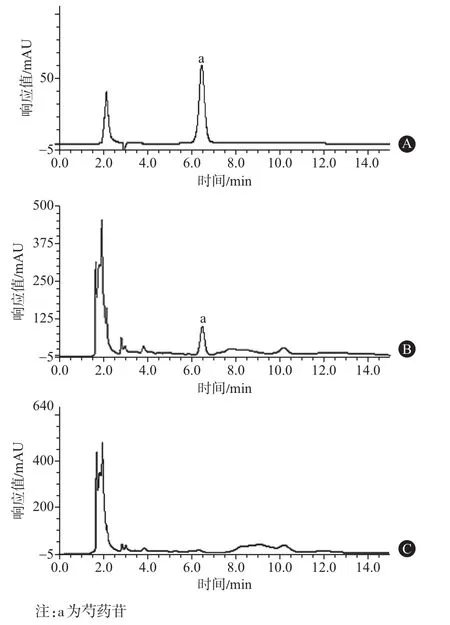
图1 各种溶液的高效液相色谱图:A为对照品;B为供试品;C为阴性供试品
2.1.6 精密度试验 精密吸取2.1.1项下的对照品溶液,重复进样6次,每次10 μL,记录芍药苷的峰面积,并计算相对标准偏差(RSD)为0.08%(n=6),表明精密度良好。
2.1.7 重复性试验 取同一批次样品,平行制备6份供试品溶液,按上述色谱条件测定芍药苷峰面积,RSD为1.82%(n=6),表明该方法重复性良好。
2.1.8 稳定性试验 取同一供试品溶液,分别于0、2、4、6、8、12 h测定,记录芍药苷的峰面积,并计算其RSD值为1.33%(n=6),表明供试品在12 h内基本稳定。
2.1.9 加样回收率试验 精密吸取已知含量的样品溶液1 mL,平行操作6份,置25 mL容量瓶中,各精密加入已知含量的芍药苷对照品贮备液2.5 mL,并用50%甲醇稀释并定容至刻度,摇匀,即得加样回收率试验供试品溶液,按2.1.4项下色谱条件进行测定,计算回收率,结果见表1。
2.2 二苯乙烯苷含量测定
2.2.1 对照品溶液的制备 精密称取2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷对照品适量,置10 mL容量瓶中,加甲醇稀释至刻度,摇匀,得对照品贮备溶液;精密吸取上述溶液1.0 mL置50 mL容量瓶中,加甲醇稀释至刻度,摇匀,配制成每1毫升含二苯乙烯苷17.654 μg的溶液。
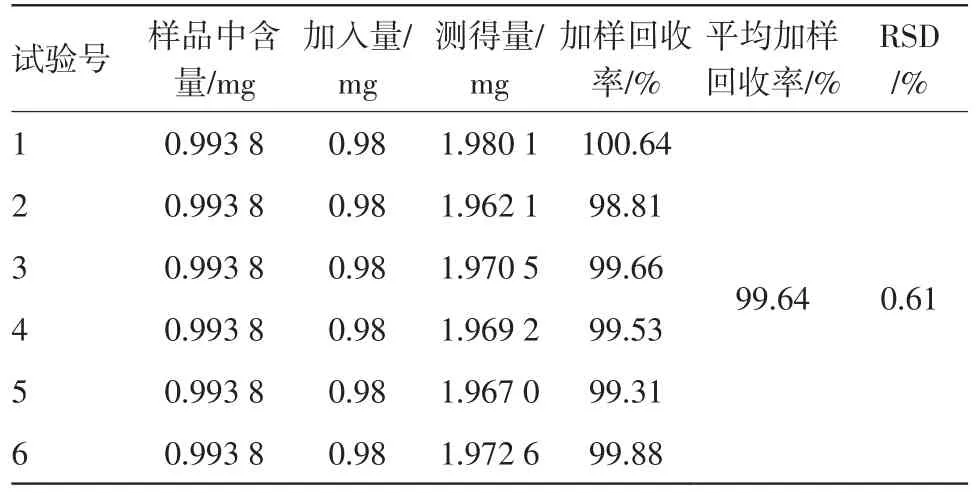
表1 芍药苷加样回收率试验结果(n=6)
2.2.2 供试品溶液的制备 取2.1.2项下的供试品溶液。
2.2.3 阴性供试品溶液的制备 精密吸取缺制何首乌的供试品溶液按2.1.3项下方法制备,即得阴性供试品溶液。
2.2.4 色谱条件与系统适用性试验[9-11]色谱柱:AccLaim 120 C18柱(4.6 mm×150 mm,5 m);流动相:乙腈-水(23∶77);流速:1.0 mL/min;柱温:30 ℃;检测波长:320 nm,进样量:10 μL。理论板数按2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷峰计算应不低于2 000。分别取对照品溶液、供试品溶液、阴性供试品溶液,按上述色谱条件进样10 μL,记录色谱图,结果表明,在与对照品色谱相应位置上,供试品溶液中二苯乙烯苷与其它组分分离度良好,阴性供试品溶液无干扰,见图2。
2.2.5 线性关系考察 取2.2.1项下配制的对照品贮备溶液,分别稀释成浓度为3.530 8、7.061 6、8.827 0、17.654 0、26.475 0、44.135 0 μg/mL的对照品溶液,按2.2.4项下色谱条件,依次进样,分别测定两次,记录二苯乙烯苷的峰面积,以二苯乙烯苷浓度(X)为横坐标,峰面积(Y)为纵坐标绘制标准曲线,得回归方程Y̑=0.581 5X+0.210 8(r=0.999 6),表明二苯乙烯苷在3.530 8~44.135 0 μg/mL范围内与峰面积呈良好的线性关系。
2.2.6 精密度试验 精密吸取2.2.1项下的对照品溶液,重复进样6次,记录二苯乙烯苷的峰面积,并计算其RSD为0.36%(n=6),表明精密度良好。
2.2.7 重复性试验 取同一批次样品,平行制备6份供试品溶液,按上述色谱条件测定二苯乙烯苷的峰面积,RSD为0.98%(n=6),表明该方法重复性良好。
2.2.8 稳定性试验 取同一供试品溶液,分别于0、2、4、6、8、12 h测定,记录二苯乙烯苷峰面积,并计算其RSD为1.12%(n=6),表明供试品在12 h内基本稳定。

图2 各种溶液的高效液相色谱图:A为对照品;B为供试品;C为阴性供试品
2.2.9 加样回收率试验 精密吸取已知含量的样品溶液1 mL,平行操作6份,置25 mL容量瓶中,各精密加入已知含量的二苯乙烯苷对照品溶液10 mL,并用50%甲醇稀释并定容至刻度,摇匀,即得加样回收率试验供试品溶液,按2.2.4项下色谱条件进行测定,计算回收率,结果见表2。

表2 二苯乙烯苷加样回收率试验结果(n=6)
2.3 益肾降糖胶囊提取液的制备按100 mL处方量称取药材,加8倍量的水,煎煮两次,每次1 h,药液过滤,合并滤液备用。
2.4 浸膏得率的测定取2.3项下的滤液,按以下各澄清工艺澄清药液,取澄清液,置干燥至恒重的蒸发皿中,水浴蒸干后,置真空干燥箱60℃干燥至恒重,移至干燥器中,冷却30 min,迅速称重。计算干浸膏得率(%)=干浸膏质量/药材质量×100%。
2.5 壳聚糖澄清工艺的优化
2.5.1 壳聚糖溶液的配制 称取10 g壳聚糖,加1%醋酸溶液1 000 mL,搅拌,静置使其充分溶胀,搅匀,即得1%壳聚糖溶液。
2.5.2 壳聚糖澄清水提液的制备 取2.3项下的滤液9份,分别将药液浓缩为药液比(药材质量:药液体积)1∶2、1∶4、1∶6的溶液各3份。
2.5.3 壳聚糖澄清工艺参数的筛选 参考相关文献[12-14],壳聚糖的澄清效果主要与药液比、壳聚糖加入量(每1克药材所需壳聚糖溶液的体积)、絮凝温度、搅拌时间、药液PH、搅拌速率、静置时间等因素有关,根据预试验结果,筛选A药液比、B壳聚糖加入量、C絮凝温度、D搅拌时间进行优化,选择L9(34)正交表设计试验,对2.5.2项下的9份提取液,按表3设计进行澄清工艺处理,将9份絮凝液室温静置24 h,离心(转速4 000 r/min,时间30 min),取上清液,将药液浓缩至100 mL,备用。以澄清液中芍药苷、二苯乙烯苷含量和浸膏得率为评价指标,采用综合加权评分法进行数据处理,三项指标权重系数分别为0.4、0.4、0.2;综合评分=芍药苷含量/芍药苷含量最大值×100×0.4+二苯乙烯苷含量/二苯乙烯苷含量最大值×100×0.4+最小浸膏得率/浸膏得率×100×0.2;满分为100分,综合评分值越大,表示澄清效果越好。试验安排及结果见表4,5。
2.5.4 统计学方法本试验正交设计选用L9(34)表头,采用正交助手ⅡV3.1分析软件进行数据分析,检验水准取α=0.05。

表3 澄清工艺正交试验因素水平表
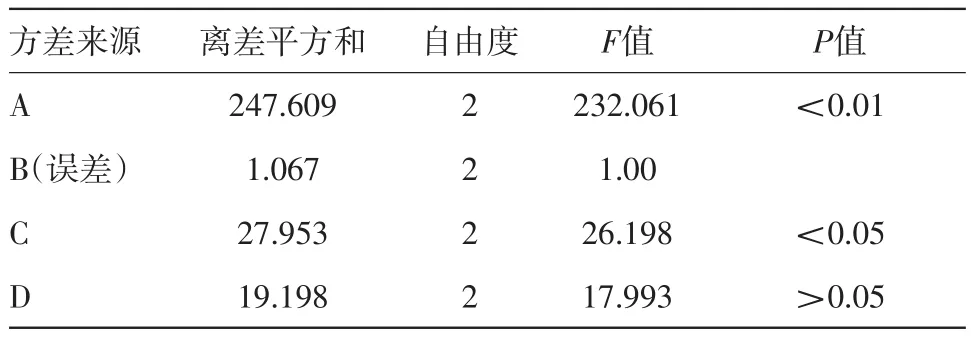
表5 综合评分方差分析结果
2.5.5 壳聚糖澄清工艺结果分析 本正交试验以芍药苷、二苯乙烯苷、浸膏得率为指标,进行综合评分。由各因素直观分析的K值高低可以得出影响絮凝效果的因素主次顺序为A>C>D>B,即药液比>絮凝温度>搅拌时间>壳聚糖加入量,最佳絮凝工艺组合为A1B1C3D3。以极差值最小的B因素为误差项进行方差分析,结果表明搅拌时间差异无统计学意义(P>0.05),药液比、絮凝温度对壳聚糖絮凝纯化工艺的影响均差异有统计学意义(P<0.01,P<0.05)[15]。
2.5.6 壳聚糖澄清工艺验证试验 按处方比例称取200 mL处方量药材,按2.3项下方法制得水提液,平行操作3份,按照最佳壳聚糖澄清工艺进行3次重复验证试验,测定芍药苷、二苯乙烯苷的含量及浸膏得率,结果分别为1.113 mg/mL、0.207 2 mg/mL、17.65%(RSD分别为0.59%、1.42%、1.82%,n=3),说明该工艺稳定可行。

表4 正交试验设计L9(34)与结果考察
2.6 醇沉工艺乙醇沉淀法能去除药液中的淀粉、树胶等多糖类和蛋白质等杂质,影响醇沉效果的主要因素有药液浓缩比(药材质量∶药液体积)和药液含醇量,故采用单因素试验对这两个因素进行考察[16-17]。
2.6.1 药液浓缩比的考察 取2.3项下的滤液3份,将药液分别浓缩至2∶1、1∶1、1∶2,加入95%乙醇,边加边搅拌,使药液含醇量为70%,药液静置24 h,离心(转速4 000 r/min,时间30 min),取上清液,将药液浓缩至100 mL。按2.1、2.2、2.4项下方法分别测定澄清液中芍药苷、二苯乙烯苷含量及浸膏得率,按2.5.3项下方法进行综合评分,结果见表6。

表6 药液浓缩比考察结果
表6结果表明:药液浓缩比为1∶2时,综合评分最高,因此选择药液浓缩比1∶2。
2.6.2 药液含醇量的考察 取2.3项下的滤液7份,将药液浓缩为1∶2,分别加入95%乙醇,边加边搅拌,使含醇量分别为50%、55%、60%、65%、70%、75%、80%,药液静置24 h,离心(转速4 000 r/min,时间30 min),取上清液,将药液浓缩至100 mL。按2.1、2.2、2.4项下方法分别测定澄清液中芍药苷、二苯乙烯苷含量及浸膏得率,按2.5.3项下方法进行综合评分,结果见表7。

表7 药液含醇量考察结果
表7结果表明:含醇量为70%时,综合评分最高,因此选择药液含醇量为70%。
2.6.3 醇沉工艺验证试验 按处方比例称取200 mL处方量药材,按2.3项下方法制得水提液,平行操作3份,将药液浓缩为1∶2,加入95%乙醇,边加边搅拌,使含醇量为70%,药液静置24 h,离心(转速4 000 r/min,时间30 min),取上清液,将上清液浓缩至200 mL,备用。测定芍药苷、二苯乙烯苷的含量及浸膏得率,结果分别为0.980 6 mg/mL、0.207 9 mg/mL、15.24%(RSD分别为0.78%、1.28%、1.22%,n=3),说明该工艺稳定可行。
2.7 最佳澄清工艺的确定将2.5.4与2.6.3项下两种工艺验证结果进行比较,壳聚糖澄清处理的样品芍药苷含量比醇沉工艺高13.5%,二苯乙烯苷的含量差别不大,但浸膏得率也高15.4%。壳聚糖澄清工艺不利于填充,可在后续成型工艺中优化,但在大规模生产中,若采取醇沉工艺,生产车间需要防爆设计,建造成本高,安全性能要求高。综合考虑生产成本、生产安全性,采用壳聚糖澄清工艺,具有更明显的优势,更适合医院制剂的发展,故最终确定益肾降糖胶囊水提液的澄清工艺采用壳聚糖絮凝澄清法,即药液浓缩比1∶2,在60℃絮凝温度,每1克药材壳聚糖加入量为0.4 mL,搅拌时间20 min。
根据最佳澄清工艺,100 mL澄清液可约得9 g干浸膏,初步设想浸膏∶辅料的比例为3∶1,采用95%乙醇制软材,过二号筛制粒,四号筛整粒,选择零号胶囊,每粒装0.5 g,可得24粒胶囊。后续具体工艺将在益肾降糖胶囊成型工艺研究中继续探讨。
3 讨论
本研究含量测定选择的指标为芍药苷、二苯乙烯苷,用于优化益肾降糖胶囊水提液的澄清工艺。益肾降糖胶囊由14味中药组成,成分复杂,芍药苷、二苯乙烯苷只是其众多有效物质的其中2种,以两种成分反映整个复方制剂的情况有一定的片面性。后续会在指标成分的选择上做进一步的研究,希望能更客观地反映整个复方制剂的情况。

