高效液相色谱法同时测定饮料中的5种添加剂
王林裴,周迎春,郑亚哲,张亚琼,李单单,华向美
(1.漯河海关,河南漯河 462000;2.启迪桑德环境资源股份有限公司,北京 101012)
食品添加剂是指为改善食品品质和色、香、味,以及为防腐和加工工艺的需要而加入食品中的化学合成或者天然物质[1]。近年来,随着食品工业的发展,食品添加剂使用频率越来越多,违规使用或超量使用食品添加剂问题也越频繁,食品质量安全问题也越来越受到各方的关注。
目前,我国允许使用的食品添加剂种类共23类,包括乳化剂、增味剂、防腐剂、抗氧化剂、着色剂等[2]2 000多种。尤其是饮料的加工制作过程中可允许加入的食品添加剂种类太多,这些添加剂大多没有营养价值,并且一旦这些添加剂使用量超标,会对人体健康造成危害[3]。例如,当摄入大量防腐剂时,轻则引起流口水、腹泻、肚子疼痛及心跳加快等症状,重则对肝脏、胃和肾脏造成严重影响,甚至增大患癌症风险[4];苯甲酸钠会在人体内反应生成苯甲酸而引起慢性苯中毒[5];食用大量的甜味剂(如糖精钠等),会影响肠胃消化酶的分泌,降低食欲。因此,检测食品中添加剂的含量对保障食品安全及维护消费者权益均有重要意义。
安赛蜜、糖精钠、苯甲酸、山梨酸、脱氢乙酸是5种常见的食品添加剂,国标没有规定同时检测这几种防腐剂、甜味剂的检测方法,而是针对不同的添加剂类别,其对应标准有3个[6-8],其样品处理方法不尽相同,过程繁琐复杂,样品量较大时,费时耗力效率低,因此建立一种可同时检测防腐剂、甜味剂的检测方法显得尤为关键[9]。
目前,已有的检测食品添加剂的方法有光度法[10]、电位滴定法[11]、毛细管电泳法[12-13]、液相色谱-质谱联用法[14-15]、气相色谱法[16]等,但是光度法、毛细管电泳法的灵敏度低、分辨率低、操作方法繁琐;气相色谱法虽然针对性较强,检测结果精确度较高,但没有广泛的使用范围[17];液质联用对试验条件要求较高;液相色谱方法[18-20]最为普遍,有效提升了检测灵敏度,有较好的分离度和准确度,在食品安全分析检测中应用广泛。
试验针对不同饮料的特点,建立高效液相色谱法同时快速测定饮料中常见食品添加剂的测定方法,将此方法应用于大批量的饮料检测中具有较高的检测效率、精密度和准确性,方法稳定可靠[21],也具有较强的实用性。
1 材料与方法
1.1 材料与试剂
菠萝啤、梨汁、水蜜桃汁,市售;乙酸铵(CH3CO2NH4,优级纯),国药化学试剂有限公司提供;甲醇(色谱纯),赛默飞世尔科技有限公司提供;安赛蜜标准溶液(DRE-C1001800)、糖精钠标准溶液(DRE-C16901010),Dr.Ehrenstorfer公司提供;山梨酸标准溶液 (BW900997-1000-L,1 000 μg/mL)、苯甲酸标准溶液 (BW900998-1000-L,1 000 μg/mL),坛墨质检标准物质中心提供;脱氢乙酸标准溶液(21680),北京曼格生物科技公司提供。
注:实验室用水是由Milli-Q Advantage A10系统制备的高纯水,所用容器使用前均用超纯水清洗晾干。
1.2 仪器与设备
Agilent 1290系列(DAD检测器) 高效液相色谱仪,美国安捷伦科技有限公司产品;Mill-Q Advantage A10型纯水器,美国Millipore科技有限公司产品;MS303S型分析天平,瑞士梅特勒-托利多科技有限公司产品;UV2600型紫外可见光分光光度计,岛津公司产品;超声仪,昆山市超声仪器有限公司产品。
1.3 溶液配制
1.3.1 流动相
溶剂A(0.02 mol/L乙酸铵溶液) 称取乙酸铵1.54 g,用水溶解,定容至1 000 mL容量瓶,经0.22 μm微孔滤膜过滤,超声脱气30 min;溶剂B为色谱纯甲醇。
1.3.2 亚铁氰化钾溶液
称取106 g亚铁氰化钾,加入适量水溶解,用水定容至1 000 mL。
1.3.3 乙酸锌溶液
称取220 g乙酸锌溶于少量水中,加入30 mL冰醋酸,用水定容至1 000 mL。
1.3.4 安赛蜜标准储备溶液(1 000 μg/mL)
准确称量安赛蜜标准品0.10 g用水溶解,定容至100 mL容量瓶。
1.3.5 糖精钠标准储备溶液(1 000 μg/mL)
准确称量糖精钠标准品0.10 g用水溶解,定容至100 mL容量瓶。
1.3.6 脱氢乙酸标准储备溶液(1 000 μg/mL)
准确称量脱氢乙酸标准品0.10 g用水溶解,定容至100 mL容量瓶。
1.3.7 5种添加剂混合标准中间溶液(50 μg/mL)
分别吸取安赛蜜、糖精钠、脱氢乙酸标准溶液储备液,以及山梨酸、苯甲酸标准溶液2.5 mL用水稀释定容至50 mL。
1.3.8 5种添加剂混合标准系列工作溶液
分别准确吸取混合标准中间液20,40,100,200,400,1 000 μL,加水定容至 1 mL,分别配制质量浓度为 1,2,5,10,20,50 μg/mL 的混合标准系列工作溶液。
1.4 试验方法
1.4.1 样品处理
称取约5.000 g样品于50 mL比色管中,加水约25 mL涡旋混匀,含二氧化碳样品置于超声清洗仪中超声处理20 min,不含蛋白质样品直接加水定容至刻度,含蛋白质样品分别加入5 mL亚铁氰化钾溶液,5 mL乙酸锌溶液,然后加水至刻度,混匀,以转速8 000 r/min离心5 min,将上清液收集经0.22 μm滤膜过滤,上机待测。同样方法作空白样。(注:不含蛋白的饮料可以不加如亚铁氰化钾和乙酸锌溶液)
1.4.2 色谱条件
色谱柱:Venusil ASB C18柱,4.6 mm×250 mm,5 μm;进样量10 μL,柱温35℃,DAD检测器检测波长230 nm,流动相A 0.02 mol/L乙酸铵溶液,流动相B甲醇,A∶B=95∶5,等梯度洗脱。
1.4.3 标准曲线
将配制好的混合标准系列工作溶液在1.4.2中色谱条件下进行分析,以混合标准系列工作溶液浓度为横坐标(X)、相应峰面积为纵坐标(Y),绘制标准工作曲线。
1.4.4 添加剂含量的计算
试样中不同添加剂的含量计算公式:

式中:X——试样中添加剂的含量,g/kg;
Co——空白样品中添加剂的质量浓度,μg/mL;
C——样品中添加剂的质量浓度,μg/mL;
V——试样稀释总体积,mL;
m——样品质量,g;
f——稀释倍数;
1 000——换算系数。
2 结果与分析
2.1 前处理方法的优越性
由于饮料中会不同程度地添加果胶、黄瓜胶、羧甲基醋酸纤维钠等添加剂来增加口感,因此对有些含乳饮料在前处理过程中需要沉淀蛋白,试验选择亚铁氰化钾和乙酸锌溶液作为蛋白沉淀剂。与国标不同的是,标准GB/T 23377—2009食品中脱氢乙酸的测定中,针对果蔬汁的测定中需要调节pH值,用固相萃取柱来提取,过程繁琐复杂;GB/T 5009.140—2003饮料中乙酰磺胺酸钾(安赛蜜) 的测定中,样品处理过程也需要用固相萃取柱上样、洗脱,过程繁琐。采用超声提取方法简单、便于操作,大大减少了前处理的时间,同时保证结果的准确性。由于这几种添加剂都易溶于水,且超声提取过程中可以加快分子运动,加速沉淀剂与溶剂之间的接触,促使某些成分脱附、溶解,加快提取过程,增大效率,经过多次试验分析得知,超声提取20 min即可满足加标回收率要求。
2.2 流动相的选择
比较了在水/甲醇及乙酸铵溶液/甲醇2种流动相体系下这5种添加剂的分离情况。
流动相乙酸铵/甲醇=90∶10见图1,流动相水/甲醇=90∶10见图2。
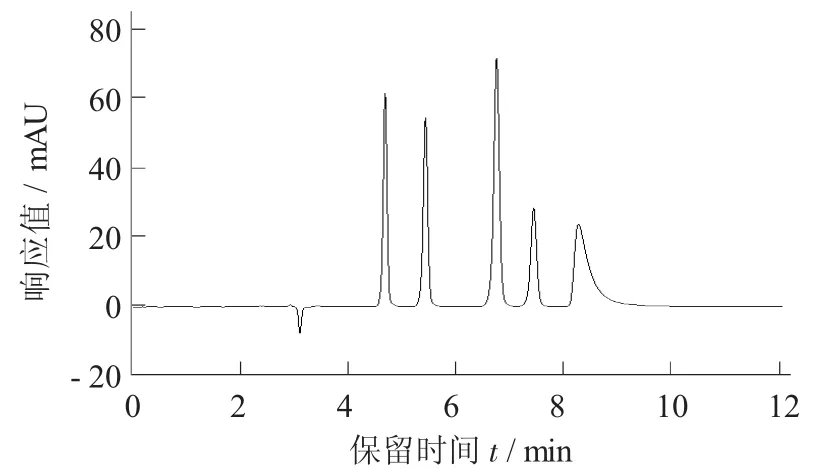
图1 流动相乙酸铵/甲醇=90∶10

图2 流动相水/甲醇=90∶10
由图1和图2可看出,乙酸铵/甲醇作为流动相时,分离效果较为理想。甲醇/水作为流动相时,各组分出峰较为密集,峰型较差,不能得到有效分离。而乙酸铵/甲醇作为流动相时,分离效果理想,且峰型尖锐且对称,与甲醇/水体系相比灵敏度也有所提高,因此选择乙酸铵/甲醇体系作为流动相。调整流动相比例来改善峰型及出峰时间,由分析可知,甲醇为10%时,这几种添加剂分离效果及峰型相对较好,因此确定流动相比例为乙酸铵∶甲醇=90∶10(V∶V)。
2.3 检测波长的选择
多种物质同时检测时,不仅要保证每种组分的灵敏度,还需定量方法简便。试验采用分光光度计在190~400 nm范围内对各组标准溶液进行光谱扫描,分析安赛蜜、糖精钠、苯甲酸、山梨酸、脱氢乙酸这5种添加剂的吸光度图谱可知,这5种组分的最大吸收波长依次为228,220,226,254,235.5 nm。为兼顾各组分的检测灵敏度,最终选择230 nm作为检测波长,此条件下绘制检测色谱图,可以完全分离,且分离效果较好。
5种添加剂的标准色谱图见图3。

图3 5种添加剂的标准色谱图
2.4 线性方程、检出限及混合标准溶液色谱图
将安赛蜜、糖精钠、苯甲酸、山梨酸和脱氢乙酸混标工作液液稀释成质量浓度分别为1,2,5,10,20,50 μg/mL混标溶液,分别进样 10 μL通过色谱条件来进行测定,以峰面积为纵坐标,各组分的质量浓度为横坐标绘制标准曲线。取标品逐级稀释进行检测,确定5种添加剂的检出限(以3倍信噪比计算,即S/N=3)和定量限(以10倍定量限计算,即S/N=10)。
5种食品添加剂的标准曲线见表1。
结果表明,各组分在线性范围内均有良好的线性关系,方法检出限为1.0~2.5 mg/kg,定量限为1.5~4.5 mg/kg。
2.5 方法精密度和重现性试验
准确称量7份空白样品平行试样,分别向其中加入等量混标溶液,使得各组混标溶液质量浓度为20 μg/mL,根据试验方法对样品进行处理后测定,以峰面积对取得的测定值进行表示。
方法精密度结果见表2。
经计算,得到5种添加剂的相对标准偏差为0.03%~0.29%,说明该方法准确可靠。

表1 5种食品添加剂的标准曲线
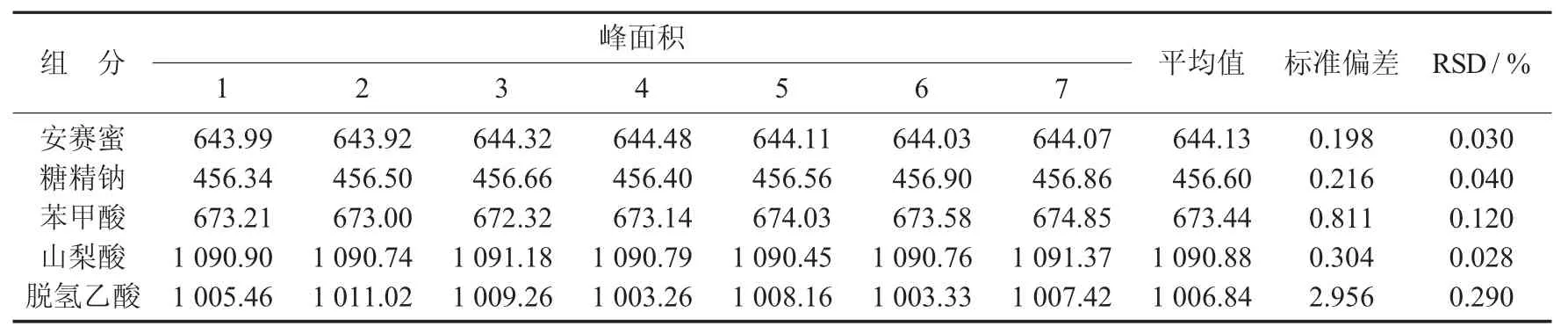
表2 方法精密度结果(n =7)
2.6 加标回收试验
以3种不同的饮料样品为基质,向其中加入5种添加剂混标溶液,做10 μg/mL和80 μg/mL 2个质量浓度水平的加标回收试验。
样品中5种食品添加剂的加标回收率见表3。

表3 样品中5种食品添加剂的加标回收率
由表3可知,5种添加剂在不同质量浓度水平的加标回收率分别为89.3%~94.2%,85.2%~93.8%,85.7%~92.4%,81.9%~92.5%,84.3%~90.0%,均满足国标GB/T 27404—2008中对回收率的要求。
2.7 方法准确度验证
采用饮料中安赛蜜定量分析质控样QC-FJ-705和果蔬汁中山梨酸、苯甲酸定量分析质控样QC-FJ-706来验证方法准确度.
实际样品测定结果见表4。

表4 实际样品测定结果/mg·kg-1
由表4可知,该方法对饮料中山梨酸和苯甲酸、安赛蜜测定结果能与标准值保持一致。与2.6部分加标回收率结果证明了该方法准确度较高,结果稳定可靠。
质控样QC-FJ-706的色谱图见图4,质控样QC-FJ-705色谱图见图5。

图4 质控样QC-FJ-706的色谱图

图5 质控样QC-FJ-705色谱图
2.8 实际样品测定
采用优化后的仪器条件和操作方法对当地抽取市售的15种饮料各3批次,分别进行5种添加剂含量的检测。
不同饮料中5种添加剂含量的测定结果见表5。

表5 不同饮料中5种添加剂含量的测定结果/g·kg-1
根据表5中测定结果,不同类别的饮料所含添加剂种类、含量有所不同。根据国家标准GB 2760—2014[1]中食品添加剂使用标准中规定,饮料类中安赛蜜最大使用量为0.3 g/kg;对于山梨酸及其钾盐的含量,乳酸菌饮料最大使用量为1.0 g/kg,饮料类最大使用量为0.5 g/kg;对于苯甲酸及其钠盐果蔬汁(浆)类饮料不超过1.0 g/kg,蛋白饮料不超过1.0 g/kg,碳酸饮料不超过0.2 g/kg,茶、咖啡、植物(类)饮不超过1.0 g/kg,特殊用途饮料不超过0.2 g/kg,风味饮料不超过1.0 g/kg;冷冻饮品中糖精钠含量不得超过0.15 g/kg;果蔬汁(浆)中脱氢乙酸含量不大于0.3 g/kg,被抽检饮料中所含这5种添加剂均在国标允许范围内添加,没有发现有超标使用情况。
3 结论
采用高效液相色谱检测法,可同时测定饮料中安赛蜜、糖精钠、苯甲酸、山梨酸、脱氢乙酸这5种常见的食品添加剂,检测结果准确、分析时间短,具有较高的灵敏度和准确度,且方法操作简单、实用性强,能够满足实际工作的需要,为食品监管部门、企业等检测机构提供技术支持。

