多囊卵巢综合征患者体质指数对体外受精-胚胎移植妊娠结局的影响
罗小琼 覃 莉 黄伟媚 韦敬锡 雷志英*
1.右江民族医学院附属医院(百色,533000);2.广西壮族自治州贵港市人民医院
多囊卵巢综合征(PCOS)发病率达5%~10%[1],可产生一系列代谢障碍,50.0%~60.0%患者体重超重或偏胖[2],体质量指数(BMI)>23 kg/m2的女性PCOS患病率增高[3-4]。肥胖不仅增加高雄激素血症,而且影响妊娠结局[5]。但超重或肥胖PCOS患者对体外受精-胚胎移植(IVF-ET)妊娠结局的影响研究较少,本研究回顾性分析了83例PCOS患者临床资料,分析BMI对妊娠结局的影响。
1 资料与方法
1.1 一般资料
收集2017年1月—2018年4月本院生殖医学中心接受IVF-ET治疗的POCS患者83例为研究对象,纳入诊断符合2003版鹿特丹POCS诊断标准[6]患者。排除标准:①疾病所致的雄激素增多症(如先天性肾上腺皮质增生症、库欣综合征等);②近3个月服用激素类药物;③遗传史;④反复流产史;⑤子宫内膜异位症、生殖道感染等可能导致流产相关疾病。
1.2 IVF-ET 治疗
所有患者月经或药物撤退性出血第3~5d开始口服达英-35片(德国先灵公司,每片含炔雌醇0.035 mg和醋酸环丙孕酮2 mg)1 片/d,连服21d,月经第18~22d给予短效促性腺激素释放激素激动剂-醋酸曲普瑞林注射液(丹东医创药业有限责任公司)皮下注射0.1 mg×20d,达降调标准后,根据患者年龄、体重、窦卵泡数使用促卵泡激素-注射用重组人促卵泡激素(长春金赛药业股份有限公司)112.5~225 IU 促排卵,结合血清性激素水平调整促卵泡激素用量。当直径≥18 mm卵泡数目占直径≥14 mm 卵泡数量的40%时,停用促性腺激素,当晚肌内注射绒促性素注射液(欧洲Merck Serono公司)10 000 IU,36~38 h 后阴道B 超引导下穿刺取卵,获卵后4~6h常规体外受精(IVF),16~18h观察受精卵情况,培养至48~72 h 后移植1~3 枚优质胚胎,以分裂卵裂球数目6~8个、碎片<20%胚胎为优质胚胎。移植后肌内注射黄体酮注射液(西南药业股份有限公司)支持治疗,剩余胚胎行玻璃化冷冻保存。胚胎移植后14d测定血绒毛膜促性腺激素阳性为生化妊娠,30d行阴道B超见妊囊者为临床妊娠。
1.3 基础性激素检测及随访
于月经2~4d (闭经≥2个月者任意1天)采集清晨空腹静脉血,美国雅培ARCHIITECT i2000SR电化学发光微粒子免疫分析仪及仪器配套试剂检测卵泡生成激素(FSH)、黄体生成激素(LH)、雌二醇(E2)水平。所有患者均随访至分娩或妊娠事件终止,统计妊娠率、流产、妊娠糖尿病等妊娠结局的发生情况。
1.4 统计学分析
2 结果
2.1 纳入对象一般情况
根据患者BMI分组,体重正常组(18.5kg/m2≤BMI<23.0kg/m2)25例(22.2±1.0 kg/m2),超重组(23.0kg/m2≤BMI<25.0kg/m2)36例(24.5±2.6 kg/m2),肥胖组(BMI≥25.0kg/m2)22例(26.0±4.2 kg/m2);3组年龄(26.8±5.6岁、25.0±6.9岁、26.4±5.0岁)、不孕时间(1.4±2.1年、1.4±2.3年、1.4±3.1年)比较未见差异(P>0.05)。
2.2 基础体温及基础性激素水平
促黄体生成素(LH)、促卵泡生成素(FSH)、雌二醇(E2)水平体重正常组均高于超重组、肥胖组(P<0.05),超重组与肥胖组比较无差异(P>0.05);基础体温各组间比较无差异(P>0.05)。见表1。

表1 各体重组基础体温及性激素水平比较
a与体重正常组对比P<0.05
2.3 促排卵情况对比
促卵泡激素使用天数肥胖组最多(P<0.05),但使用量3组未见差异(P>0.05);获卵数、受精数、优质胚胎数肥胖组均小于另外两组(P<0.05),种植率3组比较无差异(P>0.05),见表2。
2.4 妊娠结局对比
3组妊娠率比较存在差异(P>0.05);妊娠糖尿病患病率肥胖组高于另外两组(P<0.05),而体重正常组与超重组无差异(P>0.05),新生儿体重肥胖组>超重组>体重正常组(P<0.05),见表3。
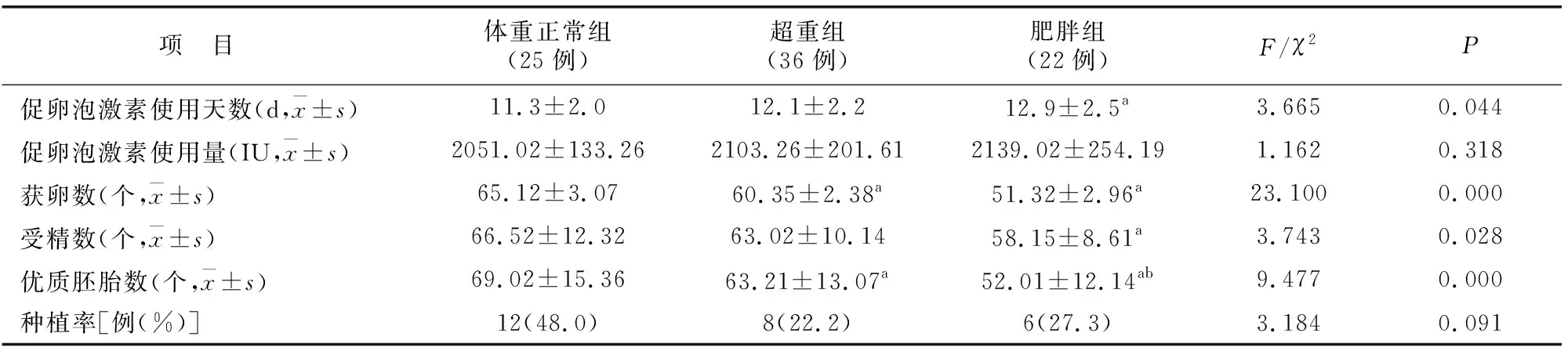
表2 各组促排卵情况对比
a与体重正常组对比b与超重组对比P<0.05

表3 各组妊娠结局及新生儿情况对比
a与体重正常组对比b与超重组对比P<0.05
3 讨论
PCOS患者临床表现存在多样性,但超重和肥胖是多数患者面临的问题。PCOS 的主要病理生理学基础是雄激素和胰岛素水平异常增高,肥胖、高雄激素、高胰岛素三者相互产生不良作用,互为因果。本研究PCOS超重、肥胖患者基础FSH 、LH、E2水平偏低,Beydoun[7]在其研究中也同样指出PCOS肥胖患者FSH水平低于体重正常患者,且随体质量指数的增高而降低,可见体重对PCOS患者性激素水平影响。分析原因可能为肥胖多伴胰岛素抵抗,导致高胰岛素血症,增强外周芳香化酶活性,增强雌激素作用,反馈抑制FSH释放。而缺乏FSH刺激的卵泡生长缓慢,发育不成熟,导致大量窦卵泡堆积,最终导致排卵障碍。
BMI对促排卵过程、卵泡及胚胎影响,本研究显示肥胖组促卵泡激素使用天数最高,获卵数、受精数、优质胚胎数最低,且优质胚胎数超重组少于体重正常组。曾晓霞[8]研究显示PCOS患者BMI越大,促卵泡激素使用量越大,使用时间越长,获卵数、优质胚胎数越少,直接影响体外受精-胚胎移植妊娠结局。Fedorcsak[9]也指出BMI与促卵泡激素使用量正相关,与获卵数负相关,提示肥胖可能降低促排卵过程中卵巢颗粒细胞对外界FSH的反应性[10]。
本研究显示BMI与PCOS患者种植率、孕周、流产率无关,与罹患妊娠糖尿病有关,肥胖组妊娠糖尿病患病率最高。Dokras[11]回顾性分析接受体外受精-胚胎移植肥胖患者的妊娠结局,结果显示肥胖并不影响临床妊娠率和活产率,但随着体重增加孕妇发生先兆子痫、妊娠期糖尿病、剖宫产等风险增高。原因可能为:PCOS 肥胖患者多存在胰岛素抵抗,妊娠期各种因素影响胰岛β细胞失代偿发展为妊娠期糖尿病[12],PCOS本身并不增加妊娠糖尿病发生风险[13],肥胖是根本原因。本研究显示肥胖组、超重组新生儿体重高于体重正常组,说明孕妇体质量过大可能是导致巨大儿的主要原因。 ALTIER[14]研究发现孕妇体质量指数过大与新生儿出生体重有关,肥胖是导致巨大儿的危险因素,分析原因认为,PCOS患者高糖血症导致胎儿处于高胰岛素血症环境中,蛋白、脂肪合成加快,脂肪降解减慢,进而导致胎儿过度发育。以上结果证实肥胖对PCOS患者IVF-ET治疗后妊娠结局有影响,临床上应重视肥胖PCOS患者生活方式,降低体质量对妊娠结局影响[15]。
综上,PCOS超重和肥胖患者在IVF-ET治疗中促卵泡激素使用时间较长,获卵数、受精数、优质胚胎数偏少,妊娠期间罹患糖尿病风险增加,新生儿体质量偏大,减少体质量可能改善IVF-ET妊娠结局。

