不同量表对短暂性脑缺血发作/缺血性脑卒中患者抗血小板治疗后出血风险的预测价值
何 伟 蒋文贤 王 琳 邓伟林 齐 立
(中国人民解放军联勤保障部队第九二四医院神经康复科,广西桂林市 541002,电子邮箱:19497510@qq.com)
对于短暂性脑缺血发作(transient ischemic attack,TIA)和缺血性脑卒中患者,常需在非急性期开始长期使用抗血小板药物治疗以预防疾病复发,然而抗血小板药物的使用使这些患者的出血风险大大增加,甚至会危及生命,因此采用适当的评估方式预测TIA和缺血性脑卒中患者使用抗血小板药物后的出血风险,对及时调整用药及促进患者康复有重要意义[1]。目前,用于评估TIA和缺血性脑卒中患者抗血小板治疗后出血风险的常用评分方法包括S2TOP-BLEED、REACH及颅内-B2LEED3S。这几种评分方式整合与出血风险相关的危险因素,并通过量表形式对出血风险进行量化评估,但这3种量表纳入的危险因素及评分标准有所差异,对不同疾病出血风险的预测价值也有所差异[2-3]。本研究旨在比较S2TOP-BLEED、REACH及颅内-B2LEED3S评分量表在TIA/缺血性脑卒中患者抗血小板治疗后出血风险中的预测价值。
1 资料与方法
1.1 临床资料 纳入2016年1月至2017年1月期间于我院就诊的TIA或缺血性脑卒中患者48例。纳入标准:(1)符合《中国急性缺血性脑卒中诊治指南2014》[4]中TIA或缺血性脑卒中的诊断标准;(2)首发患者,无前期治疗干扰;(3)处于非急性期,成功行溶栓、血管内介入等治疗;(4)影像学检查(CT、MRI)排除脑出血;(5)遵医嘱正确服用抗血小板药物治疗,治疗及随访依从性强。排除标准:(1)合并肿瘤、感染等非血管因素的患者;(2)合并严重心血管、肾、肺、造血系统等疾病的患者;(3)合并严重的心力衰竭、心律失常、意识障碍等伴随疾病的患者;(4)合并严重凝血障碍的患者;(5)病情危急,需急诊抢救的患者。
1.2 治疗方法 所有患者于成功溶栓24 h后开始口服阿司匹林(拜阿司匹林,拜耳医药保健有限公司,国药准字:J20130078;规格:100 mg×30片),100 mg/次,1次/d,并进行常规治疗,包括降压、降血糖、营养支持、神经营养及定期监测心脏功能。
1.3 治疗后随访 每个月进行1次门诊或电话随访,采用S2TOP-BLEED、REACH及颅内-B2LEED3S 3种量表进行评估。连续随访12个月,主要终点事件为出现大出血,大出血的判断标准为中枢神经系统、消化道、泌尿生殖道等部位出现较为严重的出血症状,输血量达两个单位以上,可伴发视力障碍;次要终点事件为缺血性脑卒中复发及死亡、心血管相关疾病入院或全因死亡。随访截止时间为2018年1月。统计随访截止时所有患者的出血情况并据此分组,其中出血组19例、非出血组29例;两组患者的一般资料差异无统计学意义(均P>0.05),见表1。
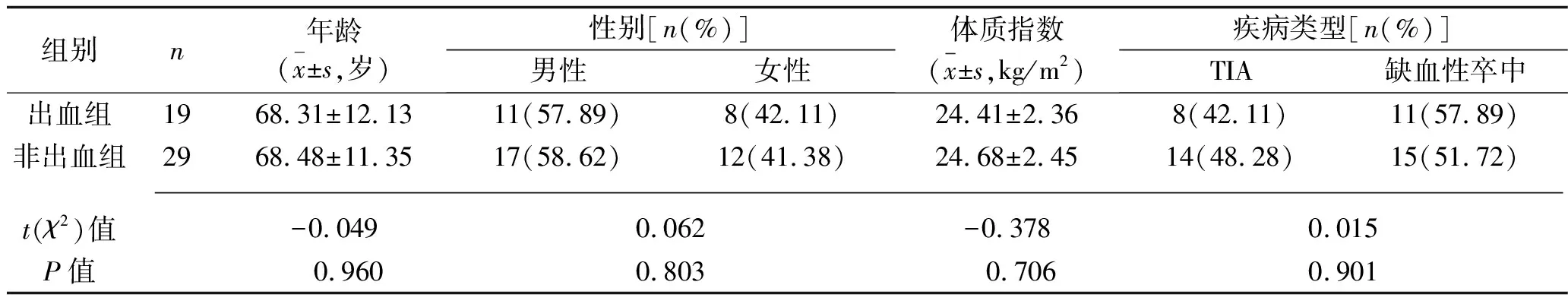
表1 两组患者一般资料的对比
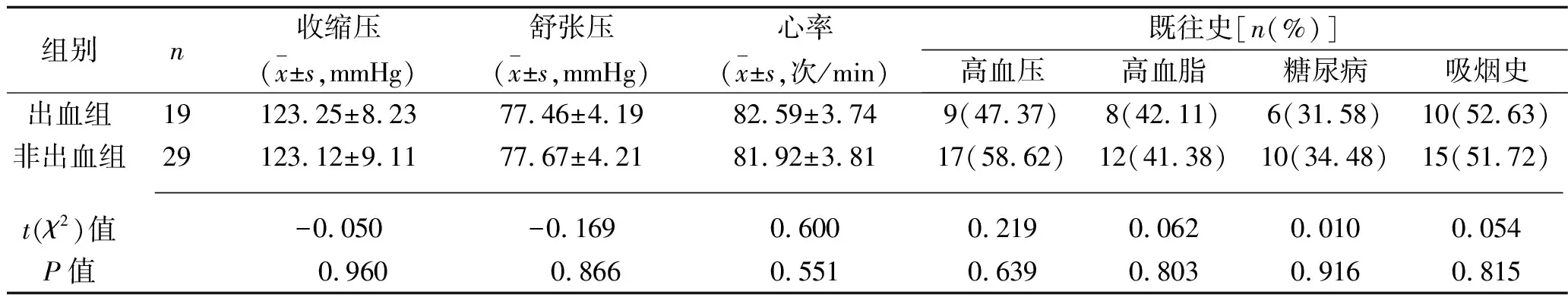
组别n收缩压(x±s,mmHg)舒张压(x±s,mmHg)心率(x±s,次/min)既往史[n(%)]高血压高血脂糖尿病吸烟史出血组19123.25±8.2377.46±4.1982.59±3.749(47.37)8(42.11)6(31.58)10(52.63)非出血组29123.12±9.1177.67±4.2181.92±3.8117(58.62)12(41.38)10(34.48)15(51.72) t(χ2)值-0.050-0.1690.6000.2190.0620.0100.054P值 0.960 0.8660.5510.6390.8030.9160.815
1.4 出血危险评估方法 患者出院时采用S2TOP-BLEED、REACH及颅内-B2LEED3S 3种量表进行评估。S2TOP-BLEED包括性别、是否吸烟、抗血小板药类型、改良Rankin量表结果、是否首次中风、血压、体质指数、老龄(>45岁)、种族和是否有糖尿病10项评估内容,总分0~28分[5];REACH包括年龄、是否吸烟、血压、血糖、血脂、周围动脉疾病、心衰、抗血小板和抗凝剂使用情况9项评估内容,总分0~24分[6];颅内-B2LEED3S包括年龄、性别、体质指数、亚洲种族、血压、心血管疾病、脑血管疾病、小血管疾病、双相抗血小板抗凝药物使用情况9项,总分0~13分[7]。所有量表分值越高提示出血风险的可能性越大。
1.5 统计学分析 采用SPSS 22.0软件进行统计分析。计量资料以(x±s)表示,组间比较采用t检验或t′检验;计数资料采用例数(构成比)表示,组间比较采用χ2检验。采用受试者工作特征(receiver operating characteristic,ROC)曲线评价患者出院时的3种量表评分对TIA/缺血性脑卒中患者抗血小板治疗后出血风险的预测效能,采用DeLong法比较曲线下面积(area under the curve,AUC)的差异,利用约登指数寻找最佳截点。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者出血危险评分的对比 出血组S2TOP-BLEED和REACH评分均高于非出血组(均P<0.05),但两组颅内-B2LEED3S评分差异无统计学意义(P>0.05)。见表2。
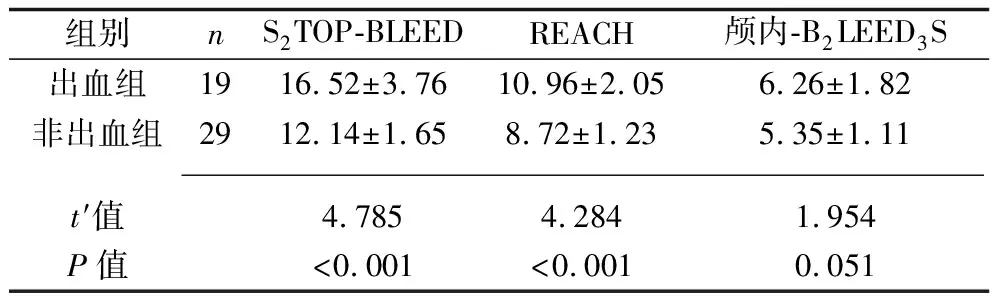
表2 两组患者3种量表的评分比较(x±s,分)
2.2 不同量表对TIA或缺血性脑卒中患者抗血小板治疗后出血风险的预测价值 S2TOP-BLEED、REACH、颅内-B2LEED3S量表预测TIA/缺血性脑卒中患者抗血小板治疗后出血风险的最佳截点分别为14分、11分、7分,其中REACH量表的AUC大于颅内-B2LEED3S量表(z=2.161,P=0.031),而S2TOP-BLEED量表的AUC均大于REACH和颅内-B2LEED3S(z=2.739,P=0.006;z=4.535,P<0.001)。S2TOP-BLEED量表的准确率、灵敏度、阳性预测值及阴性预测值均最高。见图1及表3。
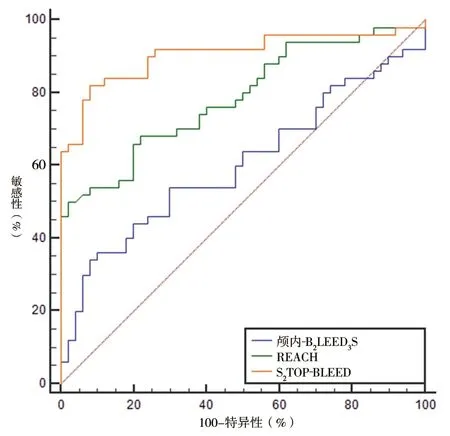
图1 不同量表预测TIA/缺血性脑卒中患者抗血小板治疗后出血风险的ROC曲线
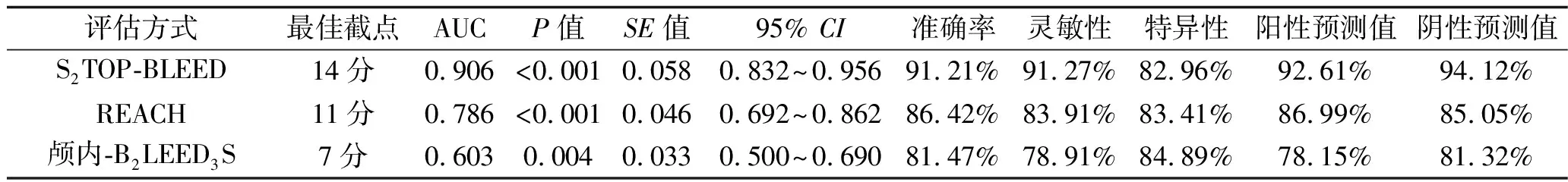
表3 不同量表预测TIA/缺血性脑卒中患者抗血小板治疗后出血风险的效能
3 讨 论
TIA和缺血性脑卒中患者使用抗血小板药物后的出血风险明显增加,这些出血事件明显增加TIA和缺血性脑卒中患者后期血管性疾病及死亡的发生[8]。出血风险增加与老龄、高血压、种族等多项危险因素有关[9],将这些影响出血风险的危险因素系统整合,构成出血风险的危险评分量表,可以对尚未出现出血并发症的患者进行风险预测,有利于临床酌情进行治疗方案的调整或加强预防措施[10]。
S2TOP-BLEED、REACH及颅内-B2LEED3S 3种量表评分方法在临床中均被用于TIA和缺血性脑卒中患者抗血小板治疗后的出血风险评估。3种量表都将与出血相关的危险因素作为评分项目,如年龄、吸烟、高血压、高血脂、抗凝及抗血小板药物使用情况等,但由于各自基于不同的人群和疾病模型,因此所涵盖的危险因素及各项目分值存在差异[11-13]。REACH评分是基于动脉粥样硬化人群模型形成的评估量表,强调了周围血管疾病和心脏疾病在出血风险中的价值[14]。颅内-B2LEED3S和S2TOP-BLEED评分均基于TIA和缺血性脑卒中模型形成,均在常见危险因素的基础上增加了种族和心脑血管疾病两个因素。颅内-B2LEED3S的分值采用二分类,较为简单,而S2TOP-BLEED是近年出现的一种危险评分,其不但基于多中心大规模TIA和缺血性脑卒中患者临床试验所得结果,并经过人群队列研究验证,而且在各项目分值上根据各危险因素的作用大小进行不同赋值[15-16]。
本研究结果显示,出血组S2TOP-BLEED和REACH评分均高于非出血组(均P<0.05),但两组颅内-B2LEED3S评分差异无统计学意义(P>0.05),提示S2TOP-BLEED和REACH评分均可用于预测TIA/缺血性脑卒中患者抗血小板治疗后出血风险。进一步行ROC曲线分析,结果显示,3种量表的AUC为0.603~0.906,对TIA/缺血性脑卒中患者抗血小板治疗后的出血风险均具有一定的预测作用,其中S2TOP-BLEED量表的AUC最大,准确率、灵敏度、阳性预测值及阴性预测值均最高,预测效能优于其他两种量表。Hilkens等[16]通过对大规模TIA和缺血性脑卒中人群进行队列研究,发现S2TOP-BLEED量表较其他量表有更好的预测出血风险的能力,与本研究结果类似。虽然3种危险评分都不同程度地涵盖了出血常见的危险因素,但各评分对于各项危险因素的具体定义及分值比例有所差异。在S2TOP-BLEED评分中,年龄(>45岁)作为一项重要评分指标被分为具体的五个梯度;由于高龄患者的出血风险明显高于年龄较低的人群,因此在S2TOP-BLEED评分中,高于65岁的各个年龄梯度所占的分数明显增加,这使得高龄这项重要的危险因素在出血预测中占据到较为重要的评估位置[17]。而REACH评分中虽然对年龄进行了分段评估,但各年龄梯度的评分分值成线性增加,无法体现高龄老年患者出血风险明显增加的这一重要因素[18]。同样,颅内-B2LEED3S评分将年龄分段截点简单定义在75岁,采用二分类评分,无法体现出高龄在出血风险预测中的重要价值[7]。此外,REACH评分的模型来自动脉粥样硬化患者,这类患者由于存在血管病变,本身即有较高的出血风险,但对于TIA和缺血性脑卒中患者并非均存在动脉粥样硬化病变,因此用该评分方式评估TIA和缺血性脑卒中患者的出血风险会降低预测效能[19]。
综上所述,与REACH及颅内-B2LEED3S量表相比,S2TOP-BLEED量表评分在预测TIA/缺血性脑卒中患者抗血小板治疗后出血风险中有较高应用价值,其中S2TOP-BLEED评分≥14分可作为判断这两类患者抗血小板治疗后出血风险高的参考指标。

