类风湿关节炎合并心血管损伤危险因素研究*
孙芳芳,张 静,范秀风
西安市第五医院(西安 710082)
类风湿关节炎属最常见的系统性自身免疫性疾病之一,流行病学调查发现类风湿关节炎患者人均寿命缩短 5~15年,其中合并心血管疾病的发病率及死亡率较正常人群明显增高[1]。国外报道类风湿关节炎患者心血管病变发生率达24.2%左右,而合并心血管病变是诱导其死亡的主要原因[2]。既往报道称类风湿关节炎患者心血管损伤风险增加,与传统心血管危险因素(如吸烟、高血脂、高血压、糖尿病等)有关[3]。近几年,有资料显示,类风湿关节炎患者全身性炎症反应及自身免疫改变,与其心血管损伤密切相关;此外,传统心血管危险因素与炎症之间存在密切关联,可能会产生协同效应,加重心血管负担,导致心血管损伤风险增加,但目前关于此方面的报道尚存在争议。基于此,本文主要纳入252例类风湿关节炎患者,开展回顾性分析,旨在探究类风湿关节炎合并心血管损伤的危险因素,现将结果报告如下。
资料和方法
1 一般资料 选择2016年10月至2018年10月于我院收治的252例类风湿关节炎患者为研究对象,开展回顾性分析,本研究获我院医学伦理委员会批准。纳入标准:①符合《类风湿关节炎诊治指南(草案)》[4]中类风湿关节炎诊断标准,关节及周围晨僵≥1 h(≥6周);近端指、掌指、腕关节区中有≥1个关节区肿胀(≥6周); ≥3个关节区软组织肿积液(≥6周);伴对称性关节炎(≥6周);存在类风湿结节;伴X线改变,如关节间隙狭窄、骨质疏松等;类风湿因子呈阳性;②年龄≥18岁;③入组前1周未接受非甾体抗炎药、生物制剂等治疗。排除标准:①伴严重肝、肾、肺、血液系统等原发性疾病;②伴各种急慢性感染或其他传染性疾病;③在类风湿关节炎起病前已确诊伴心肌梗死或脑血管事件;④伴严重贫血、心衰等;⑤妊娠期及哺乳期妇女。252例患者中,男性59例,女性193例,年龄18~78岁,平均(51.37±12.48)岁。按照心血管损伤发生情况将所有患者分为A组(合并心血管损伤,84例)、B组(未合并心血管损伤,168例)。
2 研究方法
2.1 一般资料收集: 所有患者入院后均采集病史,统计性别、年龄、身体质量指数(Body mass index,BMI)、吸烟史、饮酒史、既往史(高血压史、糖尿病史、冠心病家族史等),分析实验室基础指标(心率、血压、血脂等),并统计关节外脏器受累数及自身抗体检测结果。
2.2 实验室指标检测: 所有入选对象均于入院后第2 d晨起由研究人员使用一次性真空采血管抽肘静脉血3 ml,3000 r/min离心15 min,取上清液后置入微量离心管中,保存于-70℃冰箱中待测。具体检测指标如下:①血压:采用90217型全自动无创性便携式动态血压监测仪(美国SPACELABS公司),测定收缩压(Systolicbloodpressure,SBP)、舒张压(Diastolicbloodpressure,DBP);②血脂:采用日立7600-110型全自动生化分析仪(日本日立公司),使用酶法检测总胆固醇(Total cholesterol,TC)、三酰甘油(Three acyl glycerol,TG)水平,以超速离心结合ALBK法检测低密度脂蛋白胆固醇(Low density lipoprotein,LDL-C)、高密度脂蛋白胆固醇(High density lipoprotein,HDL-C)水平,免疫比浊法检测血脂载脂蛋白A1(Apolipoprotein A1,apoA1)、载脂蛋白B(Apolipoprotein B,apoB)水平,上述试剂盒均购自中生北控生物科技股份有限公司;③免疫功能指标:采用BN prospec 全自动特定蛋白分析仪(美国德灵公司)及配套试剂,以速率散射比浊法检测免疫球蛋白G(Immunoglobulin G,IgG)、补体C3;④其他指标:同位素稀释液相色谱/质谱法测定血尿酸(Uric acid,UA),双抗体夹心酶联免疫吸附试验检测血清C-反应蛋白(C-reactive protein,CRP),同时采用SYSMEX XE-2100血细胞分析仪测定血小板(Platelet,PLT)计数、红细胞沉降率(Erythrocyte sedimentation rate,ESR),试剂盒均购自北京九强生物技术股份有限公司,操作方案严格参考仪器及试剂说明书。
2.3 相关自身抗体检测:采用乳胶凝集法测定类风湿因子(Rheumatoid factor,RF),间接免疫荧光法检测抗角蛋白抗体(Antikeratin antibody,AKA)、抗核周因子抗体(Antiperinuclear factor,APF),并采用酶联免疫吸附试验检测抗环瓜氨酸肽(Cyclic citrullinated peptide,CCP)抗体。结果判定[5]:①RF阳性:血清1∶20稀释后,肉眼见凝集,则判断为阳性;②APF阳性:荧光显微镜下观察视野5~10个,细胞质中见圆形或椭圆形均质荧光颗粒,且大小不等,则为阳性;③AKA阳性:荧光显微镜下见角质显现板层状或线状荧光则为阳性。另外,参考李笑峰等[6]推荐的方法行抗CCP抗体阳性判断。
2.4 类风湿关节炎患者疾病活动度判断:采用欧洲风湿病防治联合会推荐的类风湿关节炎疾病活动性评分系统(Disease activity score in 28 joints,DAS28),根据压痛关节数(Tender joint count,TJC)、肿胀关节数(Swollenjoint count,SJC)、患者疼痛程度评估目标模拟标尺(Visual analogue scale,VAS)、ESR计算,DAS28=(0.56×28TJC+0.28×28SJC+0.7×lnESR+0.014×VAS。
3 观察指标 统计患者一般资料,包括一般情况(年龄、性别、BMI等)、健康行为与生活方式(吸烟、饮酒)、既往史(高血压病史、糖尿病史、冠心病家族史等)、实验室检查指标(CRP、ESR、PLT等),分析类风湿关节炎合并心血管损伤危险因素。

结 果
1 影响类风湿关节炎合并心血管损伤的单因素分析 单因素分析结果显示,类风湿关节炎合并心血管损伤与BMI、骨折病史、TC、CRP、血小板(PLT)、DAS28评分、关节外脏器受累数、RF有明显相关性(P<0.05),见表1。
2 类风湿关节炎合并心血管损伤多因素Logistic回归分析 将上述存在差异的单因素作为自变量,按连续变量(BMI、TC、CRP、PLT、DAS28评分、关节外脏器受累数)及二分类变量(RF)赋值,纳入多因素Logistic回归统计分析,采用逐步回归方法筛选变量。结果显示,BMI、骨折病史、高同型半胱氨酸血症史、甲状腺疾病史、TC、CRP、PLT、DAS28评分、关节外脏器受累数、RF是类风湿关节炎合并心血管损伤的独立影响因素(P<0.05),见表2。
讨 论
既往报道指出,类风湿关节炎患者存在致心血管系统紊乱的危险因素,包括高龄、男性、吸烟、高血压、高胆固醇血症、糖尿病等。近年来,陆雯俊等[7]研究表明,类风湿关节炎是心血管损伤的独立危险因素,会增加动脉粥样硬化疾病发生风险;而类风湿关节炎高度活动性、血清学标志物、慢性炎症状态等因素易与患者心血管损伤密切相关。
本研究多因素Logistic回归分析显示,BMI是类风湿关节炎合并心血管损伤的独立危险因素,这与Tanaka等[8]研究结论一致。高BMI会增加普通人群心血管疾病风险,而低BMI相对具有保护性,但类风湿关节炎患者一旦出现低BMI(<20 kg/m2),其心血管损伤的发生风险反而较高,这可能与类风湿关节炎患者常缺乏身体活动,伴炎症通路激活,促使低肌肉量。
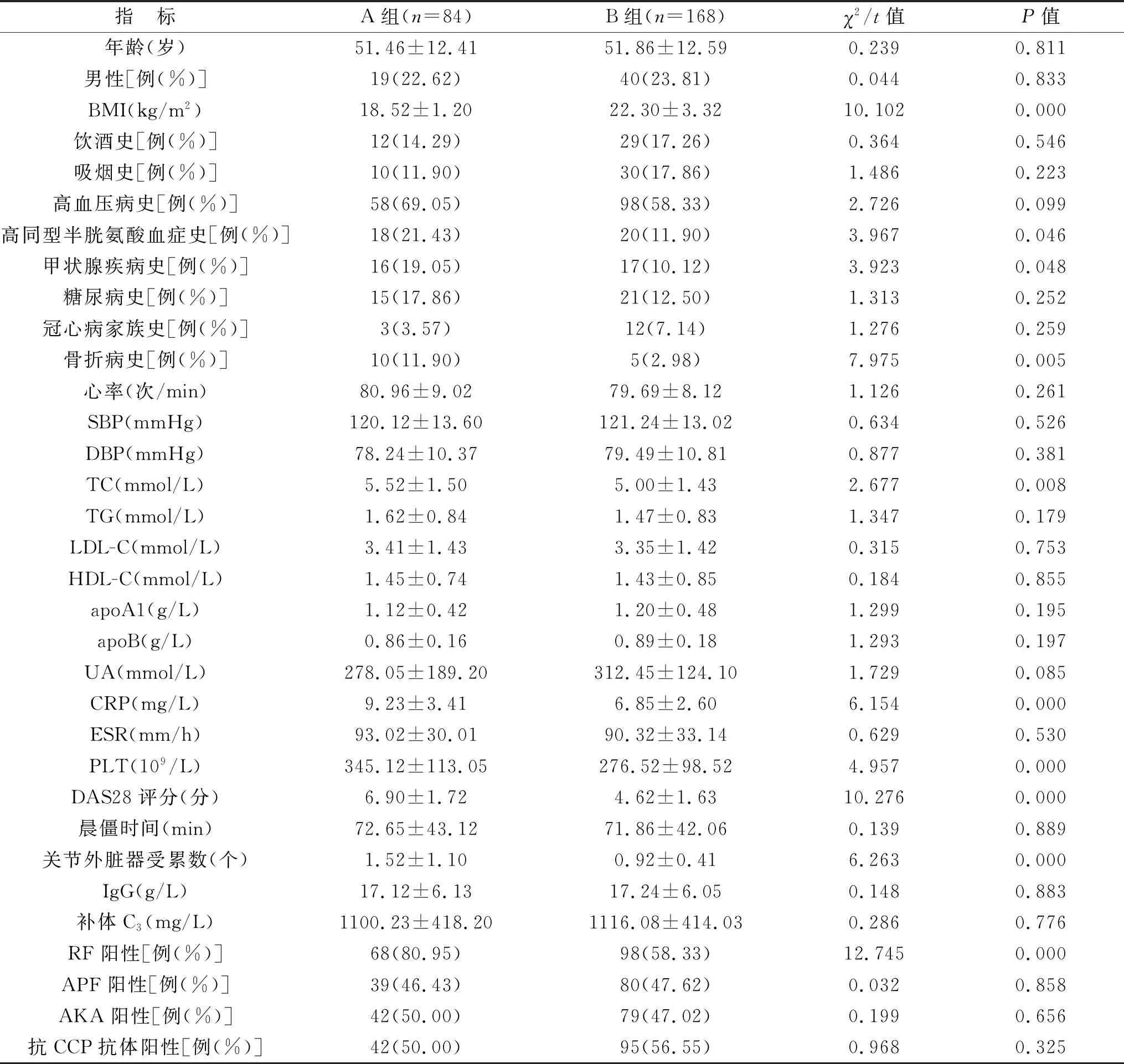
表1 影响类风湿关节炎合并心血管损伤的单因素分析
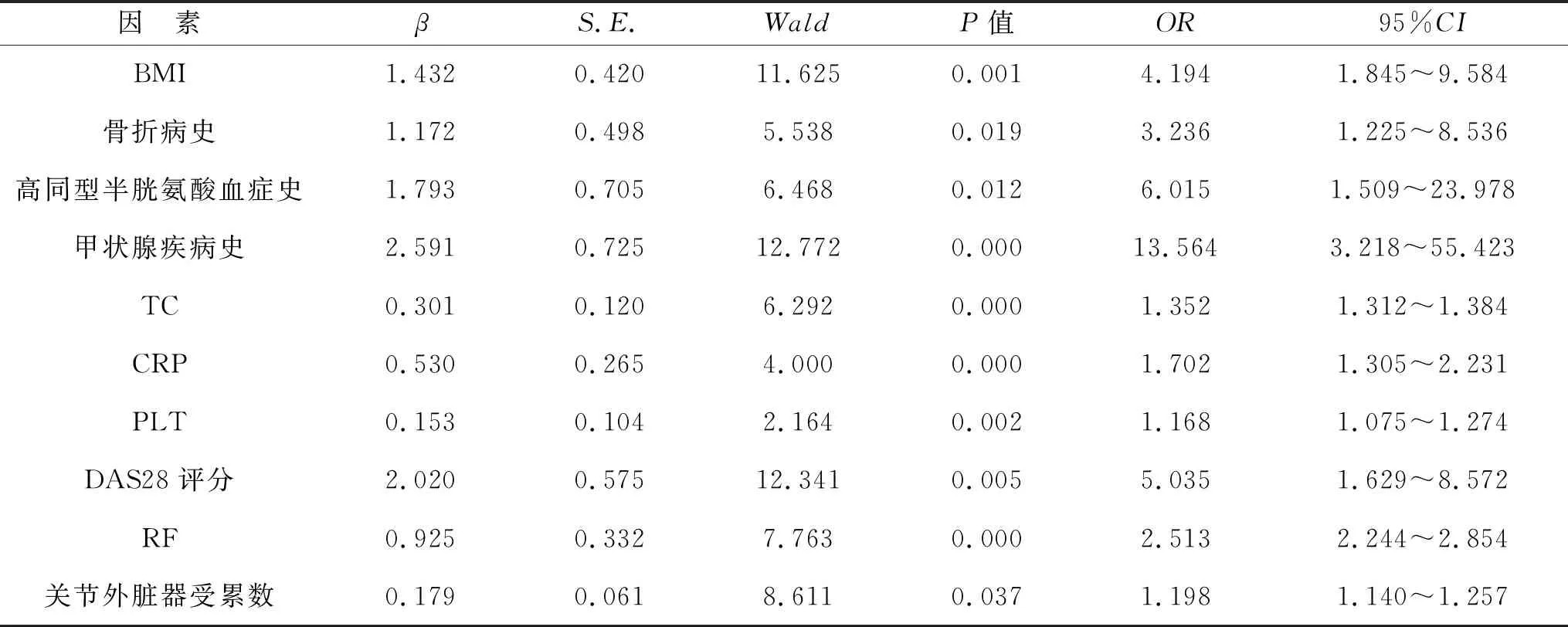
表2 类风湿关节炎合并心血管损伤多因素Logistic回归分析
高脂肪状态,即出现类风湿恶病质。一项Met分析结果证明类风湿关节炎患者中,低体质量指数与心血管损伤造成的死亡率明显相关,可能是已进展至风湿性恶病质。而研究表明,肥胖在类风湿关节炎炎症过程中起着重要作用,大约40%的类风湿关节炎女性患者患有代谢综合征,且这些患者均属典型腹型肥胖,与心血管传统危险因素密切相关。尤其是腹型肥胖,与类风湿关节炎患者胰岛素抵抗、代谢综合征、高血压、炎性负荷等因素相关。可见,肥胖和恶病质的类风湿关节炎患者是合并心血管损伤的高危人群。
本研究发现,DAS28病情活动性评分、骨折病史、RF是类风湿关节炎患者合并心血管损伤的独立危险因素,可能是由于类风湿关节炎患者患者病情活动与非特异性炎症反应有关,参与类风湿关节炎并发心血管损伤发病过程,而当患者发生骨折、RF呈阳性时,影响疾病活动度,容易诱发非特异性炎症反应,促进心血管损伤的发生。有资料显示,类风湿关节炎高疾病活动度时,患者心血管损伤发生风险明显增加,而患者疾病活动持续时间与心血管疾病风险呈正相关,这与本文研究结论相符。另有报道称随着类风湿关节炎疾病活动程度的不断增加,骨密度下降趋势加快,而控制类风湿关节炎疾病活动性,能预防患者骨密度下降,降低骨折发生率,证实骨折病史与患者并发心血管损伤密切相关。此外,有研究发现RF阳性的类风湿关节炎患者具有更强的疾病活动性,其心血管损伤发生风险高于RF阴性的类风湿关节炎患者,证实了本文结论。另外,本研究中,关节外脏器受累数目也被证实为患者合并心血管损伤的独立危险因素,可能因关节外脏器受累数目越多,患者颈动脉粥样斑块形成的发病率越高,而心血管损伤与动脉粥样斑块密切相关,故其易为患者心血管损伤危险因素。
本研究显示,TC是类风湿关节炎患者合并心血管损伤的独立危险因素,这与Sugimoto等[9]研究结论相符。研究表明,血脂异常在活动性类风湿关节炎患者中较为常见,发病极早期可能已存在血脂异常,但仅少数研究显示患者伴有动脉粥样硬化典型脂质改变。而目前已证实血栓形成、高凝状态与类风湿关节炎合并心血管损伤的发生密切相关,公认高胆固醇血症、小颗粒致密低密度脂蛋白水平升高均有致动脉粥样硬化作用。高娟等[10]研究发现,类风湿关节炎患者TG、TC、LDL-C 、HDL-C升高,在心血管损伤过程中发挥着重要作用。于高脂血症情况下,TC升高,会引起血管内膜功能性损伤,促使单核细胞、淋巴细胞、内皮细胞改变,增加黏附因子表达,促脂肪条纹进展为斑块,从而增加心血管损伤风险,这证实了本文研究结论。
本研究发现,高同型半胱氨酸血症史、甲状腺疾病史亦是类风湿关节炎合并心血管损伤的独立危险因素。究其根源,同型半胱氨酸可刺激免疫系统,诱导其发挥促炎作用,高水平炎症也可引起同型半胱氨酸水平上升;而类风湿关节炎患者往往存在高同型半胱氨酸血症,可能与接受甲氨蝶呤治疗相关,甲氨蝶呤属叶酸拮抗剂,会干扰同型半胱氨酸代谢。类风湿关节炎患者中甲状腺功能减退者心血管损伤风险更高,与血脂、高血压及血管内皮功能受损有关。另外,本研究结果显示,高血压并非是类风湿关节炎合并心血管损伤的独立危险因素,可能与多种机制(如基因多态性、抗风湿药物、炎症通路被激活等)参与类风湿关节炎患者高血压的发展有关。
本研究结果显示,CRP、PLT是类风湿关节炎合并心血管损伤的独立危险因素,提示病情活动和非特异性炎症反应与类风湿关节炎合并心血管损伤有关,这与Agca等[11]研究结论相符。类风湿关节炎属慢性炎性自身免疫性疾病,多表现为细胞及体液免疫失调、外周巨噬细胞和白细胞迁移等,而患者体内存在多种炎性细胞因子过度表达,可能参与血管内皮细胞损伤,在患者心血管疾病发病中起重要作用。目前炎性细胞因子造成心血管损伤的具体机制不明确,可能因为这些炎性因子(如CRP、IL-6等)作用于血管内皮细胞,引起血管内皮细胞高表达黏附分子,促使白细胞大量黏附,导致白细胞活化及“呼吸爆发”,氧自由基和过氧化氢等大量产生,引起内皮细胞损伤,诱导心血管损伤风险增加。其中,CRP属血管疾病危险评价因子,其浓度高低可反映疾病活动度。Castro等[12]研究发现,类风湿关节炎患者CRP、ESR、IL-6等炎症标志物与动脉粥样硬化的发生有关,其作用于脂肪组织、肝脏、骨骼肌、血管内皮等外周组织,致使动脉粥样硬化代谢功能改变,出现胰岛素抵抗、脂代谢紊乱、高凝活性、内皮功能障碍、氧化应激等,最终诱导患者动脉粥样硬化进展加速,心血管损伤加重。而PLT增高程度与患者病情严重程度呈正相关,多因病情活动期活化的滑膜细胞形成IL-2、IL-6等致炎因子,促进巨噬细胞增殖及成熟,诱导血小板生成,当滑膜炎症反应显著时,会促使巨噬细胞异常增殖,增加血小板异质性,大体积血小板增多。笔者认为,炎症使类风湿关节炎患者呈高凝状态,会加速动脉粥样硬化,斑块破裂风险高,心血管损伤风险增加。
综上,类风湿关节炎合并心血管损伤危险因素众多,包括BMI、骨折病史、TC、CRP、PLT、DAS28评分、关节外脏器受累数、RF,临床上应引起足够重视。但本文由于样本量偏小,可能存在抽样误差;Jafri等[13]称D-二聚体、TG水平升高也会增加类风湿关节炎患者并发心血管损伤风险,本文未涉及此方面,有待今后深入调查研究。

