慢消化淀粉的制备与检测及其在食品中的应用进展
孟丽维,朱慧静,王 贺
(浙江农林大学暨阳学院,浙江绍兴 311800)
0 引言
淀粉可以在各种淀粉酶的作用下酶解成葡萄糖等多种单糖,在日常活动中为人体供应能量。因淀粉有广泛的用途和低廉的价格,而且它在食品加工中具有增稠、保水和质地调节等优点,使得淀粉成为日常最普遍的食品原料。英国学者Englyst H N等人[1]在基于淀粉消化速度并且分解成葡萄糖时间的长短上,将淀粉划分为快速消化淀粉(RDS)、缓慢消化淀粉(SDS) 和抗性淀粉(RS) 3种类型。而SDS则是指实验室模拟体外消化条件(pH值5.2,温度37℃)下,在猪胰α-淀粉酶、糖化酶和转化酶等多种酶酶解20~120 min时样品水解得到的淀粉营养片段。SDS可以保持人体摄食后血糖的迟缓增加,血糖水平不会有较大的变化,并有利于糖尿病和心血管疾病等的医治[2]。
1 SDS的制备
淀粉颗粒形态有圆形、卵形和多边形,不一样品种来源的淀粉颗粒也会截然不同。经过物理、化学药品处理或酶法处理后,通过凝胶化和老化的过程可以破坏淀粉颗粒结构,从而获得一定量的缓慢消化淀粉。
1.1 物理法
物理法主要是通过高温高压处理来提高SDS含量的一种改性方法,主要的有热液处理、退火处理、辐射处理和挤压。该方法无化学试剂的残留、不使用酶制剂,是一种安全简便的改性方法。热液处理可分为韧化处理和湿热处理(HMT) 2种处理方法。HMT大多数是在较低水分条件下(≤35%) 和较高的温度(≥100℃)下的热处理过程,而韧化的条件是水分≥40%和温度小于糊化温度,二者的反应温度都高于淀粉转化成玻璃态的温度并低于淀粉糊化温度[3-4]。淀粉的湿热处理方法操作容易,在处理过程要求的只有水分含量和温度要求,湿热处理过程中影响淀粉性质显著的因素主要是水分含量、处理温度和处理时间。韧化处理的关键在于淀粉的高水分含量(60%或40%~55%) 和淀粉温度保持,这和HMT一样会导致淀粉糊化特性、颗粒结构和结晶性等的变化[5]。刘畅等人[6]用韧化的方法发现板栗淀粉的组织结构发生明显变化,SDS所含百分比随着韧化温度的上升而增加。
辐照处理是通过Ⅹ射线、γ射线等电离辐射的方式使得样品改性或加工的手段,辐射可以诱导样品发生相应的物理化学变化,从而使得样品的物理分子改变。Polesi L F等人[7]发现不论是生大米还是烹饪后的大米中SDS的含量都会随着辐照量的增加而增加。最新研究表明,螺杆挤压也被用来提高SDS含量,处理的原料有多种谷物及其混合物[8]。
1.2 化学法
化学修饰法是通过对淀粉进行酯化、交联、氧化、取代和接枝淀粉分子来实现,通过引入功能基团改变淀粉的糊化、凝胶和回生等功能特性。化学修饰法是研究生产中广泛使用的一种淀粉改性手段。大量研究表明,酸(如柠檬酸、盐酸、硫酸)通过与淀粉分子上的羟基发生酯化反应,可使淀粉分子量下降,进而提高SDS含量;酸处理的同时也会使聚合物链的柔性增大,促使其结构更加稳固,进一步提高其抵抗酶解的能力,即慢消化特性[9]。肖湘[10]用不同种类的酸依次处理绿豆淀粉,研究表明酸性热处理可以提高SDS的含量。此外,还有学者利用2-辛烯基琥珀酸酐制备SDS[11]。化学修饰法由于使用大量化学试剂,从消费者健康安全角度出发,对富含SDS的原料或加工制品的卫生安全性与营养效价更需要进行毒理学和临床试验。
1.3 酶法处理
酶法的作用原理是通过淀粉酶的酰胺化或水解作用来改变淀粉的分子结构[12]。该方法不仅具有产物消化性慢和血糖生成指数低的特点,还表现出安全性高、环境友好、特异性强、副产物少等优点。常用的酶制剂有普鲁兰酶、转糖苷酶、异淀粉酶、α-淀粉酶、β-淀粉酶、麦芽糖α-淀粉酶。既有使用单一酶修饰的,也有用2种及以上酶协同处理的[13],利用不同酶修饰制得的SDS含量也不同,不过复合酶修饰在制得的SDS含量和延缓消化特性方面表现更佳[14-15]。赵凯等人[16]将玉米淀粉酶脱支后发现淀粉各个时间段的温度都有不同程度的上升,相转变温度(PIT)的范围变窄,淀粉糊化后的焓没有较大的变化,淀粉的组织结构变得更加紧凑,从而产生了淀粉慢消化的特性。
1.4 复合处理
复合处理是指通过2种及以上方法协同处理,从而提高SDS含量的一种方法,如超声-酶法、微波处理-HMT、交联-酯化法。毕礼政[17]通过额外加入超声波处理来增加酶水解效率,这一方法不仅提高了SDS含量,也拓展了高含量SDS制备方法的范围。
2 SDS的测定
2.1 体外测定方法
2.1.1 Englyst法
Englyst法[1,18]的原理是基于SDS的定义需要在模拟体内环境的条件下,在20~120 min测定混酶消化淀粉的糖含量。其基本过程为:将0.8~4.0 g淀粉、50 mg瓜尔豆胶放入锥形瓶中,紧接着添加20 mL pH值5.2醋酸钠缓冲液,样品混匀后加入5 mL混合酶液(胰淀粉酶3 800 U/mL,糖化酶13 U/mL,转化酶190 U/mL),于37℃下水浴恒温振荡(160 r/min)反应20 min和120 min时立刻取0.5 mL上清液,用体积分数为66%乙醇20 mL进行灭酶处理,最后利用葡萄糖氧化酶-过氧化物酶来测定样品中葡萄糖的含量,样液需要检测3次后取平均值[1]。计算公式如下:
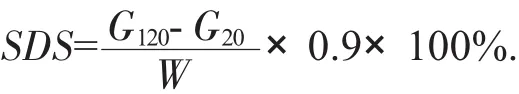
式中:
G20——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg;
G120——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg;
W——总淀粉量,mg。
2.1.2 Guraya法
Guraya法[19]的原理是在37℃条件下样品经过猪胰淀粉酶处理60 min,在相应时间水解后再将所产生的麦芽糖再用3,5-二硝基水杨酸(DNS) 处理,最后所得样液在波长540 nm处测定其吸光度,根据还原糖的含量计算出SDS含量。
取0.2 g样置于锥形瓶中,加入15 mL磷酸缓冲液(pH值6.89),混匀后加入1%29 U/mg猪胰α-淀粉酶,在37℃条件下水浴恒温振荡(160 r/min)反应一定时间后沸水浴2 min左右灭酶,之后经DNS法处理后用分光光度计在波长540 nm处测定还原糖含量,样液需要检测3次后取平均值[19],从而推算出慢消化淀粉含量。计算公式如下:
SDS=(G120-G20)×0.9×100%.
式中:G20——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg;G120——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg。
2.1.3 Miao法
Miao法[20]是在Englyst法的基础上做出改进,用葡萄糖试剂盒来代替葡萄糖氧化酶法,更加简化了试验操作。其基本步骤如下:称量200 mg样品置于反应容器中,添加15 mL pH值5.2醋酸钠缓冲液(0.2 mol/L),混匀后添加猪胰α-淀粉酶(29 U/mg)和糖化酶(15 U/mL)的混酶溶液10 mL,于37℃水浴恒温振荡器(150 r/min) 中反应20 min和120 min,取适量的上清液经过葡萄糖试剂盒处理后于波长510 nm处测吸光度,根据还原糖含量计算出SDS含量。计算公式如下:
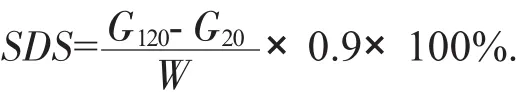
式中:G20——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg;
G120——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg;
W——总淀粉量,mg。
2.2 体内测定方法
Jenkins D J等人[21]于1981年第一次提出了血糖指数(Glycemic index,GI):摄入富有价值的碳水化合物50.0 g的食品后,在人体消化一段时间后(通常为2 h)人体内与摄取等量的白面包或葡萄糖在同样条件下,二者消化所表现出的血糖应答的百分含量,通常体内法和体外法都是测定慢消化淀粉含量的常用方法,但至今依然没有统一的、标准精确的定量测量慢消化淀粉方法,在大量慢消化淀粉体内试验后,发现慢消化淀粉的含量大小可以用增多血糖生成指数(Extended GI,EGI)来代替[2,22]。体内测定法是根据GI值来推算SDS含量,体外法是在实验室内模拟淀粉在人体内的情况,根据淀粉在酶的作用下20~120 min内水解所释放的葡萄糖量计算慢消化淀粉的含量。
挑选10名无病史的志愿者(男女各5人),先在10 h未进食的状态下测定血糖含量,再食用50.0 g淀粉样品(5 min内吃完)后,依次测定摄入淀粉后20 min时和120 min时的血糖含量,把葡萄糖作为标准对照组[23]来推算SDS的含量,公式如下:
SDS=(G120-G20)×0.9×100%.
式中:G20——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg;
G120——样品水浴振荡反应20 min时所分解所得的葡萄糖总量,mg。
2.3 SDS的测定方法比较
体外测定慢消化淀粉含量的方法见表1。

表1 体外测定慢消化淀粉含量的方法
Englyst法是采用3种酶的混合酶液来模拟淀粉样品进入到胃和肠道内被消化、酶水解成为葡萄糖的过程,同时又使用葡萄糖氧化酶法准确测定SDS含量,所以Englyst法测得的SDS的含量与体内法比较接近。其次,2种体外法所参与酶解的酶液相比Englyst法有所欠缺,水解后产生的物质不仅有葡萄糖,还有多种其他糖,如麦芽糖、糊精,而葡萄糖试剂盒法和DNS法都只能测出样品中还原糖含量,不能检测出全部的水解产物,但Miao法所用的酶更加接近Englyst法的酶,所以Guraya法测得的SDS含量与体内法相比较偏低。体内法是将人体作为研究对象,结果较为精准[24],但由于人体健康造成损伤和体内法较高的测试费,体内法作为常用的测定方法并不适宜。因此,4种方法中最适合用于测定SDS含量的方法是Englyst法。
3 SDS在食品加工中的应用
当前,追求健康和营养的均衡饮食已成为食品消费的新潮流。SDS具有特别的营养及代谢特性,高含量的SDS使得碳水化合物在人体内有规律及持续地吸收和释放,并最终获得适当的血糖和胰岛素应答,SDS还可维持饱腹感,降低饥饿感。因此,在食品中用适量的SDS取代面粉,这不会使食品的感官和品质有较大改变,还能赋予食品特定的功能特性。
SDS作为一种优质食品添加剂或功能配料可用于面包、饼干、披萨、薯条、发酵饮料、糖果、馅料、奶酪、冰激凌等食品的制作中。现今,商业开发成功的产品主要为饼干,如法国达能研发中心开发出了低GI和高SDS的EDP系列饼干、亿滋国际开发的belViTa焙朗早餐饼。目前,关于SDS在食品中的应用更多的研究还停留在实验室阶段。国内很多学者将不同来源淀粉制备得到的SDS开发制作饼干,鲜见有将其开发出面包产品的报道。国外围绕SDS在食品中的应用报道则较多。Agama-Acevedo E等人[25]发现曲奇饼干中添加了富含直链淀粉的香蕉淀粉后,其SDS含量增多。Román L等人[26]在研究制作面包时发现挤压香蕉淀粉不仅不会影响面包的感官,还会因其促进SDS的形成而使其表现出缓慢消化的特性。Giuberti G等人[27]研究指出面包中SDS生成量与添加的玉米淀粉(直链淀粉含量高)的比例呈正比,且血糖生成指数也逐渐变小,他们认为该款面包具有潜在的功能特性。Lu Z H等人[28]发现以胶囊化的豌豆淀粉制作的豌豆面包可以显著提高SDS含量(23.9%),远高于白面包(0.2%),并显示出良好感官品质和消费者可接受的风味。Martínez M M等人[29]报道了低水分面包更有利于SDS的生成,SDS含量的增加会提高面包的健康功能。
4 结语
近年来,国内外学者在SDS制备、检测分析等方面的研究取得了一定进展。SDS作为一种新型的食品资源,市场应用潜力巨大。将来,对兼具营养与功能的SDS研究会日益增多。研究重心应聚焦在SDS制造技术、SDS结构与生理功能及SDS在食品等领域的应用等方面。

