高效液相色谱间接紫外检测法测定甲醇和乙醇含量
张红医, 陈 跃, 马红玉, 李美婷, 何怡帆, 周 灿
(河北大学 a. 化学与环境科学学院; b. 化学教学研究所;c. 化学国家级实验教学示范中心, 河北 保定 071002)
0 引 言
就目前常用的分离检测技术而言,毛细管电泳或离子色谱主要使用水基缓冲液,因此被认为是绿色分离技术[1]。根据Welch等[2]的测算,一台配备了传统尺寸色谱柱的传统液相色谱仪器每天至少产生1 L的废液,并且这些废液中往往包含了较高含量的影响健康和环境安全的有机溶剂。据文献估计,世界上有13万台液相色谱仪正在使用[3],那么每年将产生3 400万L化学废液。
为了响应绿色化学的要求,围绕着减少液相色谱废液的产生、降低废液的处理费用,近年来绿色液相色谱分析法的研究日益得到重视。绿色液相色谱的一个突出的做法就是使用小内径,如UPLC(内径2.1 mm或1 mm)的柱子代替内径4.6 mm的传统液相色谱柱HPLC[4]。超高效液相色谱(UHPLC)不仅采用了更小内径的柱子,而且采用了更短的柱子,显著降低了分析时间,进而大大降低了分析过程中溶剂的消耗和废液的产生[5-6]。绿色液相色谱的另一个做法就是从液相色谱的流动相入手,例如:用乙醇代替乙腈做流动相[7-8]、过热水色谱(Superheated Water Chromatography)[9-10]、离子液体作为流动相改性剂或流动相[11-12]。
尽管如此,绿色液相色谱实验在本科生仪器分析实验课程及其实验教材中还没有得到应有的重视[13-14]。在我校自编的实验教材中,也只有一个实验涉及到了超高效液相色谱法[14]。本文在文献[15]的基础上,形成了一个适合本科生实验的绿液相色谱方法。该方法采用间接紫外检测法对溶液中甲醇、乙醇含量进行了测定。该实验的开设会带来如下三方面的好处。① 激励学生的学习热情。从方法上讲,该实验采用反相液相色谱间接检测法,其有别于目前常见的直接紫外检测法,会使学生有耳目一新的感觉。从检测对象来看,样品是生活中常见的酒品或生物燃料,会使学生感到一种亲近感。② 学会并掌握一种评价液相色谱流动相的环境评价标准(Environmental Assessment Tool, EAT)[16]的小程序,为其今后从文献中选择和评价液相色谱方法提供了一个新视角和新工具。③ 更重要的是该实验向学生们直接传递了可持续发展、绿色化学(Green chemistry)、绿色分析化学(Green Analytical Chemistry, GAC)[17]和绿色液相色谱法(Green reversed phase high performance liquid chromatography)[18]等先进的理念,以及化学工作者在推进绿色化学研究和应用中所应担负的社会责任。通过深入挖掘该实验中的“绿色、生态、环保”等与社会主义核心价值观相关的思想政治元素,在一定程度上起到了“课程思政”的育人作用[19]。
1 原理和实验
1.1 原理和程序
(1) 间接检测的基本原理[20]。间接光度液相色谱检测法一般是在流动相体系中加入一种在检测波长范围内具有较高吸收系数的试剂(称为紫外洗脱试剂),以形成高的紫外吸收本底。当样品引入到色谱柱内后,无紫外吸收的待测组分与紫外洗脱试剂发生相互作用或者在色谱柱上产生竞争保留,由于基流的变化而导致吸收信号的变化,产生组分色谱峰。间接光度检测时既会出现正方向色谱峰也会出现负方向色谱峰,一般符合表1所示的规律。

表1 间接光度法中的正负峰规律
(2) 液相色谱流动相环境评价标准原理和计算程序。Koller等[21]采用从不同数据库中提取的数据,充分考虑了物质的物理、化学、环境和安全性质计算出了安全因子S、健康因子H和环境因子E。在计算方法中,通过规定可替代的数据源,有效地解决了因物理、化学、或者毒性数据缺失所产生的制约因素。S,H和E数据可用于高度刻画和区分不同溶剂和化学品。
基于13种最常用的液相色谱有机溶剂,Gaber等[16]创立了一种简单工具(HPLC-EAT),该方法可以以计算得分的办法来识别所选HPLC方法的绿色性。HPLC-EAT 法可以计算从等度洗脱到三元梯度等不同运行模式下的不同流动相的HPLC-EAT指标量。当纯水流动相或含有改性剂(或者盐缓冲液)的水溶液做流动相时,因为有机溶剂的重要作用,因而将它们的S、H和E设为零
HPLC-EAT=S1m1+H1m1+E1m1+S2m2+
H2m2+E2m2+ … +Snmn+
Hnmn+Enmn
式中:S、H和E分别是Koller等所用的安全因子、健康因子和环境因子;n代表溶剂数目;m代表溶剂质量。HPLC-EAT计算程序和使用手册可以从下面网页的右侧区域免费下载:https://pubs.rsc.org/en/Content/ArticleLanding/2011/GC/c0gc00667j#!。divAbstract该程序的运行需要在Java环境下。
1.2 仪器与试剂
(1) 仪器。LC-20AD型高效液相色谱仪(岛津,日本),配有Diamonsil反相C18色谱柱(150 mm × 4.6 mm,5 μm,Dikma)、SPD-20A紫外/可见分光光度检测器(岛津,日本)、CBM-10A型在线工作站(岛津,日本),7725i手动进样阀(美国)及AT-330型色谱柱恒温箱;SKCH-10S超声波清洗仪(昆山超声仪器有限公司);SZ-93自动蒸馏水器(上海亚荣生化仪器厂)。
(2) 试剂。甲醇、丙酮均为色谱级试剂,乙醇为分析纯试剂,实验用水为双蒸水,实验样品为白酒和烹饪用生物燃料等。测试样品溶液和流动相使用前要经0.22 μm滤膜过滤。
1.3 实验步骤
(1) 样品溶液制备。醇基燃料:量取一定体积的样品,并定量转移到蒸馏瓶中进行水浴蒸馏,接收80 ℃以内的馏分。馏分直接进样分析,进样体积5 μL。白酒:过滤后直接进样分析,进样体积5 μL。
(2) 反相液相色谱条件的设定。流动相:丙酮/水(4 / 96),流速:0.8 ml/min,检测波长:233 nm,进样体积:5 μL,柱温30 ℃。
(3) 标准曲线制备。配制系列浓度混合标准工作液(乙醇:1%、5%、10%、20%、30%、40%、50%,甲醇:1%、3%、5%、10%、20%)进行反相高效液相色谱测定。以峰面积为纵坐标,标准溶液浓度为横坐标,通过Origin绘制工作曲线,得到线性回归方程、线性范围和相关系数等数据。
(4) 实际样品的测定。在相同的仪器条件下,测定样品溶液。用标准工作曲线对样品进行定量测定。
2 实验要点
2.1 流动相的优化
丙酮具有明显的紫外吸收,它在流动相中所占的比例对间接光度检测中起着决定性的作用。当以10%(体积百分数)的甲醇为样品,进样体积保持5 μL不变的条件下,对流动相中丙酮的百分含量进行研究。由图1可见,当丙酮含量较低时(2%)时,甲醇的峰面积也较低;当丙酮含量在3%~4%时,甲醇的峰面积达到最大;当丙酮含量高于4%后,甲醇的峰面积开始明显下降。因此,选择4%丙酮作为最优流动相。
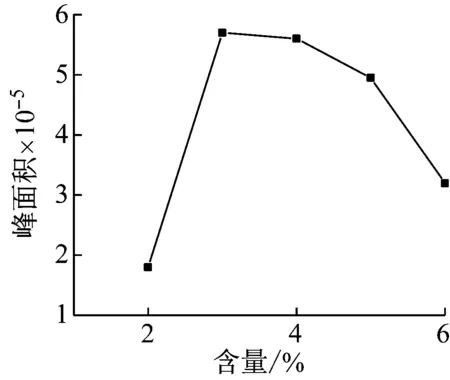
图1 甲醇峰面积随流动相中丙酮百分含量的变化
2.2 检测波长的优化
在丙酮与水体积比为4%的流动相条件下,考察了不同检测波长对甲醇的峰面积的影响。由图2可见,随着检测波长220~233 nm逐渐增大,甲醇的峰面积也逐渐增大。当检测波长在233 nm 和236 nm时,甲醇的峰面积基本保持不变。当检测波长在236~250 nm范围内依次变大时,对应的甲醇峰面积却逐渐降低。因此,选择233 nm 作为最佳检测波长。
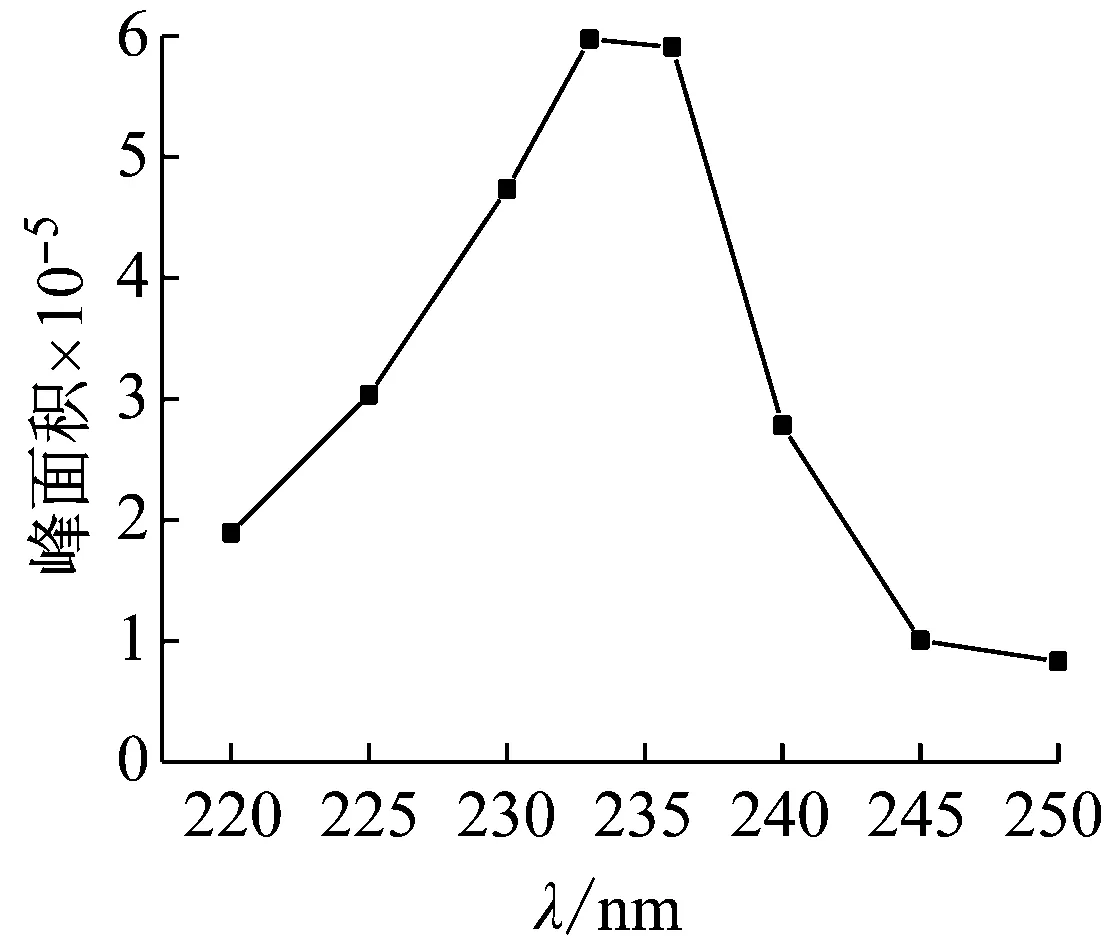
图2 甲醇峰面积随检测波长的变化
2.3 典型色谱图与样品分析
在最佳的色谱条件为:以丙酮/水(4/96,体积分数)为流动相,流速0.8 mL/min,检测波长设定为233 nm,进样体积为5 μL,色谱柱温度为30 ℃,将不同浓度的甲醇和乙醇标准溶液注射到色谱柱内进行色谱分析。甲醇和乙醇混合溶液的典型色谱图如图3所示。从图3可以看出,每个色谱图都有3个色谱峰,其中1#峰为甲醇峰,2#峰为乙醇峰,3#峰为系统峰。由于甲醇和乙醇以及作为紫外洗脱试剂使用的丙酮都不带电荷,且1#甲醇峰的保留时间短于3#系统峰的保留时间,2#乙醇峰的保留时间长于3#系统峰的保留时间,所以,甲醇应为正峰,乙醇应为负峰。系统峰有时为正峰,有时为负峰,但该峰的保留时间均在2.78 min。当只注射甲醇水溶液时,甲醇峰为正峰,而此时的系统峰为负峰。随着甲醇的浓度依次增大,甲醇峰将随之增大,而系统峰也将向着负峰方向逐渐增大。当只注射乙醇水溶液时,乙醇峰为负峰,而此时系统峰为正峰还是负峰,会受乙醇浓度的影响。当乙醇浓度小于1%时,系统峰为负峰;而当乙醇浓度高于1%时,系统峰为正峰[22]。
在最佳条件下,分别制作甲醇和乙醇的工作曲线。甲醇(正峰)和乙醇(负峰)的工作曲线分别为:
其中Y为峰面积,X为体积百分数。将取自某饭店的醇基燃料经蒸馏处理后,测得其蒸馏后乙醇含量为23.26%,甲醇的含量为4.90%。实验测得某品牌白酒为36%,其标示量为38%。图4为经处理后的含醇燃料的色谱图。
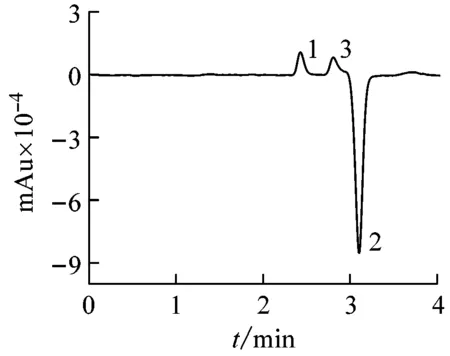
(a) 1% methanol + 2% ethanol
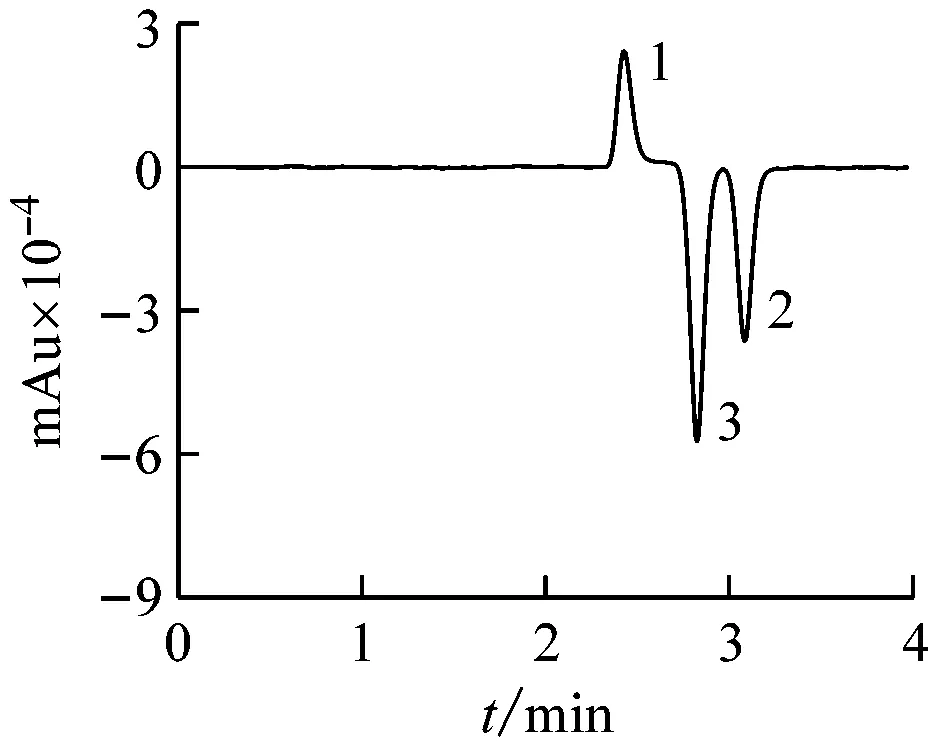
(b) 2% methanol + 1% ethanol
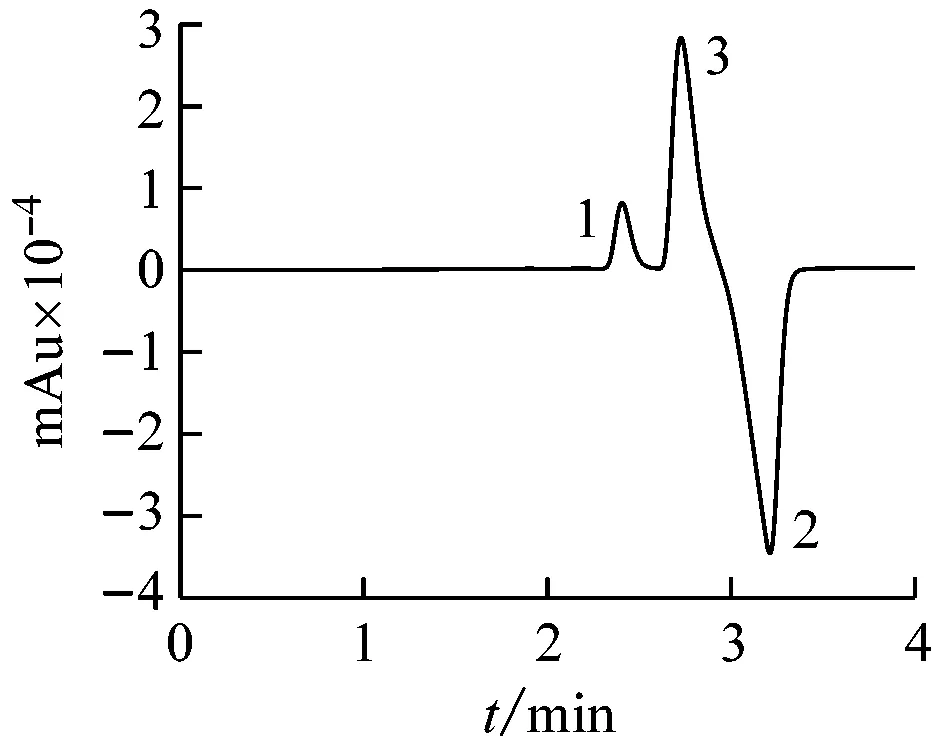
(c) 10% methanol + 20% ethanol
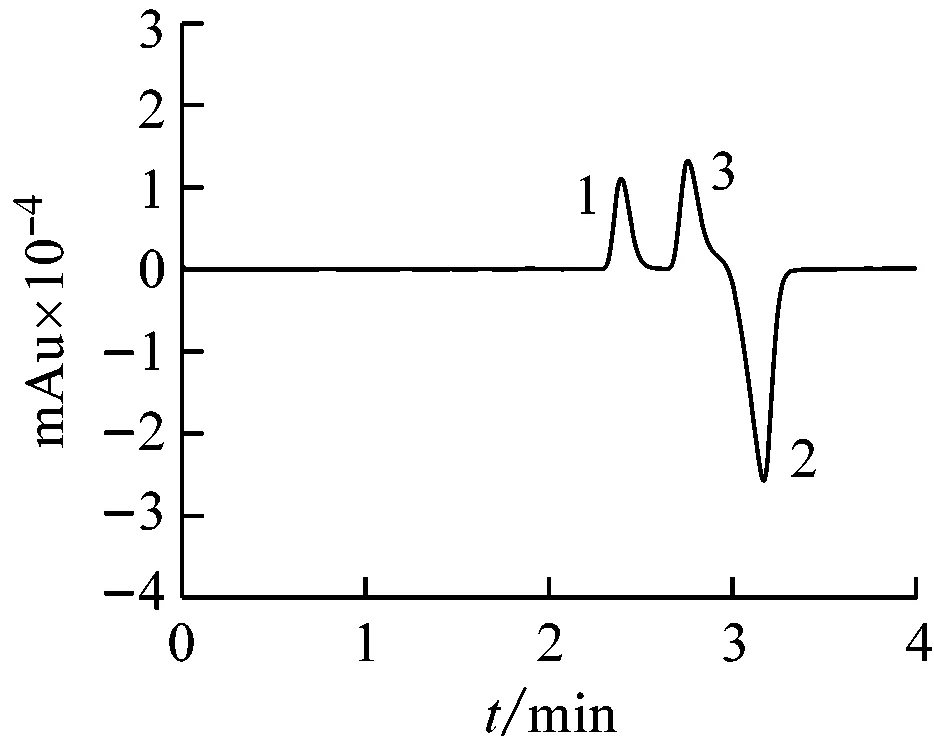
(d) 20% methanol + 10% ethanol
1—methanol; 2—ethanol; 3—system peak.
图3 不同甲醇和乙醇浓度所对应的液相色谱图
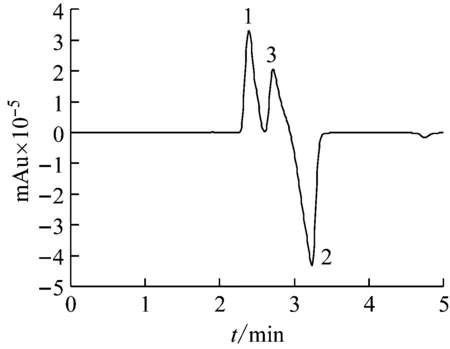
图4 经蒸馏处理后的生物燃料的典型色谱图
2.4 液相色谱流动相环境评价(EAT)的计算
通过Web of Science检索发现文献[23]是HPLC测定甲醇的最经典方法。该方法在HPLC分析前需要对甲醇进行衍生化处理,所用的流动相为正己烷-二氯甲烷 (9∶1)。用HPLC-EAT程序分别对本文所介绍的液相色谱流动相以及文献[23]的流动相进行EAT评价。由图5可见新方法的总EAT得分小于0.017 5,而文献[23]所对应的总EAT得分大于25。显而易见,从绿色化学的角度来看,本文所推荐的液相色谱法显著优于文献[23],而且本文的方法可以同时实现甲醇和乙醇的测定。
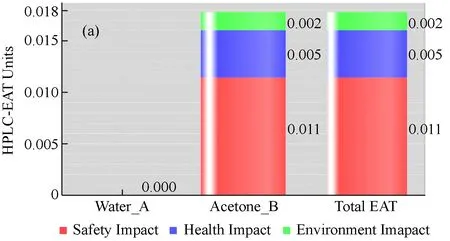
(a) HPLC Environment Assessment Chart
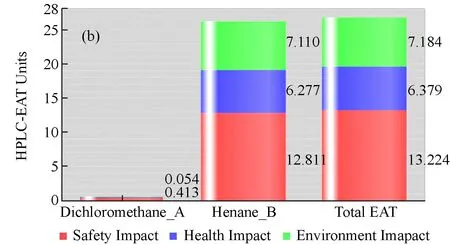
(b) HPLC Environment Assessment Chart
3 结 语
本文推荐了一个可用于甲醇和乙醇同时检测的绿色液相色谱分析法实验,该方法用4%的丙酮水溶液作为流动相。该流动相的EAT得分值小于0.017 5,其绿色指数显著优于测定甲醇的经典HPLC方法[23](EAT得分25)。它起到了对目前仪器分析实验中绿色色谱实验匮乏的一点弥补作用。从实验时间来看,该方法实验消耗少,分析时间短,可在4 min内完成,十分适合做本科生的实验。从实验内容看,间接光度检测丰富了学生对检测方法的全面理解,初步了解液相色谱中系统峰的概念。从实验的推广和实用性来看,可以让学生掌握HPLC-EAT程序的使用,掌握对液相色谱方法进行评价的一个新的指标,掌握一种测定白酒类和生物燃料中甲醇和乙醇的一种新方法。

