体质量指数正常的多囊卵巢综合征患者肥胖指标与糖脂代谢的相关性
董冰莹,那芷菁,焦娇,王秀霞
(中国医科大学附属盛京医院妇产科,沈阳 110022)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是育龄期女性最常见的一种内分泌紊乱性疾病,主要临床表现为稀发排卵或者无排卵、高雄激素血症或高雄激素体征、卵巢多囊样改变。PCOS的发病率为5%~10%,在中国育龄期妇女中发病率为5.6%,在排卵性不孕症患者中发病率高达70%[1-3]。已有研究[4-5]证实,PCOS与Ⅱ型糖尿病、血脂异常、高血压、肥胖、代谢综合征等代谢疾病相关,PCOS患者多伴有肥胖。目前研究认为,肥胖、高雄激素、胰岛素抵抗的恶性循环在PCOS的发生和发展中起重要作用。对于肥胖型PCOS患者,改善生活方式、控制体质量是一线治疗方法。而对于体质量指数(body mass index,BMI)正常的PCOS患者的糖脂代谢状态和管理国内外报道较少且结论不一[6-8]。临床上通常将BMI作为衡量PCOS患者是否肥胖的指标,近年来世界卫生组织推荐将体脂率(percentage of body fat,PBF)作为判定肥胖的新标准。PBF能准确反映人体内的脂肪含量,其结果较BMI更为精确。本研究旨在通过观察BMI正常的PCOS患者的糖脂代谢特点,分析肥胖指标BMI、PBF与糖脂代谢的相关性,为BMI正常的PCOS患者的代谢管理提供一定的理论基础和新的思路。
1 材料与方法
1.1 研究对象及分组
选取2017年6月至2018年2月间在中国医科大学附属盛京医院生殖医学中心就诊的BMI正常的PCOS患者90例作为研究组,选择同期就诊的年龄、BMI匹配且排卵正常的不孕症患者80例作为对照组。
研究组的入选标准:(1)18.5 kg/m2≤BMI≤24.9 kg/m2。(2)符合鹿特丹诊断标准,①稀发排卵或者无排卵;②高雄激素血症或者高雄激素体征;③超声检查提示单侧或双侧卵巢内2~9 mm卵泡数≥12个,和(或)一侧或双侧卵巢体积≥10 mL;④以上3项中符合2项并排除引起高雄激素血症的其他原因,如先天性肾上腺皮质增生、库欣综合征、分泌雄激素的肿瘤等。对照组的入选标准:(1)18.5 kg/m2≤BMI≤24.9 kg/m2;(2)卵泡期性激素检测正常;(3)23 d≤月经周期≤35 d,B超监测排卵正常。
所有研究对象均无发热及急性感染,并排除肝肾疾病、肿瘤、心脑血管疾病,无高泌乳素血症、甲状腺功能异常、子宫内膜异位症、卵巢早衰等疾病。至少3个月内未使用过任何激素类药物和(或)影响糖脂代谢的药物。本研究通过中国医科大学附属盛京医院医学伦理委员会批准。
1.2 方法
1.2.1 标本收集:研究对象于月经周期第3~5天采空腹12 h静脉血,分离出血清,测定空腹血糖(fasting glucose,FGLU)、空腹胰岛素(fasting insulin,FINS)和血脂浓度。
1.2.2 资料收集:行体格检查,获得身高、体质量、BMI和PBF。PBF测定方法:受试者在同一天上午,在空腹、膀胱排空状态下,采用人体成分分析仪进行体质成分测量。
1.2.3 生化指标检测:采用化学发光法,用全自动免疫分析仪测定FINS。采用酶法试剂盒,用全自动生化分析仪测定FGLU、总胆固醇(total cholesterol,TC)、甘油三酯(triglycerides,TG)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)。
1.3 统计学分析
采用SPSS 19.0软件进行统计分析。符合正态分布的计量资料以±s表示,采用独立样本t检验进行比较。计数资料以率(%)表示,采用χ2检验进行比较。预测性试验采用受试者工作特征(receiver operating characteristic curve,ROC)曲线分析,绘制ROC曲线并计算各指标对应的ROC曲线下面积、灵敏度和特异度。P< 0.05为差异有统计学意义。
2 结果
2.1 2组患者一般特征和糖脂代谢相关指标的比较
研究组PBF、TC、TG、FINS水平均高于对照组,差异有统计学意义(均P< 0.05),而LDL-C、HDL-C、FGLU水平的差异无统计学意义(均P> 0.05)。见表1。
2.2 2组患者代谢指标异常发生率的比较
研究组患者TC、TG、FINS水平异常发生率均高于对照组(P< 0.05),见表2。
2.3 肥胖指标预测BMI正常的PCOS患者出现FINS水平异常的价值
绘制BMI、PBF预测出现FINS水平异常的ROC曲线。研究组中,BMI、PBF对预测BMI正常的PCOS患者出现FINS水平异常具有参考价值(AUC=0.712,P=0.001;AUC=0.625,P=0.049),见图1。BMI预测BMI正常的PCOS患者出现FINS水平异常的最佳界值为23 kg/m2,其诊断的灵敏度为66.7%,特异度为70.2%;PBF预测的最佳界值为37.75%,其诊断的灵敏度为39.4%,特异度为87.7%。对照组中,BMI、PBF对排卵正常女性出现FINS水平异常不具有预测价值(P> 0.05)。
3 讨论
肥胖型PCOS患者糖脂代谢紊乱的发生率高达47.9%[3],肥胖型PCOS与代谢紊乱的相关性已被证实,而BMI正常的PCOS患者与糖脂代谢的相关性研究较少。ZOHRABI等[9]对30名来自印度的BMI正常的PCOS患者进行研究,发现BMI正常的PCOS患者
FINS水平显著高于对照组,其他指标无显著差异。TOLA等[10]的研究显示,来自哈萨克斯坦的34名BMI正常的PCOS患者其HDL-C、FINS、FGLU水平与对照组均有明显差异,但LDL-C、TG、TC水平无差异,这可能与PCOS的临床表现具有高度异质性有关,不同地域、种族之间会存在代谢差异。本研究对来自中国北方的BMI正常的PCOS患者进行了研究,结果显示,其PBF、TC、TG和FINS水平均明显高于对照组,这可能与中国北方人群女性的PBF较高、腹部脂肪堆积较多有关[11]。
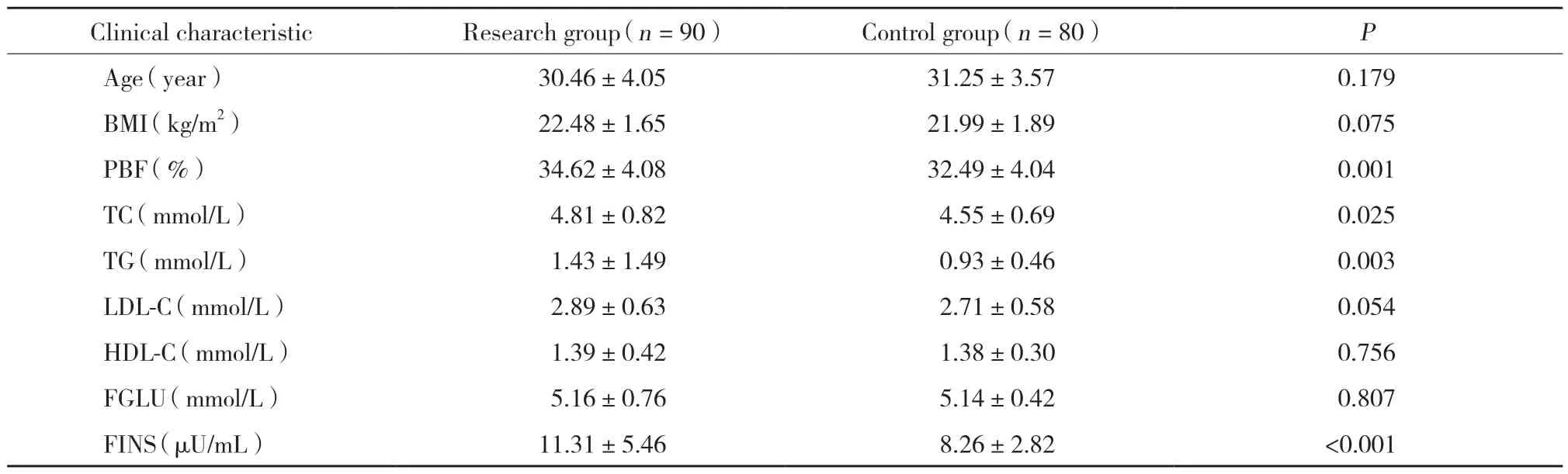
表1 2组患者一般特征和糖脂代谢指标的比较Tab.1 Intergroup comparison of clinical characteristics and metabolic profile
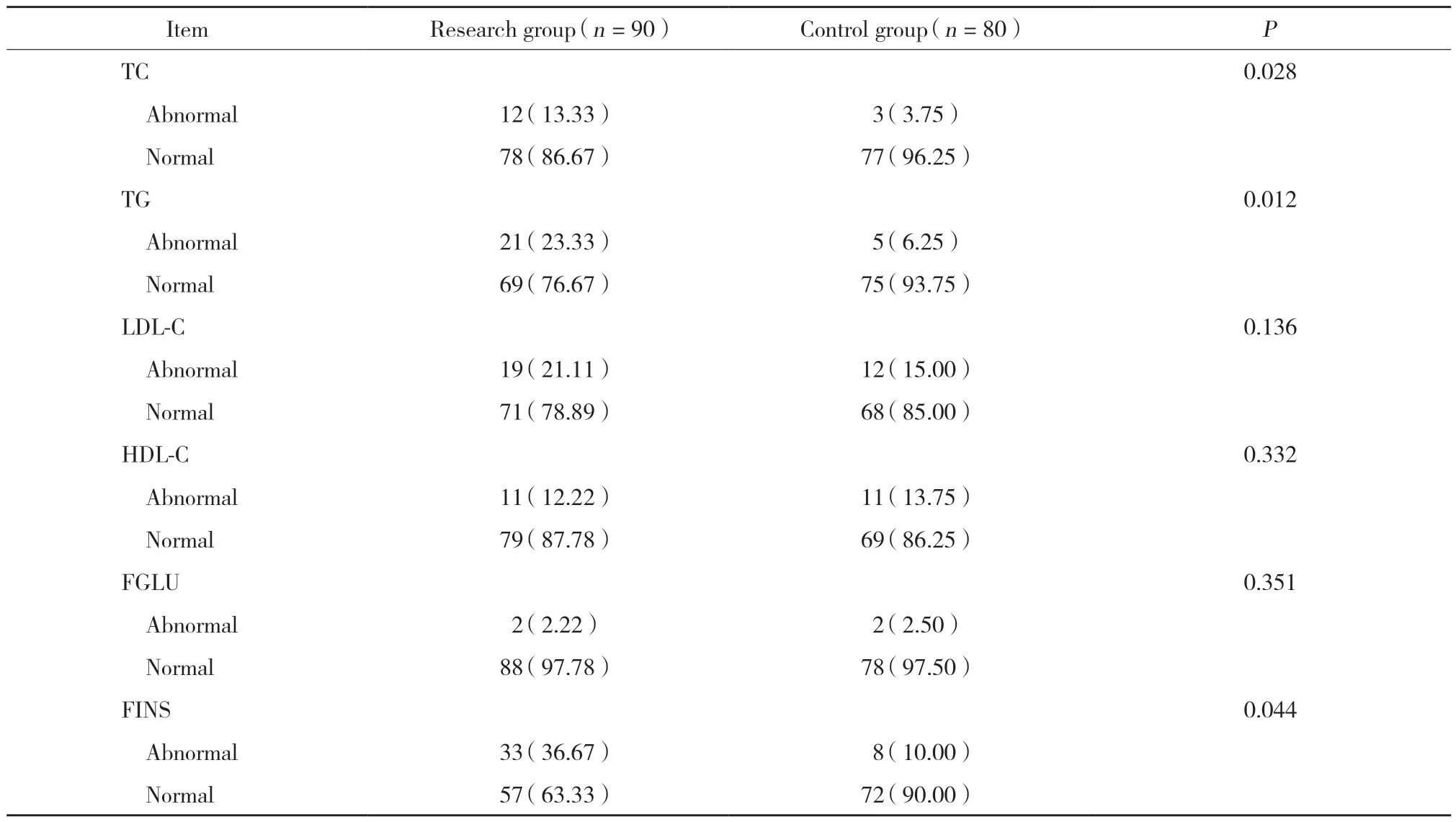
表2 2组患者糖脂代谢指标异常发生率的比较[n (%)]Tab.2 Intergroup comparison of abnormalities of glycolipid metabolism [n (%)]

图1 BMI、PBF预测研究组和对照组FINS水平异常的ROC曲线Fig.1 Receiver operating characteristic curve analysis of body mass index and percentage of body fat for the prediction of abnormal fasting insulin levels between groups
虽然不同研究中糖脂代谢与BMI正常的PCOS患者的相关性存在一定差异,但是其共同点为BMI正常的PCOS患者其FINS水平明显高于对照组[8-10]。本研究中,BMI正常的PCOS患者的高胰岛素血症发生率为36.67%。YAO等[12]认为胰岛素抵抗和高胰岛素血症是代谢异常发生的最初表现,胰岛素抵抗可引起血糖升高、TG的分解代谢下降、HDL-C下降和LDL-C上升,大大增加了糖尿病和心脑血管疾病的患病风险。因此,FINS水平异常可能是PCOS人群发生糖脂代谢异常的预警,有利于PCOS人群代谢紊乱的早期干预。
脂肪组织具有重要的内分泌功能,其分泌的细胞因子可通过不同的机制导致胰岛素抵抗和高脂血症,从而引起糖脂代谢紊乱的发生[12-13]。因此,准确判定是否肥胖对临床预防代谢相关疾病的发生具有重要意义。目前临床常用BMI作为衡量肥胖的标准,近年来利用生物电阻抗原理测定的PBF可以准确反映体内脂肪含量、比例和分布。本研究首次通过ROC曲线分析了BMI和PBF预测BMI正常的PCOS患者出现FINS水平异常的价值。BMI≥23 kg/m2预测FINS水平异常的灵敏度高达66.7%,具有较好的预测价值,提示BMI≥23 kg/m2时就应该关注PCOS人群的代谢风险。PBF≥37.75%预测FINS水平异常的特异度高达87.7%,可为BMI正常的PCOS患者的代谢评估提供参考价值,提示PBF≥37.75%时应重视对PCOS人群的体质量、代谢管理。因此,BMI和PBF作为简便、无创的检查方法,对于PCOS患者FINS水平异常的预测具有较高的价值。
综上所述,BMI正常的PCOS患者仍存在代谢异常的风险,BMI正常的PCOS患者FINS水平异常发生率较高,BMI和PBF可作为预测BMI正常的PCOS患者出现FINS水平异常的一种无创性检查方法。

