锁定钢板复合个性化同种异体骨治疗胫骨近端骨巨细胞瘤术后骨缺损有限元分析
沈健坚,刘姮莹,丁焕文,张志成,姜志强,李 颖
骨巨细胞瘤(giant cell tumor of bone,GCT)属于交界性骨肿瘤,发病率占所有原发性骨肿瘤的5%~20%[1-3],胫骨近端和股骨远端较为常见,约占全身GCT的60%~70%[4]。对于胫骨近端GCT,主要的手术方式包括肿瘤刮除术、肿瘤切除术和截肢术,而肿瘤切除后的重建方式主要有自体骨/异体骨/骨水泥+内固定、肿瘤型假体/异体骨复合肿瘤型假体重建等[5]。目前对于胫骨近端GCT整块切除术后重建的生物力学,相关研究较为匮乏。本文对锁定钢板复合个性化同种异体骨重建胫骨近端GCT术后骨缺损进行生物力学有限元分析,旨在为临床治疗提供力学参考数据。
1 资料与方法
1.1 建立双下肢骨关节和肿瘤病灶区域三维解剖模型
选择1例胫骨近端GCT患者(男,42岁,175 cm/70 kg),采用64排双源螺旋CT(SIEMENS公司,德国)进行双下肢骨骼薄层扫描,层厚0.75 mm,获取双下肢骨关节的二维图像数据,以DICOM格式输出保存。采用1.5T MRI扫描仪(SIEMENS公司,德国)对肿瘤病灶区域进行薄层扫描,层厚1 mm,选择T2脂肪抑制序列图像并以BMP格式输出保存。分别将骨关节和肿瘤病灶数据导入Mimics软件(Materialise公司,比利时),通过阈值分割、区域增加、面罩编辑、三维重建等操作,建立双下肢骨关节和肿瘤病灶三维解剖模型(图1,2)。
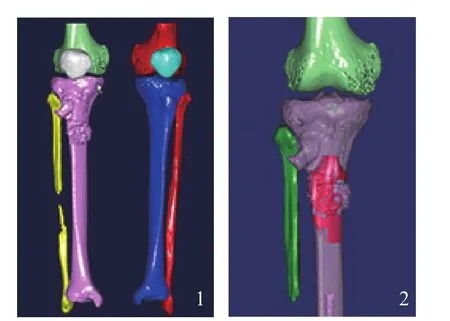
图1 双下肢骨关节三维解剖模型 图2肿瘤病灶三维解剖模型
1.2 肿瘤病灶的测量和切除范围的确定
将双下肢骨关节和肿瘤病灶的三维模型以STL文件导入Imageware软件(EDS公司,美国),通过点云对齐工具将肿瘤病灶与下肢骨关节三维模型进行图像融合。计算机辅助分析肿瘤的区域形状和浸润范围,根据恶性骨肿瘤的外科切除原则来确定肿瘤的近端和远端切除范围。
1.3 计算机辅助设计个性化骨修复体和内固定物
根据Imageware软件中肿瘤病灶切除范围的参数结果,设计肿瘤病灶近端和远端截骨平面,近端设计为由3个截骨面组成的梯形截骨面,远端设计为与胫骨干垂直的截骨平面(图3)。通过镜像工具建立胫骨镜像体,通过点云对齐,拟合肿瘤病灶切除范围及镜像体的轮廓线,建立个性化骨修复体的轮廓线。通过曲面构建工具,拟合个性化骨修复体的曲面,将胫骨近端、远端和个性化骨修复体曲面以iges格式保存。
将胫骨近端、远端和个性化骨修复体曲面导入UG NX软件(SIEMENS公司,德国),通过链接面、缝合曲面工具,生成三维实体模型。导入肿瘤病灶近端和远端截骨平面,通过修剪体工具将个性化骨修复体修剪成与肿瘤病灶切除范围完全匹配的模型结构,同样根据肿瘤远端截骨平面修剪胫骨远端三维实体模型。通过链接面、缝合曲面工具形成封闭的实体,将个性化骨修复体近端切除部分与胫骨近端进行布尔逻辑求和,生成胫骨近端三维实体模型。
选择16孔Golf锁定加压钢板(天津威曼公司),激光抄数获取点数据,将其导入UG NX软件,进一步拟合成曲线和曲面,形成三维实体模型,以STL文件导出保存。其中螺钉三维模型设计为直径3.5 mm的圆柱体。

图3 肿瘤病灶近端、远端截骨平面的设计

图4 锁定钢板复合个性化同种异体骨的三维模型
1.4 建立钢板固定修复肿瘤切除后骨缺损三维实体模型
将胫骨近端、胫骨远端、腓骨、个性化骨修复体、钢板和螺钉三维实体模型以STL格式导入Mimics软件,在CMF/Simulation模块中利用Reposition工具的平移、旋转功能,按照骨肿瘤切除术后重建骨缺损的方法、进行模型装配,建立钢板固定修复肿瘤切除后骨缺损三维模型(图4)。以STL文件保存并导入Geomagic Studio(Geomagic公司,美国)逆向工程软件,通过开流型、松弛、平滑、祛除特征等工具进行光滑处理,后借助探测轮廓线、编辑轮廓线、升级/约束、构建曲面片、松弛曲面片、编辑曲面片、构造栅格等工具构造曲面片,最后通过拟合曲面工具形成封闭的三维实体模型,以iges格式保存。
1.5 钢板固定修复肿瘤切除后骨缺损的有限元仿真分析
将建立的三维实体模型数据导入ANSYS WORKBENCH 2.0软件(ANSYS公司,美国)的DM模块中,其中布尔逻辑运算设置为Add Frozen,生成锁定钢板固定修复胫骨近端骨缺损的有限元模型。
参考灰度值赋值法构建的胫骨材料属性数值[6],添加胫骨近端和个性化同种异体骨的材料属性为弹性模量8 GPa、泊松比0.3,胫骨远端和腓骨的材料属性为弹性模量11 GPa、泊松比0.3;锁定加压钢板和螺钉为Ti-6AL-4v,其材料属性为弹性模量110 GPa、泊松比0.3[7]。模拟轴向加压时锁定钢板和螺钉的接触皆定义为Bonded焊接,胫骨近端与个性化骨修复体、个性化骨修复体与胫骨远端、胫腓骨接触定义为No seperation;网格划分选择Sizing划分方法,胫骨近端、骨缺损修复体、胫骨远端和腓骨网格大小为3 mm,钢板和螺钉为1 mm,生成554 781个节点、353 208个四面体的网格单元(图5)。如图6所示,边界条件约束为胫骨下关节面和腓骨外踝,且X、Y、Z6个方向的自由度均定义为0。根据步行时胫骨近端承受3倍体重的轴向载荷[8],且内外侧平台载荷分配比例为60%:40%[9],计算F=70 kg× 9.8 N/kg× 3=2 058 N,插入载荷类型为Force,胫骨内外侧平台为受力点,分别施加在内侧平台1 235 N、外侧平台823 N,方向定义为垂直向下。插入求解的选项为等效应力、整体位移和方向位移,进行仿真力学分析。
2 结果
在模拟3倍体重的轴向载荷作用力下,胫骨骨骼的等效应力集中分布在胫骨中下段1/3前内侧,锁定钢板的等效应力集中分布在与骨缺损区域相对应的锁定钢板中段,钢板前后缘应力分布均匀、应力大小在11.527~23.055 Mpa,最大应力发生在钢板近端第5枚螺钉与钉孔接触处(25.936 MPa,图7)。
如图8,9所示,在轴向位移分布上,胫骨近端内侧平台、个性化同种异体骨近端在Z轴上最大位移分别是0.293、0.272 mm。在侧方位移分布上,胫骨近端在X、Y轴上最大方向位移分别为0.718、0.571 mm,胫骨近端整体向内侧、前方移位;个性化同种异体骨近端和远端在X、Y轴上的最大方向位移分别为0.668、0.572 mm和0.095、0.370 mm,均存在向内侧、前方移位。

图5 有限元网格模型

图6 边界和载荷的设定

图7 模拟轴向加压试验的应力分布云图

图8 胫骨近端各方向位移分布云图
3 讨论
目前普遍认为,对于CampanacciⅠ、Ⅱ级以及软组织肿块可以切除的Ⅲ级GCT,囊内扩大刮除术仍然是标准的治疗方式,但术后复发率高达10%~40%[5];肿瘤整块切除术虽然可以大大降低术后局部复发率,但存在术后假体相关并发症发生率较高、肢体功能不佳等问题[10]。多中心回顾性研究表明,扩大刮除+结构性植骨/骨水泥+内固定的术后患者功能优于大块切除+假体重建[11]。如何在整块切除肿瘤病灶的同时能够实施结构性植骨+内固定,以期达成更低的肿瘤复发率和更好的肢体功能,是本研究的目标之一。

图9 个性化骨修复体各方向位移分布云图
我们通过计算机辅助设计方法建立三维解剖模型和实体模型,精确测量和分析肿瘤范围,实现肿瘤整块切除及个性化同种异体骨+锁定钢板重建骨缺损。然而,这种重建方式的生物力学性能如何,目前仍缺乏相关报道。李继锋等[12]对成人胫骨近端不同长度的骨缺损尸体标本进行体外力学测试,结果提示,胫骨近端内侧骨皮质缺损≥15 mm或外侧骨皮质缺损≥20 mm时生物力学性能将显著降低。但这一测试方法并不能充分反映上述重建方式的力学情况。
随着数字医学和工程力学的快速发展,有限元法目前被广泛应用于骨科生物力学研究,特别是在人工关节假体重建肿瘤型骨缺损方面,能够准确预测肿瘤假体的应力分布和稳定性,为指导假体设计和优化内固定方式提供生物力学依据[13-14]。莫富灏等[15]利用有限元分析正常站立状态下肿瘤型铰链式膝关节置换术后股骨-假体-胫骨复合体的应力分布,结果显示应力明显集中分布在股骨前1/3区域,与术后远期出现的股骨皮质穿破位置一致。马立敏等[16]建立骨水泥+锁定钢板修复股骨远端不同长度缺损的三维有限元模型,结果发现,随着骨缺损长度的增加,应力分布无明显改变,但骨水泥位移明显增加,提示发生螺钉松动或断裂的风险加大。可见通过有限元分析,能够准确分析肿瘤型骨缺损重建术后假体、内固定物应力集中的位置,有助于预测可能出现的并发症。
本研究基于胫腓骨及肿瘤病灶的图像数据建立三维解剖模型,精准模拟肿瘤整块切除术、个性化同种异体骨+锁定钢板修复骨缺损过程,最后建立的有限元模型能够客观真实地反映重建术后胫骨近端骨缺损的解剖结构属性。
进一步对有限元模型进行生物力学分析,结果显示,在模拟正常人体单足行走、胫骨平台承受峰值接近3倍体重的轴向载荷下,等效应力主要集中分布在与骨缺损区域相对应的锁定钢板,这是由于胫骨和钢板的弹性模量不一,弹性模量大的物体会承受更多的应力,产生应力遮挡效应[17]。而最大应力发生在钢板近端第5枚螺钉与钉孔接触处,提示此处可能是最早发生螺钉断裂的部位。理想的内固定物其等效应力分布应均匀且应力值较小,本研究中钢板前后缘应力分布均匀、应力大小在11.527~23.055 Mpa,远低于锁定钢板的屈服强度(894~1 034 Mpa)[18],提示其可提供足够的力学稳定性。
Bottlang等[19]研究证实骨折断端轴向微动在0.2~1 mm的范围内,可促进骨折愈合。本研究方向位移分析结果显示,胫骨近端内侧平台在轴向压缩方向(Z轴)的最大位移为0.293 mm,个性化同种异体骨近端最大位移为0.272 mm,具有促进断端骨愈合的作用。胫骨近端和个性化同种异体骨近端在X轴上最大方向位移分别为0.718、0.668 mm,个性化同种异体骨远端在Y轴上最大方向位移分别为0.370mm,证实其存在不同方向的侧方移动剪切力,而有限范围内的侧方剪切力位移可促进早期骨痂形成[20]。总之,基于上述有限元模型分析结果,可以推测在人体正常行走过程中,锁定钢板复合个性化同种异体骨重建术后骨缺损,可以为截骨平面提供有效的轴向压缩和侧方剪切力的刺激,利于截骨断端的骨愈合。
然而,由于骨缺损范围较大,相对应的钢板整体承受较大的应力,同种异体骨远期愈合过程中可能会出现骨吸收、骨不愈合而导致内固定失败。因此,我们在彻底切除肿瘤病灶的基础上,应减少对正常骨质的切除,降低内固定应力集中的范围;至于钢板长度上的选择,应尽可能超过骨缺损远端5~6枚螺孔,以分散应力,避免术后发生钢板和螺钉的松动断裂。
本研究的不足之处在于:①本研究在建模上采用简化模型法,忽略了肌肉、韧带组织建模以及在施载条件下肌肉和韧带组织的力量分布情况。②未进行模型的疲劳分析和循环分析,对其可能发生的钢板和螺钉松动、断裂预测不足。今后将通过X线片随访观察来验证螺钉、钢板的受力情况,同时对锁定钢板复合同种异体骨重建胫骨近端巨大骨缺损的尸体标本模型,进行体外力学测试,探讨内固定失败与研究结果的相关性,从而为胫骨近端GCT术后骨缺损重建提供生物力学指导依据。

