国家药物政策框架构建下的我国药物政策改革逻辑分析与研究
——基于2009-2019年的药物政策文本分析Δ
崔兆涵,吕兰婷(中国人民大学公共管理学院,北京100872)
2001年世界卫生组织(WHO)提出了国家药物政策的概念与相应的框架;“新医改”以来,我国在药物领域的改革政策不断完善,政策体系呈现出从碎片走向整合的趋势。目前,我国尚未出台纲领性的国家药物政策文件;但实际上,很可能已经结合我国药物领域的实际情况按照一定的逻辑构建起了国家药物政策体系。本文中,笔者通过梳理我国“新医改”以来出台的药物领域的相关改革政策文件,分析我国国家药物政策构建情况和药物政策体系构建逻辑,旨在为完善我国国家药物政策体系提供参考。
1 相关概念
1.1 国家药物政策
1975年,WHO首次提出了“国家药物政策”的概念,并于1988年和2001年分别发布了两个版本的国家药物政策指南,并基于此开发了相关的政策工具以协助WHO成员国制定和实施国家药物政策。总体来讲,国家药物政策是指由政府制定的有关药物领域的目标、原则、战略和工作方法等的指导性文件,用于构建一个整合的政策框架,将药物领域中的主要相关方囊括其中,包括公共部门和私人部门,并协调各方行动,平衡各方利益,进而实现药物领域的政策目标。WHO提出,国家药物政策作为正式的政策文件出台是非常关键的,能够有助于相关各方就药物领域改革目标达成共识,并在此基础上对政府各个部门以及各个相关方之间的责任进行清晰的界定[1]。
1.2 国家药物政策体系
国家药物政策是一个包含政策目标和政策行动要素的完整体系。WHO所倡导的国家药物政策框架有3个主要目标,即促进药品可及性、保障药品质量和促进合理用药,并在这3个主要目标的指导下,制定了9项政策行动要素,构成了完整的国家药物政策体系,包括基本药物制度、可负担性、药物资金筹措、供应系统、质量保障、合理用药、研发、人力资源、监测与评价。以上9项政策行动要素都直接或间接与1项或多项国家药物政策目标相关[2],详见表1。由此可见,WHO的国家药物政策指南可以说是建立在基本药物制度理念与政策框架基础上的,这是因为在20世纪70年代WHO大力推行基本药物制度的背景下,基本药物的理念渗透到了国家药物政策框架中[3]。但从各国国家药物政策体系构建的实践来讲,各国国家药物政策的要素与目标均基本遵照了WHO所提出的政策框架,并没有局限于基本药物制度,而更多是将基本药物政策镶嵌于各国国家药物政策之中[4-5]。因此,本文在对我国药物政策进行分析的时候,也不局限于国家基本药物制度相关的政策,而是将范围拓展至全部药物领域的政策。
2 研究设计与方法
2.1 研究内容与步骤
本研究在对国家药物政策相关内容和概念进行梳理与介绍的基础上,主要对以下两个问题进行研究:(1)分析我国国家药物政策的构建情况;(2)分析我国“新医改”以来国家药物政策框架构建背景下我国药物政策的改革逻辑。研究步骤如下:
第一,对2009-2019年我国药物领域发布的政策文本进行收集整理,确定政策文本分析框架,并对政策文件的政策力度进行评估打分;第二,根据国家药物政策中9项政策行动要素的内涵与外延,对“新医改”实施以来的药物政策文本进行归类分析,确定政策文本中所包含的药物政策行动要素及其相关顺序,并结合政策力度分析,对国家药物政策框架的构建情况进行分析;第三,根据国家药物政策框架,对不同领域的改革措施进行提取归纳,进而对我国国家药物政策构建背景下的改革逻辑进行分析。
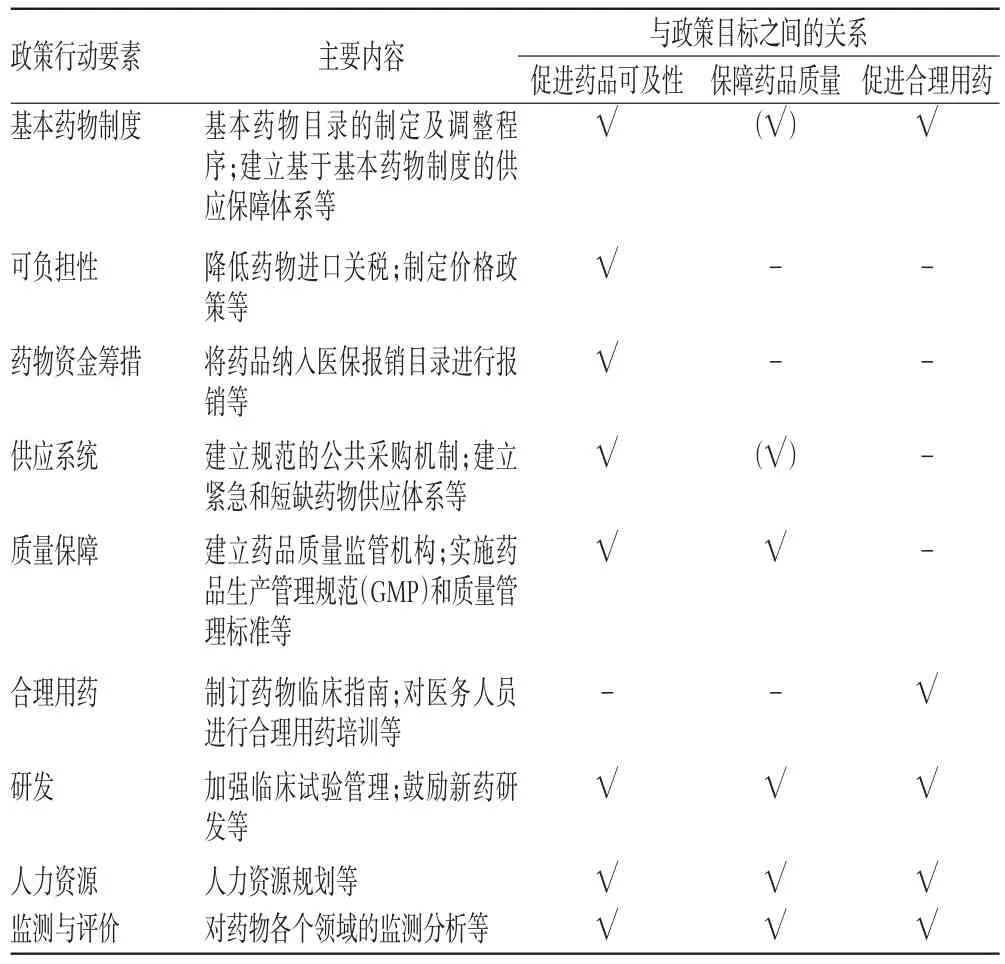
表1 国家药物政策行动要素内容及与政策目标之间的关系Tab 1 Elements of national medicine policy and their relationship to policy objectives
2.2 资料来源
检索药物政策相关的部门网站,包括卫生部门、药监部门、发改部门、医保部门、财政部、工信部、商务部网站以及中国政府网(国务院)等。本课题研究的是“新医改”之后国家药物政策框架的构建情况,因此收集的政策文本发布的时间段为2009年-2019年4月。所收集的政策文本包括针对某一具体药物领域的改革政策、涉及多个领域的改革政策以及包括药物领域的综合类改革政策等。政策文本是否应该被纳入,由多名课题组成员进行交叉判断。收集的政策文本信息包括政策名称、发文部门、发文时间和政策文本内容等。
2.3 政策力度与政策主题相关性评估
药物政策涉及的环节众多,对应的政策发布类型和发文部门级别不同,且存在主要政策和配套政策的区分,均导致了不同政策文本力度的差异。为更加清晰地对“新医改”以来药物政策领域的改革逻辑进行分析,需要对药物政策力度进行区分。本研究参考彭纪生(2008)[6]、芈凌云(2017)等[7]的相关研究,并参照国务院颁布的《行政法规制定程序条例》,将相关政策按照发文类型和发文层级划分为5个级别,并分别赋予1~5的分值,详见表2。在评估过程中,由课题组成员进行政策力度评分,并进行交叉验证后将其分数作为权重。在判断某一药物政策文本主题与药物政策框架行动要素的相关性时,对于包含多个主题的政策文本,由课题组对该文本包含的不同主题按相关性进行排序,即按照相关性分别赋值0~9分进行排序,最相关的主题赋分为9,完全不相关的则赋分为0,并进行交叉验证。由政策力度分数和主题相关性评分相乘,得到该政策的政策主题得分;该年度内所有政策的政策主题得分相加即为该年度政策主题得分,用于判断当年度改革重点。政策力度评分与主题相关性评分示例详见表3。

表2 政策力度评分标准Tab 2 Scoring criteria for policy strength assessment

表3 政策力度评分与主题相关性评分示例Tab 3 Example of policy strength score and topic relevance score
3 结果
3.1 “新医改”以来药物政策发布基本情况
本研究共纳入药物政策文本277份,从政策类型来看,针对某个具体环节的领域政策有153件(55.2%),涉及多个环节的行业政策有100件(36.1%),涉及医改其他领域的综合类改革政策有24件(8.7%);从发文部门来看,药物领域涉及的部门众多,其中药监部门牵头的政策文本为154件(55.6%),卫生部门牵头的政策文本为60件(21.7%),由于药物领域涉及利益主体众多,同时随着医疗、医保、医药“三医联动”改革的深化,由中共中央、国务院、全国人大牵头发布的政策文本为41件(14.8%),详见表4(其中,药监部门包括国家药品监督管理局、原国家食品药品监督管理总局、原国家食品药品监督管理局;卫生部门包括国家卫健委、原国家卫生计生委、原卫生部;中共中央包括中共中央及中共中央办公厅;国务院包括国务院、国务院办公厅、国务院医改办、国务院纠风办;医保部门主要指国家医保局)。从发文时间来看,2015年之后药物政策发布数量总体上呈上升趋势,详见图1。
3.2 按国家药物政策框架主题分类分析结果
根据国家药物政策框架中9个政策行动要素的内涵,将“新医改”以来我国发布的药物政策文本的数量与政策力度进行统计分析,并提取主要改革措施,分析结果见表5~表7。
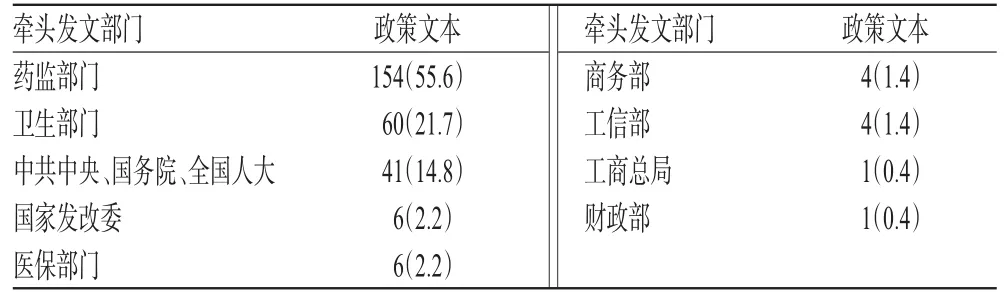
表4 2009-2019年各相关部门发布的药物政策数量及占比统计[件(%%)]Tab 4 Number and proportion of medicine policies issued by related department in 2009-2019[piece(%%)]
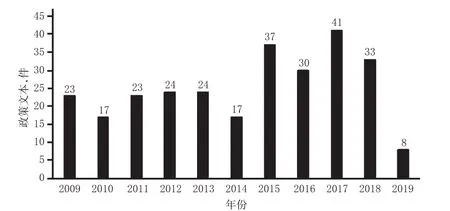
图1 2009-2019年药物政策发布数量变化情况Fig 1 Changes of medicine policy number in 2009-2019
3.2.1 基本药物制度 基本药物制度相关的政策包括了基本药物的遴选、生产、流通、采购、使用、支付等。从发布的文件数量来看,2009-2019年基本药物制度相关的政策文本数量为40件(如表5所示),其中2009-2010年发布数量较多,其他年份发布数量相对较少。从政策主题得分来看,基本药物制度政策主题得分在2009-2010年排名较为靠前(如表6所示)。从政策内容来看,基本药物制度主要针对的是药物使用环节,通过制定基本药物目录、基本药物目录管理办法以及临床应用指南和处方集等指导和规范基本药物在基层医疗机构的使用,并通过加强基本药物生产供应保障、质量监管,构建基本药物招标采购制度,以及提高基本药物的医保支付比例等方式确保基本药物制度的执行与实施(如表7所示)。值得注意的是,基本药物政策在2015年之后发布的数量相对较少;直至2018年,国务院办公厅发布了《关于完善国家基本药物制度的意见》,并印发了2018年版《国家基本药物目录》,使得基本药物制度建设在“健康中国”战略背景下的重要性得以再次彰显[8]。
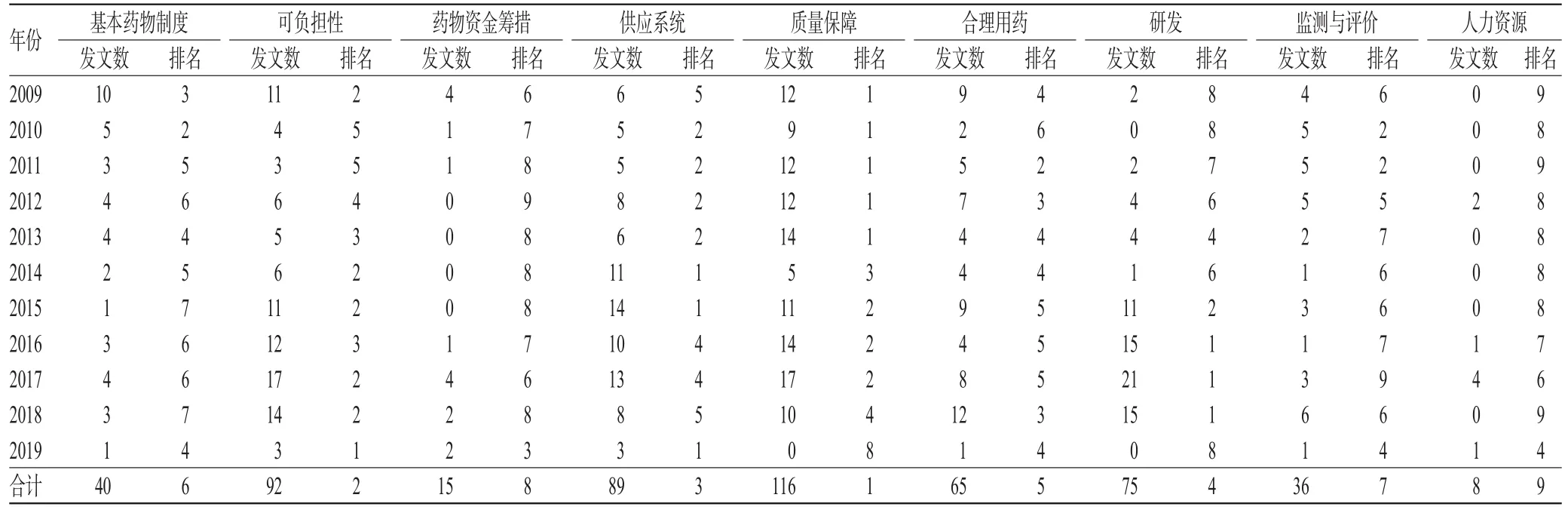
表5 2009-2019年不同主题政策文本发布数量及排名情况Tab 5 Number and ranking of policy texts of different themes in 2009-2019
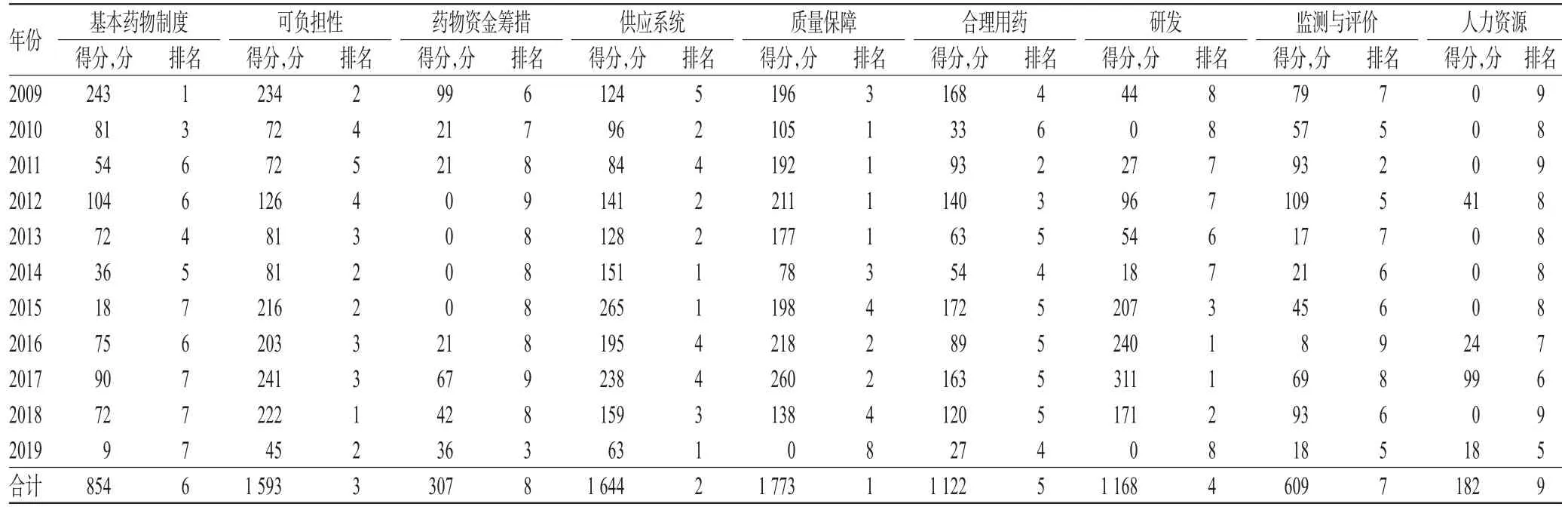
表6 2009-2019年不同主题政策相关性得分及排名情况Tab 6 Policy relevance scores and rankings of different themes in 2009-2019

表7 不同主题政策改革措施归纳情况Tab 7 Reform measures of different policy themes
3.2.2 可负担性 可负担性政策主要与药物的使用、流通、采购、支付等环节相关。从发布数量来看,可负担性的相关政策文本总共有92件,在9个政策主题中排名第2,其中发布数量在2009年和2013-2019年均位居前列,上述各年排名分别为2、3、2、2、3、2、2、1(如表5所示);2009-2019年可负担性的政策主题总得分为1 593分,年度政策主题相关性得分同样是在2009年和2013-2019年均位居前列,排名分别为2、3、2、2、3、3、1、2(如表6所示)。从政策内容来看,可负担性在使用环节主要是通过药品“零差率”、合理用药以及提倡对基本药物和仿制药的使用来降低患者药品方面的费用负担;在流通环节,主要是通过压缩流通环节,挤压流通环节中的药价来降低药品价格;在采购环节,则是通过分类采购、带量采购以及药品谈判等方式来降低药品价格;在支付环节,则采用通过调整医保目录,将谈判药物等纳入医保目录等,进而降低患者负担;与此同时,在生产环节,通过实施仿制药一致性评价,促进仿制药的生产和使用,从而降低患者负担(如表7所示)。
3.2.3 药物资金筹措 药物资金筹措所涉及的主要为医保支付环节。从发布数量来看,药物资金筹措的发布数量较少,总发布数量为15件(如表5所示),其政策主题总得分为307,历年中政策主题得分也相对较低(如表6所示)。从政策内容来看,药物资金筹措政策主要包括将药物纳入医保目录以筹措药物资金,以及对贫困弱势或特定人群(结核病、艾滋病等)进行财政支持等政策。其中,出台政策较多的年份为2017年,包括新版医保目录的印发、谈判药物纳入医保目录等(如表7所示)。
3.2.4 供应系统 供应系统政策主要涉及药物生产、流通、采购等环节。从发布数量来看,2009-2019年,供应系统相关政策文本数量为89件,仅次于“质量保障”和“可负担性”两个政策主题。从发文年度来看,供应系统政策的发布数量在2010-2015年和2019年数量均排名靠前,排名分别为2、2、2、2、1、1、1(如表5所示)。供应系统政策主题总得分为1 644分,位居第2位;2010、2012-2015、2019年的政策主题得分较高,排名分别为2、2、2、1、1、1(如表6所示)。从政策内容来看,供应系统在药物生产环节主要包括短缺药品、特殊药品生产供应保障、生产规范等方面的政策;药品流通环节包括药物批发、药品零售、药品配送、药品经营质量保障等方面的政策;药物采购环节包括药品招标、药品集中采购等方面的政策;与此同时,在使用环节上,通过督促医疗机构及时回款以及在带量采购中确保使用量等政策,促进药品企业及时足量地保障药品供应(如表7所示)。
3.2.5 质量保障 质量保障政策主要涉及生产、流通、使用等环节,包括生产质量保障、经营质量保障、药品使用规范、药物不良反应监测等方面的政策。从发布数量来看,“新医改”以来,质量保障主题的政策数量最多,为116件,其中2009-2017年的发布数量均排名靠前,排名分别为1、1、1、1、1、3、2、2、2(如表5所示)。质量保障政策主题总得分为1 773分,排名第1;各年度政策主题得分也均位居前列(如表6所示)。从政策内容来看,在生产环节,原卫生部出台了新版GMP(2010),并由药监部门牵头在药品生产环节进行了专项整治并开展了仿制药一致性评价;在流通环节,卫生部门在2010年和2015年分别发布两个版本的《药品经营管理规范》(GSP),并通过加强对药品流通环节的专项整治、实施“两票制”等政策对流通环节进行规范;在使用环节,主要通过加强药物不良反应监测以及加强合理用药来进行质量保障;与此同时,在采购环节通过按质量层次进行招标采购、优先采购通过一致性评价的药品等政策,促进药品质量的提升(如表7所示)。
3.2.6 合理用药 合理用药相关政策主要针对的是药物使用环节。从发布数量来看,合理用药政策发布总数为65件,其中2011、2012和2018年的发布数量排名靠前,排名分别为2、3、3(如表5所示)。合理用药政策主题总得分为1 122分,其中2011-2012年的政策主题得分较高,排名分别为2、3(如表6所示),主要是这两年发布了较多关于抗菌药物临床应用以及关于药物不良反应监测的政策。从政策内容来看,合理用药的政策包括药品“零差率”以及公立医院药学服务转型、临床抗菌药物、辅助药物使用监测、药占比控制、药物不良反应监测以及相关的合理用药方面的绩效考核;此外,在支付环节,医保部门在处方审核方面的相关工作也在一定程度上促进了合理用药(如表7所示)。
3.2.7 研发 研发相关政策主要针对的就是药物研发环节。从发布数量来看,研发相关政策的发布总数为75件,其中2015-2018年的发布数量排名靠前,排名分别为2、1、1、1(如表5所示)。政策主题总得分为1 168分,其中2015-2018年的政策主题得分较高,排名分别为3、1、1、2(如表6所示)。从政策内容来看,药品研发相关政策呈现出了显著的阶段性,在第一阶段(2009-2014年),药品研发相关政策主要是针对药物研发不同阶段的技术指导;第二阶段(2015-2018年),国家从2015年正式开启了药品审批审评制度的改革并发布了一系列鼓励药物研发创新的政策,主要包括临床实验数据自查、优化审评审批、开展上市生产许可持有人制度、推进临床试验改革、药物质量和监管体系与国际标准接轨等(如表7所示)。
3.2.8 监测与评价 监测与评价相关政策主要针对生产、流通和使用环节。从发布数量来看,药品监测与评价相关政策的发布总数为36件,其中在2010-2011年的发布数量排名靠前,排名分别为2、2(如表5所示)。政策主题总得分为609分,其中在2011年政策主题得分较高,排名第2(如表6所示)。从政策内容来看,监测与评价相关政策主要包括由监管部门对药品生产、流通、采购、使用等环节的监测以及电子监测体系的建立与相应监测技术的应用,并逐步构建起药物全流程、全周期的监管与追溯体系等(如表7所示)。
3.2.9 人力资源 人力资源相关政策主要针对使用环节。从发布数量来看,人力资源政策的发布总数为8件,在2009-2019年均排名靠后(如表5所示)。其政策主题总得分为182分,各制度的政策主题得分均排名靠后(如表6所示)。目前来看,人力资源政策主要是作为“合理用药”与“药物质量保障”这两个主题的政策的配套政策。随着医改的深入,执业药师在药物政策领域中的重要性也愈发显现,标志性事件为2017年《中华人民共和国药师法(草稿征求意见稿)》(以下简称“《药师法》”)颁布,并正式进入立法程序(如表7所示)。
4 讨论
4.1 我国药物政策框架已初步建立,但尚不均衡
“新医改”实施以来,在基本药物制度、可负担性、药物资金筹措、供应系统、人力资源、监测与评价、质量保障、研发、合理用药9项政策行动要素上均出台了相关的政策文件,虽然尚未出台纲领性的国家药物政策框架的文件,但实质上已经初步构建起了国家药物政策框架,但是仍存在不均衡的情况,突出体现在人力资源和药物资金筹措方面的政策文本数量与政策力度稍显不足。目前,我国药物相关的人力资源政策主要是针对执业药师的政策,政策范围较窄,且主要是以其他改革领域的配套政策出现,正式的《药师法》仍然尚未出台,在人力资源培训等其他方面也没有出台专门的政策文件。我国药物资金筹措的主要措施是将药物纳入医保目录之中,但医保目录调整周期较长,且并未建立动态调整机制,因此有关药物资金筹措的政策较少。另外,国家药物政策框架中的不均衡之处还体现在有关合理用药的制度建设尚不完善,合理用药相关政策主要包括对公立医院药占比的控制和对医务人员处方行为合理性的考核,以及对抗菌药物和辅助用药使用的限制。但其政策内涵较窄,并未将其范围扩大到所有药物的使用范围,且尚未建立起针对合理用药的绩效考核指标体系[9],对公立医院和医务人员合理用药难以发挥实质性的促进作用。
4.2 我国药物政策框架的主线和目标较为明确
本研究通过对“新医改”以来药物政策重点领域的分析可以发现,我国药物政策框架的构建具有两条明确的主线,2009-2019年每年均为重点改革的领域,分别为质量保障和可负担性。与质量保障与可负担性两条主线相对应,“提质”和“降费”是我国药物领域改革的两个主要目标。
“提质”即提高药品质量,主要集中在研发和生产环节,主要是通过提高质量标准(药品质量保障、仿制药质量与疗效一致性评价)和优化增量水平(鼓励创新药物)。“药品质量保障”主要集中于生产和流通环节,以2010年新版GMP和2015年版GSP为核心构建了药物生产和经营质量保障体系,同时配合专项生产流通整治与督查行动,确保药物质量安全。长期以来,我国的创新药物和仿制药的质量均与发达国家存在较大差距,造成了外企原研药在定价和招标采购中的“超国民待遇”[10]。因此,针对已经上市销售的仿制药,可通过质量和疗效一致性评价淘汰大批不达标的低水平仿制药。针对还未上市的药物,则鼓励创新药物的研发和生产,同时通过临床数据自查核查、优化审批审评流程等措施来提高新药审评审批效率,解决审评审批积压的问题[11]。与此同时,通过药品注册分类改革、临床试验改革、对接国际药品研发技术与标准、推进上市许可持有人制度试点工作等改革措施来共同鼓励药物创新与研发。同时,在药物的使用、采购和纳入医保目录等方面提供相应的激励政策,进而促进我国整体药物质量水平的提升。
“降费”主要是从“价”和“量”两个方面开展。在降价方面,在改革之初通过实行政府指导定价直接限定药品的最高销售价格;在药品价格放开之后,又在生产、流通、采购等多个环节采取多项措施共同促进药品价格的下降。例如,在生产环节,在通过仿制药一致性评价的基础上,鼓励临床使用仿制药,同时加强低价常用药物的供应保障;在流通环节,通过减少流通环节等措施,挤压流通环节价格“水分”[12];在采购环节,通过建立公立医院集中采购制度、实行带量采购、实行区域甚至全国范围内的采购价格联动等方式对药价持续施压[13]。用药量则主要与使用环节和支付环节相关。在使用环节,一方面通过实现药品“零差率”销售,减少医务人员“大处方”行为的动机;另一方面,通过对药占比的控制以及对合理用药的监测,提高医院处方行为的合理化;在支付环节,则主要是通过医保基金对公立医院和医务人员药物使用情况的监测和考核进而对处方行为进行约束以及通过支付方式的改革促进公立医院在控费方面的工作[14]。
4.3 “新医改”后的国家药物政策从“以需求端为主的改革”向“供给端改革和需求端改革并重”转变
根据改革重点的不同,我国“新医改”后的国家药物政策可以大致分为两个阶段:第一个阶段(2009-2013年),改革重点主要是国家基本药物制度的建设、合理用药和监测与评价;第二个阶段(2014-2019年),改革重点是供应系统和研发。前后两个阶段改革重点的转变体现了我国药物政策从“以需求端(公立医院和患者)为主的改革”向“供给端(生产企业、流通企业)改革和需求端改革并重”转变。
在第一个阶段(2009-2013年),以需求端作为改革重点,该阶段药物领域的改革以国家基本药物制度建设为核心,推动基层医疗机构运行机制的改革,并开启了县级公立医院综合改革;该阶段药物领域的改革重点还包括了合理用药制度和监测与评价,同时还有以降低药价为目的的多次行政性降价[15],同样主要是对应药物需求端的改革。在该阶段,药物供给端的改革主要是配合需求端改革开展的[16]:一方面,供应保障体系的改革主要是以配合基本药物制度的建立与实施以及公立医院改革的需要;另一方面,作为药物供给端政策主题的“质量保障”,虽然建立了以新版GMP和GSP为核心的药品质量保障体系,但仍主要是以事后监管和专项整治为主,并未系统性提高我国药品质量,也并未改善我国药品低水平重复生产的局面;另外,作为供给端重要环节的药物研发在该阶段并未得到足够的重视。从政策目的来看,“降费”在本阶段的重要性高于“提质”。
在第二个阶段(2014-2019年),药物需求端的改革已经取得一定成效,同时供给端改革的滞后限制了需求端改革的深入,研发和生产水平的落后限制了我国药物领域的整体发展。结合经济领域供给侧结构性改革的大背景,该阶段在继续推进药物需求端改革深化的同时,在药物供给端也开展了系统性改革:在需求端,公立医院综合改革范围不断扩大,药品加成全面取消,公立医院药学部门服务模式转型更加强调合理用药的重要性[17],同时在公立医院集中采购制度上的改革亦不断深入,采取多种创新方式降低药品采购价格;在供给端,一方面,在继续加强药物供应保障和质量保障工作的基础上,通过在生产环节的仿制药一致性评价和研发环节的鼓励创新研发系统性提升我国药品质量,另一方面,通过需求端在采购、使用、支付等方面的政策引导促进供给端的改革。从政策目的来看,在本阶段“提质”和“降费”的重要性是相当的。
4.4 药品采购环节在整体药物领域改革中的重要性不断加强
药物领域作为市场化程度较高的领域,在2015年取消大部分药品的行政定价之后,采购环节在整个药物改革领域中的重要性不断加强。采购环节作为药物从供给端和需求端对接的环节,对药物价格的最终形成起到了重要作用[18],因而能够有效调动和推动其他环节的改革。在供给端,通过对创新药物、通过仿制药一致性评价、实施“两票制”企业等药物的优先采购,促进药物供给端改革政策的落实;在需求端,通过集中采购,进一步降低药品采购价格,进而降低公立医院药品费用和患者负担。另外,在带量采购模式的试点中,在“以量换价”的工作思路下,要求公立医院优先使用带量采购的药品,进而能够进一步推动公立医院在用药环节的合理性以及公立医院运营管理的精细化。与此同时,在2018年的国务院机构改革中,国家医保局成立,承担了药品采购的工作,将进一步促进药品采购与医保支付标准的对接,强化医保基金作为最终支付方的议价地位,进一步加强了采购环节在整个药物改革中的抓手作用。
5 政策建议
5.1 增强国家药物政策的均衡性
建议加强在人力资源和药物资金筹措方面的政策力度,并深化和完善合理用药方面的改革。在药物人力资源方面,在需求端,应继续加强完善执业药师政策,加快推进《药师法》的出台;在供给端,应加强对药学科研人员的培养和教育,提升药物研发水平;与此同时,由于药物领域专业性强,应加强对药政执法人员的能力建设及对药物政策研究人员的培养。在药物资金筹措方面,应尽快建立和完善医保目录的动态调整机制,推动药物经济学评价在医保准入环节的应用[19]。在合理用药方面,在当前公立医院综合改革全面推开、药品加成全部取消的背景下,应加快推动公立医院药学部门的转型和药学服务模式的创新,推动医务人员的合理用药;与此同时,应建立由主管部门组织设计针对合理用药的考核评价体系,并将其纳入公立医院和医务人员的绩效考核中[20]。
5.2 加强顶层设计,增强药物政策部门间的协调性
从目前药物政策发布情况来看,虽然国家药物政策的框架已经初步建立,但是药物领域的管理涉及多个政府部门,同时随着公立医院综合改革的深化,以及“三医联动”的不断加强,药物政策在政策协调性等方面仍有较大的提升空间[19]。建议组建由相关部门组成的药物政策协调委员会,由卫生部门牵头,包括医保部门、药监部门、工信部门、商务部门等,负责对国家药物政策框架的顶层设计以及对涉及多个环节药物政策的出台和落实进行协调推动,并择机出台国家药物政策的纲领性文件,增强药物政策的协调性[21]。
5.3 进一步发挥药品采购环节的改革抓手作用
药品采购作为连接供给端和需求端的关键环节,应进一步发挥药品采购制度建设在药物改革领域的抓手作用。一方面,在药品采购由国家医保局主管的背景下,推动采购环节与医保支付环节的对接,探索医保支付标准与采购价格的衔接方式,进一步发挥医保基金在降低药品价格方面的议价作用;另一方面,持续推进药品带量采购试点工作,并加强与仿制药质量和疗效一致性评价以及鼓励创新药物研发等改革工作的衔接,同时要兼顾各方的合法利益[22],引导产业健康合理发展。与此同时,继续巩固公立医院综合改革的成果,加强药物采购环节的规范性,进一步切断公立医院与药品生产经营企业的灰色利益链条,对违法违规行为加大打击和处罚力度。
6 结语
本研究通过对“新医改”以来我国药物领域政策文件的梳理与分析发现,我国药物政策领域的政策体系基本按照国家药物政策框架开展,同时结合我国药物领域改革的实际情况,已经形成了我国药物领域的改革逻辑,并且取得了较大成效。接下来,应重点补足政策短板,加强顶层设计,进一步深化药物领域的改革,完善我国药物政策体系。
(作者声明:本文无实际或潜在的利益冲突。)

