巨细胞病毒大肠炎的临床特征分析
张馨梅,赵有财,张振玉
南京医科大学附属南京医院(南京市第一医院) 1.消化科;2.病理科,江苏 南京 210006
巨细胞病毒(cytomegalovirus,CMV)属疱疹病毒科DNA病毒,CMV感染在成人中普遍存在,文献报道其血清阳性率为40%~100%[1]。健康个体初次感染CMV时常常无症状或仅为传染性单核细胞增多综合征样表现,之后病毒持续潜伏存在,当免疫功能不健全或缺陷时,潜伏病毒再激活,从而导致CMV感染性疾病[2]。CMV最常侵犯的器官为视网膜,其次为大肠[3]。临床上也可见到免疫健全的CMV肠炎患者。CMV大肠炎临床发病率低,可引起消化道出血、穿孔等严重并发症,并被认为与炎症性肠病(inflammatory bowel disease, IBD)急性发作、病情复发、药物难治性和并发症的风险相关[4]。本文对2012年1月1日至2018年10月31日南京医科大学附属南京医院(南京市第一医院)收治的16例CMV大肠炎患者的临床、内镜和病理等情况进行总结分析,为正确识别CMV肠炎,及时抗病毒治疗,改善患者预后提供参考。
1 资料与方法
1.1 临床资料包括年龄、性别、基础病史,免疫状况、临床表现、并发症、治疗情况及转归。免疫缺陷定义为以下情况之一:获得性免疫缺陷综合征,器官移植术后,6个月内使用过免疫抑制剂、糖皮质激素或化疗药物[5]。疾病缓解定义为临床症状消失。
1.2 内镜资料病变范围、黏膜形态及溃疡特征。
1.3 病理学资料对结肠镜检查的活检标本或手术切除标本包埋、切片后进行HE染色及CMV免疫组化染色。CMV大肠炎的诊断依据为HE染色观察到包涵体和(或)CMV免疫组化阳性。

2 结果
2.1 一般信息及基础疾病2012年1月1日至2018年10月31日,消化科住院患者中共查找到16例CMV大肠炎患者,男9例,女7例;IBD 10例(UC 8例,CD 2例);免疫健全者10例,免疫缺陷者6例(其中5例为6个月内使用硫唑嘌呤、环磷酰胺或糖皮质激素的IBD患者,1例为艾滋病患者)。免疫健全者年龄(55±15)岁(26~70岁),免疫缺陷者年龄(40±16)岁(26~73岁),差异无统计学意义(P>0.05)。IBD患者年龄(47.4±16.8)岁(26~73岁),非IBD患者年龄(51.3±17.1)岁(26~68岁),差异无统计学意义(P>0.05)。
除IBD以外,患者合并的肠道相关疾病包括:慢性血吸虫肠病、阑尾炎;非肠道慢性疾病包括:高血压、冠心病、糖尿病、脑梗死。各基础疾病在免疫健全者及免疫缺陷者中的分布差异无统计学意义(P>0.05)(见表1)。
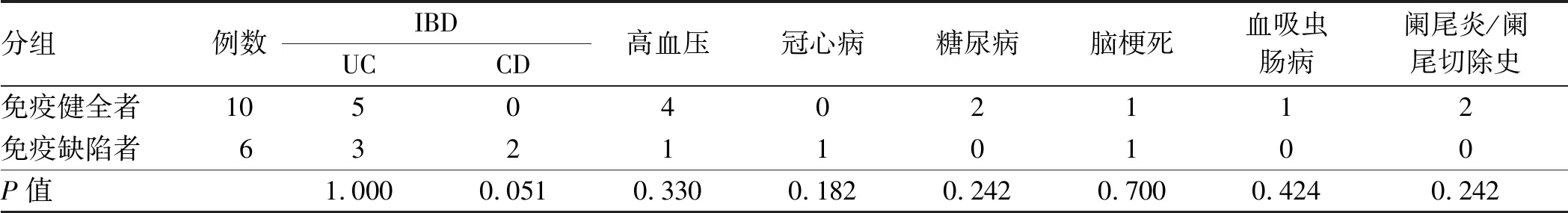
表1 免疫健全及免疫缺陷的CMV大肠炎患者的基础疾病比较Tab 1 Comparison of underlying diseases between immunocompetent and immunodeficient CMV colitis patients
2.2 临床表现CMV大肠炎的主要临床表现为腹痛、腹泻、便血、发热。其中,IBD患者合并CMV大肠炎者腹泻比例显著高于非IBD患者(P<0.05),其余症状在两组间比较,差异无统计学意义(P>0.05)(见表2)。1例CD患者确诊CMV肠道感染时无明显自觉症状。2例糖尿病患者表现为以腹痛、腹胀为首发症状的假性肠梗阻。

表2 IBD合并CMV大肠炎的患者与非IBD的CMV大肠炎患者的临床症状比较Tab 2 Comparison of symptoms between CMV colitis patients with IBD and those without IBD
2.3 内镜特征16例患者中,10例为广泛结肠炎,2例为左半结肠炎,4例为右半结肠炎。CMV肠炎的镜下表现多种多样,16例患者中可观察到的黏膜特征包括:纵行溃疡、不规则溃疡、深凿溃疡、广泛黏膜剥脱、鹅卵石样改变、浅小溃疡或糜烂。其中,单纯浅小溃疡或糜烂仅出现于非IBD患者(见表3)。
IBD合并CMV大肠炎的内镜特征:UC合并CMV大肠炎:8例UC患者中,7例为广泛结肠受累,1例为左半结肠受累。内镜下溃疡表现包括不规则溃疡、纵行溃疡、深凿溃疡、鹅卵石样改变和黏膜剥脱(见图1)。CD合并CMV大肠炎:2例CD患者中,1例为广泛结肠节段性受累,1例为以右半结肠为主的节段性受累。2例患者均存在不规则溃疡,其中1例同时存在典型的鹅卵石样改变。
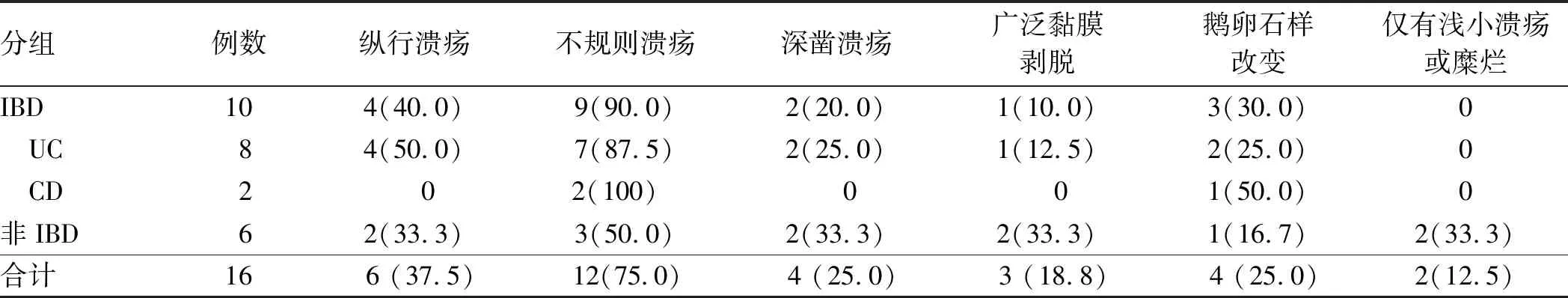
表3 CMV大肠炎患者的内镜特征
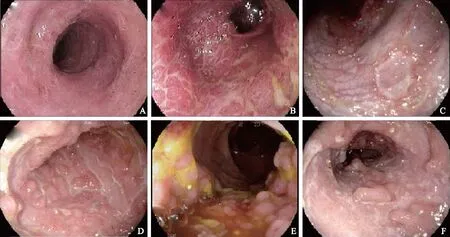
图1 UC合并CMV感染的内镜表现 A: 典型UC的内镜表现; B:不规则溃疡; C:深凿溃疡; D:纵行溃疡; E:鹅卵石样改变; F:广泛黏膜剥脱;Fig 1 Endoscopic findings in UC patients with CMV colitis A: classic UC endoscopic imaging; B: irregular ulceration; C: punched-out ulceration; D: longitudinal ulceration; E: cobblestone-like appearance; F: wide mucosal defect
2.4 组织学特征15例为肠镜标本,1例为手术标本(1例UC患者因并发中毒性巨结肠行急诊全结肠切除术)。 16例均为免疫组化阳性,其中3例观察到包涵体(见图2)。
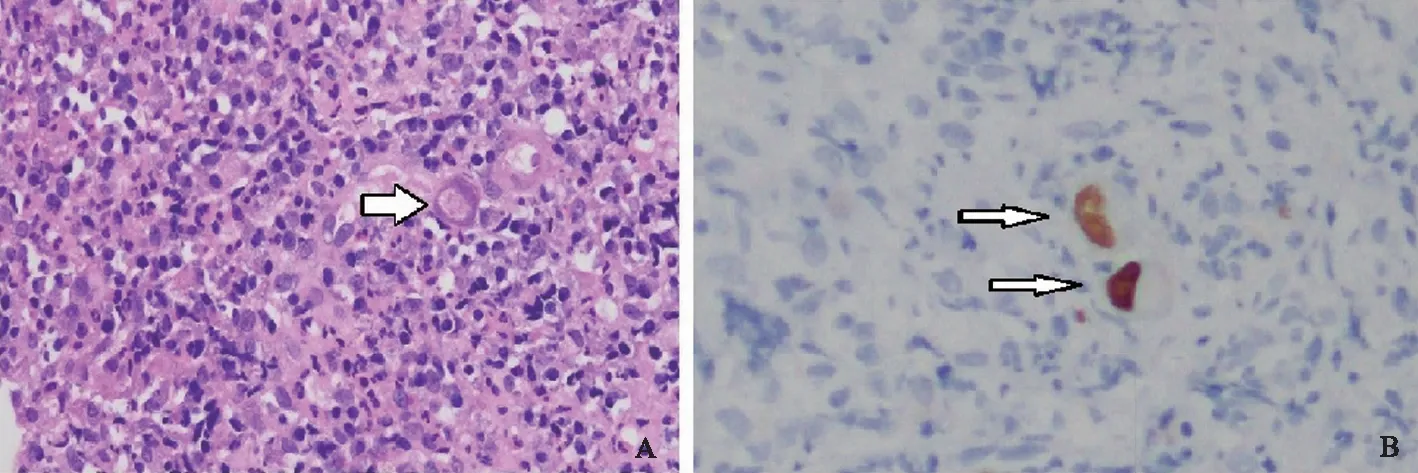
图2 CMV的病理检查结果 A: HE染色(400×),箭头所指为包涵体;B:免疫组化染色(400×),箭头所指为染色阳性区域
2.5 治疗及转归除1例UC患者并发中毒性巨结肠行急诊全结肠切除术以外,其余患者均接受更昔洛韦抗病毒治疗(5 mg/kg,2次/d,共14 d)。抗病毒治疗总体缓解率为86.7%。具体治疗情况及转归按基础疾病分别阐述如下:UC:8例患者中,3例半年内有糖皮质激素和/或免疫抑制剂使用史(疗程超过2周),其中1例为上述并发中毒性巨结肠后行结肠切除的患者,另2例予更昔洛韦治疗,同时糖皮质激素减量,治疗后缓解。5例无激素或免疫抑制剂暴露史的患者中,3例单纯予更昔洛韦治疗后缓解,2例予更昔洛韦联合糖皮质激素治疗后缓解。CD:2例患者中,1例抗病毒治疗前后均无明显自觉症状,另1例持续糖皮质激素联合硫唑嘌呤控制原发病,抗病毒治疗前症状即得到缓解。糖尿病伴假性肠梗阻:2例均予更昔洛韦治疗,其中1例腹痛、腹胀缓解,另1例并发巨结肠,出院时仍未能完全缓解。艾滋病:1例,经更昔洛韦治疗后发热消失,腹泻好转,后转至传染病专科医院。慢性血吸虫肠病:1例,经吡喹酮抗血吸虫及更昔洛韦抗病毒治疗后,腹痛、腹泻、便血等临床症状无明显缓解,最终死于消化道大出血。其余2例,经抗病毒治疗后症状缓解,复查肠镜,黏膜损伤愈合或好转。
3 讨论
CMV为常见人体感染病毒,尽管在人群中的总体感染率较高,但绝大多数处于初次感染后的潜伏状态,并不产生显性症状。当人体发生免疫系统紊乱时,潜伏病毒再次激活,从而发生CMV疾病。CMV大肠炎是免疫缺陷患者较常见的机会感染性疾病之一。临床工作中我们观察到CMV大肠炎也存在于免疫健全的患者中,本研究中,免疫健全者占所有CMV大肠炎患者的62.5%。台湾邱正堂教授观察的69例CMV大肠炎患者中,免疫健全的患者占61%,与我们的比例相似。免疫健全者发生CMV感染的危险因素包括:危重的病情、妊娠、肾衰竭、糖尿病、未治疗的恶性肿瘤、输血、肠道黏膜缺损等[5]。本研究中,免疫健全组患者平均年龄高于免疫缺陷组,合并高血压、糖尿病的比例大于免疫缺陷组,但差异均无显著性,考虑与本研究样本量较小有关。免疫健全组的高龄趋势,理论上使其糖尿病、高血压、冠心病、脑梗死等慢性疾病的发生概率升高,患者存在多重慢性病,一般情况较差,可能为其发生CMV大肠炎的危险因素。
本研究中IBD患者占62.5%,其中80%为UC患者。IBD患者为CMV大肠炎的易感人群。文献报道,在急性重度IBD中CMV感染率为21%~34%,激素抵抗者的CMV感染率为33%~36%[6-7]。目前认为,IBD患者感染CMV的高危因素主要包括:IBD本身的炎症反应特点,患者较普遍的糖皮质激素及免疫抑制治疗史,营养不良状况及CMV对炎性组织的趋化作用[8]。CMV感染在CD患者中的发病率比在UC中低得多,这可能是由于CD以Th1型炎性过程为主,多表达抑制CMV激活的IFN-γ,而UC以表达刺激CMV激活的TNF-α为主[9-10]。
CMV大肠炎的常见临床症状包括腹痛、腹泻、便血、发热、纳差等,并不具有特异性。我们的研究中观察到,CMV大肠炎的具体症状与炎症程度、累及范围及患者合并的基础疾病状态相关。例如糖尿病伴假性肠梗阻的患者主要表现为腹胀、腹痛。IBD患者合并CMV感染时腹泻的发生率显著高于非IBD的CMV大肠炎患者。目前越来越多的证据表明,CMV感染可以影响IBD疾病进程。CMV感染与IBD急性发作、复发、药物难治性和并发症的风险相关。当IBD患者,尤其是UC患者出现高热,之前稳定的病情迅速恶化,出现激素抵抗时,需警惕合并CMV感染[11-13]。
CMV大肠炎的内镜表现异质性较大。我们观察到的非IBD患者的内镜表现包括:纵行溃疡、不规则溃疡、深凿溃疡、黏膜剥脱、鹅卵石样改变及单纯浅小溃疡或糜烂,与文献报道的一致[14-15]。除单纯浅小溃疡或糜烂之外,其他所有的内镜表现均可见于IBD合并CMV感染的患者。UC患者合并CMV感染时可出现一些特征性的黏膜缺损。一项研究分析了73例UC患者(CMV阳性15例,阴性58例)内镜下黏膜及溃疡改变,发现以下病变在CMV阳性患者中更易出现:广泛的黏膜剥脱、极易出血性、深凿溃疡、纵行溃疡及鹅卵石样改变,而不规则溃疡在CMV阳性患者中的敏感性为100%[16]。北京协和医院杨红等的研究发现,深凿溃疡与组织学检出大量包涵体高度相关[17]。本研究中,UC合并CMV感染最常见的内镜表现依次为不规则溃疡、纵行溃疡、深凿溃疡、鹅卵石样改变及黏膜剥脱,基本与文献相符。对于CD患者,文献未报道可鉴别CMV阳性者与阴性者的内镜下依据。
组织HE染色观察到包涵体可诊断CMV感染。HE染色诊断特异性高(92%~100%),但敏感性低(10%~87%)。而单克隆抗体检测CMV早期抗原的免疫组化法敏感度为78%~93%,目前被认为是诊断CMV感染的金标准[18]。本研究中所有患者均依据免疫组化法确诊,但其中仅3例观察到包涵体,可能与取材部位不理想有关。CMV包涵体多存在于黏膜血管周围及溃疡基底部,浅表黏膜活检结果可能并不准确。血清学检测及血液或粪便PCR检测也是诊断CMV感染的重要手段。当临床、内镜高度怀疑CMV感染而组织学不能提供确诊依据时,较高的血浆CMV DNA载量也可提示存在CMV相关疾病[11]。由于我院早期未开展CMV PCR检测项目,以及活检取材的局限性,实际CMV大肠炎的患者数量可能是被低估的。
除1例UC患者并发中毒性巨结肠行急诊全结肠切除术以外,本研究其余15例患者均接受更昔洛韦抗病毒治疗。其中13例住院期间疾病获得好转,但并非均与抗病毒治疗存在因果关系。2例UC患者抗病毒同时联合足量糖皮质激素治疗后缓解,2例CD患者抗病毒治疗开始前即因原发病得到控制而症状缓解。上述患者对抗病毒治疗的反应提示,IBD合并CMV感染是否需要抗病毒治疗,应进行个体化选择,临床过程考虑与CMV感染无关时无需抗病毒治疗[4,11-12,19-21]。抗病毒治疗后症状未能缓解的2例分别为:1例糖尿病并发巨结肠者,1例慢性血吸虫肠病并发消化道大出血者。此2例患者均存在基础的肠道功能受损,CMV感染可能为诱发严重并发症的重要因素。对于此类危重患者,尽早的抗病毒治疗有望提高患者的生存率。
CMV大肠炎临床少见,若不能及时诊治,可导致消化道大出血、巨结肠等严重并发症。当存在免疫缺陷或多重慢性病、一般情况较差的患者出现腹痛、腹泻、便血、发热等症状时,应想到CMV大肠炎。IBD患者是CMV大肠炎的易感人群,CMV感染与难治性UC关系密切。当UC患者出现高热,之前稳定的病情迅速恶化,内镜下出现特征性溃疡,并且强化治疗3 d内仍无效果时,需警惕合并CMV感染。尽早的抗病毒治疗可改善CMV大肠炎的预后。对于患有IBD及其他肠道基础疾病的患者,抗病毒治疗同时,应兼顾肠道原发病的治疗。由于本研究纳入患者数量有限,仅初步探讨了CMV大肠炎的临床特征,而CMV大肠炎异质性较大,未来仍需进一步的临床观察和研究。

