山东省动物源细菌耐药性的现状、问题及应对措施
李有志 冯涛 魏茂莲 魏秀丽
摘要:基于对山东省动物源细菌耐药性和兽用抗菌药使用情况的调研,分析了山东省动物源细菌耐药性现状和存在的问题,并提出了防控策略。需深化绿色生态产品新制剂的研究;加强高效、低毒新型抗菌药研制,优化畜禽养殖环境生态系统控制;加快完善细菌耐药性监测体系构建,严格落实兽用抗菌药分类和科学精准使用药物;推进兽用抗菌药减量化示范行动等综合措施,从根本上遏制兽用抗菌药滥用,以期降低细菌耐药性的发生和发展,保障畜禽产品质量安全。
關键词:动物源细菌;耐药性;问题;防控策略
Present Situation, Problems and Countermeasures of DrugResistance of Zoonotic Bacteria in Shandong Province
Li Youzhi, Feng Tao, Wei Maolian, Wei Xiuli
Abstract
Based on the investigation on drug resistance of zoonotic bacteria and use of veterinary antimi-crobial in Shandong Province, the present situation and problems of drug resistance were analyzed, and theprevention and control strategies were put forward. It should be necessary to deepen the research on new prep-arations of green ecological products, strengthen the development of new antimicrobial agents with high effi-ciency and low toxicity, optimize the ecosystem control of livestock and poultry breeding environment, acceler-ate the improvement and construction of a monitoring system for bacterial drug resistance, strictly carry out theclassification of veterinary antimicrobial drugs and scientific and accurate use of drugs, and promote the com-prehensive measures to reduce the use of anti - bacterial drugs , so as to control the abuse of veterinary antimi-crobial drugs, reduce the occurrence and the development of the drug resistance of bacteria, and ensure thesafety of product quality of livestock and poultry.
Keywords
Zoontic bacterial; Drug resistance;Problem;Prevention and control strategy
近年来,随着人们对食品安全和公共卫生安全的高度重视,畜牧领域的环境污染、兽药残留和细菌耐药性问题越来越受到关注。“3·15晚会曝光饲料非法添加”、“毒鸡蛋事件”等聚焦兽药残留、违禁用药等突出问题,2017年12月新华通讯社以“我国可能出现无药可治的超级细菌”为标题,详细报道了我国农业抗生素滥用问题。我国动物源细菌耐药性非常严重[1-3],相关问题已引起国家和有关部门的高度重视,农业农村部首次把“开展兽用抗菌药综合治理”列入2018年全国兽医工作要点,5月19日在重庆组织启动了“兽用抗菌药使用减量化行动”,深入开展养殖环节抗菌药使用减量化示范创建活动。
1 动物源细菌耐药性的现状
1.1 兽用抗菌药物使用情况
我国批准使用的兽用抗菌类药物主要有B -内酰胺类、氨基糖苷类、大环内酯类、糖肽类、多肽类、氯霉素类和四环素类等8类,共56个品种;合成抗菌药主要品种有磺胺类、喹诺酮类及其他,共3类45个品种。
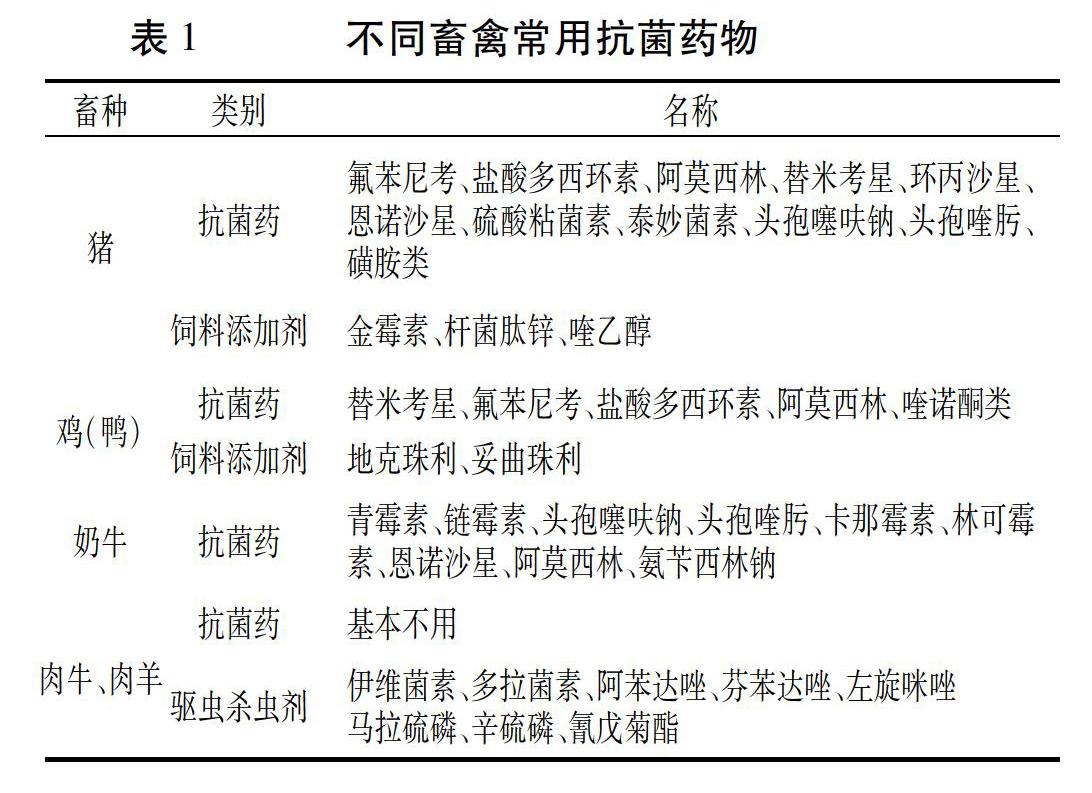
山东省日前开展兽用抗菌药物使用专题调研,前三位的畜禽品种分别是生猪、奶牛和肉鸡,约占全部抗菌药物的70%左右;宠物及水产用约28%;肉牛、肉羊除疫苗防疫、驱虫外,基本不用抗菌药。抗菌药以氨基糖苷类、B -内酰胺类、四环素类、磺胺类、大环内酯类、氯霉素类较多。饲料药物添加剂主要使用金霉素预混剂、杆菌肽锌、地克珠利(肉鸡)等(表1)。商品猪出栏每头需要抗菌药费用10~15元左右,肉鸡每只需要抗菌药费用0.5~0.8元,每头泌乳奶牛年抗菌药费用300~400元,以上数据不包括防疫用疫苗费用。
1.2 动物源细菌耐药性情况
山东省是畜牧养殖大省,近30年来养殖业快速发展,至2017年底,全省肉蛋奶总产量1490万吨;兽药生产企业近300家,省级以上标准化养殖示范企业近300家,规模养殖比重达71%。集约化和规模化养殖对病原菌的防控需要抗生素作为保障,但由于整体的抗药性监测体系薄弱,大量使用抗菌药物造成细菌耐药性快速发展,我国已成为世界上动物源细菌耐药性最严重的国家之一,并陷入“耐药性上升一用药量/种类上升一耐药性再上升”恶性循环。
兽医临床常用的四环素类、B -内酰胺类和喹诺酮类等抗菌药物疗效已严重下降甚至失效;常见病原菌(大肠杆菌、金黄色葡萄球菌、链球菌、副猪嗜血杆菌、胸膜肺炎放线杆菌、巴氏杆菌、支原体、沙门氏菌、克雷伯菌、绿脓假单胞菌等)临床分离株可耐受的药物达5—20种,出现无药可用的尴尬局面。不仅如此,人、畜共用同类甚至同种抗生素,加之一些人畜共患病原菌尤其是食源性病原菌(如沙门氏菌、弯曲杆菌等)多重耐药株的出现和在人畜之间流行,对我国的动物源食品安全和公众卫生构成了严重威胁[1-3]。
张利锋等对山东大型肉鸡养殖场、屠宰场分离的373株大肠杆菌进行药物敛感性检测、blaCTX-M基因核酸检测及序列分析。结果表明菌株对头孢他啶、头孢噻肟和哌拉西林耐药率高,依次是89.3%、92.8%和91.7%,头孢菌素类药物间存在交叉耐药性,菌株blaCTX-M基因的携带率高达54.7%,来自养殖和销售等不同环节的菌株携带的blaCTX -M基因集中在4个亚型,分别是blaCTX-M-55、blaCTX-M-65、blaCTX -M-14和blaCTX-M-27,提示肉鸡食品链不同环节可能存在大肠杆菌耐药性的传播[4]。
刘建民等对2010年以来分离自山东省潍坊市发病肉鸭的232株大肠杆菌进行了药敏试验,发现洛美沙星、培氟沙星、氧氟沙星、诺氟沙星的耐药率为54.31%~82.76%,质粒介导氟喹诺酮类耐药基因( PMQR)携带率达到58.19%,26.29%的菌株携带两种PMQR基因,1.72%的菌株携带三种PMQR基因。未检测到qnr 4、qnrB、qnr C、qnr D与Qep A基因;qnr S、oqxA和oqxB基因在山东省禽源致病性大肠杆菌中分布较为广泛,其检出率依次为19.83%、41.81%和26.29%[5]。
刁有江等从山东部分地区的规模化肉鸭场分离到致病性大肠杆菌92株,对19种受试药存在不同程度的耐药性。70%以上的大肠杆菌分离株对氨苄青霉素、阿莫西林、多西环素、痢菌净、环丙沙星、恩诺沙星、诺氟沙星、磺胺甲基异恶唑/甲氧苄啶8种抗菌药耐药;此外,还有50%以上的菌株对卡那霉素、氧氟沙星以及黏菌素3种抗菌药表现为耐药。所有分离株均为多重耐药菌株。78.26%的分离株对8种或8种以上的受试药耐药[6]。
王昌健采集山东部分地区的病猪病料分离大肠杆菌菌株79株,对红霉素、磺胺嘧啶、氨苄西林的耐药性非常高(100%分别占5、3、4个地区);对多粘菌素敏感性高达100%;对头孢噻肟耐药性为21.51%;对环丙沙星的耐药率最高达82.72%,对洛美沙星、加替沙星、恩诺沙星、左氟沙星、诺氟沙星耐药率分别为15.19%、20.20%、21.51%、26.58%、27.84%,对链霉素、复方新诺明、多西环素、氟苯尼考、庆大霉素的耐药率均在58%以上,基本上不能用于临床治疗[7]。
冯敏燕等采用96点阵药敏检测法,测定从临床上分离鉴定的2008 -2014年山东省不同地区鸡场的210株大肠杆菌对14种抗生素的耐药性。结果显示13种(多西环素除外)的耐药性在这7年间有所增长,其中对10种抗生素的耐受性在7年间近乎翻了1倍甚至更高。根据监测结果,建议在山东地区暂停使用头孢噻呋治疗鸡大肠杆菌病,推荐使用多西霉素、大观霉素,将庆大霉素、新霉素、恩诺沙星、氟苯尼考作为次级药物使用[8]。
王娟等采用微量肉汤稀释法对298株生猪屠宰环节中沙门氏菌进行8大类13种药物的药敏试验。结果显示多西环素、四环素的耐药率较高,分别为97.99%、80.20%,对粘杆菌素E最为敏感,耐药率仅为2.01%,多重耐药率为81.88%,优势耐药谱型为四环素一多西环素[9]。
孙璐等从山东省不同地市肉鸡屠宰生产链中分离的233株沙门氏菌对庆大霉素的耐药率最高(100%);对多西环素、氨苄西林、大观霉素、四环素、氟苯尼考和磺胺异恶唑耐药率分别为84.94%、75.73%、67.78%、56.00%、52.00%和50.00%。72.00%的菌株表现为多重耐药(≥3),产生了57种耐药谱型[10]。
李秀梅等采用纸片扩散法测定从奶牛场分离的121株金黄色葡萄球菌对6种抗生素的敏感性:耐苯唑西林金黄色葡萄球菌( MRSA)为26株,占21.5%;对苯唑西林敏感菌(MSSA)为93株,占76.9%;中介菌株为2株,占1.6%;金黄色葡萄球菌对6种抗生素耐药率最低的是头孢噻肟,为2株,占1.6%。MSSA对大部分抗生素仍保持良好的敏感性,而MRSA表现为多重耐药性[11]。
由以上文献可以看出山东省不同地区、不同年代,大肠杆菌、沙门氏菌、金黄色葡萄球菌对不同药物的耐药水平有所不同,但随着年代的变化,耐药性逐年升高,且为多重耐药性,耐药基因在产业链中可以传播;氟喹诺酮类药物的多种药物耐药率居高不下,农业农村部于2016年1月1日开始禁止经营及使用洛美沙星、培氟沙星、氧氟沙星、诺氟沙星等4种人兽共用抗菌药物用于食品动物,也是出于人类健康和生态安全考虑。头孢菌素类药物的耐药性近两年也有所提升,磺胺类药物、四环素类药物的耐药性普遍很高。
中小规模养殖场驻场兽医认为,现在单纯用抗菌药物来防治动物疫病难度越来越大、成本越来越高,多数药物按照推荐剂量进行治疗往往效果不理想,加大用药量的现象比较普遍。鉴于细菌耐药性问题已经列为了本世纪最重要的公共安全事件之一,动物源细菌耐药性问题可能会成为继兽药残留之后动物源性食品贸易的又一技术壁垒,因此运用互联网尽快建成山东省细菌耐药性监测大数据平台,实现一药多菌、一菌多药的时空查询迫在眉睫。
1.3 相关法律法规、监测标准
1.3.1 法律法规我国涉及动物源细菌耐药性的法律尚缺失,三个行政法规从不同层面强调了动物源细菌耐药性监测的重要性,对细菌耐药性监测防控工作起到了提纲挈领的作用。
(1)2016年8月25日,國家卫生计生委等14部门联合发布的《遏制细菌耐药国家行动计划(2016-2020年)》提出:到2020年健全医疗机构、动物源抗菌药物应用和细菌耐药监测网络,人兽共用抗菌药物或易产生交叉耐药性的抗菌药物作为动物促生长应用逐步退出,加强兽用抗菌药物监督管理,制定兽用抗菌药物安全使用指导原则和管理办法,推动动物专用抗菌药物和可替代抗菌药物的动物疾病预防与促生长产品研究与开发等措施,使动物源主要耐药菌增长率得到有效控制。
(2)2017年5月12日国家发展改革委、农业农村部、质检总局、林业局联合发布的《全国动植物保护能力提升工程建设规划(2017-2025年)》提出:兽药质量监察能力建设主要是建设中国兽医药品监察所和省级兽药检验机构的动物源细菌耐药性监测实验室。
(3)2017年6月23日农业农村部发布的《全国遏制动物源细菌耐药行动计划(2017-2020年)》明确提出六大行动:一是实施“退出行动”,推动促生长用抗菌药物逐步退出;二是实施“监管行动”,强化兽用抗菌药物监督管理;三是实施“监测行动”,健全动物源细菌耐药性监测体系;四是实施“监控行动”,强化兽用抗菌药物残留监控;五是实施“示范行动”,开展兽用抗菌药物使用减量化示范创建;六是实施“宣教行动”,加强从业人员培训和公众宣传教育。
1.3.2 监测标准和方法 目前,国内动物源细菌耐药性监测技术缺少统一的行业标准,201 8年农业农村部的监测标准都以《2018年动物源细菌耐药性监测计划》附件的形式发布。我国动物源细菌耐药性监测的过程控制,主要针对病死畜禽、健康畜禽和新鲜牛奶等。同时,为保证动物源细菌耐药性监测采样过程的规范性和代表性,除了无菌采样的基本要求外,还要求各监测单位须将定点采样和随机采样相结合,每个耐药性监测实验室每年选择10~20个养殖场或屠宰厂(要求规模化养殖场和小型养殖场各占一半)进行随机采样,选择2个定点养殖场为跟踪监测场。
各监测单位采用相同的方法开展目标菌的分离和鉴定,主要包括大肠杆菌、肠球菌、沙门氏菌、金黄色葡萄球菌、弯曲杆菌等,检测手段日趋多元化。
(1)耐藥表型检测[12]。琼脂扩散法:纸片扩散法、E-Test;稀释法:微量肉汤稀释法、琼脂稀释法。目前欧盟等国际通用的检测方法为微量肉汤稀释法,我国多采用微量肉汤稀释法[13]。山东省农业科学院根据CLSI、EUCAST标准,结合自行研制的智能化药敏检测仪,制定了山东省地方标准DB37/T 2806-2016《兽医病原菌琼脂稀释法药物敏感性试验规范》,准确定量检测动物源细菌对抗菌药物的最小抑菌浓度值(MIC值),然后登陆动物源细菌耐药性数据库,将采样信息以及耐药性检测结果录入数据库,运用数据库的强大分析功能,统一进行结果的汇总分析和数据的溯源。
(2)耐药基因型检测。PCR技术:普通PCR、多重(元)PCR、PCR - RFLP,LAMP等;DNA 测序:基因突变分析;基因探针:DNA探针、RNA探针;基因芯片:可同时检测多个已知的重要耐药基因;全基因组测序:具有较好敏感性和特异性,可全面分析耐药基因。
1.4 山东省动物源细菌耐药性监测情况
动物源细菌的耐药性问题已在世界范围内引起广泛关注,世界卫生组织( WHO)、世界动物卫生组织(OIE)和联合国粮农组织(FAO)均建议各国特别是发展中国家,尽快建立切实可行的检测监测方法,开展细菌耐药性调查,建立国家监测网,控制以致消除细菌耐药性问题。20世纪90年代中期,发达国家意识到细菌耐药性的潜在危害,先后成立了国家耐药性监测系统,如美国的NARMS、瑞典的SWARM、丹麦的DAN - MAP、加拿大的CIPARS等,分别监测动物、食品和人体内分离的食源性病原菌耐药性,并发布耐药性监测年度报告。
我国自2008年起由农业农村部牵头成立了国家兽药安全评价(耐药性监测)实验室,开始组建动物源细菌耐药性监测系统,监测范围覆盖全国22个省(自治区)和4个直辖市[13],并根据耐药性风险评估结果停止了粘菌素用作饲料添加药物,禁用了4种人用喹诺酮类抗菌药物,但整个监测系统覆盖的取样点数量依然较小,监测细菌的种类也仅限于沙门氏菌、大肠杆菌、金黄色葡萄球菌和弯曲杆菌等8种。2018年《动物源细菌耐药性监测计划》监测单位由原来的各省市畜牧兽医局扩展到包括科研院所在内的23家,监测力度进一步加强。
山东省是国内最早开展细菌耐药性监测工作的省份之一,早在2008年山东省兽药质量检验所就对多发的大肠杆菌、沙门氏菌、肠球菌、金黄色葡萄球菌等常见病原菌进行分离、鉴定并建立菌株保藏库,开展了耐药机理研究。2012年山东省农业科学院畜牧兽医研究所、莱阳市大房禽病研究所、六和、中慧、民和、春雪、益生、仙坛和九联等9家单位签订了《山东省鸡病原菌抗药性监测与合理精确用药的倡议》,在大型养殖企业建立了细菌耐药性检测实验室。2016年1月,山东省农业科学院与山东省畜牧兽医局共建“山东省兽医抗药性监测网”(Varms),采集收藏了2007年至今的万株耐药菌株和耐药信息,撰写了我国首部兽医抗药性监测与防控年报;2016-2018年连续举办了三届“齐鲁国际讲堂”,成立了“中欧兽医药敏试验合作实验室”、“中英噬菌体合作研发实验室”,加强了在这一领域与发达国家及人医、疾控的广泛交流与合作。
1.4.1 Varms近十年菌株库 2007-2017菌株总数为10512株,主要包括大肠杆菌、沙门氏菌、金黄色葡萄球菌、肺炎克雷伯菌、变形杆菌、铜绿假单胞菌、里默氏菌、肠球菌等;菌株覆盖山东各地市重点养殖企业,少数来自广东、河南、吉林等地;菌株来源包括种鸡、肉鸡、肉鸭、猪、奶牛、毛皮动物等畜种及对应环境和从业人员;菌株包括来自感染动物的内脏病原菌分离株、健康动物粪样、鼻拭子正常菌群的分离株。
1.4.2 药敏数据库 2010-2017细菌药敏MIC数据共为65163个,药物包括临床常用荮物,细菌抗药表型具体到确定的MIC值。根据CLSI、EUCAST和山东省地方标准(Varms),可以查询菌株的MIC分布和抗药率。
1.4.3 主要细菌的抗药状况 对于临床常见药物,所有细菌表现出普遍抗药性。综合看来,大肠杆菌抗药率最高,沙门氏菌次之,金黄色葡萄球菌相对较低;从2010-2017年,大肠杆菌对常用药物的抗药率普遍较高,在2013年和2014年出现抗药高峰,近年有下降趋势;综合看来,肉鸡和猪来源的细菌抗药性普遍高于奶牛源分离的细菌,不同畜种对不同药物又呈现出不同的抗药性水平。
健康动物来源的大肠杆菌和病料来源的大肠杆菌在不同药物的抗药性上存在一定差异,总体来讲,健康来源的大肠杆菌抗药性略高。来自健康动物的大肠杆菌可以做为山东畜牧行业抗药性水平的指示菌,其抗药性水平在一定程度上说明养殖业抗药性背景。山东省内重点养殖地区抗药性水平高,存在显著的地区差异,据此可以开展轮换用药和分级管理。
2 动物源细菌耐药性问题分析
2.1 养殖环节抗菌药滥用问题突出
细菌耐药性的产生与抗菌药物滥用密切相关。一些中小规模养殖场由于饲养方式粗放、临床兽医缺乏等原因,兽药使用档案记录不全或未建档案,往往盲目地向饲料和饮水中投放抗菌药进行群体性预防和治疗,又不设休药期,直接导致了严重的动物细菌耐药和产品药残超标。在生产中目前能替代抗菌药物的临床解决方案不多,除疫苗产品外,其它中兽药产品、抗菌肽类和微生态制剂等因显性成本高或疗效不明显难以被养殖者认同,缺少行之有效的绿色高效制剂替代解决方案。
2.2 对耐药性带来危害的认识不清
过量使用抗菌药物造成的细菌耐药性不仅体现在养殖环节,也对整个食品安全和公共卫生造成了严重后果,影响波及到经济社会和生态各个环节。目前,人们对卫生健康领域的耐药性有了一定的认识,相关法律法规和措施逐步健全,但对畜牧领域的耐药性问题认识仍不到位,特别是以减抗替抗为方向的健康养殖模式研究很少,养殖废弃物处理方面也少见针对抗菌药处理的研究,由此造成以原型和代谢物形式进入环境的抗菌药最终到达人体,对生态环境和人类健康造成很大损害。
2.3 耐药性监测体系机制未有效建立
山东省动物源细菌耐药性监测工作起步较晚,目前仍存在体系化薄弱、监测覆盖范围小和技术力量单薄等诸多问题,监测还仅停留在省级层面和科研领域,养殖企业参入的主动性和检测数据的实用性不强。监测的标准体系尚未有效形成,多年来检测的依据还仅仅停留在部颁指令上,行业标准或规范对这一领域的指导性有待提高。政策法规的配套出台严重滞后,工作更多地是靠行政命令推行和参与者的自觉行为,至今未有对过量使用抗菌药物造成细菌耐药的处罚措施,未形成通过对药物敏感性测定指导临床动物用药的体制机制。
3 细菌耐药性控制对策与措施
畜牧业中疫病防控、动物促生长和细菌耐药性监测是一个系统工程,需要采取综合防控战略。通过开发绿色饲料添加剂提高动物机体免疫力、优化畜禽养殖环境、严格执行防疫制度和科学精准使用抗菌药等综合措施,才能从根本上遏制兽用抗菌药滥用,减少动物源细菌耐药性产生。
3.1 严格兽用抗菌药分类和使用管理
首先要加强兽药在审批、生产和使用环节的监督管理,严格区分处方与非处方用药、人用药和动物用药,严格规定兽用抗菌药的休药期,逐步禁止抗菌药在饲料中的添加使用。目前,美国和欧盟都已全面禁止将抗菌药物用作饲料添加剂,我国也停止了硫酸粘菌素用于动物促生长,并禁止了氧氟沙星等4种氟喹诺酮类药物在食品动物中使用;农业农村部2638号公告决定2019年4月30日后禁止在食品动物中使用氨苯胂酸、洛克沙砷、喹乙醇相关制剂[14];今后还应继续加大在这一领域的整治力度。同时,严格新兽药注册和临床使用审批,对新批准抗菌药进行包括耐药性在内的系统安全评价,做好投放市场后的跟踪监测,全面评价细菌耐药性情况。
3.2 加快细菌耐药性监测体系构建
充分发挥国家在细菌耐药性领域的政策、组织和人才资源,统筹规划区域布局,加快构建覆盖全国的区域性、省级、科研机构和企业细菌耐药性监测体系。在“国家兽药安全评价(耐药性监测)实验室”的统一指导下,依托国家动物源细菌耐药性数据库系统,开发相关软件,建立数据转换統一标准模块、分析模块、算法库等,实现数据汇集、数据信息快速分析、实时监控、信息共享等功能,建立国家“互联网+细菌耐药性大数据平台”。以全国动物源细菌耐药性监测技术平台为依托,持续开展区域性动物源细菌的耐药性监测、耐药趋势的追踪和报告,综合药物、动物和细菌三要素,研究建立MIC折点(MIC breakpoint( Ecoff值)[15]标准。加强耐药性风险评估方法研究,制定耐药性风险评估标准,为行政部门和兽医临床提供及时、准确的细菌耐药技术支撑,指导养殖企业临床精准选用抗菌药物,提高治疗效果以及控制耐药菌的扩散和传播。
3.3 深化绿色植物提取类新制剂研究
绿色植物类产品如微生态制剂、中兽药、抗菌肽、酸化剂、免疫增强剂等,以其残留低、不易产生耐药性等特点深受规模养殖企业青睐。着力解决传统微生态制剂疗效不确切,作用机制不明确的问题,开发能够在肠道定植的精准微生态制剂并进行作用机制机理的研究。中兽药对畜禽具有多方位调节和治疗作用,很多中草药中的多糖类、有机酸类、生物碱类、苷类和挥发油类等.都对增加动物机体免疫力有特效,可有效替代抗菌药物在动物促生长方面的作用。研发具有天然抗菌性的中兽药产品和增强机体免疫力的中兽药保健品,突破天然药物超微粉碎、发酵和纯化等现代化工艺技术,深入研究能实现工业化生产的精油、多糖和多酚类成分的提取分离等关键技术,为市场提供更多的绿色投入品。
3.4 支持窄谱、高效、低毒新型抗菌药及生物制剂的研制
目前多数兽药企业从改变抗菌药剂型、研发缓释产品和仿制药等人手,在当前兽用抗菌药减量化的大背景下,对兽药行业转型具有积极意义。此外,生物制品预防动物疫病一直是大型生物制品企业的研发重点,细菌疫苗能显著提高易感动物对病原菌的抵抗力,降低病原菌感染的发生率,有利于感染性疾病的预防。噬菌体作为特异性细菌病毒,裂解细菌效率高,无残留,可以针对流行菌株筛选裂解性噬菌体定点清除而不造成肠道菌群紊乱[16]。随着国家兽用抗菌药使用减量化行动的实施,噬菌体、基因工程疫苗和复合干扰素的研发必将迎来历史性的发展机遇期。
3.5 优化畜禽养殖环境生态系统控制
顺应“保健为先、预防为主、养防结合、健康养殖”的行业大趋势,把动物疫病防控的重点前移,强化养殖舍环境控制和粪污无害化处理,降低病原微生物的传播风险,从源头上控制疫病的发生,减少抗菌药物的使用带来的耐药性风险。养殖舍环境控制应综合应用信息化、智能化和网络化技术,优化软硬件配置,融合温度、湿度、空气、光照、饲喂、清粪等各要素自动控制,利用动态的物联网技术实现实时监控,为动物饲养创造适宜的环境条件。养殖粪污处理在国家环保督察的大背景下正如火如荼展开,但粪污资源化须慎重考虑抗菌药物残留的影响,若处理不彻底的抗菌药随水肥进入土壤,势必诱导细菌产生耐药性基因随食物链进人人体,对人类健康造成严重伤害,因此应加大在这一领域的技术研究和监控。
3.6 推进兽用抗菌药减量化示范行动
农业农村部在2018年5月19日重庆全国畜博会上举行了“兽用抗菌药使用减量化行动”启动仪式,拉开了全国性兽用抗菌药综合治理的序幕,也标志着我国细菌耐药性监测工作进入了新征程。兽用抗菌药综合治理是一个系统工程,需要政府、科研、检验、推广和企业等全员参入,协调开展、统筹推进。这一过程中,各方应深抓国家政策出台的有利契机,深入推进抗菌药物减量示范创建,加快制定不同养殖区域的畜禽用药指导目录,有效激发起养殖企业参人的积极性。同时,充分发挥电视、报纸和互联网等媒体作用,加强科学用药控制细菌耐药性的培训和宣传,进一步提高养殖从业人员和基层兽医合理、规范用药意识,减少和杜绝抗菌药物的滥用。
参考文献:
[1] 沈建忠.国外兽药残留和动物源细菌耐药性现状及应对[J].兽医导刊,2017(13):5-6.
[2] 马苏,沈建忠.动物源细菌耐药性监测国内外比较[J].中国兽医杂志,2016,52(9):121 -123.
[3] 吴聪明,我国动物源病原菌的耐药现状与防控对策[J],兽医导刊,2013 (11):50 -53.
[4] 张利锋,齐静,罗成旺,等。鸡源大肠桿菌B-内酰胺类药敏及bla_( CTX - M)基因携带状况的探讨[J].检验医学与临床,2016 .13( 9):1153 - 1155.
[5] 刘建民,张瑞华,姜世金.潍坊市肉鸭源大肠杆菌喹诺酮类药物耐药性的检测[J].家禽科学,2015 (11):17 -20.
[6] 刁有江,范学政.山东部分地区规模化肉鸭场致病性大肠杆菌优势血清型调查与耐药性检测[J].医学动物防制,2015,31(5):476 -480.
[7] 王昌健.猪源大肠杆菌的分离鉴定、耐药性分析及联合药敏试验的研究[D].泰安:山东农业大学,2016.
[8] 冯敏燕,傅剑,杨世发,等.山东省鸡源性大肠杆菌耐药变化趋势监测[J].中国兽医学报,2017,37(2):250 -253.
[9] 王娟,刘鲜鲜,张倩,等.山东生猪屠宰环节沙门氏菌血清型及耐药性测试[J].中国人兽共患病学报,2017,33(6):517 - 521.
[10]孙璐,王娟,黄秀梅,等.山东省肉鸡屠宰生产链中沙门菌耐药性分析及毒力基因检测[J].中国家禽,2016,38 (24):22 - 27.
[11] 李秀梅,杨宏军,肖红,等.山东省牛源金黄色葡萄球菌耐药谱分析及mecA耐药基因检测[J].山东农业科学,2012,44(3):13 -16.
[12] 曲志娜.养殖场动物源细菌耐药性监测与风险控制[J].兽医导刊,2017 (13):10 -12.
[13] 张纯萍,宋立,吴辰斌,等.我国动物源细菌耐药性监测系统简介[J].中国动物检疫,2017(3):34 - 38.
[14] 农业农村部.中华人民共和国农业部公告第2638号[EB/OL]. http://www. moa. gov. cn/govpublic/SYJ/201801/t20180112_6134888.htm.2018 -1 - 11.
[15]刘玉庆,李璐璐,骆延波,等.EUCAST欧盟药敏试验标准[s].北京:中国标准出版社,2016.
[16]张庆,齐静,李璐璐,等.我国兽医抗药性特点与生态防控[J].山东农业科学,2018,50(7):1-5.

